文档内容
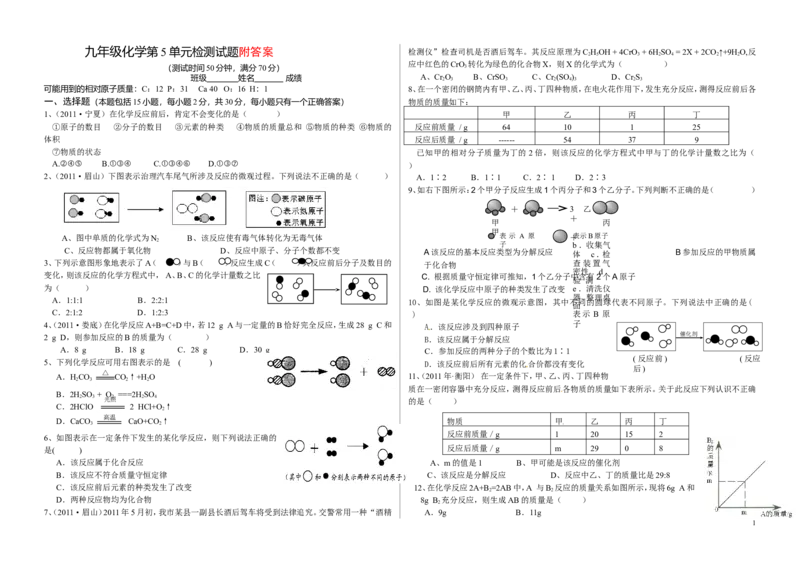
九年级化学第5单元检测试题附答案 检测仪”检查司机是否酒后驾车。其反应原理为C HOH + 4CrO + 6H SO = 2X + 2CO ↑+9H O,反
2 5 3 2 4 2 2
应中红色的CrO 转化为绿色的化合物X,则X的化学式为( )
(测试时间50分钟,满分70分) 3
班级 姓名 成绩 A、Cr 2 O 3 B、CrSO 3 C、Cr 2 (SO 4 ) 3 D、Cr 2 S 3
可能用到的相对原子质量:C:12 P:31 Ca 40 O:16 H:1 8、在一个密闭的钢筒内有甲、乙、丙、丁四种物质,在电火花作用下,发生充分反应,测得反应前后各
一、选择题(本题包括15小题,每小题2分,共30分,每小题只有一个正确答案) 物质的质量如下:
1、(2011·宁夏)在化学反应前后,肯定不会变化的是( ) 甲 乙 丙 丁
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类 ⑥物质的 反应前质量 / g 64 10 1 25
体积 反应后质量 / g ------ 54 37 9
⑦物质的状态 已知甲的相对分子质量为丁的 2倍,则该反应的化学方程式中甲与丁的化学计量数之比为(
A.②④⑤ B.①③④ C.①③④⑥ D.①③⑦ )
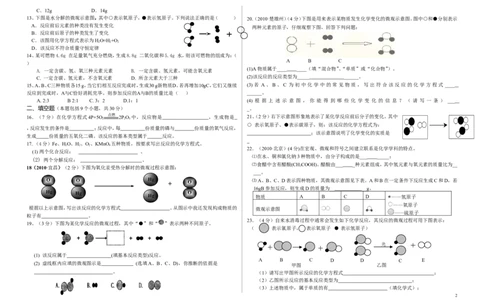
2、(2011·眉山)下图表示治理汽车尾气所涉及反应的微观过程。下列说法不正确的是( ) A.1∶2 B.1∶1 C.2∶ 1 D.2∶3
9、如右下图所示:2个甲分子反应生成1个丙分子和3个乙分子。下列判断不正确的是( )
+ 3 乙
+
甲 丙
甲
A、图中单质的化学式为N B、该反应使有毒气体转化为无毒气体 表示 A 原 +表示B原子
2
子 b.收集气
C、反应物都属于氧化物 D、反应中原子、分子个数都不变 A该反应的基本反应类型为分解反应 体 c . 检 B参加反应的甲物质属
3、下列示意图形象地表示了A( )与B( )反应生成C( )其反应前后分子及数目的 于化合物 查装置气
密性 d.
变化,则该反应的化学方程式中, A、B、C的化学计量数之比 C. 根据质量守恒定律可推知,1个乙分子中含有2个A原子
验 满
为( ) D. 该化学反应中原子的种类发生了改变 e.清洗仪
器、整理桌
A.1:1:1 B.2:2:1 10、如图是某化学反应的微观示意图,其中不同的圆球代表不同原子。下列说法中正确的是(
面
C.2:1:2 D.1:2:3 ) 表示 B 原
4、(2011·娄底)在化学反应A+B=C+D中,若12 g A与一定量的B恰好完全反应,生成28 g C和 A.该反应涉及到四种原子 子
2 g D,则参加反应的B的质量为( ) B.该反应属于分解反应 催化剂→
A.8 g B.18 g C.28 g D.30 g C.参加反应的两种分子的个数比为1∶1
(反应前) (反应
5、下列化学反应可用右图表示的是 ( ) D.该反应前后所有元素的化合价都没有变化
后)
A.HCO
△
C O↑+H O 11、(2011年·衡阳) 在一定条件下,甲、乙、丙、丁四种物
2 3 2 2
质在一密闭容器中充分反应,测得反应前后各物质的质量如下表所示。关于此反应下列认识不正确
B.2HSO + O ===2HSO
2 3 光照2 2 4
的是( )
C.2HClO 2 HCl+O ↑
2
D.CaCO
高温
CaO+CO ↑ 物质 甲 乙 丙 丁
3 2 [
反应前质量/g 1 20 15 2
6、如图表示在一定条件下发生的某化学反应,则下列说法正确的
是( ) 反应后质量/g m 29 0 8
A.该反应属于化合反应 A、m的值是1 B、甲可能是该反应的催化剂
B.该反应不符合质量守恒定律 C、该反应是分解反应 D、反应中乙、丁的质量比是29:8
C.该反应前后元素的种类发生了改变 12、在化学反应2A+B =2AB中,A 与B 反应的质量关系如图所示,现将6g A和
2 2
D.两种反应物均为化合物 8g B 充分反应,则生成AB的质量是( )
2
7、(2011·眉山)2011年5月初,我市某县一副县长酒后驾车将受到法律追究。交警常用一种“酒精 A.9g B.11g
1C.12g D.14g
13、下图是水分解的微观示意图,其中○表示氧原子,●表示氢原子。下列说法正确的是( ) 20.( 2010·楚雄州)(4分)下图是用来表示某物质发生化学变化的微观示意图。图中○和●分别表示
A.反应前后元素的种类没有发生变化
两种元素的原子,仔细观察下图,回答下列问题:
B.反应前后原子的种类发生了变化
C.该图用化学方程式表示为HO=H+O
2 2 2
D.该反应不符合质量守恒定律
14、某可燃物4.6g 在足量氧气充分燃烧,生成8.8g 二氧化碳和5.4g 水,则该可燃物的组成为:(
A B C
)
(1)A物质属于____ ____(填“混合物”、“单质”或“化合物”)。
A. 一定含碳、氢、氧三种元素元素 B. 一定含碳、氢元素,可能含氧元素
C. 一定含碳、氢元素,不含氧元素 D. 所含元素大于三种 (2)该反应的反应类型为_____ ______。
15、A、B、C三种物质各15 g,当它们相互反应完成时,生成30 g新物质D。若再增加10gC,它们又继续 (3)若 A、B、C 为初中化学中的常见物质,写出符合该反应的化学方程式 ____
反应到完成时,A与C恰好消耗完毕。则参加反应的A与B的质量比是( ) ______。
A. 2:3 B 2:1 C. 3:2 D.1:1 (4) 根 据 上 述 示 意 图 , 你 能 得 到 哪 些 化 学 变 化 的 信 息 ? ( 请 写 一 条 ) ___
二、填空题(本题包括9个小题,共30分) _。
16.(7分)在化学方程式4P+5O 点燃 2PO 中,反应物是 ,生成物是 21、(2分)右下示意图形象地表示了某化学反应前后分子的变化。其中
2 2 5
○ 表示氧原子、●表示碳原子,则:该反应的化学方程式为:
,反应发生的条件是 ;反应中,每 份质量的磷与 份质量的氧气反应,
;该示意图说明了化学变化的实质是
生成 份质量的五氧化二磷。该反应的基本类型属于 反应。
17. (4分)Fe、HO、H、O、KMnO 五种物质,按要求写出反应的化学方程式。
2 2 2 4
22.(2010·北京)(4分)在宏观、微观和符号之间建立联系是化学学科的特点。
(1) 两个化合反应: 、
⑴在水、铜和氯化钠3种物质中,由分子构成的是___ _____;
(2) 两个分解反应: 、
⑵食醋中含有醋酸(CHCOOH)。醋酸由___ _种元素组成,其中氢元素与氧元素的质量比为__
18(2010·宜昌)(2分)下图为氧化汞受热分解时的微观过程示意图: 3
___。
O O Hg
+ O
⑶A、B、C、D表示四种物质,其微观示意图见下表。A和B在一定条件下反应生成C和D,若
16gB参加反应,则生成D的质量为__ __g。
Hg Hg O
Hg 物质 A B C D ——氢原子
——氧原子
根据以上示意图,写出该反应的化学方程式 。从图示中我还发现构成物质的 微观示意图
——硫原子
粒子有 。
23.(4分)自来水消毒过程中通常会发生如下化学反应,其反应的微观过程可用下图表示:
19、(3分)下图为某化学反应的微观过程,其中“●”和“ ”表示两种不同原子。
( 表示氯原子, 表示氧原子 ,表示氢原子)
光 +
+ +
(1) 该反应属于 (填基本反应类型)反应。
A B C D D C E
(2) 虚线框内应填的微观图示是 (选填A、B、C、D),你推断的依据是 甲图 乙图
。 (1)请写出甲图所示反应的化学方程式 ;
(2)乙图所示反应的基本反应类型为 ;
(3)上述物质中,属于单质的有 (填化学式);
2(4)以甲图为例分析,你能总结出的一条结论是 。 17. (1) 3Fe+2O 点燃 Fe O、 2H+O 点燃 2HO
2 3 4 2 2 2
三、实验题(本题1个小题,共4分)
通电 △
24. (4分)质量守恒定律是物质科学中的一条重要规律,具体表述为:参加化学反应的各物质的质 (2) 2H 2 O 2H 2 ↑+O 2 ↑ 、2KMnO 4 K 2 MnO 4 +MnO 2 +O 2 ↑
量总和,等于反应后生成的各物质的质量总和。 △
18 2HgO 2Hg+O↑ 。分子、原子 。
2
19、(3分) (1)分解 (2) D 质量守恒定律(或化学反应前后原子种类、数目不变)。
20. (1)单质 (2)化合反应。 (3) 2H +O
点燃
2HO。 (4)化学反应前后,元素的种类不变。
2 2 2
21、(2分)2CO+ O
点燃
2CO 原子发生了重新组合
2 2
22. (4分) ⑴水; ⑵ 3 1:8。 ⑶ 18。
(1)某科学兴趣小组的同学设计了如下三个实验装置(天平略)来验证质量守恒律。其中,只有A 23.(4分)(1)HO+Cl == HCl+HClO;;(2)分解反应;(3)Cl 、O;
2 2 2 2
装置能用来验证质量守恒定律,B、C装置则不能。否定B、C装置的理由是: (4)化学反应前后原子的种类、数目不变。
。 24.(1)B装置内发生的反应属于物理变化。C装置内产生的气体会逸出到空气中。
(2)小明将C装置进行改进,如图D所示。 (2) ①锥形瓶内有大量气泡产生气球变大。
② 气球变大后,受到空气的浮力,方向竖直向上,导致天平称量反应后物质质量的读数偏
①此实验的现象是 。
②待完全反应后,将装置D置于天平上称量,所得数据较反应前的小。若整个操作过 小。
程无差错,则造成上述实验误差的原因是 三、计算题(本题共1小题,共6分)
。
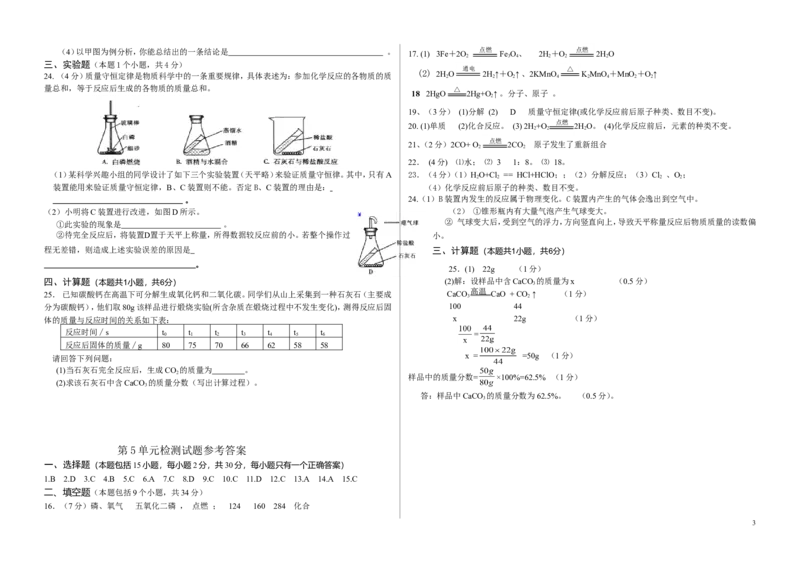
25.(1) 22g (1分)
四、计算题(本题共1小题,共6分) (2)解:设样品中含CaCO
3
的质量为x (0.5分)
高温
25. 已知碳酸钙在高温下可分解生成氧化钙和二氧化碳。同学们从山上采集到一种石灰石(主要成 CaCO CaO + CO ↑ (1分)
3 2
分为碳酸钙),他们取80g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固 100 44
体的质量与反应时间的关系如下表: x 22g (1分)
反应时间∕s t 0 t 1 t 2 t 3 t 4 t 5 t 6 =
反应后固体的质量∕g 80 75 70 66 62 58 58
请回答下列问题: x = =50g (1分)
(1)当石灰石完全反应后,生成CO 的质量为 。
2
样品中的质量分数= ×100%=62.5% (1分)
(2)求该石灰石中含CaCO 的质量分数(写出计算过程)。
3
答:样品中CaCO 的质量分数为62.5%。 (0.5分)。
3
第5单元检测试题参考答案
一、选择题(本题包括15小题,每小题2分,共30分,每小题只有一个正确答案)
1.B 2.D 3.C 4.B 5.C 6.A 7.C 8.D 9.C 10.C 11.D 12.C 13.A 14.A 15.C
二、填空题(本题包括9个小题,共34分)
16.(7分)磷、氧气 五氧化二磷 , 点燃 ; 124 160 284 化合
3