文档内容
2019 年普通高等学校招生全国统一考试
化学
注意事项:
1. 答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2. 回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改
动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在
本试卷上无效。
3. 考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:
一、选择题:本题共6小题,每小题2分,共12分,在每小题给出的四个选项中,只有一项
是符合题目要求的。
1. 某试剂瓶标签上安全标志如图,该试剂是
A. 氨水 B. 乙酸 C. 氢氧化钠 D. 硝酸
【1题答案】
【答案】D
【解析】
【详解】A.氨水具有腐蚀性,但不具有氧化性,A不符合题意;
B.乙酸具有腐蚀性,但不具有氧化性,B不符合题意;
C.氢氧化钠具有腐蚀性,但不具有氧化性,C不符合题意;
.
D硝酸具有腐蚀性,同时具有氧化性,D符合题意;
故合理选项是D。
2. 我国古代典籍中有“石胆……浅碧色,烧之变白色者真”的记载,其中石胆是指
A. B.
第1页 | 共20页C. D.
【2题答案】
【答案】A
【解析】
【详解】在选项给出的四种物质中只有 、 晶体有色,而 和
均为无色晶体, 加热分解生成 CuSO 和 HO,CuSO 呈白色;而
4 2 4
加热发生分解反应,生成的Fe O 呈红棕色,所以符合题意的物质是 ,故合
2 3
理选项是A。
3. 反应C H(g) C H(g)+H(g) H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能
2 6 2 4 2
提高乙烷平衡转化率的是 △
A. 增大容器容积 B. 升高反应温度
C. 分离出部分氢气 D. 等容下通入惰性气体
【3题答案】
【答案】D
【解析】
【分析】
【详解】A.该反应的正反应是气体体积增大的吸热反应,增大反应容器的容积,体系的压强减小,化学平
衡正向移动,能提高乙烷平衡转化率,A不符合题意;
B.该反应的正反应是气体体积增大的吸热反应,升高反应温度,化学平衡正向移动,可提高乙烷的平衡转
化率,B不符合题意;
C.分离出部分氢气,减少了生成物浓度,平衡正向移动,可提高乙烷的平衡转化率,C不符合题意;
D.等容下通入惰性气体,体系的总压强增大,物质的浓度不变,因此化学平衡不移动,对乙烷的平衡转化
率无影响,D符合题意;
故合理选项是D。
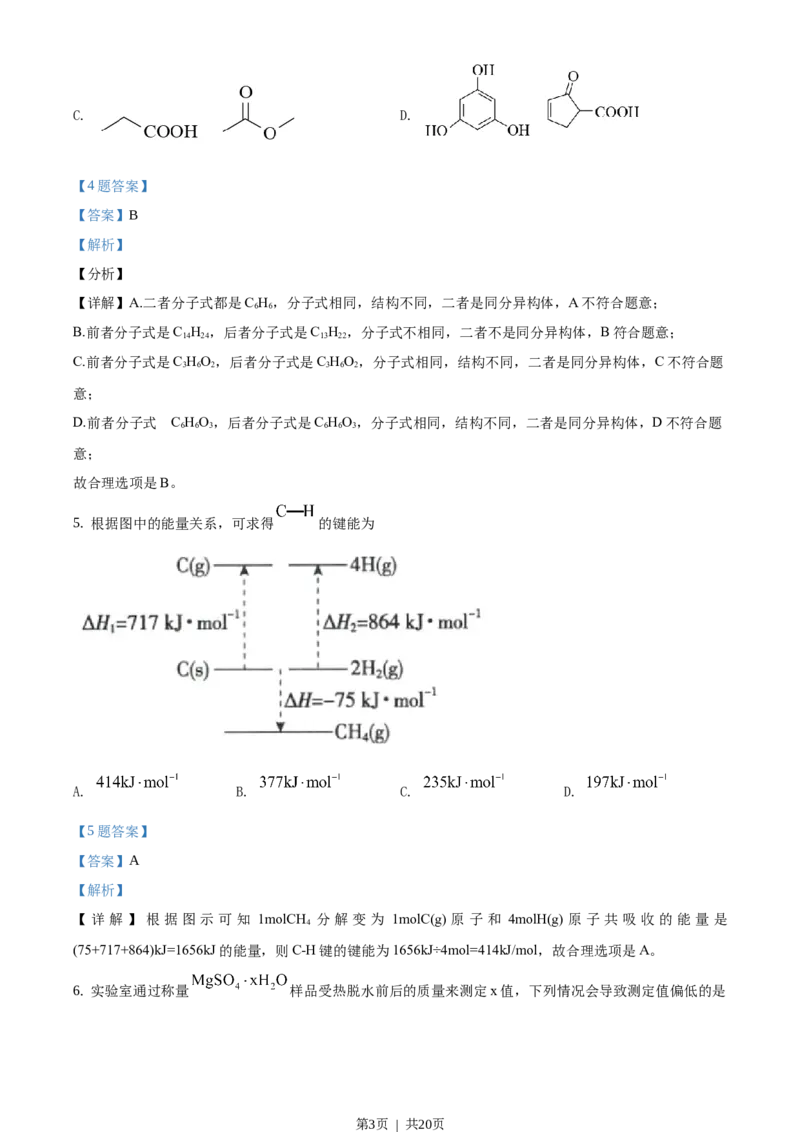
4. 下列各组化合物中不互为同分异构体的是
A. B.
第2页 | 共20页C. D.
【4题答案】
【答案】B
【解析】
【分析】
【详解】A.二者分子式都是C H,分子式相同,结构不同,二者是同分异构体,A不符合题意;
6 6
B.前者分子式是C H ,后者分子式是C H ,分子式不相同,二者不是同分异构体,B符合题意;
14 24 13 22
C.前者分子式是C HO,后者分子式是C HO,分子式相同,结构不同,二者是同分异构体,C不符合题
3 6 2 3 6 2
意;
D.前者分子式 是C HO,后者分子式是C HO,分子式相同,结构不同,二者是同分异构体,D不符合题
6 6 3 6 6 3
意;
故合理选项是B。
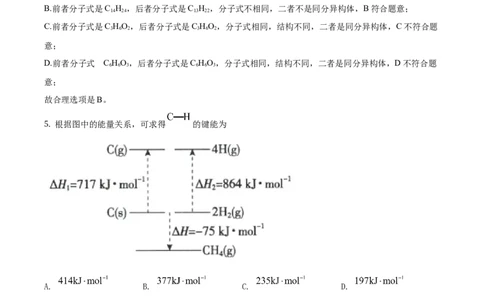
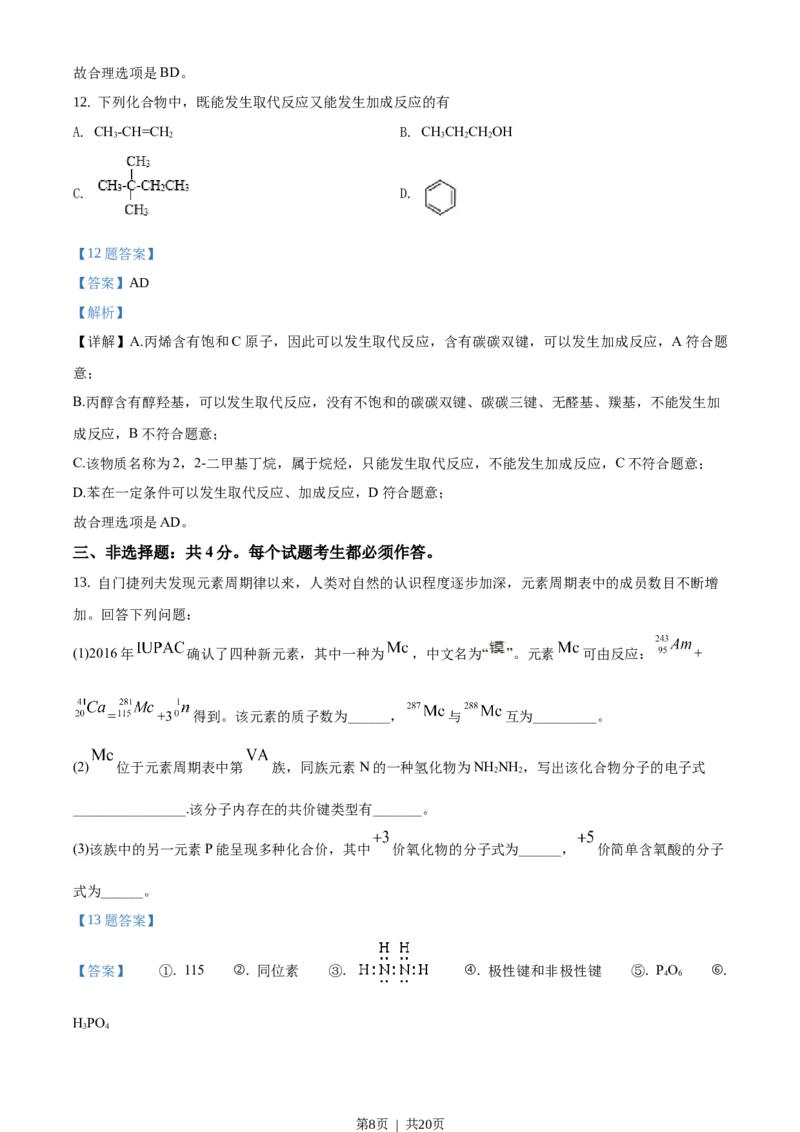
5. 根据图中的能量关系,可求得 的键能为
A. B. C. D.
【5题答案】
【答案】A
【解析】
【 详 解 】 根 据 图 示 可 知 1molCH 分 解 变 为 1molC(g) 原 子 和 4molH(g) 原 子 共 吸 收 的 能 量 是
4
(75+717+864)kJ=1656kJ的能量,则C-H键的键能为1656kJ÷4mol=414kJ/mol,故合理选项是A。
6. 实验室通过称量 样品受热脱水前后的质量来测定x值,下列情况会导致测定值偏低的是
第3页 | 共20页A. 实验前试样未经干燥 B. 试样中含有少量碳酸氢铵
C. 试样中含有少量氯化钠 D. 加热过程中有试样迸溅出来
【6题答案】
【答案】C
【解析】
【详解】A.实验前试样未经干燥,加热后剩余固体质量偏少,导致结晶水含量偏高,A不符合题意;
B.试样中含有少量碳酸氢铵,碳酸氢铵受热分解成氨气、二氧化碳和水,加热分解后剩余固体质量偏少,
导致结晶水含量偏高,B不符合题意;
C.试样中含有少量氯化钠,氯化钠受热不分解,加热分解后剩余固体质量偏大,导致结晶水的含量偏低,
C符合题意;
D.加热过程中有试样迸溅出来,加热分解后剩余固体质量偏少,会使结晶水的质量偏高,导致结晶水的含
量偏高,D不符合题意;
故合理选项是C。
二、选择题:本题共6小题,每小题4分,共24分。每小趣有一个或两个选项符合题意,若
正确答案只包括一个选项,多选得0分;若正确答案包括两个选项,只选一个且正确得2分,
选两个且都正确得4分,但只要选错一个就得0分。
7. 今年是门捷列夫发现元素周期律150周年,联合国将2019年定为“国际化学元素周期表年”。下列有关
化学元素周期表的说法正确的是
A. 元素周期表共有18列
B. VIIA族元素的非金属性自上而下依次减弱
C. 主族元素均呈现与其族数相同的最高化合价
D. 第二周期主族元素的原子半径自左向右依次增大
【7题答案】
【答案】AB
【解析】
【详解】A.元素周期表共有18纵行,也就是共有18列,A正确;
B.由于同一主族的元素从上到下,原子半径逐渐增大,原子获得电子的能力逐渐减弱,所以VIIA族元素
的非金属性自上而下依次减弱,B正确;
C.主族元素一般呈现与其族数相同的最高化合价,O、F非金属性强,O没有与族序数相等的最高正化合价,
F没有正价,C错误;
D.第二周期主族元素的原子半径自左向右依次减小,D错误;
故合理选项是AB。
第4页 | 共20页8. 微型银-锌电池可用作电子仪器的电源,其电极分别是 和 ,电解质为 溶液,电池总
反应为 ,下列说法正确的是
A. 电池工作过程中, 溶液浓度降低
B. 电池工作过程中,电解液中 向负极迁移
C. 负极发生反应
D. 正极发生反应
【8题答案】
【答案】BC
【解析】
【分析】根据电池反应式知,Zn 失电子发生氧化反应而作负极,氧化银作正极,负极发生反应
Zn+2OH--2e-=Zn(OH) ,正极上发生反应:Ag O+HO+2e-=2Ag+2OH-,放电时,电解质溶液中阴离子向负
2 2 2
极移动、阳离子向正极移动,以此解答该题。
【详解】A.根据电池工作原理可知,在电池工作过程中,KOH的物质的量不变,但反应消耗水,使
c(KOH)增大,A错误;
B.根据同种电荷相互排斥,异种电荷相互吸引的原则,电池工作过程中,电解液中 向负极迁移,B正
确;
C.负极上锌失电子发生氧化反应,电极反应式为Zn+2OH--2e-=Zn(OH) ,C正确;
2
D.正极上Ag O获得电子,发生还原反应,由于电解质溶液为碱性,不可能大量存在H+,电极反应式为
2
Ag O+HO+2e-=2Ag+2OH-,D错误;
2 2
故合理选项是BC。
【点睛】本题考查新型电池的工作原理的知识,明确各个电极上发生的反应是解本题关键,难点是电极反
应式的书写,要结合电解质溶液酸碱性书写,易错选项是D。
9. 一定温度下,AgCl(s) Ag+(aq)+Cl-(aq)体系中,c(Ag+)和c(Cl-)的关系如图所示。下列说法正确的是
第5页 | 共20页A. a、b、c三点对应的K 相等
sp
B. AgCl在c点的溶解度比b点的大
C. AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl-)
D. b点的溶液中加入AgNO 固体,c(Ag+)沿曲线向c点方向变化
3
【9题答案】
【答案】AC
【解析】
【分析】A.溶度积常数只与温度有关;
B.AgCl在溶液中存在沉淀溶解平衡,向溶液中加入与AgCl电离产生的相同离子时,根据沉淀溶解平衡的
影响因素分析移动方向,判断物质溶解度大小;
C.根据AgCl在溶液中的沉淀溶解平衡电离产生的Ag+、Cl-的关系判断离子浓度大小;
D.向AgCl饱和溶液中加入AgNO 固体,溶液中c(Ag+)会增大。
3
【详解】A.a、b、c三点对应的AgCl的沉淀溶解平衡所处的温度相同,而溶度积常数K 只与温度有关,
sp
温度相同,则K 相等,A正确;
sp
B. 在AgCl溶于水形成的饱和溶液中c(Ag+)=c(Cl-),在AgCl(s) Ag+(aq)+Cl-(Aq)平衡体系中
c(Ag+)·c(Cl-)=K (AgCl),若溶液中c(Cl-)大,则溶液中c(Ag+)小,AgCl的溶解度小,在b点溶液中c(Cl-)小
sp
于c点,则溶解度b点大于c点,B错误;
C.根据溶解平衡AgCl(s) Ag+(aq)+Cl-(aq)可知,在AgCl溶于水形成的饱和溶液中,溶解的AgCl电离产
生的Cl-、Ag+的浓度相等,c(Ag+)=c(Cl-),C正确;
D.在b点的溶液中加入AgNO 固体,溶液中c(Ag+)增大,则c(Cl-)减小,所以c(Ag+)变化应该是沿曲线
3
向a点方向变化,D错误;
故合理选项是AC。
【点睛】本题考查难溶电解质的溶解平衡及溶度积常数等知识,解答本题时注意把握横坐标、纵坐标的含
义及曲线变化趋势,了解图像曲线的意义。
10. 下列说法正确的是
第6页 | 共20页A. 和 都属于两性氧化物 B. 悬浊液和乳浊液的分散质均为液态
C. 和 中的金属都呈现两种价态 D. 葡萄糖溶液和淀粉溶液都具有丁达尔效应
【10题答案】
【答案】C
【解析】
【详解】A.MgO是碱性氧化物,A错误;
B.悬浊液的分散质是固体小颗粒,B错误;
C. 可表示为FeO·Fe O,Fe元素化合价为+2、+3价; 可表示为2PbO·PbO,Pb元素化合价为
2 3 2
+2、+4价;因此二者中的金属都呈现两种价态,C正确;
D.葡萄糖分子是小分子,葡萄糖溶液中溶质分子直径小于1nm,所以葡萄糖溶液不能产生丁达尔效应,D
错误;
故合理选项是C。
的
11. 能正确表示下列反应 离子方程式为
A. 向FeBr 溶液中通入过量Cl:2Fe2++Cl=2Fe3++2Cl-
2 2 2
B. 向碳酸钠溶液中通入少量CO:CO2-+CO +H O=2HCO -
2 3 2 2 3
C. 向碘化钾溶液中加入少量双氧水:3HO+I-=IO -+3H O
2 2 3 2
D. 向硫化钠溶液中通入过量SO :2S2-+5SO+2H O=3S↓+4HSO -
2 2 2 3
【11题答案】
【答案】BD
【解析】
【分析】
【详解】A.FeBr 电离产生的Fe2+、Br-都具有还原性,向该溶液中通入过量Cl ,Fe2+、Br-都会被氧化,离
2 2
子方程式为:2Fe2++4Br-+3Cl=2Fe3++2Br +6Cl-,A错误;
2 2
B.向碳酸钠溶液中通入少量CO,NaCO、CO、HO发生反应生成NaHCO ,反应的离子方程式为:CO2-
2 2 3 2 2 3 3
+CO +H O=2HCO -,B正确;
2 2 3
的
C.H O 具有氧化性,在酸性条件下,会将I-氧化为I,反应 离子方程式为:HO+2H++2I-=I +2H O,C错
2 2 2 2 2 2 2
误;
D.向硫化钠溶液中通入过量SO ,由于酸性HSO >H S,由于SO 过量,发生的反应有:S2-
2 2 3 2 2
+2SO+2H O=HS+2HSO -,SO + 2H S=3S↓+2H O,总反应方程式为2S2-+5SO+2H O=3S↓+4HSO -,D正确;
2 2 2 3 2 2 2 2 2 3
第7页 | 共20页故合理选项是BD。
12. 下列化合物中,既能发生取代反应又能发生加成反应的有
A. CH-CH=CH B. CHCHCHOH
3 2 3 2 2
C. D.
【12题答案】
【答案】AD
【解析】
【详解】A.丙烯含有饱和C原子,因此可以发生取代反应,含有碳碳双键,可以发生加成反应,A符合题
意;
B.丙醇含有醇羟基,可以发生取代反应,没有不饱和的碳碳双键、碳碳三键、无醛基、羰基,不能发生加
成反应,B不符合题意;
C.该物质名称为2,2-二甲基丁烷,属于烷烃,只能发生取代反应,不能发生加成反应,C不符合题意;
D.苯在一定条件可以发生取代反应、加成反应,D符合题意;
故合理选项是AD。
三、非选择题:共4分。每个试题考生都必须作答。
13. 自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增
加。回答下列问题:
(1)2016年 确认了四种新元素,其中一种为 ,中文名为“ ”。元素 可由反应: +
= +3 得到。该元素的质子数为______, 与 互为_________。
(2) 位于元素周期表中第 族,同族元素N的一种氢化物为NH NH ,写出该化合物分子的电子式
2 2
________________.该分子内存在的共价键类型有_______。
(3)该族中的另一元素P能呈现多种化合价,其中 价氧化物的分子式为______, 价简单含氧酸的分子
式为______。
【13题答案】
【答案】 ①. 115 ②. 同位素 ③. ④. 极性键和非极性键 ⑤. PO ⑥.
4 6
HPO
3 4
第8页 | 共20页【解析】
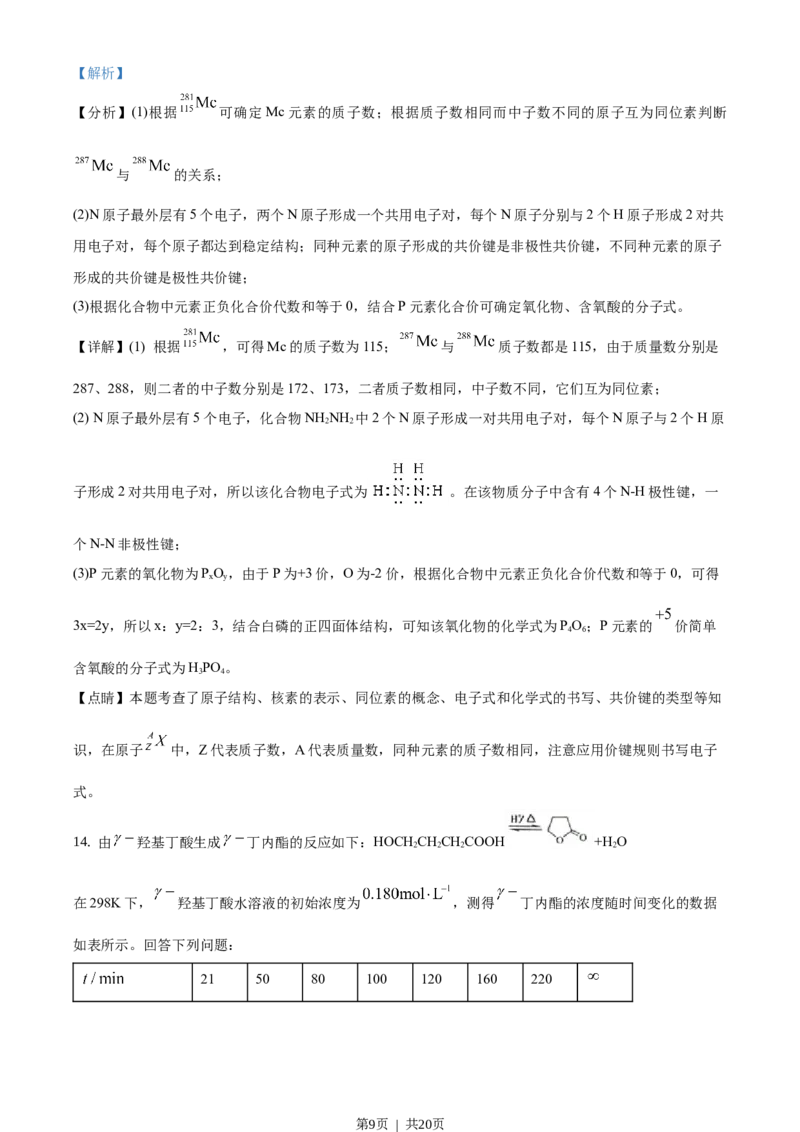
【分析】(1)根据 可确定Mc元素的质子数;根据质子数相同而中子数不同的原子互为同位素判断
与 的关系;
(2)N原子最外层有5个电子,两个N原子形成一个共用电子对,每个N原子分别与2个H原子形成2对共
用电子对,每个原子都达到稳定结构;同种元素的原子形成的共价键是非极性共价键,不同种元素的原子
形成的共价键是极性共价键;
(3)根据化合物中元素正负化合价代数和等于0,结合P元素化合价可确定氧化物、含氧酸的分子式。
【详解】(1) 根据 ,可得Mc的质子数为115; 与 质子数都是115,由于质量数分别是
287、288,则二者的中子数分别是172、173,二者质子数相同,中子数不同,它们互为同位素;
(2) N原子最外层有5个电子,化合物NH NH 中2个N原子形成一对共用电子对,每个N原子与2个H原
2 2
子形成2对共用电子对,所以该化合物电子式为 。在该物质分子中含有4个N-H极性键,一
个N-N非极性键;
(3)P元素的氧化物为PO,由于P为+3价,O为-2价,根据化合物中元素正负化合价代数和等于0,可得
x y
3x=2y,所以x:y=2:3,结合白磷的正四面体结构,可知该氧化物的化学式为PO;P元素的 价简单
4 6
含氧酸的分子式为HPO 。
3 4
【点睛】本题考查了原子结构、核素的表示、同位素的概念、电子式和化学式的书写、共价键的类型等知
识,在原子 中,Z代表质子数,A代表质量数,同种元素的质子数相同,注意应用价键规则书写电子
式。
14. 由 羟基丁酸生成 丁内酯的反应如下:HOCH CHCHCOOH +H O
2 2 2 2
在298K下, 羟基丁酸水溶液的初始浓度为 ,测得 丁内酯的浓度随时间变化的数据
如表所示。回答下列问题:
21 50 80 100 120 160 220
第9页 | 共20页0.024 0.050 0.071 0.081 0.090 0.104 0.116 0.132
(1)该反应在50~80min内的平均反应速率为_____ 。
(2)120min时 羟基丁酸的转化率为______。
(3)298K时该反应的平衡常数 _____。
(4)为提高 羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是______。
【14题答案】
【答案】 ①. 0.0007 ②. 0.5(50%) ③. ④. 将 丁内酯移走
【解析】
【分析】(1)根据υ= 计算反应速率;
(2)根据物质的转化率= 计算;
(3)根据化学平衡常数K= 计算化学平衡常数;
(4)根据影响化学平衡移动的因素,分析判断。
【详解】(1) υ= = =0.0007mol/(L·min);
(2)在120min时反应产生的 丁内酯的物质的量浓度0.090mol/L,则反应消耗的 羟基丁酸的浓度为
0.090mol/L,由于反应开始时 羟基丁酸的浓度0.180mol/L,所以 羟基丁酸的转化率为
=50%;
(3)298K的摄氏温度为25℃,水为液态,则此时该反应的平衡常数K= =
= ;
第10页 | 共20页(4)为提高 羟基丁酸的平衡转化率,使化学平衡正向移动,除适当控制反应温度外,还可采取的措施是
及时分离出 丁内酯。
【点睛】本题考查了有关化学反应速率、化学平衡的知识,包括化学反应速率、物质的平衡转化率、化学
平衡常数的计算及提高物质转化率的措施等,掌握化学反应速率和化学平衡理论基础知识是解题关键因素。
15. 无机酸有机酯在生产中具有广泛的应用,回答下列问题:
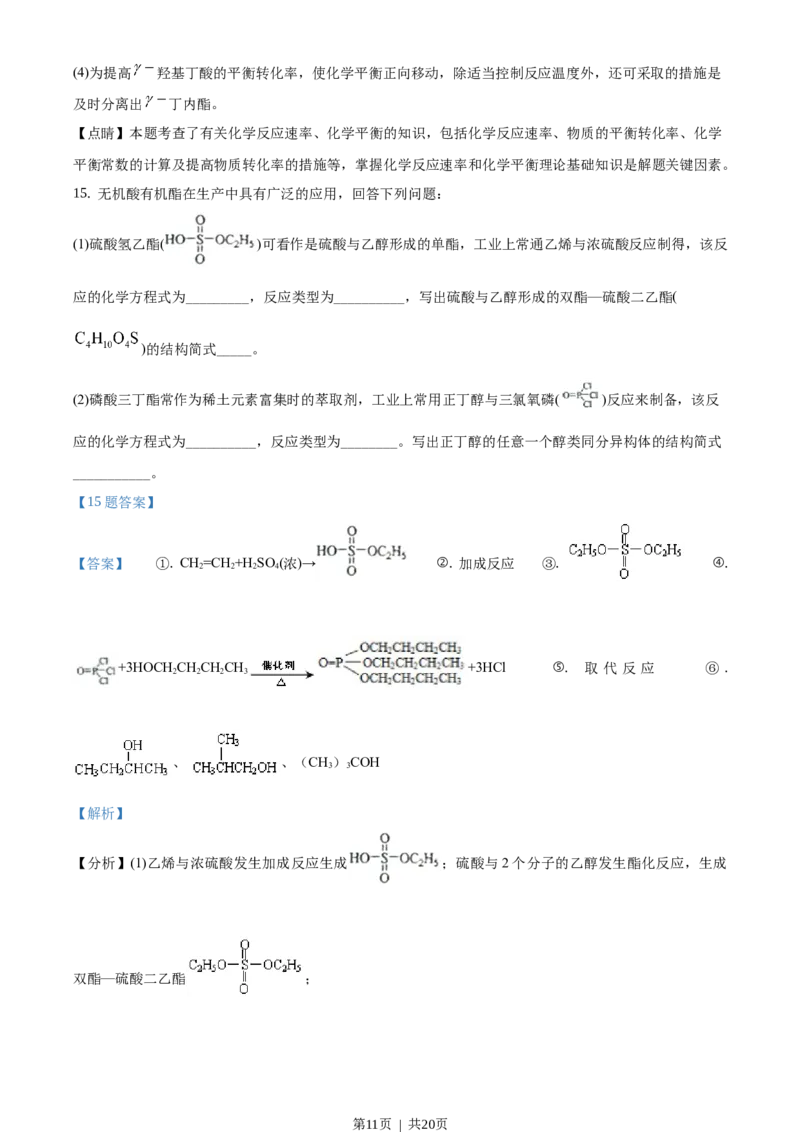
(1)硫酸氢乙酯( )可看作是硫酸与乙醇形成的单酯,工业上常通乙烯与浓硫酸反应制得,该反
应的化学方程式为_________,反应类型为__________,写出硫酸与乙醇形成的双酯—硫酸二乙酯(
)的结构简式_____。
(2)磷酸三丁酯常作为稀土元素富集时的萃取剂,工业上常用正丁醇与三氯氧磷( )反应来制备,该反
应的化学方程式为__________,反应类型为________。写出正丁醇的任意一个醇类同分异构体的结构简式
___________。
【15题答案】
【答案】 ①. CH=CH +H SO (浓)→ ②. 加成反应 ③. ④.
2 2 2 4
+3HOCH CHCHCH +3HCl ⑤. 取 代 反 应 ⑥ .
2 2 2 3
、 、(CH)COH
3 3
【解析】
【分析】(1)乙烯与浓硫酸发生加成反应生成 ;硫酸与2个分子的乙醇发生酯化反应,生成
双酯—硫酸二乙酯 ;
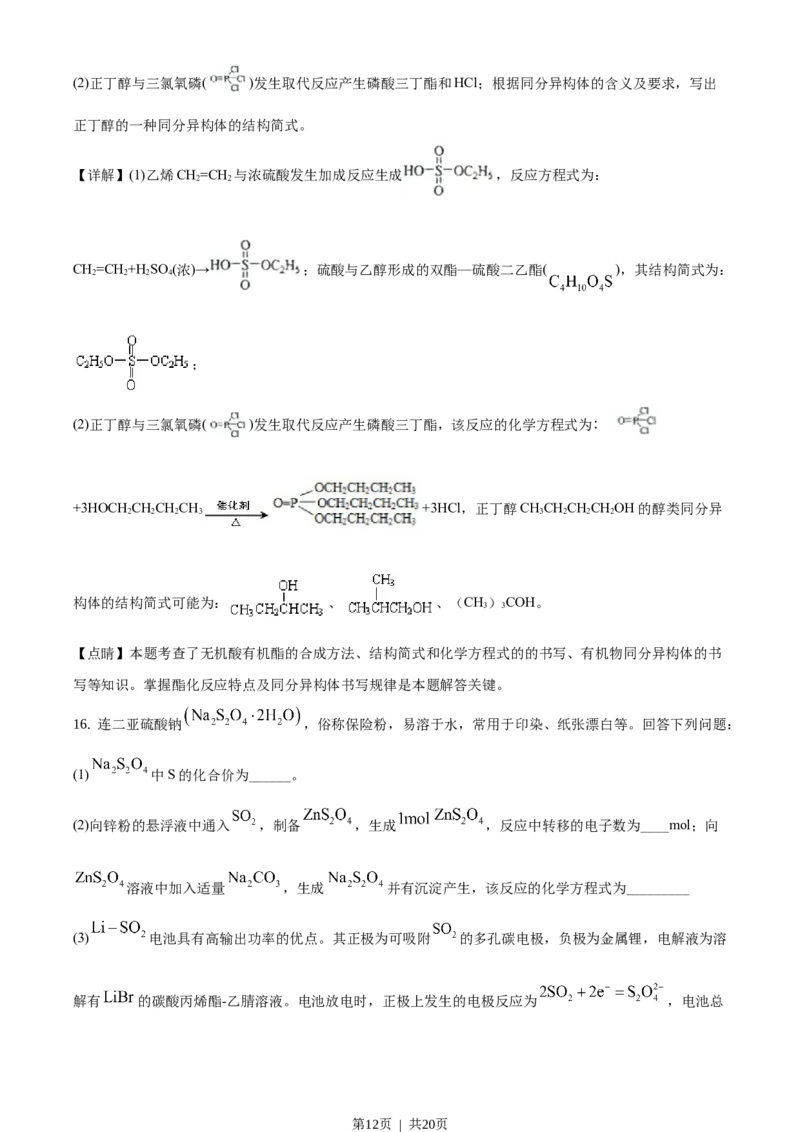
第11页 | 共20页(2)正丁醇与三氯氧磷( )发生取代反应产生磷酸三丁酯和HCl;根据同分异构体的含义及要求,写出
正丁醇的一种同分异构体的结构简式。
【详解】(1)乙烯CH=CH 与浓硫酸发生加成反应生成 ,反应方程式为:
2 2
CH=CH +H SO (浓)→ ;硫酸与乙醇形成的双酯—硫酸二乙酯( ),其结构简式为:
2 2 2 4
;
(2)正丁醇与三氯氧磷( )发生取代反应产生磷酸三丁酯,该反应的化学方程式为:
+3HOCH CHCHCH +3HCl,正丁醇CHCHCHCHOH的醇类同分异
2 2 2 3 3 2 2 2
构体的结构简式可能为: 、 、(CH)COH。
3 3
【点睛】本题考查了无机酸有机酯的合成方法、结构简式和化学方程式的的书写、有机物同分异构体的书
写等知识。掌握酯化反应特点及同分异构体书写规律是本题解答关键。
16. 连二亚硫酸钠 ,俗称保险粉,易溶于水,常用于印染、纸张漂白等。回答下列问题:
(1) 中S的化合价为______。
(2)向锌粉的悬浮液中通入 ,制备 ,生成 ,反应中转移的电子数为____mol;向
溶液中加入适量 ,生成 并有沉淀产生,该反应的化学方程式为_________
(3) 电池具有高输出功率的优点。其正极为可吸附 的多孔碳电极,负极为金属锂,电解液为溶
解有 的碳酸丙烯酯-乙腈溶液。电池放电时,正极上发生的电极反应为 ,电池总
第12页 | 共20页反应式为____________。该电池不可用水替代混合有机溶剂,其原因是_______________。
【16题答案】
【 答 案 】 ① . +3 ②. 2 ③. ④.
⑤. 与水反应
【解析】
【分析】(1)根据化合物中所有元素正负化合价的代数和等于 0,结合常见的Na为+1价,O为-2价判断S
元素的化合价;
(2)根据反应前后Zn元素的化合价的变化判断转移电子的物质的量,根据质量守恒定律书写反应方程式;
(3)负极上是Li失去电子变为Li+,根据闭合回路中电子转移数目相等,结合正极反应式,叠加,可得总反
应方程式;Li是比较活泼的金属,可以与水反应产生相应的碱和氢气。
【详解】(1)在 中Na为+1价,O为-2价,由于化合物中所有元素正负化合价的代数和等于0,所
以S元素化合价为+3价;
(2)向锌粉的悬浮液中通入SO ,制备ZnS O,反应前Zn为单质中的0价,反应后变为ZnS O 中的+2价,
2 2 4 2 4
所以每生成 ZnS O,反应中转移的电子数为2mol;向ZnS O 溶液中加入适量NaCO,生成NaSO
2 4 2 4 2 3 2 2 4
并有沉淀产生,生成的沉淀为ZnCO ,则该反应的化学方程式为NaCO+ ZnS O=Na SO+ZnCO ↓;
3 2 3 2 4 2 2 4 3
(3) 电池具有高输出功率的优点,负极是Li失去电子,电极反应式为Li-e-=Li+,电池放电时,正
极上发生的电极反应为 ,根据闭合回路中电子转移数目相等,将两个电极反应式叠加,
可得电池总反应式为 。锂是碱金属,比较活泼,可以与水发生反应生成LiOH和
H,所以该电池不可用水替代。
2
【点睛】本题考查了化合物中元素化合价的标定、氧化还原反应中的电子转移、化学方程式的书写及原电
池反应原理的应用的知识。掌握化学反应基本原理及元素化合物的基础知识是解题关键。
17. 干燥的二氧化碳和氨气反应可生成氨基甲酸铵固体,化学方程式为:
,在四氯化碳中通入二氧化碳和氨制备氨基甲酸铵的
实验装置如下图所示,回答下列问题:
第13页 | 共20页(1)装置1用来制备二氧化碳气体:将块状石灰石放置在试管中的带孔塑料板上,漏斗中所加试剂为____;
装置2中所加试剂为____;
(2)装置4中试剂为固体NH Cl和Ca(OH) ,发生反应的化学方程式为________;试管口不能向上倾斜的原
4 2
因是__________。装置3中试剂为KOH,其作用为______________。
(3)反应时三颈瓶需用冷水浴冷却,其目的是_______________________。
【17题答案】
【答案】 ①. 稀盐酸 ②. 浓HSO ③. Ca(OH) +2NHCl CaCl +2NH↑+2H O ④. 防止
2 4 2 4 2 3 2
冷凝水倒流到管底部使试管破裂 ⑤. 干燥剂(干燥氨气) ⑥. 降低温度,使平衡正向移动提高产量
【解析】
【分析】在装置1中稀盐酸与CaCO 发生反应产生CO 气体,在装置2中用浓硫酸干燥CO 气体,将干燥
3 2 2
的CO 通入三颈烧瓶中;在装置4中Ca(OH) 与NH Cl混合加热发生复分解反应产生NH ,经装置3盛有
2 2 4 3
KOH 固体的干燥管干燥后通入三颈烧瓶中,与 CO 发生反应 2NH (g)+CO (g) NH COONH(s)
2 3 2 2 4
△H<0,制取得到NH COONH。
2 4
【详解】(1)装置1用来制备二氧化碳气体,反应方程式为CaCO +2HCl=CaCl +CO ↑+H O,在试管的带孔
3 2 2 2
塑料板上放置块状CaCO ,在长颈漏斗中放置稀盐酸;装置2中所加试剂为浓硫酸,作用是干燥CO 气体;
3 2
(2)在装置4中试剂为固体NH Cl和Ca(OH) ,二者混合加热发生反应制取氨气,发生反应的化学方程式为
4 2
Ca(OH) +2NHCl CaCl +2NH↑+2H O;试管口不能向上倾斜的原因是:防止冷凝水倒流到管底部使试
2 4 2 3 2
管破裂。装置3中试剂为KOH,其作用为干燥氨气。
(3)反应时三颈瓶需用冷水浴冷却,原因是2NH (g)+CO (g) NH COONH(s) △H<0的正反应是放热反
3 2 2 4
应,降低温度,化学平衡向放热的正反应方向移动,从而可提高产物的产量。
【点睛】本题考查了化学实验基本操作的知识。涉及仪器的使用,试剂的选择、装置的作用、操作的目的
及外界条件对化学平衡移动的影响等知识,体现了化学在实际生产中的应用。
四、选考题:共20分,请考生从第18、19题中任选一题作答。如果多做,则按所做的第一
题计分。第18、19题的第Ⅰ题为选择题,在给出的四个选项中,有两个选项是符合题目要求
的,请将符合题目要求的选项标号填在答题卡相应位置:第Ⅱ题为非选择题,请在答题卡相
第14页 | 共20页应位置作答并写明小题号。
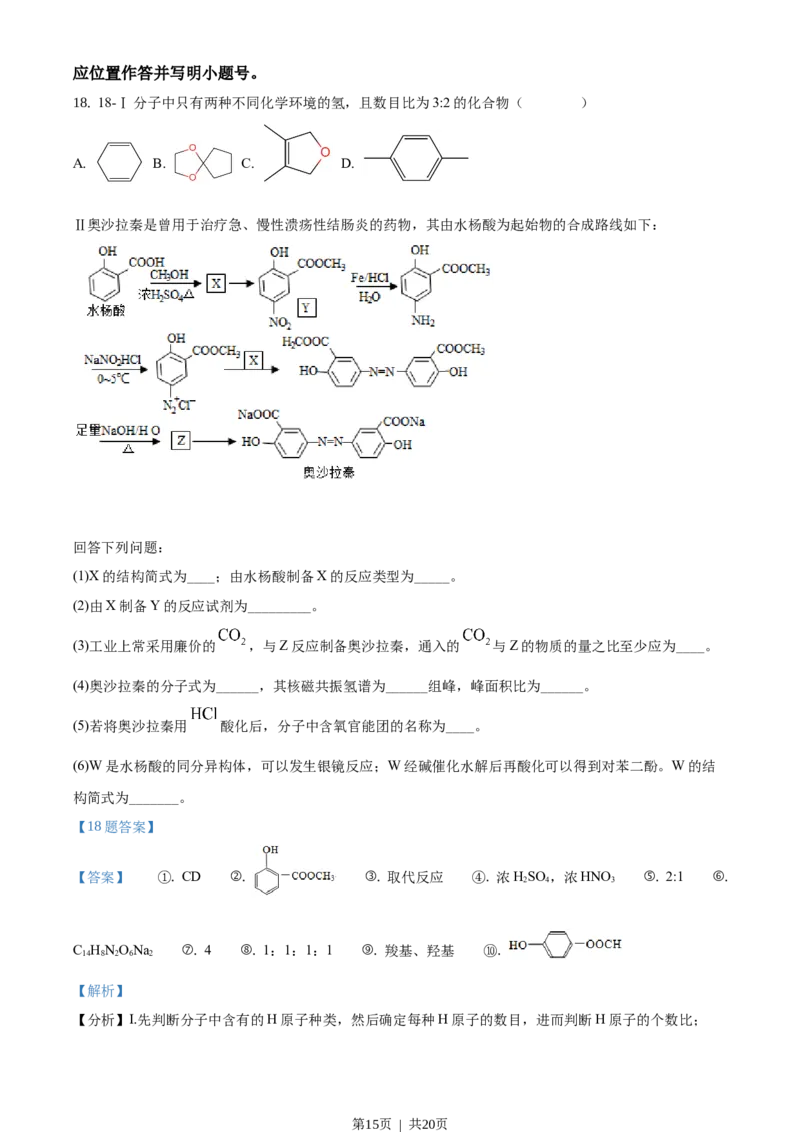
18. 18-Ⅰ分子中只有两种不同化学环境的氢,且数目比为3:2的化合物( )
A. B. C. D.
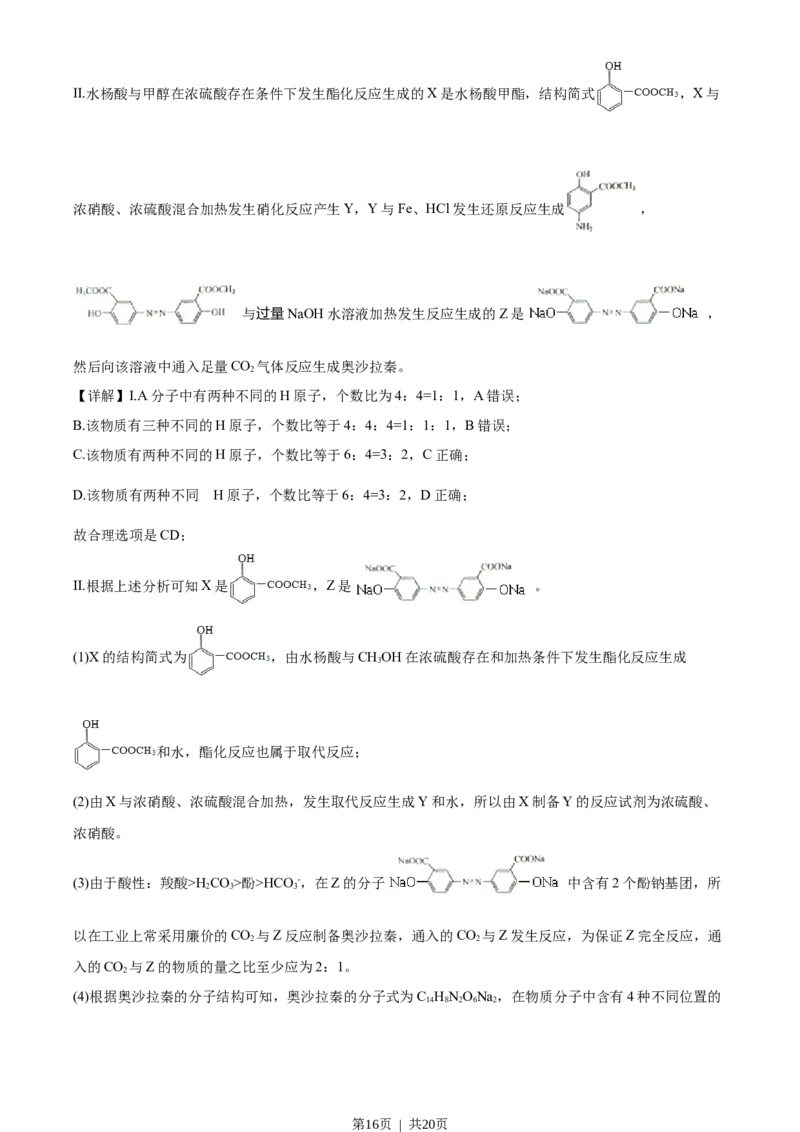
Ⅱ奥沙拉秦是曾用于治疗急、慢性溃疡性结肠炎的药物,其由水杨酸为起始物的合成路线如下:
回答下列问题:
(1)X的结构简式为____;由水杨酸制备X的反应类型为_____。
(2)由X制备Y的反应试剂为_________。
(3)工业上常采用廉价的 ,与Z反应制备奥沙拉秦,通入的 与Z的物质的量之比至少应为____。
(4)奥沙拉秦的分子式为______,其核磁共振氢谱为______组峰,峰面积比为______。
(5)若将奥沙拉秦用 酸化后,分子中含氧官能团的名称为____。
(6)W是水杨酸的同分异构体,可以发生银镜反应;W经碱催化水解后再酸化可以得到对苯二酚。W的结
构简式为_______。
【18题答案】
【答案】 ①. CD ②. ③. 取代反应 ④. 浓HSO ,浓HNO ⑤. 2:1 ⑥.
2 4 3
C HNONa ⑦. 4 ⑧. 1:1:1:1 ⑨. 羧基、羟基 ⑩.
14 8 2 6 2
【解析】
【分析】I.先判断分子中含有的H原子种类,然后确定每种H原子的数目,进而判断H原子的个数比;
第15页 | 共20页II.水杨酸与甲醇在浓硫酸存在条件下发生酯化反应生成的X是水杨酸甲酯,结构简式 ,X与
浓硝酸、浓硫酸混合加热发生硝化反应产生Y,Y与Fe、HCl发生还原反应生成 ,
与过量NaOH水溶液加热发生反应生成的Z是 ,
然后向该溶液中通入足量CO 气体反应生成奥沙拉秦。
2
【详解】I.A分子中有两种不同的H原子,个数比为4:4=1:1,A错误;
B.该物质有三种不同的H原子,个数比等于4:4:4=1:1:1,B错误;
C.该物质有两种不同的H原子,个数比等于6:4=3:2,C正确;
的
D.该物质有两种不同 H原子,个数比等于6:4=3:2,D正确;
故合理选项是CD;
II.根据上述分析可知X是 ,Z是 。
(1)X的结构简式为 ,由水杨酸与CHOH在浓硫酸存在和加热条件下发生酯化反应生成
3
和水,酯化反应也属于取代反应;
(2)由X与浓硝酸、浓硫酸混合加热,发生取代反应生成Y和水,所以由X制备Y的反应试剂为浓硫酸、
浓硝酸。
(3)由于酸性:羧酸>H CO>酚>HCO-,在Z的分子 中含有2个酚钠基团,所
2 3 3
以在工业上常采用廉价的CO 与Z反应制备奥沙拉秦,通入的CO 与Z发生反应,为保证Z完全反应,通
2 2
入的CO 与Z的物质的量之比至少应为2:1。
2
(4)根据奥沙拉秦的分子结构可知,奥沙拉秦的分子式为C HNONa,在物质分子中含有4种不同位置的
14 8 2 6 2
第16页 | 共20页H原子,所以其核磁共振氢谱为4组峰,峰面积比为1:1:1:1。
(5)若将奥沙拉秦用 酸化后,得到的物质分子结构为 ,在该分子中含氧官
能团的名称为羧基、羟基。
(6)W是水杨酸的同分异构体,可以发生银镜反应,说明W中含醛基;W经碱催化水解后再酸化可以得到对
苯二酚。W的结构简式为 。
【点睛】本题考查了有机物的推断,涉及物质结构的推断、同分异构体的书写、反应类型的判断、反应条
件的判断等。掌握各种官能团对物质性质的决定作用是解题关键,本题同时考查了学生接受信息、应用信
息解决问题的能力。
19. Ⅰ.下列各组物质性质的比较,结论正确的是( )
A. 分子的极性: B. 物质的硬度:
C. 物质的沸点: D.在 中的溶解度:
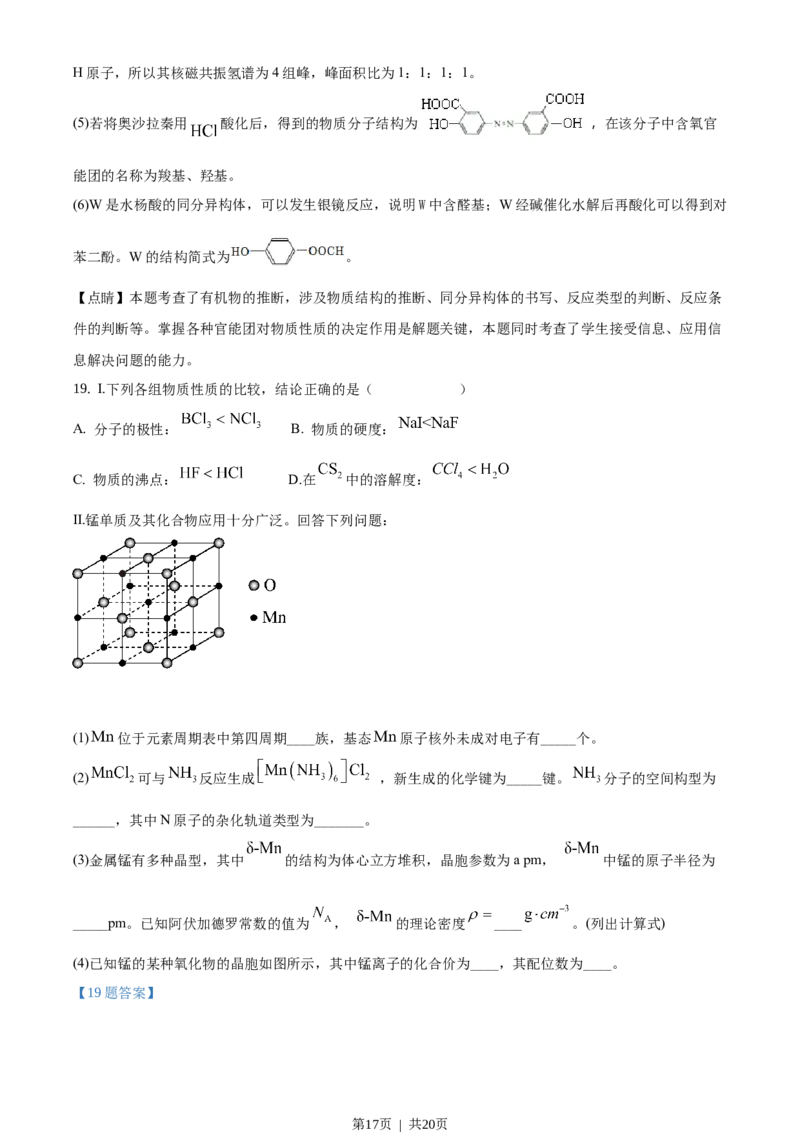
Ⅱ.锰单质及其化合物应用十分广泛。回答下列问题:
(1) 位于元素周期表中第四周期____族,基态 原子核外未成对电子有_____个。
(2) 可与 反应生成 ,新生成的化学键为_____键。 分子的空间构型为
______,其中N原子的杂化轨道类型为_______。
(3)金属锰有多种晶型,其中 的结构为体心立方堆积,晶胞参数为a pm, 中锰的原子半径为
_____pm。已知阿伏加德罗常数的值为 , 的理论密度 ____ 。(列出计算式)
(4)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为____,其配位数为____。
【19题答案】
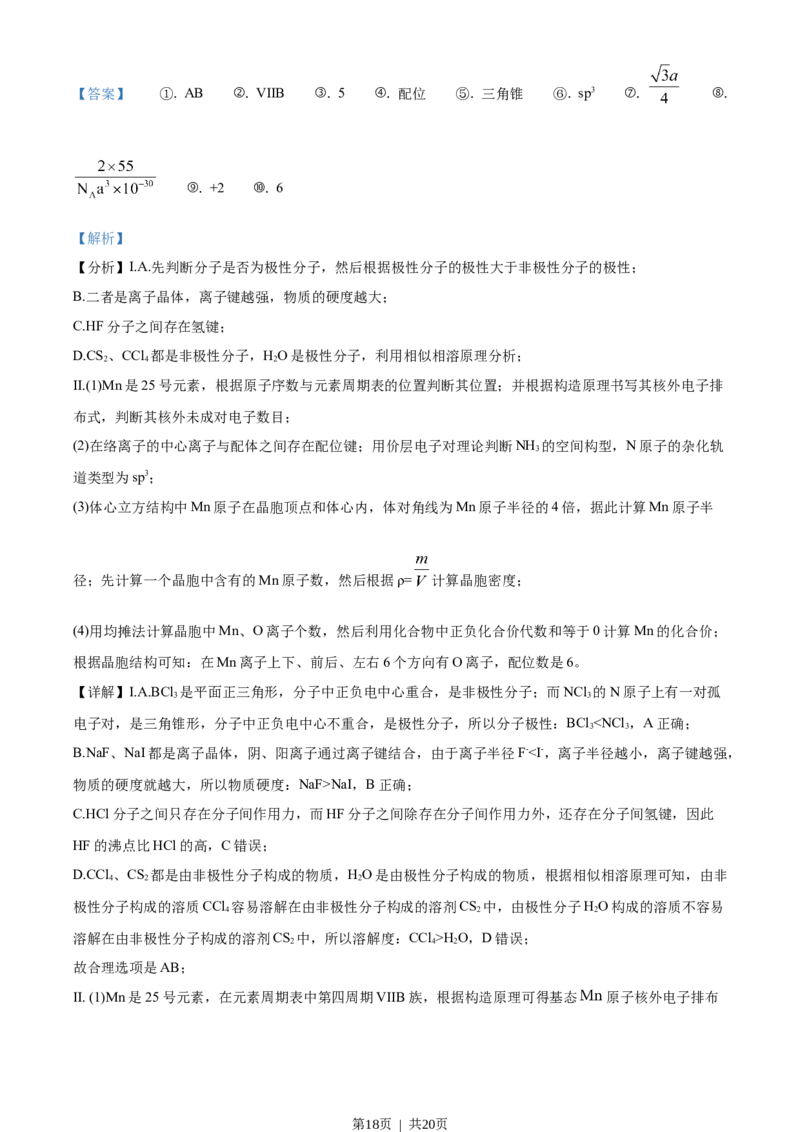
第17页 | 共20页【答案】 ①. AB ②. VIIB ③. 5 ④. 配位 ⑤. 三角锥 ⑥. sp3 ⑦. ⑧.
⑨. +2 ⑩. 6
【解析】
【分析】I.A.先判断分子是否为极性分子,然后根据极性分子的极性大于非极性分子的极性;
B.二者是离子晶体,离子键越强,物质的硬度越大;
C.HF分子之间存在氢键;
D.CS 、CCl 都是非极性分子,HO是极性分子,利用相似相溶原理分析;
2 4 2
II.(1)Mn是25号元素,根据原子序数与元素周期表的位置判断其位置;并根据构造原理书写其核外电子排
布式,判断其核外未成对电子数目;
(2)在络离子的中心离子与配体之间存在配位键;用价层电子对理论判断NH 的空间构型,N原子的杂化轨
3
道类型为sp3;
(3)体心立方结构中Mn原子在晶胞顶点和体心内,体对角线为Mn原子半径的4倍,据此计算Mn原子半
径;先计算一个晶胞中含有的Mn原子数,然后根据ρ= 计算晶胞密度;
(4)用均摊法计算晶胞中Mn、O离子个数,然后利用化合物中正负化合价代数和等于0计算Mn的化合价;
根据晶胞结构可知:在Mn离子上下、前后、左右6个方向有O离子,配位数是6。
【详解】I.A.BCl 是平面正三角形,分子中正负电中心重合,是非极性分子;而NCl 的N原子上有一对孤
3 3
电子对,是三角锥形,分子中正负电中心不重合,是极性分子,所以分子极性:BCl NaI,B正确;
C.HCl分子之间只存在分子间作用力,而HF分子之间除存在分子间作用力外,还存在分子间氢键,因此
HF的沸点比HCl的高,C错误;
D.CCl 、CS 都是由非极性分子构成的物质,HO是由极性分子构成的物质,根据相似相溶原理可知,由非
4 2 2
极性分子构成的溶质CCl 容易溶解在由非极性分子构成的溶剂CS 中,由极性分子HO构成的溶质不容易
4 2 2
溶解在由非极性分子构成的溶剂CS 中,所以溶解度:CCl >H O,D错误;
2 4 2
故合理选项是AB;
II. (1)Mn是25号元素,在元素周期表中第四周期VIIB族,根据构造原理可得基态 原子核外电子排布
第18页 | 共20页式1s22s22p63s23p63d54s2,根据核外电子排布规律可知,该原子核外的未成对电子有5个;
(2)MnCl 中的Mn2+上有空轨道,而NH 的N原子上有孤电子对,因此二者反应可形成络合物
2 3
,则新生成的化学键为配位键。NH 的价层电子对数为3+ ,且N原子上
3
有一对孤电子对,所以NH 分子的空间构型为三角锥形,其中N原子的杂化轨道类型为sp3杂化。
3
(3)体心立方结构中Mn原子在晶胞顶点和体心内,体对角线为Mn原子半径的4倍,由于晶胞参数为
apm,则 ,则Mn原子半径r= pm;在一个Mn晶胞中含有的Mn原子数为 ,
则根据晶体密度ρ= 可得晶胞密度ρ= = = g/cm3;
(4)在晶胞中含有的Mn离子数目为: ,含有的O离子数目为: ,Mn离子:
O离子=4:4=1:1,所以该氧化物的化学式为MnO,化合物中元素正负化合价代数和等于0,由于O的化
合价为-2价,所以Mn的化合价为+2价;根据晶胞结构可知:在Mn离子上、下、前、后、左、右6个方
向各有一个O离子,所以Mn离子的配位数是6。
【点睛】本题考查了物质结构与性质的知识,涉及分子的极性、物质的熔沸点、硬度、溶解性的比较、原
子核外电子排布及与其在周期表位置的关系、晶胞结构与计算等。在考查学生对知识的掌握的同时,考查
了学生的空间想象能力及数学计算能力。
第19页 | 共20页第20页 | 共20页