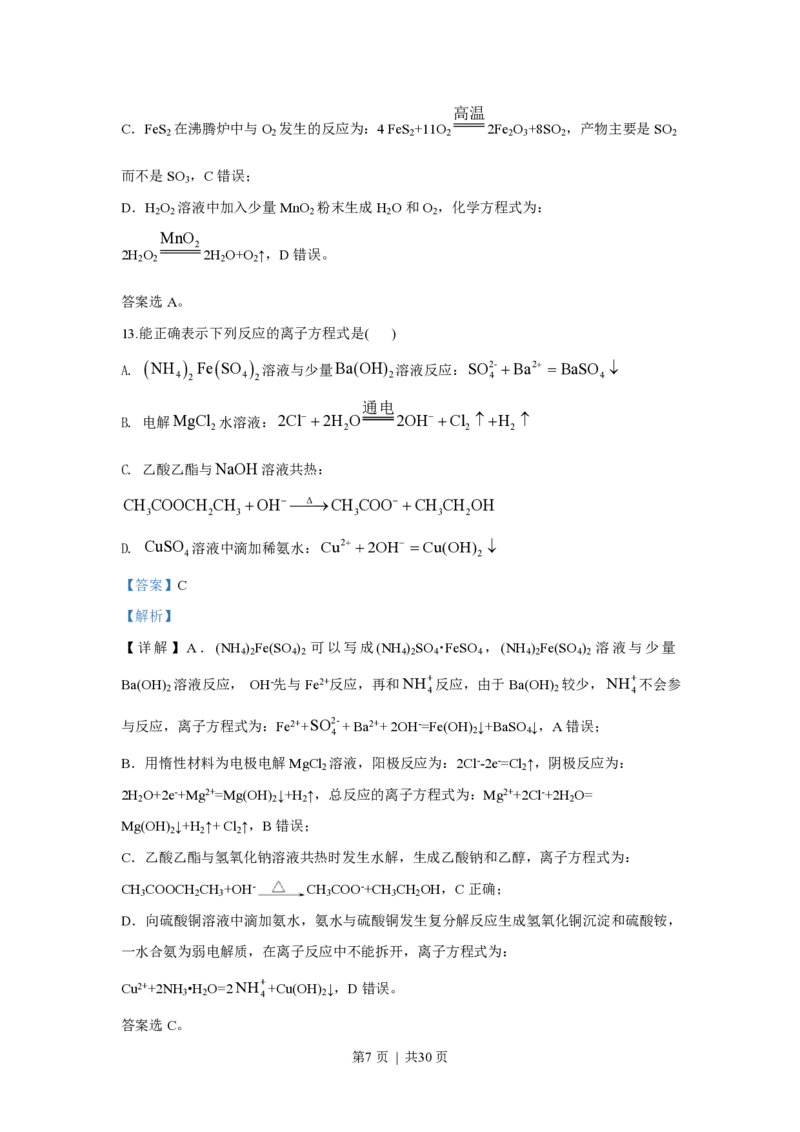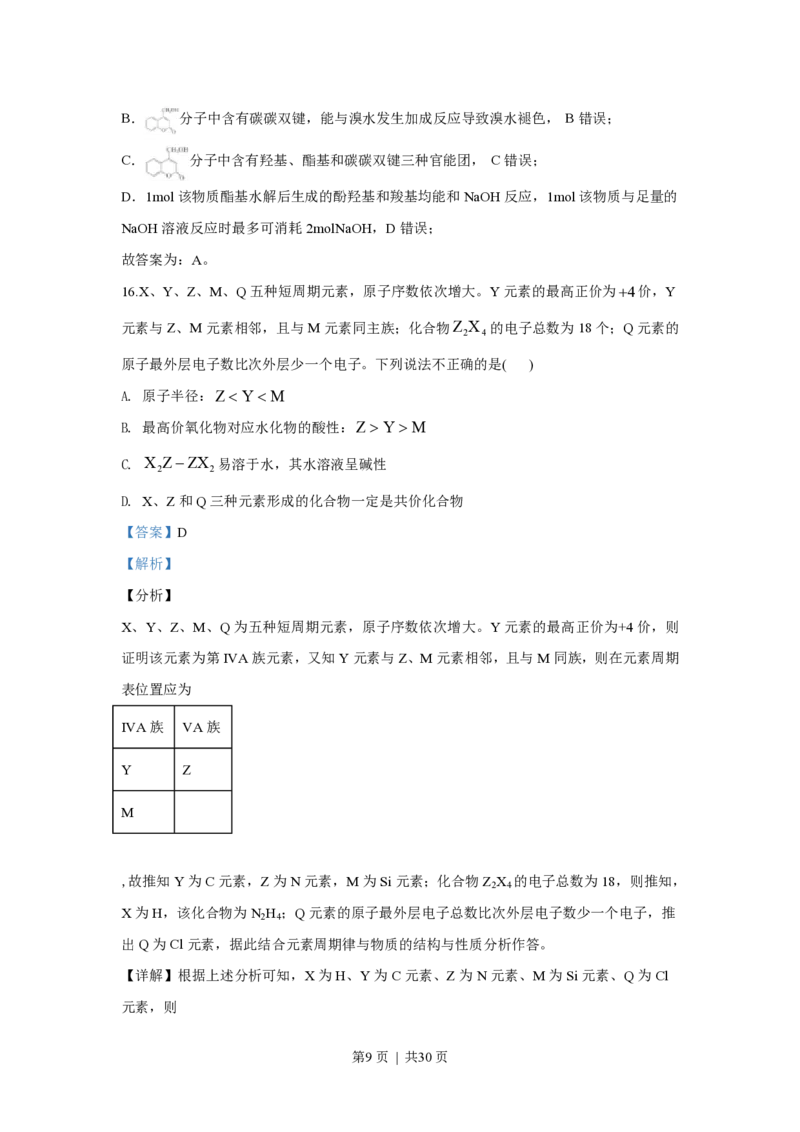文档内容
化学试题
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Mg 24 Al 27 Si 28
S 32 Cl 35.5 K 39 Ca 40 Mn 55 Fe 56 Cu 64 Zn 65 Ag 108 I 127 Ba
137
一、选择题(本大题共 25小题,每小题 2分,共 50分。每小题列出的四个备选
项中只有一个是符合题目要求的,不选、多选、错选均不得分)
1.水溶液呈酸性的是( )
A. NaCl B. NaHSO C. HCOONa D.
4
NaHCO
3
【答案】B
【解析】
【详解】A.NaCl是强酸强碱盐,其不能水解,故其水溶液呈中性,A不符合题意;
B.NaHSO 是强酸的酸式盐,其属于强电解质,其在水溶液中的电离方程式为
4
NaHSO =Na++H++SO2-,故其水溶液呈酸性,B符合题意;
4 4
C.HCOONa属于强碱弱酸盐,其在水溶液中可以完全电离,其电离产生的HCOO-可以发
生水解,其水解的离子方程式为HCOO-+H O⇌HCOOH+OH-,故其水溶液呈碱性,C不
2
符合题意;
D.NaHCO 是强碱弱酸盐,既能发生电离又能发生水解,但其水解程度大于电离程度,故
3
其水溶液呈碱性,D不符合题意。
综上所述,本题答案为B。
2.固液分离操作中,需要用到的仪器是( )
A. B. C. D.
第1页 | 共30页【答案】C
【解析】
【详解】A.该仪器是干燥管,不能用于固液分离,A不符合题意;
B.该仪器为蒸馏烧瓶,不能用于固液分离,B不符合题意;
C.该仪器为普通漏斗,常用于过滤以分离固液混合物,C符合题意;
D.该仪器为牛角管,又叫接液管,连接在冷凝管的末端以收集蒸馏产生的蒸气所冷凝成的
液体,不能用于固液分离,D不符合题意。
综上所述,本题答案为C。
3.下列物质在熔融状态下不导电的是( )
A. NaOH B. CaCl C. HCl D. K SO
2 2 4
【答案】C
【解析】
【详解】A.NaOH属于离子化合物,其在熔融状态下能电离成自由移动的Na+和OH-,故
其在熔融状态下能导电,A不符合题意;
B.CaCl 属于离子化合物,其在熔融状态下能电离成自由移动的Ca2+和Cl-,故其在熔融状
2
态下能导电,B不符合题意;
C.HCl是共价化合物,其在熔融状态下不能电离成离子,故其在熔融状态下不导电,C符
合题意;
D.K SO 属于离子化合物,其在熔融状态下能电离成自由移动的K+和SO2-,故其在熔融
2 4 4
状态下能导电,D不符合题意。
综上所述,本题答案为C。
4.下列物质对应的组成不正确的是( )
A. 干冰:CO B. 熟石灰:CaSO ×2H O
2 4 2
C. 胆矾:CuSO ×5H O D. 小苏打:NaHCO
4 2 3
【答案】B
【解析】
【详解】A.干冰为固体二氧化碳,故A正确;
B.熟石灰成分为Ca(OH) ,CaSO ·2H O为生石膏,故B错误;
2 4 2
第2页 | 共30页C.胆矾为五水合硫酸铜晶体,故C正确;
D.小苏打是碳酸氢钠的俗名,故D正确;
答案选B。
5.下列表示不正确的是( )
A. 乙烯的结构式: B. 甲酸甲酯的结构简式:C H O
2 4 2
C. 2-甲基丁烷的键线式: D. 甲基的电子式:
【答案】B
【解析】
【详解】A.结构式是每一对共用电子对用一个短横来表示,乙烯分子中每个碳原子和每个
氢原子形成一对共用电子对,碳原子和碳原子形成两对共用电子对,故A正确;
B.结构简式中需要体现出特殊结构和官能团,甲酸甲酯中要体现出酯基,其结构简式为
HCOOCH ,故B错误;
3
C.键线式中每个端点为一个C原子,省略C—H键,故C正确;
D.甲基中碳原子和三个氢原子形成3对共用电子对,还剩一个成单电子,故D正确;
答案选B。
6.下列说法不正确的是( )
A. 天然气是不可再生能源
B. 用水煤气可合成液态碳氢化合物和含氧有机物
C. 煤的液化属于物理变化
D. 火棉是含氮量高的硝化纤维
【答案】C
【解析】
【详解】A.天然气是由远古时代的动植物遗体经过漫长的时间变化而形成的,储量有限,
是不可再生能源,A选项正确;
B.水煤气为CO和H ,在催化剂的作用下,可以合成液态碳氢化合物和含氧有机物(如甲
2
醇),B选项正确;
C.煤的液化是把煤转化为液体燃料,属于化学变化,C选项错误;
D.火棉是名为纤维素硝酸酯,是一种含氮量较高的硝化纤维,D选项正确;
第3页 | 共30页答案选C。
7.下列说法正确的是( )
A. 35Cl和37Cl是两种不同的元素 B. 单晶硅和石英互为同素异形体
C. HCOOH和HOCH CHO互为同系物 D. H与Na在元素周期表中处于同一
2
主族
【答案】D
【解析】
【详解】A.35Cl和37Cl是Cl元素的两种不同核素,属于同种元素,A选项错误;
B.同素异形体是指同种元素组成的不同种单质,而单晶硅为硅单质,而石英是SiO ,两者
2
不属于同素异形体,B选项错误;
C.同系物是指结构相似,分子组成上相差若干个CH 的有机化合物,HCOOH和HOCH CHO
2 2
结构不相似,不属于同系物,C选项错误;
D.H和Na在元素周期表种均处于第IA族,D选项正确;
答案选D。
8.下列说法不正确的是( )
A. Cl-会破坏铝表面的氧化膜
B. NaHCO 的热稳定性比Na CO 强
3 2 3
C. KMnO 具有氧化性,其稀溶液可用于消毒
4
D. 钢铁在潮湿空气中生锈主要是发生了电化学腐蚀
【答案】B
【解析】
【详解】A.Cl-很容易被吸附在铝表面的氧化膜上,将氧化膜中的氧离子取代出来,从而破
坏氧化膜,A选项正确;
B.碳酸氢钠受热分解可产生碳酸钠、水和二氧化碳,则稳定性:NaHCO <Na CO ,B选
3 2 3
项错误;
C.KMnO 具有强氧化性,可使病毒表面的蛋白质外壳变形,其稀溶液可用于消毒,C选项
4
正确;
D.钢铁在潮湿的空气中,铁和碳、水膜形成原电池,发生电化学腐蚀,腐蚀速率更快,D
第4页 | 共30页选项正确;
答案选B。
9.下列说法不正确的是( )
A. 高压钠灯可用于道路照明
B. SiO 可用来制造光导纤维
2
C. 工业上可采用高温冶炼黄铜矿的方法获得粗铜
D. BaCO 不溶于水,可用作医疗上检查肠胃的钡餐
3
【答案】D
【解析】
【详解】A.高压钠灯发出的黄光射程远、透雾能力强,所以高压钠灯用于道路照明,故A
正确;
B.二氧化硅传导光的能力非常强,用来制造光导纤维,故B正确;
C.黄铜矿高温煅烧生成粗铜、氧化亚铁和二氧化硫,故C正确;
D.碳酸钡不溶于水,但溶于酸,碳酸钡在胃酸中溶解生成的钡离子为重金属离子,有毒,
不能用于钡餐,钡餐用硫酸钡,故D错误;
答案选D。
加热
10.反应MnO +4HCl(浓) MnCl +Cl↑+2H O中,氧化产物与还原产物的物质的
2 2 2 2
量之比是( )
A. 1:2 B. 1:1 C. 2:1 D. 4:1
【答案】B
【解析】
【详解】由反应方程式可知,反应物MnO 中的Mn元素的化合价为+4价,生成物MnCl
2 2
中Mn元素的化合价为+2价,反应物HCl中Cl元素的化合价为-1价,生成物Cl 中Cl元素
2
的化合价为0价,故MnCl 是还原产物,Cl 是氧化产物,由氧化还原反应中得失电子守恒
2 2
可知,n(Cl ):n(MnCl )=1:1,B符合题意;
2 2
答案选B。
11.下列有关实验说法不正确的是( )
A. 萃取Br 时,向盛有溴水的分液漏斗中加入CCl ,振荡、静置分层后,打开旋塞,先将
2 4
第5页 | 共30页水层放出
B. 做焰色反应前,铂丝用稀盐酸清洗并灼烧至火焰呈无色
C. 乙醇、苯等有机溶剂易被引燃,使用时须远离明火,用毕立即塞紧瓶塞
D. 可用AgNO 溶液和稀HNO 区分NaCl、NaNO 和NaNO
3 3 2 3
【答案】A
【解析】
【详解】A.CCl 的密度比水的密度大,故萃取 Br 时,向盛有溴水的分液漏斗中加入
4 2
CCl ,振荡、静置分层,打开旋塞,先将CCl 层放出,A操作错误;
4 4
B.做焰色反应前,先将铂丝用稀盐酸清洗并灼烧至无色的目的是排除铂丝上粘有其它金属
元素,对待检测金属元素的干扰,B操作正确
C.乙醇、苯等有机溶剂属于易燃物品,故使用时必须远离明火和热源,用毕立即塞紧瓶塞,
防止失火,C操作正确;
D.氯化银、亚硝酸银都是难溶于水的白色固体,所以硝酸银滴入氯化钠溶液和亚硝酸钠溶
液中都有白色沉淀生成,但是氯化银不溶于稀硝酸,而亚硝酸银溶于稀硝酸;硝酸银溶液滴
入硝酸钠溶液中没有明显现象,故D操作正确。
答案选A。
12.下列说法正确的是( )
A. Na O在空气中加热可得固体Na O
2 2 2
B. Mg加入到过量FeCl 溶液中可得Fe
3
C. FeS 在沸腾炉中与O 反应主要生成SO
2 2 3
D. H O 溶液中加入少量MnO 粉末生成H 和O
2 2 2 2 2
【答案】A
【解析】
【详解】A.无水状态下 Na O 比 Na O 更稳定,Na O 在空气中加热可以生成更稳定的
2 2 2 2
Na O ,A正确;
2 2
B.Mg加入到FeCl 溶液中,Mg具有较强的还原性,先与Fe3+反应,生成Mg2+和Fe2+,
3
若Mg过量,Mg与Fe2+继续反应生成Mg2+和Fe,但由于反应中FeCl 过量,Mg已消耗完,
3
所以无Mg和Fe2+反应,所以不会生成Fe,B错误;
第6页 | 共30页高温
C.FeS 在沸腾炉中与O 发生的反应为:4 FeS +11O 2Fe O +8SO ,产物主要是SO
2 2 2 2 2 3 2 2
而不是SO ,C错误;
3
D.H O 溶液中加入少量MnO 粉末生成H O和O ,化学方程式为:
2 2 2 2 2
MnO
2
2H O 2H O+O ↑,D错误。
2 2 2 2
答案选A。
13.能正确表示下列反应的离子方程式是( )
A. NH FeSO 溶液与少量Ba(OH) 溶液反应:SO2- +Ba2+ =BaSO ¯
4 2 4 2 2 4 4
通电
B. 电解MgCl 水溶液:2Cl- +2H O 2OH- +Cl +H
2 2 2 2
C. 乙酸乙酯与NaOH溶液共热:
CH COOCH CH +OH- ¾Δ¾®CH COO- +CH CH OH
3 2 3 3 3 2
D. CuSO 溶液中滴加稀氨水:Cu2+ +2OH- =Cu(OH) ¯
4 2
【答案】C
【解析】
【详解】A.(NH ) Fe(SO ) 可以写成(NH ) SO ‧FeSO ,(NH ) Fe(SO ) 溶液与少量
4 2 4 2 4 2 4 4 4 2 4 2
Ba(OH) 溶液反应, OH-先与Fe2+反应,再和NH+反应,由于Ba(OH) 较少,NH+不会参
2 4 2 4
与反应,离子方程式为:Fe2++SO2-+ Ba2++ 2OH-=Fe(OH) ↓+BaSO ↓,A错误;
4 2 4
B.用惰性材料为电极电解MgCl 溶液,阳极反应为:2Cl--2e-=Cl ↑,阴极反应为:
2 2
2H O+2e-+Mg2+=Mg(OH) ↓+H ↑,总反应的离子方程式为:Mg2++2Cl-+2H O=
2 2 2 2
Mg(OH) ↓+H ↑+ Cl ↑,B错误;
2 2 2
C.乙酸乙酯与氢氧化钠溶液共热时发生水解,生成乙酸钠和乙醇,离子方程式为:
CH COOCH CH +OH- CH COO-+CH CH OH,C正确;
3 2 3 3 3 2
D.向硫酸铜溶液中滴加氨水,氨水与硫酸铜发生复分解反应生成氢氧化铜沉淀和硫酸铵,
一水合氨为弱电解质,在离子反应中不能拆开,离子方程式为:
Cu2++2NH •H O=2NH++Cu(OH) ↓,D错误。
3 2 4 2
答案选C。
第7页 | 共30页14.下列说法不正确的是( )
A. 相同条件下等质量的甲烷、汽油、氢气完全燃烧,放出的热量依次增加
B. 油脂在碱性条件下水解生成的高级脂肪酸盐是肥皂的主要成分
C. 根据纤维在火焰上燃烧产生的气味,可以鉴别蚕丝与棉花
D. 淀粉、纤维素、蛋白质都属于高分子化合物
【答案】A
【解析】
【详解】A.由于等质量的物质燃烧放出的热量主要取决于其含氢量的大小,而甲烷、汽油、
氢气中H的百分含量大小顺序为:汽油<甲烷<氢气,故等质量的它们放出热量的多少顺序
为:汽油<甲烷<氢气,故A错误;
B.油脂在碱性条件下发生水解反应生成甘油和高级脂肪酸盐,高级脂肪酸盐是肥皂的主要
成分,故B正确;
C.蚕丝主要成分是蛋白质,灼烧时有烧焦羽毛的气味,而棉花则属于纤维素,灼烧时则基
本没有气味,故C正确;
D.高分子通常是指相对分子质量在几千甚至上万的分子,淀粉、纤维素和蛋白质均属于天
然高分子化合物,故D正确。
故答案为:D。
15.有关 的说法正确的是( )
A. 可以与氢气发生加成反应 B. 不会使溴水褪色
C. 只含二种官能团 D. 1mol该物质与足量NaOH溶液反
应,最多可消耗1mol NaOH
【答案】A
【解析】
【分析】
中含有羟基、酯基和碳碳双键三种官能团,根据官能团的性质进行解答。
【详解】A. 分子中含有苯环和碳碳双键,都能与H 发生加成反应, A正确;
2
第8页 | 共30页B. 分子中含有碳碳双键,能与溴水发生加成反应导致溴水褪色, B错误;
C. 分子中含有羟基、酯基和碳碳双键三种官能团, C错误;
D.1mol该物质酯基水解后生成的酚羟基和羧基均能和NaOH反应,1mol该物质与足量的
NaOH溶液反应时最多可消耗2molNaOH,D错误;
故答案为:A。
16.X、Y、Z、M、Q五种短周期元素,原子序数依次增大。Y元素的最高正价为+4价,Y
元素与Z、M元素相邻,且与M元素同主族;化合物Z X 的电子总数为18个;Q元素的
2 4
原子最外层电子数比次外层少一个电子。下列说法不正确的是( )
A. 原子半径:Z< Y< M
B. 最高价氧化物对应水化物的酸性:Z> Y > M
C. X Z-ZX 易溶于水,其水溶液呈碱性
2 2
D. X、Z和Q三种元素形成的化合物一定是共价化合物
【答案】D
【解析】
【分析】
X、Y、Z、M、Q为五种短周期元素,原子序数依次增大。Y元素的最高正价为+4价,则
证明该元素为第IVA族元素,又知Y元素与Z、M元素相邻,且与M同族,则在元素周期
表位置应为
IVA族 VA族
Y Z
M
,故推知Y为C元素,Z为N元素,M为Si元素;化合物Z X 的电子总数为18,则推知,
2 4
X为H,该化合物为N H ;Q元素的原子最外层电子总数比次外层电子数少一个电子,推
2 4
出Q为Cl元素,据此结合元素周期律与物质的结构与性质分析作答。
【详解】根据上述分析可知,X为H、Y为C元素、Z为N元素、M为Si元素、Q为Cl
元素,则
第9页 | 共30页A. 同周期元素从左到右原子半径依次减小,同主族元素从上到下原子半径依次增大,则原
子半径比较:Z(N)0 D.
1 2 1 2 3 4
ΔH >ΔH
3 4
【答案】B
【解析】
【详解】碳酸氢根的电离属于吸热过程,则CO2-(aq)+H+(aq)=HCO-(aq)为放热反应,所以
3 3
△H <0;
1
CO
3
2-(aq)+H
2
O(l)HCO
3
-(aq)+OHˉ(aq)为碳酸根的水解离子方程式,CO
3
2-的水解反应为吸
热反应,所以△H >0;
2
OHˉ(aq)+H+(aq)=H O(l)表示强酸和强碱的中和反应,为放热反应,所以△H <0;
2 3
醋酸与强碱的中和反应为放热反应,所以△H <0;
4
但由于醋酸是弱酸,电离过程中会吸收部分热量,所以醋酸与强碱反应过程放出的热量小于
强酸和强碱反应放出的热量,则△H >△H ;
4 3
综上所述,只有△H <△H 正确,故答案为B。
1 2
23.常温下,用0.1mol×L-1氨水滴定10mL浓度均为0.1mol×L-1的HCl和CH COOH的混
3
合液,下列说法不正确的是( )
A. 在氨水滴定前,HCl和CH COOH的混合液中c
Cl-
>c
CH
COO-
3 3
B. 当滴入氨水10mL时,c NH+ +cNH ×H O=c CH COO- +cCH COOH
4 3 2 3 3
C. 当滴入氨水20mL时,cCH COOH+c H+ =cNH ×H O+c OH-
3 3 2
D. 当溶液呈中性时,氨水滴入量大于20mL,c
NH+