文档内容
高一化学
注意事项:
1.答卷前,考生务必将自己的姓名、考生号等填写在答题卡指定位置。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。
如需改动,用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡
上。写在本试卷上无效。
3.考试结束后,将答题卡交回。
可能用到的相对原子质量:N14 O16 Na23 Al27 Fe56 Co59 Ni59 Cu64
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.中国传统文化博大精深,蕴含着丰富的化学知识。下列说法正确的是
A.“零落成泥碾作尘,只有香如故”中的“香”体现了分子是由原子构成的
B.“白毛浮绿水,红掌拨清波”中“白毛”的主要成分是蛋白质
C.“故人西辞黄鹤楼,烟花三月下扬州”中的“烟花”与核外电子的跃迁有关
D.“雷声千嶂落,雨色万峰来”,雷雨时少量O 转化成O ,O 和O 互为同分异构体
2 3 2 3
2.下列化学用语错误的是
A.NH 的VSEPR模型为三角锥形
3
B.CO 分子的空间结构模型:
2
C.HCl分子中σ键的形成:
D.Na
2
O
2
的电子式:Na+[:
‥
‥
O:
‥
‥
O:]2-
Na+
3.现有a、b、c、d四种烃,其球棍模型如下。下列有关说法错误的是
a b c d
A.工业上合成一氯乙烷,通常选b为原料
B.d的名称为异戊烷
C.c和d互为同系物
D.a的二氯代物有2种
4.下列说法错误的是
A.各电子层含有的原子轨道数为n2
B.硫元素中,3p 、3p 、3p 轨道相互垂直,且能量相等
x y z
C.4s电子能量较高,总是在比3s电子离核更远的地方运动
D.镁原子由1s22s22p63s13p1→1s22s22p63s2时,原子释放能量,由激发态转化成基态
高一化学试题 第 1 页 共 8 页
{#{QQABZQaAogggAIAAARhCEQUaCAOQkBAAAagOwBAIoAAAwQFABCA=}#}5.下列关于晶体的说法错误的是
A.可用X射线衍射鉴别晶体与非晶体
B.分子晶体中分子间作用力越大,分子越稳定
C.金刚石、食盐、冰的熔点依次降低
D.SiO 晶体中每个硅原子与4个氧原子以共价键相结合
2
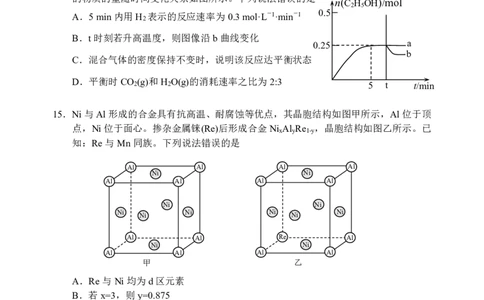
6.某同学为了探究原电池工作原理,设计了如图装置进行实验(反应后的溶液不饱和),
下列说法错误的是
A
A.铁极质量减轻 铁 石墨
B.电流表指针发生偏转时,石墨极上有气体生成
C.铁极电极反应式:Fe-2e-=Fe2+
稀硫酸
D.若转移0.2mole-,则溶液增重5.6g
7.下列说法正确的是
A.基态 Br的核外电子排布式为[Ar]4s24p5
35
B.基态原子最外层电子排布为4s1的元素一定是s区元素
C.基态原子核外电子排布,先排满K层再排L层、先排满M层再排N层
D.3p能级上只有一个空轨道的基态原子和3p能级上只有一个未成对电子的基态原
子,其对应元素一定属于同一周期
8.合理应用和处理含硫的化合物,在生产生活中有重要意义。利用甲烷可以除去SO ,反
3
应方程式为8SO 3 (g)+6CH 4 (g) S 8 (g)+6CO 2 (g)+12H 2 O(g) ,S 8 不溶于水,易溶于
CS ,其结构如图。下列说法正确的是
2
A.S 中S原子与S-S键的个数比为2:1
8
B.键角:CO >CH >H O
2 4 2
C.方程式中各化合物的中心原子均采取sp3杂化
D.方程式中各物质属于非极性分子的有3种
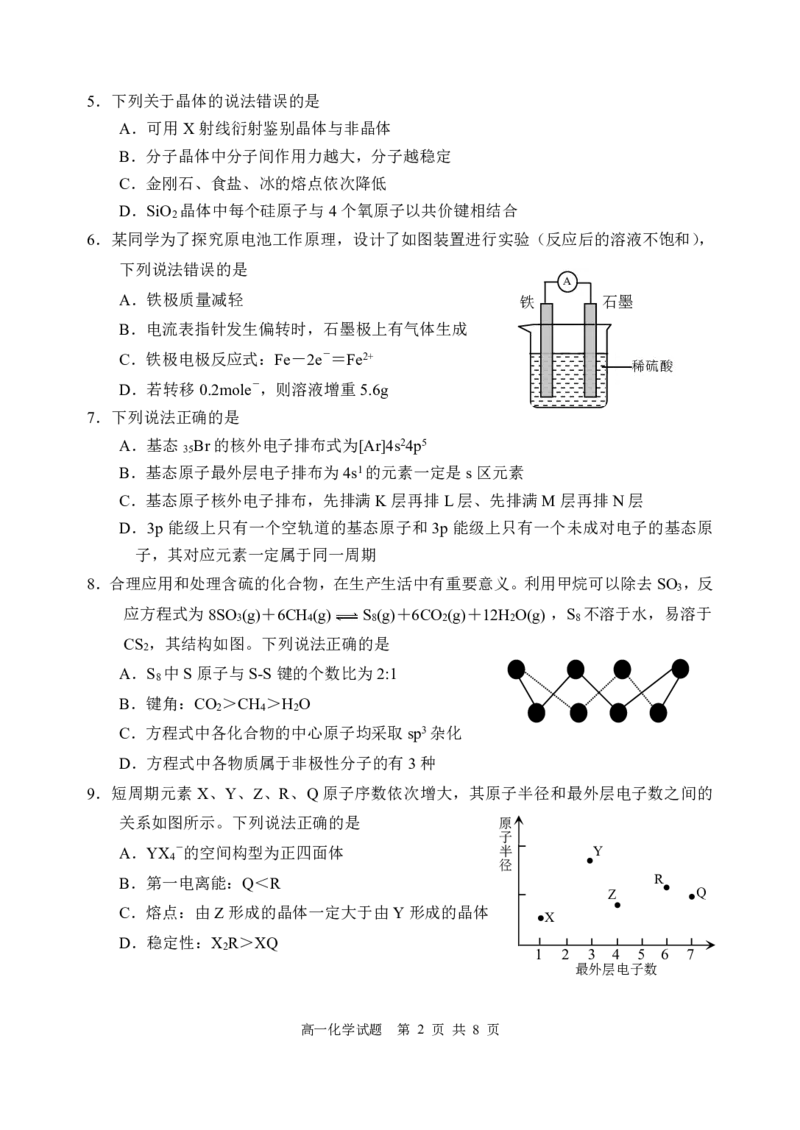
9.短周期元素X、Y、Z、R、Q原子序数依次增大,其原子半径和最外层电子数之间的
关系如图所示。下列说法正确的是 原
子
A.YX -的空间构型为正四面体 半 Y
4 径
B.第一电离能:Q<R R
Z Q
C.熔点:由Z形成的晶体一定大于由Y形成的晶体
X
D.稳定性:X R>XQ
2
1 2 3 4 5 6 7
最外层电子数
高一化学试题 第 2 页 共 8 页
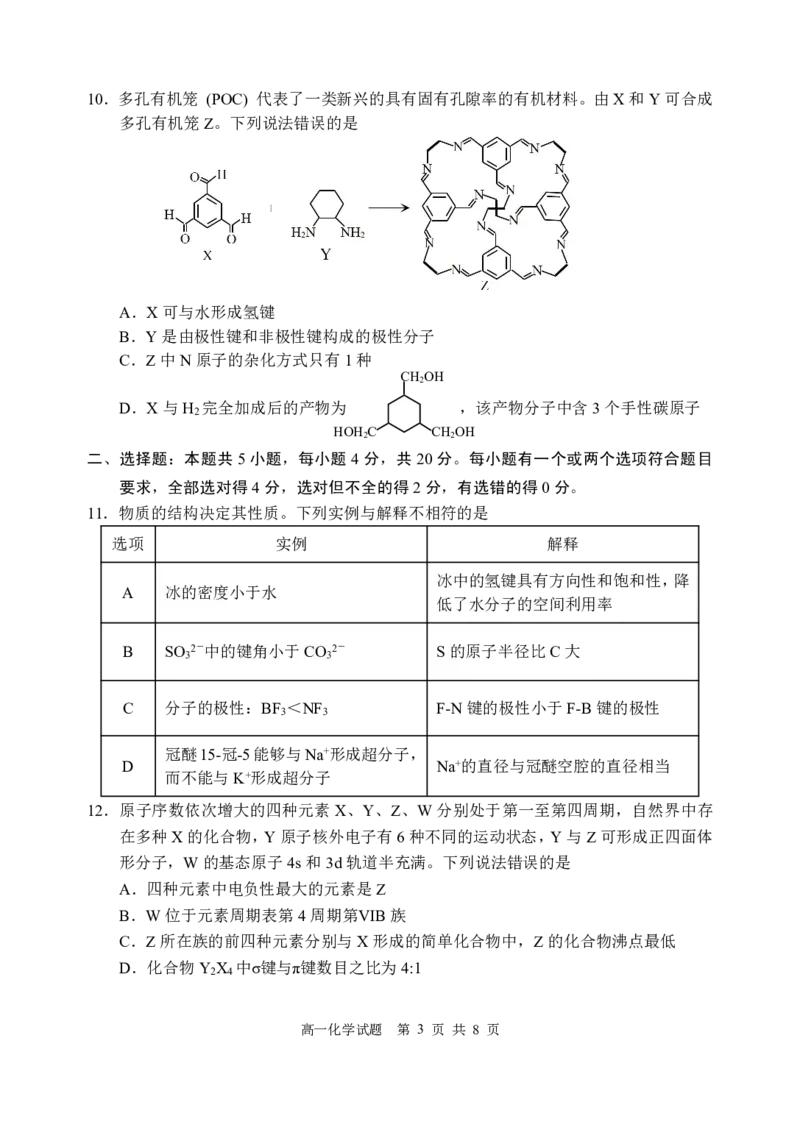
{#{QQABZQaAogggAIAAARhCEQUaCAOQkBAAAagOwBAIoAAAwQFABCA=}#}10.多孔有机笼 (POC) 代表了一类新兴的具有固有孔隙率的有机材料。由X和Y可合成
多孔有机笼Z。下列说法错误的是
N
A.X可与水形成氢键
B.Y是由极性键和非极性键构成的极性分子
C.Z中N原子的杂化方式只有1种
CH2OH
D.X与H 完全加成后的产物为 ,该产物分子中含3个手性碳原子
2
HOH2C CH2OH
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目
要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.物质的结构决定其性质。下列实例与解释不相符的是
选项 实例 解释
冰中的氢键具有方向性和饱和性,降
A 冰的密度小于水
低了水分子的空间利用率
B SO 2-中的键角小于CO 2- S的原子半径比C大
3 3
C 分子的极性:BF <NF F-N键的极性小于F-B键的极性
3 3
冠醚15-冠-5能够与Na+形成超分子,
D Na+的直径与冠醚空腔的直径相当
而不能与K+形成超分子
12.原子序数依次增大的四种元素X、Y、Z、W分别处于第一至第四周期,自然界中存
在多种X的化合物,Y原子核外电子有6种不同的运动状态,Y与Z可形成正四面体
形分子,W的基态原子4s和3d轨道半充满。下列说法错误的是
A.四种元素中电负性最大的元素是Z
B.W位于元素周期表第4周期第ⅥB族
C.Z所在族的前四种元素分别与X形成的简单化合物中,Z的化合物沸点最低
D.化合物Y X 中σ键与π键数目之比为4:1
2 4
高一化学试题 第 3 页 共 8 页
{#{QQABZQaAogggAIAAARhCEQUaCAOQkBAAAagOwBAIoAAAwQFABCA=}#}13.某汽车安全气囊中主要含有气体发生剂叠氮化钠(NaN )、主氧化剂Fe O 、助氧化剂
3 2 3
KClO 、冷却剂NaHCO 等物质。当汽车发生碰撞时,NaN 分解放出热量并产生大量
4 3 3
气体,使气囊迅速膨胀,从而起到保护作用。下列说法错误的是
A.NaN 中N -的空间构型为角形
3 3
B.FeO 将碰撞分解反应生成的Na氧化,该反应为置换反应
2 3
C.KClO 属于离子化合物,含有离子键和共价键
4
D.NaHCO 作冷却剂的原因是因为NaHCO 分解是吸热反应
3 3
14.利用CO 和H 合成乙醇的反应为2CO (g)+6H (g) C H OH(g)+3H O(g)(已知该反
2 2 2 2 2 5 2
应为放热反应)。向2L体积固定的容器中充入1molCO 和3molH ,测得C H OH
2 2 2 5
的物质的量随时间变化关系如图所示。下列说法错误的是
n(C H OH)/mol
2 5
A.5min内用H 表示的反应速率为0.3mol·L-1·min-1 0.5
2
B.t时刻若升高温度,则图像沿b曲线变化
0.25 a
b
C.混合气体的密度保持不变时,说明该反应达平衡状态
D.平衡时CO (g)和H O(g)的消耗速率之比为2:3
2 2 5 t t/min
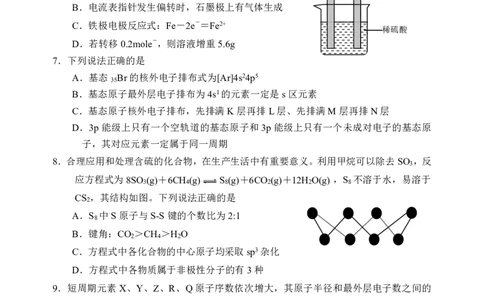
15.Ni与Al形成的合金具有抗高温、耐腐蚀等优点,其晶胞结构如图甲所示,Al位于顶
点,Ni位于面心。掺杂金属铼(Re)后形成合金Ni Al Re ,晶胞结构如图乙所示。已
x y 1-y
知:Re与Mn同族。下列说法错误的是
Al Al Al Al
Ni Ni
Al Al Al Al
Ni Ni
Ni Ni Ni Ni
Ni Ni
Al Al Re Al
Ni Ni
Al Al Al Al
甲 乙
A.Re与Ni均为d区元素
B.若x=3,则y=0.875
C.镍铝合金中,Ni和Al的配位数均为4
D.图甲的晶胞参数为apm,阿伏加德罗常数为N ,则晶体密度为
A
30
2.04×10 −3
3
A g·cm
高一化学试题 第 4 页 共 8 页
{#{QQABZQaAogggAIAAARhCEQUaCAOQkBAAAagOwBAIoAAAwQFABCA=}#}三、非选择题:本题共5小题,共60分。
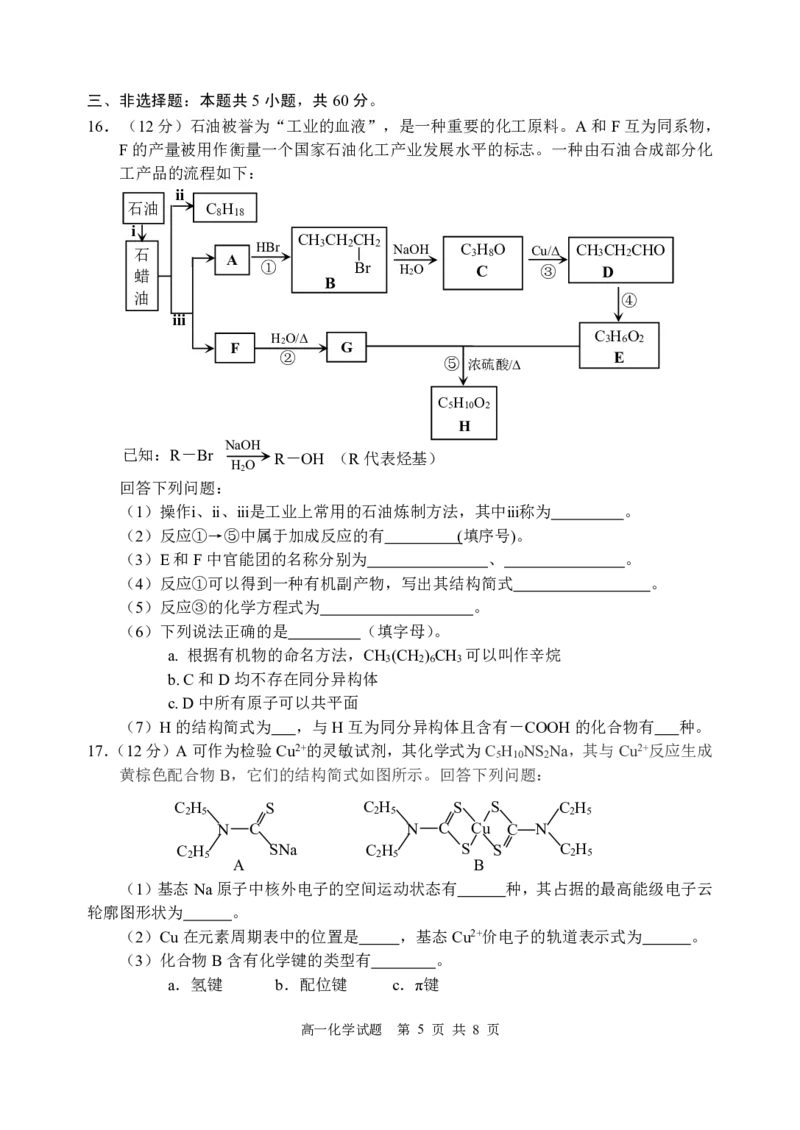
16
.(12分)石油被誉为“工业的血液”,是一种重要的化工原料。A和F互为同系物,
F的产量被用作衡量一个国家石油化工产业发展水平的标志。一种由石油合成部分化
工产品的流程如下:
ⅱ
石油 C H
8 18
ⅰ
CH CH CH
石 HBr 3 2 2 NaOH C 3 H 8 O Cu/∆ CH 3 CH 2 CHO
蜡 A ① Br H2O C ③ D
B
油 ④
ⅲ
F
H2O/∆
G
C 3 H 6 O 2
② ⑤ 浓硫酸/∆ E
C H O
5 10 2
H
NaOH
已知:R-Br R-OH (R代表烃基)
H2O
回答下列问题:
(1)操作ⅰ、ⅱ、ⅲ是工业上常用的石油炼制方法,其中ⅲ称为 。
(2)反应①→⑤中属于加成反应的有 (填序号)。
(3)E和F中官能团的名称分别为 、 。
(4)反应①可以得到一种有机副产物,写出其结构简式 。
(5)反应③的化学方程式为 。
(6)下列说法正确的是 (填字母)。
a. 根据有机物的命名方法,CH (CH ) CH 可以叫作辛烷
3 2 6 3
b.C和D均不存在同分异构体
c.D中所有原子可以共平面
(7)H的结构简式为 ,与H互为同分异构体且含有-COOH的化合物有 种。
17.(12分)A可作为检验Cu2+的灵敏试剂,其化学式为C H NS Na,其与Cu2+反应生成
5 10 2
黄棕色配合物B,它们的结构简式如图所示。回答下列问题:
C 2 H 5 S C 2 H 5 S S C 2 H 5
N C N C Cu C N
C 2 H 5 SNa C 2 H 5 S S C 2 H 5
A B
(1)基态Na原子中核外电子的空间运动状态有 种,其占据的最高能级电子云
轮廓图形状为 。
(2)Cu在元素周期表中的位置是 ,基态Cu2+价电子的轨道表示式为 。
(3)化合物B含有化学键的类型有 。
a.氢键 b.配位键 c.π键
高一化学试题 第 5 页 共 8 页
{#{QQABZQaAogggAIAAARhCEQUaCAOQkBAAAagOwBAIoAAAwQFABCA=}#}(4)下列曲线表示S所在主族元素性质随原子序数的变化趋势,其中正确的是 (填
序号)。
第 非 最 电
一 金 高 负
电 • O 属 正 性 • O
离 能 • S Se 性 •S • Se 价 • O • S S • e •S Se
• • •
O
0 0 0 0
原子序数 原子序数 原子序数 原子序数
a b c d
NH
C
(5)胍(H2N NH2 )是平面形分子,其组成元素的电负性由大到小的顺序为
(用元素符号表示)。胍中三个N原子的杂化方式 (填“相同”或“不同”)。
胍分子内存在类似苯的大π键,苯分子内的大π键可表示为 ,则胍中的大π键可表示
为 。胍易吸收空气中的水蒸气,其原因是 6 。
Π6
18.(12分)Co3+可形成[Co(NH ) ]Cl 、[Co(NH ) ]Cl 等多种配合物。回答下列问题:
3 6 3 3 5 3
(1)探究[Co(NH ) ]Cl 的结构
3 5 3
①取0.001mol[Co(NH ) ]Cl 溶于水,与0.1mol·L-1AgNO 溶液完全反应,消耗20mL
3 5 3 3
AgNO 溶液,则[Co(NH ) ]Cl 中Co3+的配位数为 。
3 3 5 3
②将[Co(NH ) ]Cl 与适量的NaNO 溶液在一定条件下混合可发生反应生成
3 5 3 2
[Co(NH ) NO ]Cl ,则[Co(NH ) NO ]Cl 中形成配位键时可能提供孤电子对的原子是
3 5 2 2 3 5 2 2
(填序号)。
A.N B.N、O C.N、Cl D.N、O、Cl
(2)制备[Co(NH ) ]Cl 晶体
3 6 3
[Co(NH ) ]Cl 在冷水中微溶,可溶于热水,其制备的工艺流程如图所示(已知:活性炭
3 6 3
作催化剂)。
CoCl2 ·6H2O
浓氨水双氧水活性炭 沸水
NH4Cl溶液 反应 操作X 溶解 操作Y 系列操作 [Co(NH3)6]Cl3 晶体
溶液a 固体b
①“固体b”主要成分为 。“操作Y”的名称为 。“系列操作”的名称为
蒸发浓缩, ,过滤、 。
②“反应”前需将溶液温度控制到10℃以下,原因是 。可选用_______
降低溶液温度。
③若“反应”中有0.34gH O 参加反应,则理论上参加反应的CoCl ·6H O的质量为
2 2 2 2
g[已知:Mr(CoCl ·6H O)=238]。
2 2
高一化学试题 第 6 页 共 8 页
{#{QQABZQaAogggAIAAARhCEQUaCAOQkBAAAagOwBAIoAAAwQFABCA=}#}19.(12分)元素周期表中的8种元素a、b、c、d、e、f、g、h,原子序数依次增大。
元素 有关描述
a 基态原子价电子排布为nsnnpn
b 最高价氧化物对应的水化物与其最简单氢化物反应可生成一种盐
c 电负性最强的元素
d 基态原子的最外层p轨道有两个电子的自旋方向与其他电子的自旋方向相反
e 人体中含量最多的金属元素
f 基态原子3d轨道上有4个未成对电子
g g2+的d轨道中有10个电子
h 单质在金属活动性顺序表中排在最末位
回答下列问题:
(1)同周期主族元素中第一电离能比b小的元素有 种。基态g2+的价电子排布
式为 。
(2)b与c可形成化合物b c ,分子中各原子均满足8电子稳定结构。b c 的结构式
2 2 2 2
为 (用元素符号表示,下同)。
(3)d与e形成的化合物的电子式为 。
(4)c 和d可分别与氧形成氧化物Oc 和d O,则Oc 的熔、沸点 (填“高于”
2 2 2
或“低于”)d O,原因是 。
2
(5)已知:两成键元素间电负性差值大于1.7时,形成离子键,小于1.7时,形成共
价键。f、d两元素可形成化合物fd ,f、d的电负性分别为1.8和3.0,则推断fd 是 化
3 3
合物(填“共价”或“离子”),设计一个简单的实验方案证明该推断 。
(6)g2+、h+分别与ab-形成配离子[g(ab) ]2-、[h(ab) ]-。工业上常用g的单质与
4 2
[h(ab) ]-反应生成[g(ab) ]2-和h的单质,该反应的离子方程式为 。
2 4
高一化学试题 第 7 页 共 8 页
{#{QQABZQaAogggAIAAARhCEQUaCAOQkBAAAagOwBAIoAAAwQFABCA=}#}20.(12分)氮与其他元素可形成多种物质,回答下列问题:
H H
(1)N与H、B可形成氨硼烷(结构式为 H—N→B—H ),是一种新型储氢材料。
H H
H—N—H键角:NH BH NH (填“>”“<”或“=”),原因是 。
3 3 3
(2)氮与锂形成的一种晶体,是由Li N平面层(如图1所示)和非密置层的Li交替排
x
列形成,Li N平面层的Li排列如石墨层中的C,N处于六元环的中心。则x= 。
x
N
B
图1 图2
(3)立方氮化硼属于原子晶体,其晶胞结构如图2所示。
①硼原子处于氮原子围成的 (填空间结构)空隙中。
②立方氮化硼晶胞沿体对角线的投影图为 (填序号,图中 表示N原子的
投影位置, 表示B原子的投影位置)
1
1 1
1 1 1 1 1 1
1
1 1 1 1
1
a b c d
(4)氮化钴属于立方晶系,经Li掺杂得催化剂X,经Cu掺杂得催化剂Y。
B
N
z Li
Li掺杂 Cu掺杂
y Co
120°
x Cu
X A 氮化钴 Y
①X属于六方晶系,A点原子的分数坐标为(0,0,0),B点原子位于与其相邻的三个
Co原子位置的中心,则B点原子的分数坐标为 。
②Y属于立方晶系,晶胞参数为anm。Y的化学式为 。Co原子形成的空间构
型为正八面体,则距离最近的2个Co原子核间距为 nm。Y晶体密度为ρ ,
则阿伏加德罗常数N 可表示为 (用含a、ρ的式子表示)。 −3
A g·cm
高一化学试题 第 8 页 共 8 页
{#{QQABZQaAogggAIAAARhCEQUaCAOQkBAAAagOwBAIoAAAwQFABCA=}#}