文档内容
2019年上海市黄浦区中考化学一模试卷
六、选择题(共20分)
1.(3分)属于稀有气体的是( )
A.H B.He C.O D.N
2 2 2
2.(3分)放入水中形成乳浊液的是( )
A.淀粉 B.蔗糖 C.食盐 D.植物油
3.(3分)自来水厂将水进行净化的过程中,属于化学变化的是( )
A.挥发 B.沉降 C.过滤 D.消毒
4.(3分)属于活性炭物理性质的是( )
A.稳定性 B.吸附性 C.还原性 D.可燃性
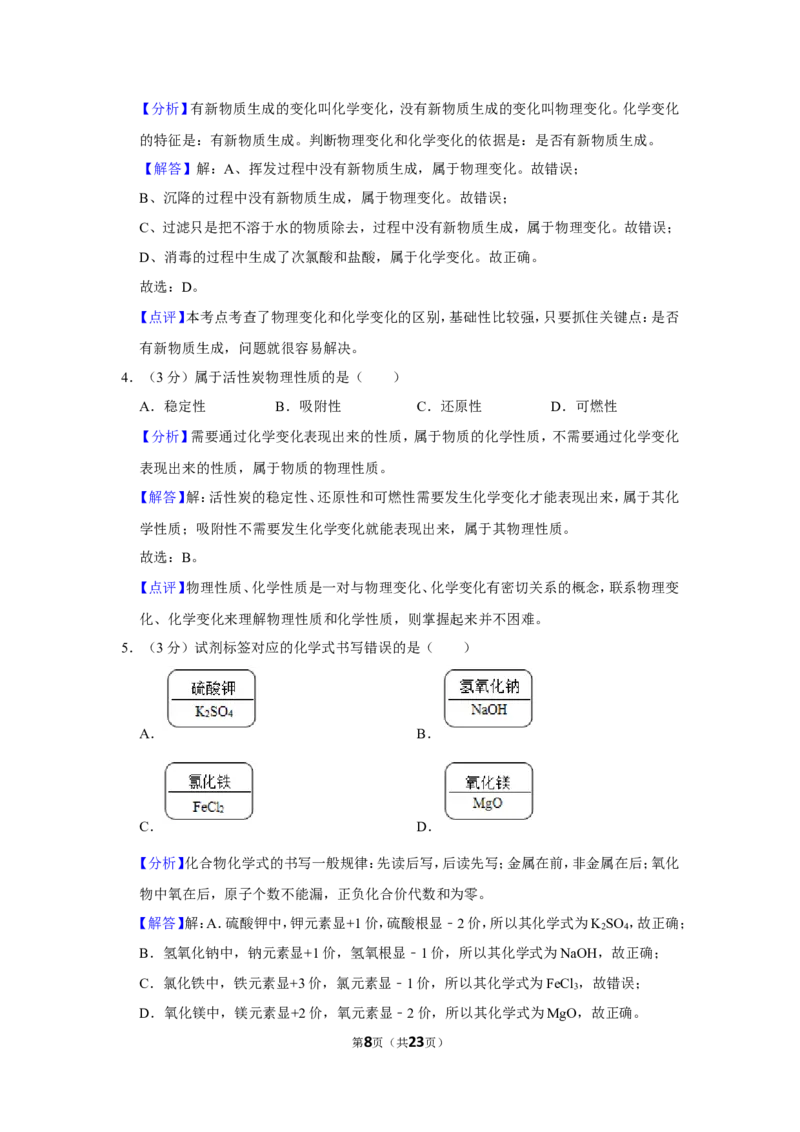
5.(3分)试剂标签对应的化学式书写错误的是( )
A. B.
C. D.
6.(3分)物质在氧气中燃烧的主要现象描述正确的是( )
A.木炭:产生红色火焰 B.红磷:产生大量白烟
C.镁条:生成黑色固体 D.硫粉:生成二氧化硫
7.(3分)物质对应的类别正确的是( )
A.胆矾:化合物 B.木炭:单质
C.冰:混合物 D.天然气:纯净物
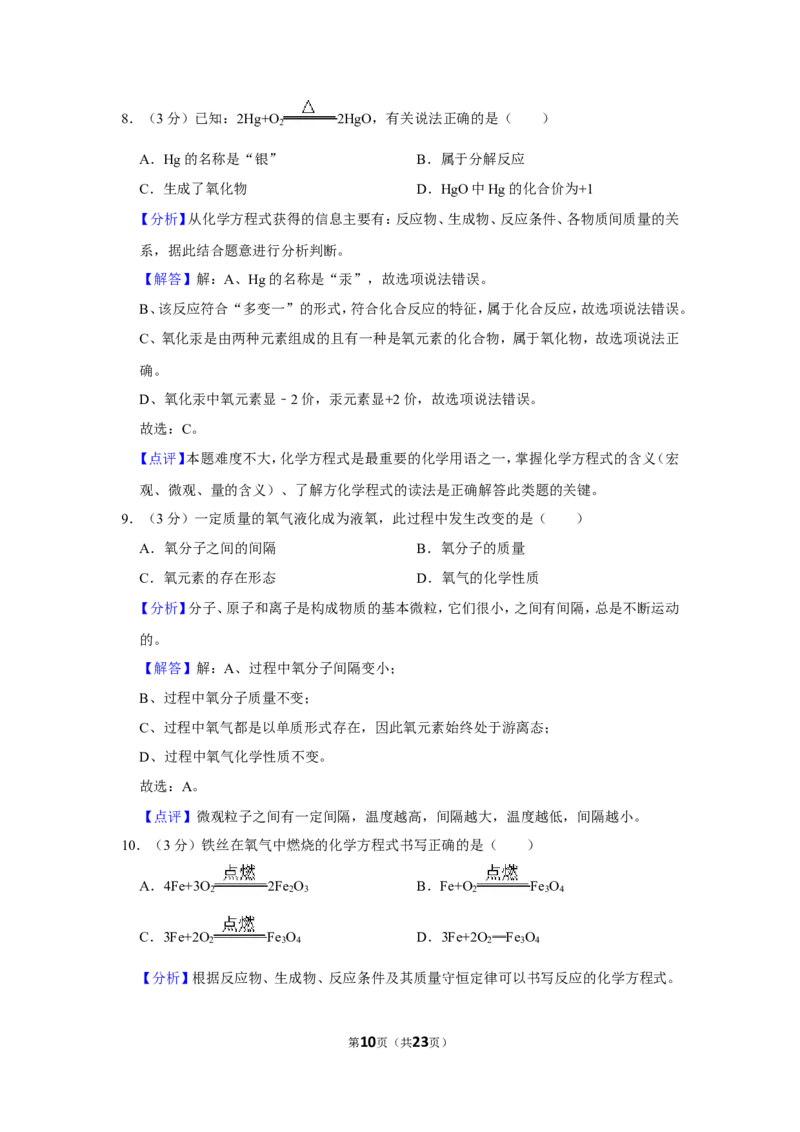
8.(3分)已知:2Hg+O 2HgO,有关说法正确的是( )
2
A.Hg的名称是“银” B.属于分解反应
C.生成了氧化物 D.HgO中Hg的化合价为+1
9.(3分)一定质量的氧气液化成为液氧,此过程中发生改变的是( )
A.氧分子之间的间隔 B.氧分子的质量
C.氧元素的存在形态 D.氧气的化学性质
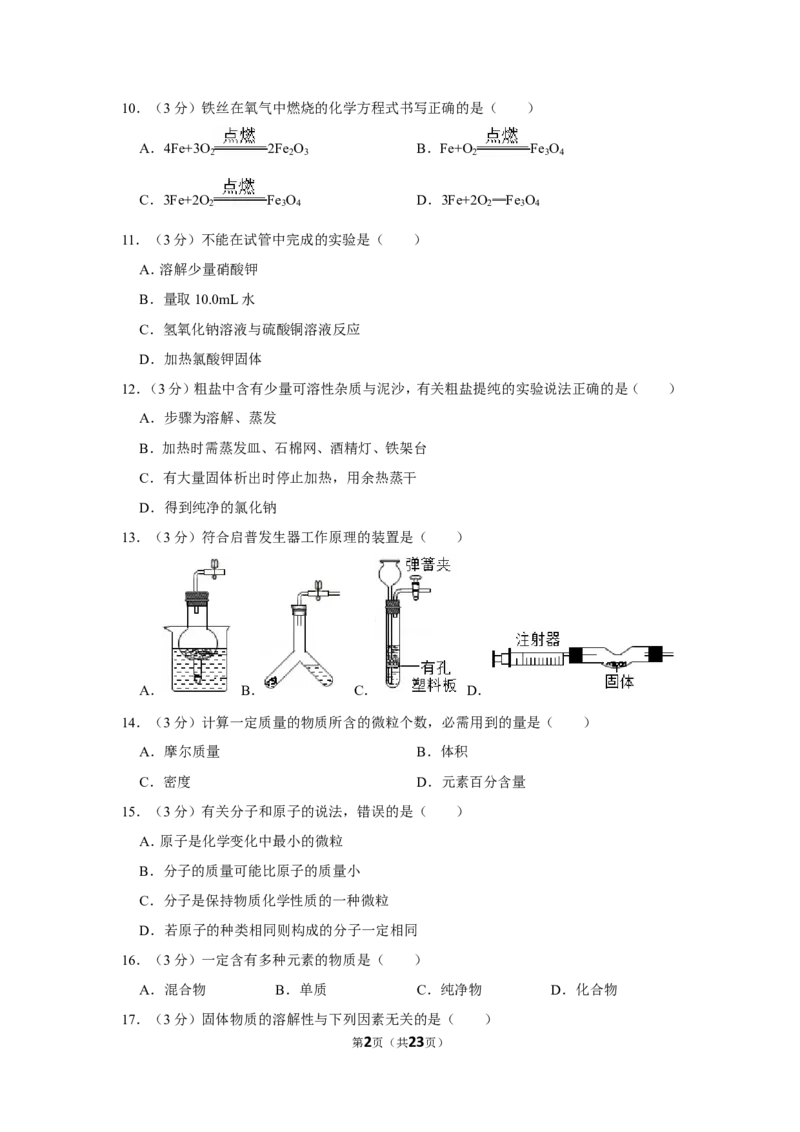
第1页(共23页)10.(3分)铁丝在氧气中燃烧的化学方程式书写正确的是( )
A.4Fe+3O 2Fe O B.Fe+O Fe O
2 2 3 2 3 4
C.3Fe+2O Fe O D.3Fe+2O ═Fe O
2 3 4 2 3 4
11.(3分)不能在试管中完成的实验是( )
A.溶解少量硝酸钾
B.量取10.0mL水
C.氢氧化钠溶液与硫酸铜溶液反应
D.加热氯酸钾固体
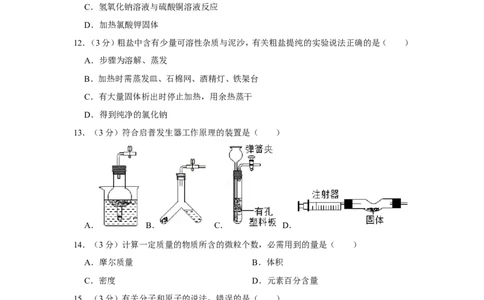
12.(3分)粗盐中含有少量可溶性杂质与泥沙,有关粗盐提纯的实验说法正确的是( )
A.步骤为溶解、蒸发
B.加热时需蒸发皿、石棉网、酒精灯、铁架台
C.有大量固体析出时停止加热,用余热蒸干
D.得到纯净的氯化钠
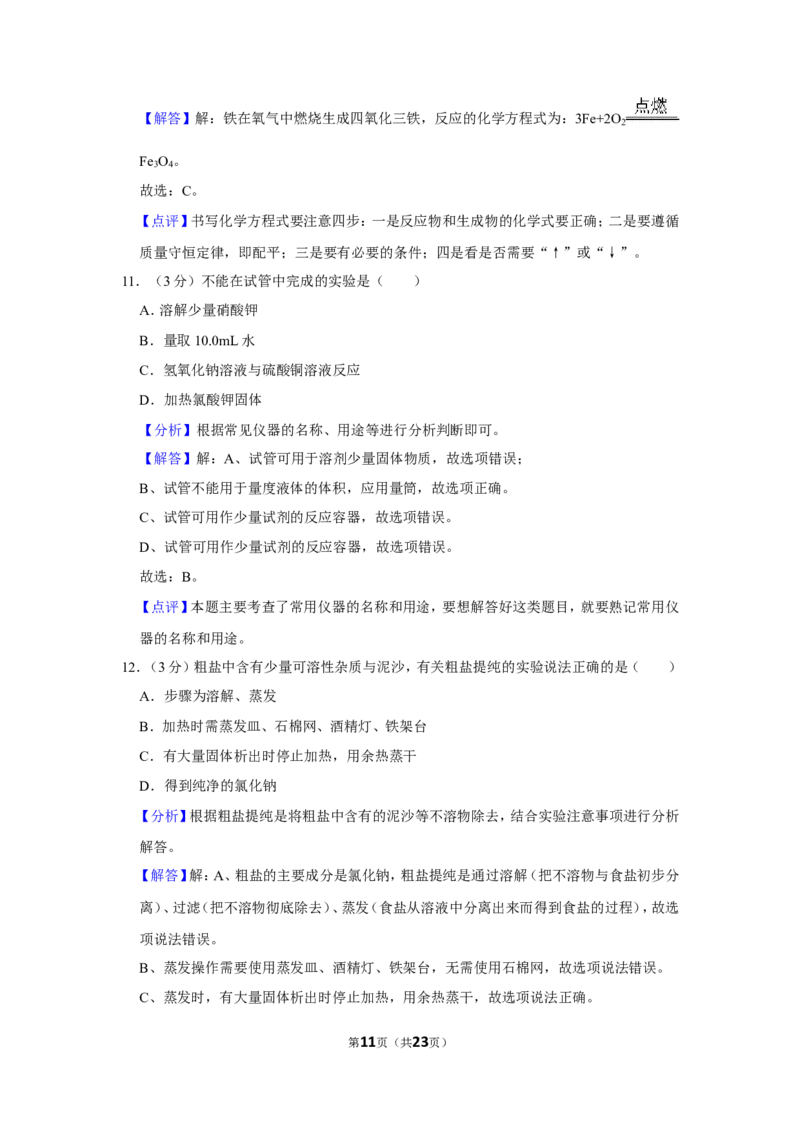
13.(3分)符合启普发生器工作原理的装置是( )
A. B. C. D.
14.(3分)计算一定质量的物质所含的微粒个数,必需用到的量是( )
A.摩尔质量 B.体积
C.密度 D.元素百分含量
15.(3分)有关分子和原子的说法,错误的是( )
A.原子是化学变化中最小的微粒
B.分子的质量可能比原子的质量小
C.分子是保持物质化学性质的一种微粒
D.若原子的种类相同则构成的分子一定相同
16.(3分)一定含有多种元素的物质是( )
A.混合物 B.单质 C.纯净物 D.化合物
17.(3分)固体物质的溶解性与下列因素无关的是( )
第2页(共23页)A.温度的高低 B.溶质的性质 C.压力的大小 D.溶剂的性质
18.(3分)所含氧元素质量最多的物质是( )
A.2mol氧气 B.18mL水 C.3g臭氧 D.6.02×1023个二氧化碳分子
19.(3分)关于元素化合价的说法一定正确的是( )
A.单质中元素的化合价最低
B.非金属元素在化合物中显负价
C.同种元素在同一化合物里化合价相同
D.化合物中各元素化合价的代数和等于零
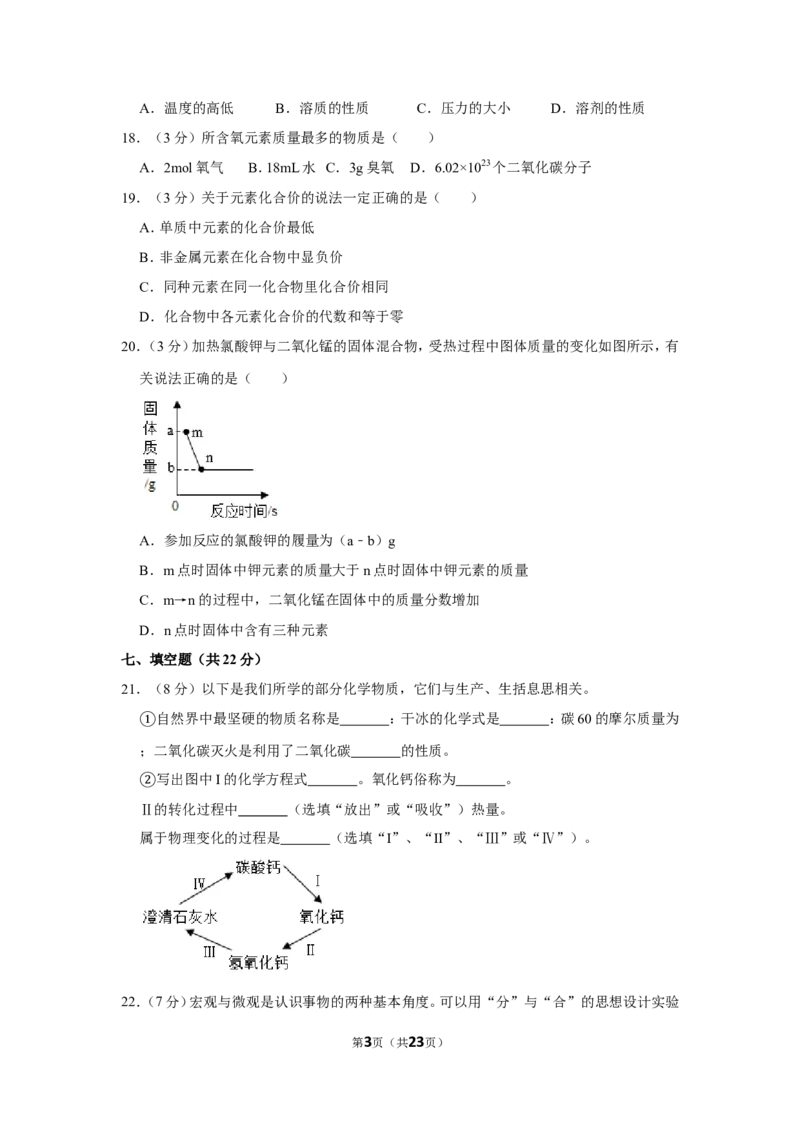
20.(3分)加热氯酸钾与二氧化锰的固体混合物,受热过程中图体质量的变化如图所示,有
关说法正确的是( )
A.参加反应的氯酸钾的履量为(a﹣b)g
B.m点时固体中钾元素的质量大于n点时固体中钾元素的质量
C.m→n的过程中,二氧化锰在固体中的质量分数增加
D.n点时固体中含有三种元素
七、填空题(共22分)
21.(8分)以下是我们所学的部分化学物质,它们与生产、生括息思相关。
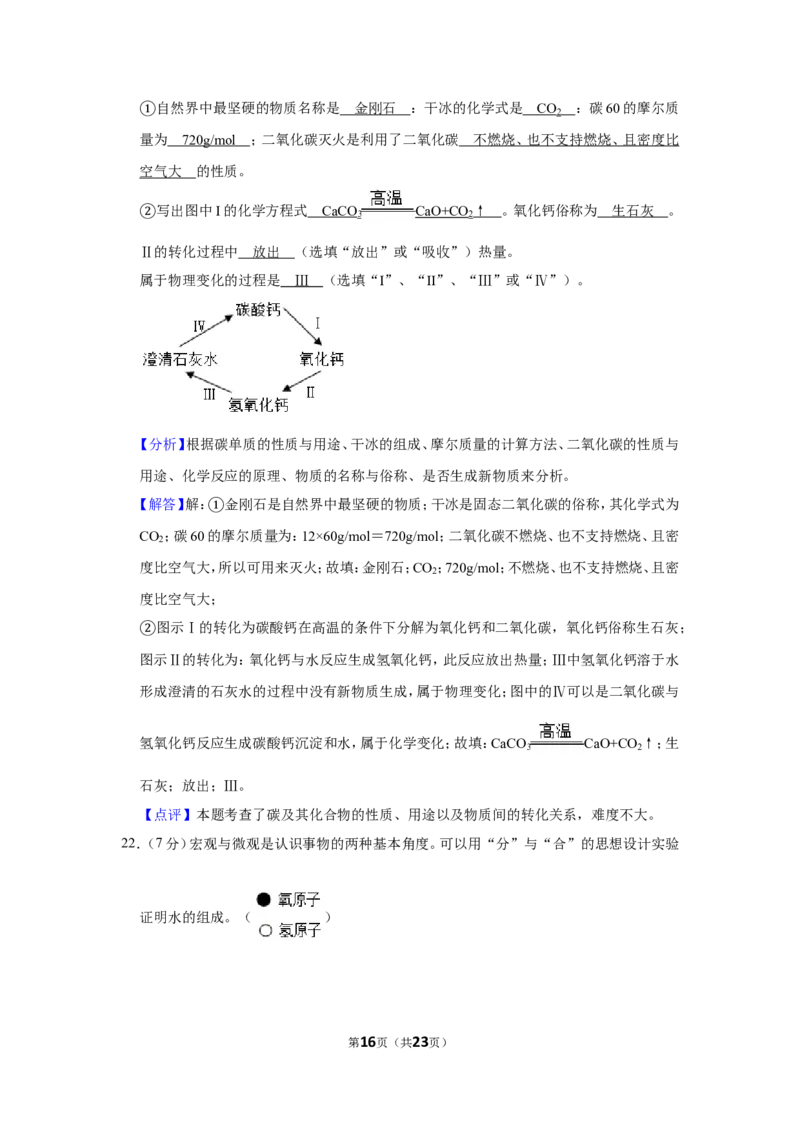
自然界中最坚硬的物质名称是 :干冰的化学式是 :碳60的摩尔质量为
①;二氧化碳灭火是利用了二氧化碳 的性质。
写出图中I的化学方程式 。氧化钙俗称为 。
②Ⅱ的转化过程中 (选填“放出”或“吸收”)热量。
属于物理变化的过程是 (选填“I”、“II”、“Ⅲ”或“Ⅳ”)。
22.(7分)宏观与微观是认识事物的两种基本角度。可以用“分”与“合”的思想设计实验
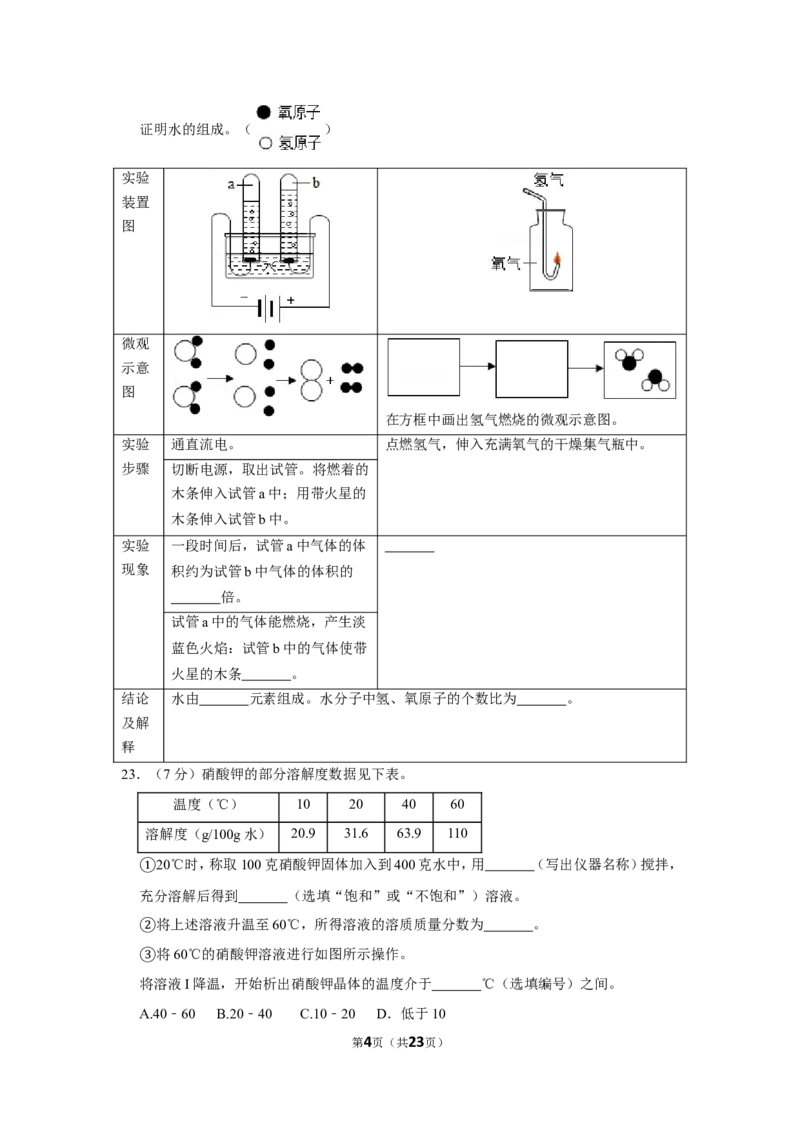
第3页(共23页)证明水的组成。( )
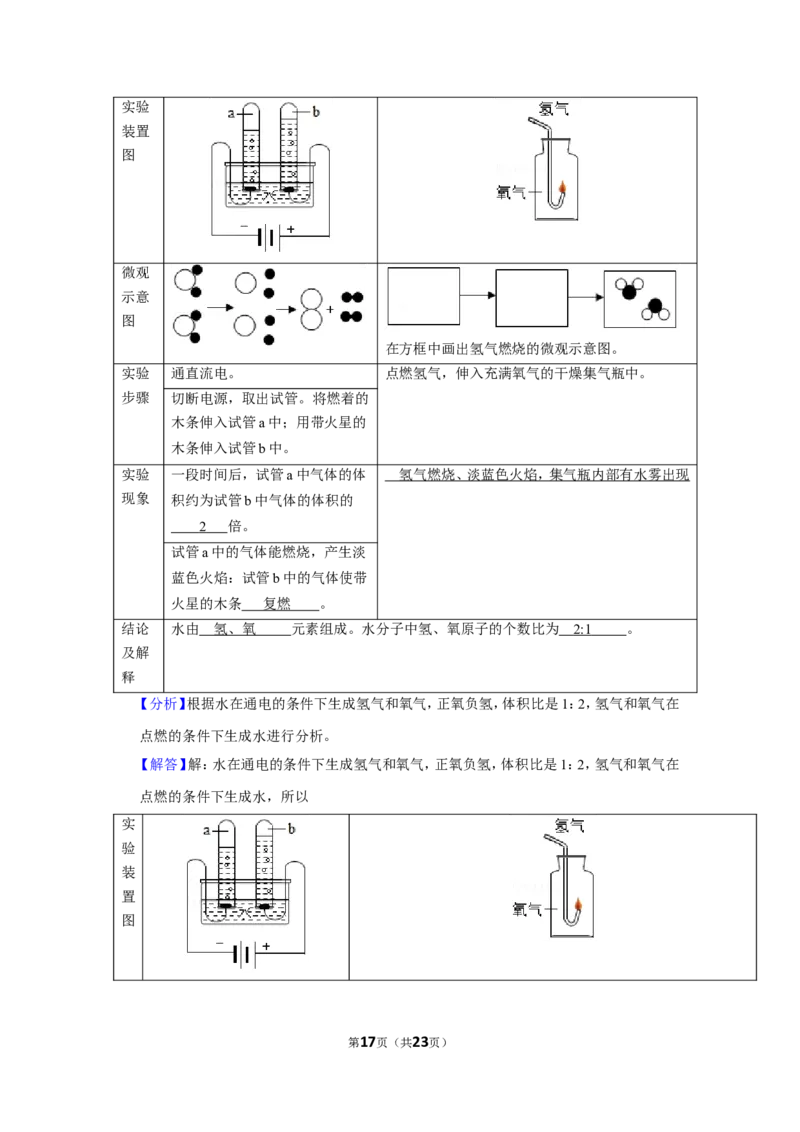
实验
装置
图
微观
示意
图
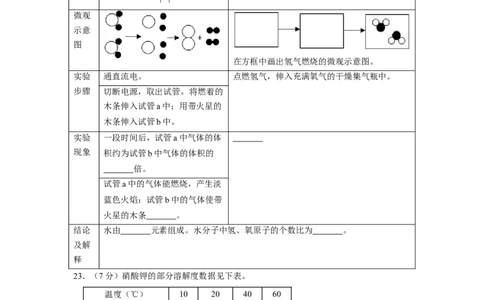
在方框中画出氢气燃烧的微观示意图。
实验 通直流电。 点燃氢气,伸入充满氧气的干燥集气瓶中。
步骤 切断电源,取出试管。将燃着的
木条伸入试管a中;用带火星的
木条伸入试管b中。
实验 一段时间后,试管a中气体的体
现象 积约为试管b中气体的体积的
倍。
试管a中的气体能燃烧,产生淡
蓝色火焰:试管b中的气体使带
火星的木条 。
结论 水由 元素组成。水分子中氢、氧原子的个数比为 。
及解
释
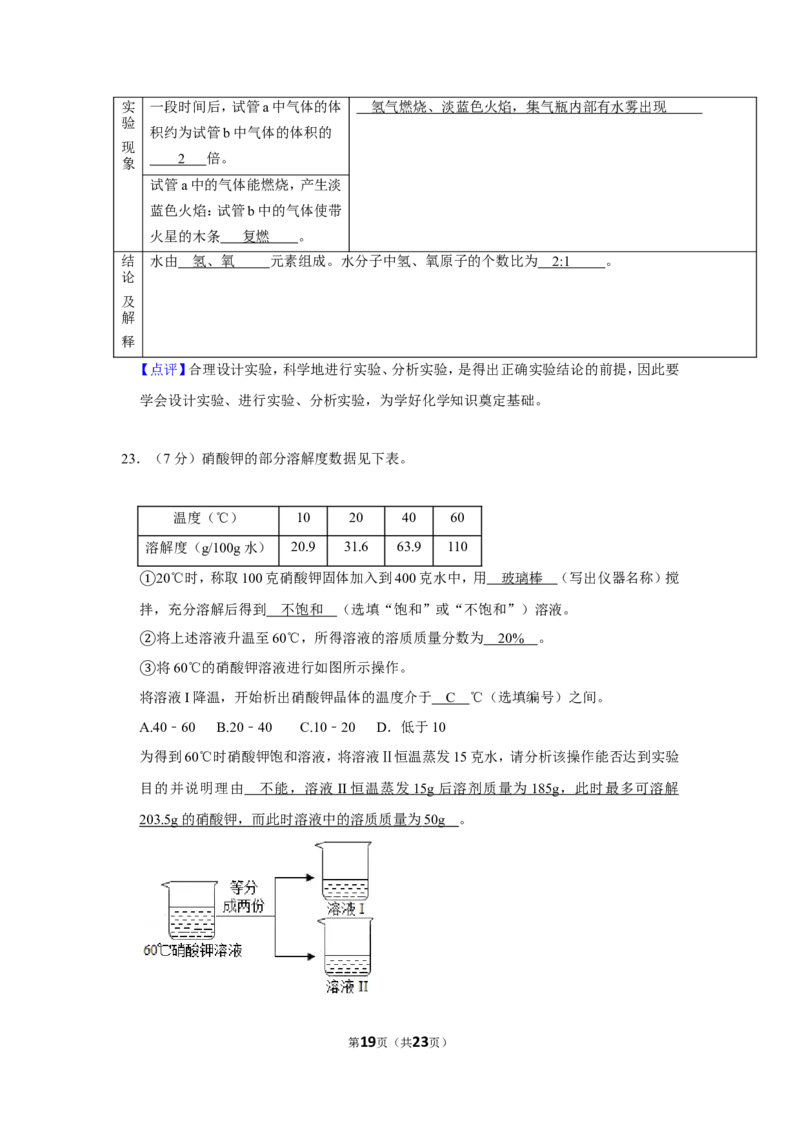
23.(7分)硝酸钾的部分溶解度数据见下表。
温度(℃) 10 20 40 60
溶解度(g/100g水) 20.9 31.6 63.9 110
20℃时,称取100克硝酸钾固体加入到400克水中,用 (写出仪器名称)搅拌,
①充分溶解后得到 (选填“饱和”或“不饱和”)溶液。
将上述溶液升温至60℃,所得溶液的溶质质量分数为 。
②将60℃的硝酸钾溶液进行如图所示操作。
③将溶液I降温,开始析出硝酸钾晶体的温度介于 ℃(选填编号)之间。
A.40﹣60 B.20﹣40 C.10﹣20 D.低于10
第4页(共23页)为得到60℃时硝酸钾饱和溶液,将溶液Ⅱ恒温蒸发15克水,请分析该操作能否达到实验
目的并说明理由 。
八、简答题(共18分)
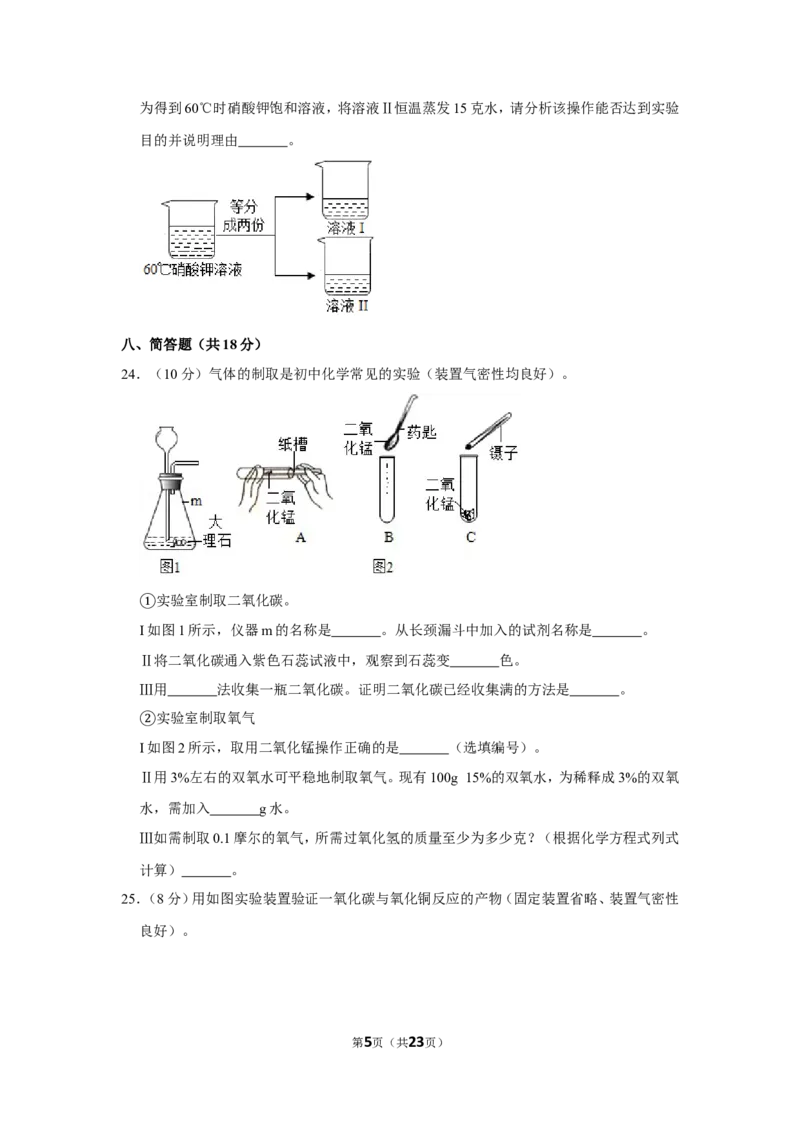
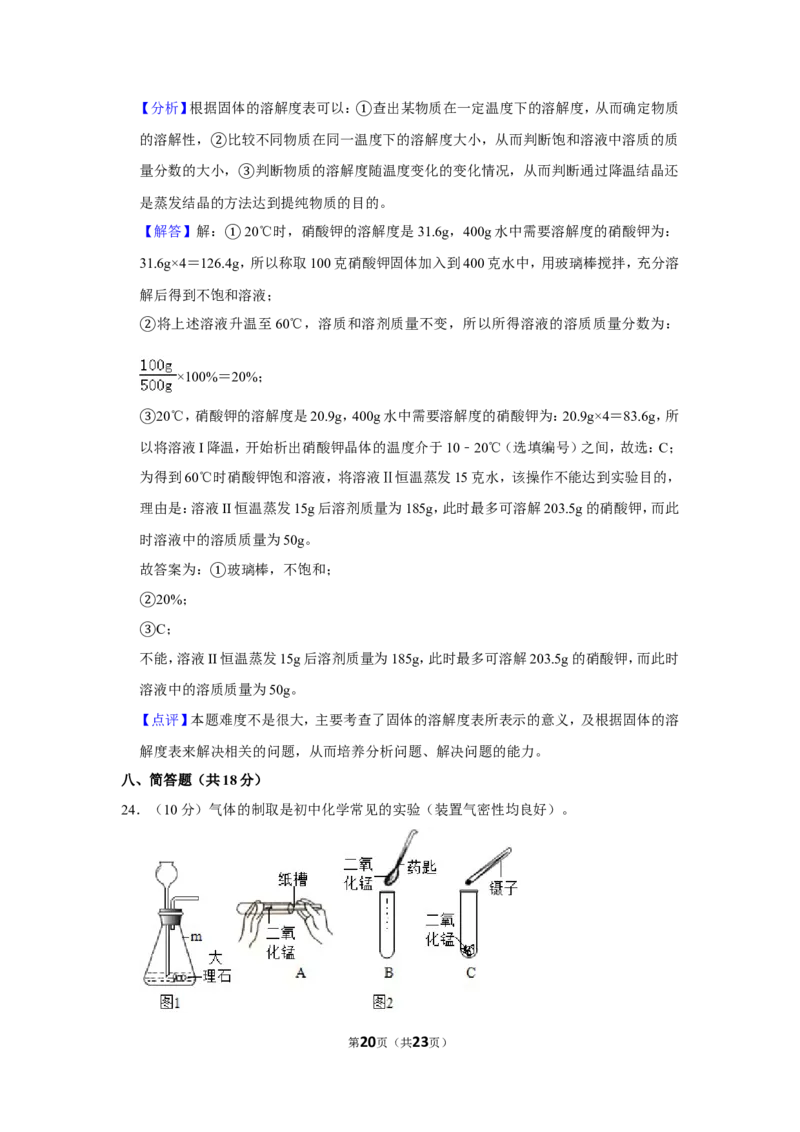
24.(10分)气体的制取是初中化学常见的实验(装置气密性均良好)。
实验室制取二氧化碳。
①I如图1所示,仪器m的名称是 。从长颈漏斗中加入的试剂名称是 。
Ⅱ将二氧化碳通入紫色石蕊试液中,观察到石蕊变 色。
Ⅲ用 法收集一瓶二氧化碳。证明二氧化碳已经收集满的方法是 。
实验室制取氧气
②I如图2所示,取用二氧化锰操作正确的是 (选填编号)。
Ⅱ用3%左右的双氧水可平稳地制取氧气。现有100g 15%的双氧水,为稀释成3%的双氧
水,需加入 g水。
Ⅲ如需制取0.1摩尔的氧气,所需过氧化氢的质量至少为多少克?(根据化学方程式列式
计算) 。
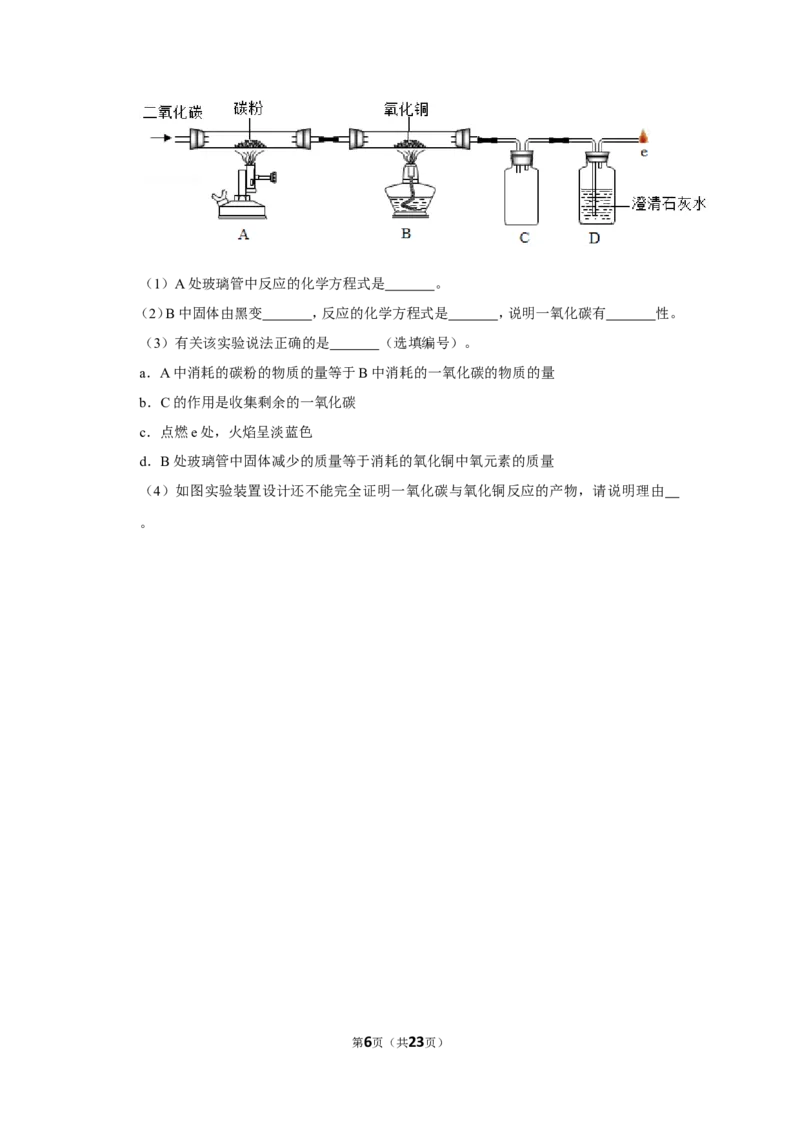
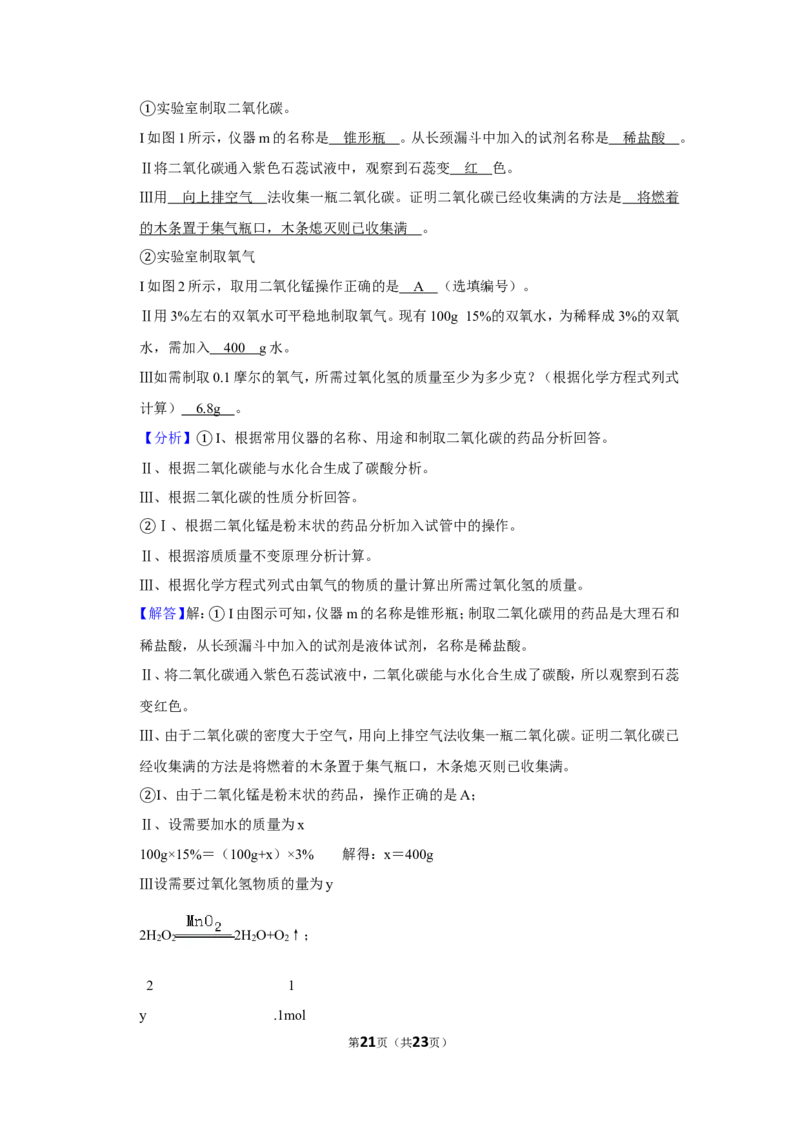
25.(8分)用如图实验装置验证一氧化碳与氧化铜反应的产物(固定装置省略、装置气密性
良好)。
第5页(共23页)(1)A处玻璃管中反应的化学方程式是 。
(2)B中固体由黑变 ,反应的化学方程式是 ,说明一氧化碳有 性。
(3)有关该实验说法正确的是 (选填编号)。
a.A中消耗的碳粉的物质的量等于B中消耗的一氧化碳的物质的量
b.C的作用是收集剩余的一氧化碳
c.点燃e处,火焰呈淡蓝色
d.B处玻璃管中固体减少的质量等于消耗的氧化铜中氧元素的质量
(4)如图实验装置设计还不能完全证明一氧化碳与氧化铜反应的产物,请说明理由
。
第6页(共23页)2019年上海市黄浦区中考化学一模试卷
参考答案与试题解析
六、选择题(共20分)
1.(3分)属于稀有气体的是( )
A.H B.He C.O D.N
2 2 2
【分析】空气中各成分的体积分数分别是:氮气大约占空气体积的78%、氧气大约占空气
体积的21%、稀有气体大约占空气体积的0.94%、二氧化碳大约占空气体积的0.03%、水
蒸气和其它气体和杂质大约占0.03%;稀有气体是氦、氖、氩、氪、氙等气体的总称。
【解答】解:A、氢气不是空气的成分,故选项错误;
B、稀有气体是氦、氖、氩、氪、氙等气体的总称,故选项正确;
C、氧气大约占空气体积的21%,不是稀有气体;故选项错误;
D、氮气大约占空气体积的78%,不是稀有气体;故选项错误;
故选:B。
【点评】本考点考查了空气中各种气体的含量,同学们要加强记忆有关的知识点,在理解
的基础上加以应用,本考点基础性比较强,主要出现在选择题和填空题中。
2.(3分)放入水中形成乳浊液的是( )
A.淀粉 B.蔗糖 C.食盐 D.植物油
【分析】溶液是指一种物质或几种物质分散到另一种物质中,形成均一稳定的混合物。具
有三个特点:均一、稳定、混合物;悬浊液是固体颗粒悬浮于液体中形成不均一、不稳定的
混合物;乳浊液是液体小液滴分散到另一种物质中形成不均一、不稳定的混合物。
【解答】解:A、淀粉不溶于水,与水混合形成悬浊液,故A错;
B、蔗糖易溶于水,形成均一稳定的混合物,属于溶液,故B错;
C、食盐易溶于水形成均一稳定的混合物,属于溶液,故C错;
D、植物油不溶于水,植物油小液滴分散到水中形成的是乳浊液,故D正确。
故选:D。
【点评】溶液是均一稳定的混合物,悬浊液、乳浊液不均一、不稳定,掌握它们之间的区别
和联系。
3.(3分)自来水厂将水进行净化的过程中,属于化学变化的是( )
A.挥发 B.沉降 C.过滤 D.消毒
第7页(共23页)【分析】有新物质生成的变化叫化学变化,没有新物质生成的变化叫物理变化。化学变化
的特征是:有新物质生成。判断物理变化和化学变化的依据是:是否有新物质生成。
【解答】解:A、挥发过程中没有新物质生成,属于物理变化。故错误;
B、沉降的过程中没有新物质生成,属于物理变化。故错误;
C、过滤只是把不溶于水的物质除去,过程中没有新物质生成,属于物理变化。故错误;
D、消毒的过程中生成了次氯酸和盐酸,属于化学变化。故正确。
故选:D。
【点评】本考点考查了物理变化和化学变化的区别,基础性比较强,只要抓住关键点:是否
有新物质生成,问题就很容易解决。
4.(3分)属于活性炭物理性质的是( )
A.稳定性 B.吸附性 C.还原性 D.可燃性
【分析】需要通过化学变化表现出来的性质,属于物质的化学性质,不需要通过化学变化
表现出来的性质,属于物质的物理性质。
【解答】解:活性炭的稳定性、还原性和可燃性需要发生化学变化才能表现出来,属于其化
学性质;吸附性不需要发生化学变化就能表现出来,属于其物理性质。
故选:B。
【点评】物理性质、化学性质是一对与物理变化、化学变化有密切关系的概念,联系物理变
化、化学变化来理解物理性质和化学性质,则掌握起来并不困难。
5.(3分)试剂标签对应的化学式书写错误的是( )
A. B.
C. D.
【分析】化合物化学式的书写一般规律:先读后写,后读先写;金属在前,非金属在后;氧化
物中氧在后,原子个数不能漏,正负化合价代数和为零。
【解答】解:A.硫酸钾中,钾元素显+1价,硫酸根显﹣2价,所以其化学式为K SO ,故正确;
2 4
B.氢氧化钠中,钠元素显+1价,氢氧根显﹣1价,所以其化学式为NaOH,故正确;
C.氯化铁中,铁元素显+3价,氯元素显﹣1价,所以其化学式为FeCl ,故错误;
3
D.氧化镁中,镁元素显+2价,氧元素显﹣2价,所以其化学式为MgO,故正确。
第8页(共23页)故选:C。
【点评】本题难度不大,考查化合物化学式的书写方法,掌握化合物化学式的书写方法是
正确解答此类题的关键。
6.(3分)物质在氧气中燃烧的主要现象描述正确的是( )
A.木炭:产生红色火焰 B.红磷:产生大量白烟
C.镁条:生成黑色固体 D.硫粉:生成二氧化硫
【分析】A、根据木炭在氧气中燃烧的现象进行分析判断。
B、根据红磷在氧气中燃烧的现象进行分析判断。
C、根据镁条在氧气中燃烧的现象进行分析判断。
D、根据硫在氧气中燃烧的现象进行分析判断。
【解答】解:A、木炭在氧气中燃烧,发出白光,生成能使澄清石灰水变浑浊的气体,故选项
说法错误。
B、红磷在空气中燃烧,产生大量的白烟,故选项说法正确。
C、镁条在氧气中剧烈燃烧,发出耀眼的白光,生成一种白色固体,故选项说法错误。
D、硫在氧气中燃烧,发出明亮的蓝紫色火焰,生成二氧化硫是实验结论而不是实验现象,
故选项说法错误。
故选:B。
【点评】本题难度不大,掌握常见物质燃烧的现象即可正确解答,在描述物质燃烧的现象
时,需要注意光和火焰、烟和雾、实验结论和实验现象的区别。
7.(3分)物质对应的类别正确的是( )
A.胆矾:化合物 B.木炭:单质
C.冰:混合物 D.天然气:纯净物
【分析】纯净物由一种物质组成,混合物由两种或两种以上的物质组成;
单质是由一种元素组成的纯净物,化合物是由不同种元素组成的纯净物。
【解答】解:A、胆矾是硫酸铜晶体,是由不同种元素组成的纯净物,属于化合物;
B、木炭主要成分是碳,还含有一些杂质,属于混合物;
C、冰是水的固体,是由一种物质组成的,属于纯净物;
D、天然气主要成分是甲烷,还含有一些杂质,属于混合物。
故选:A。
【点评】判断纯净物和混合物时,就是判断物质的物质组成;判断是否是单质、化合物时,
既要判断元素组成,又要判断物质组成。
第9页(共23页)8.(3分)已知:2Hg+O 2HgO,有关说法正确的是( )
2
A.Hg的名称是“银” B.属于分解反应
C.生成了氧化物 D.HgO中Hg的化合价为+1
【分析】从化学方程式获得的信息主要有:反应物、生成物、反应条件、各物质间质量的关
系,据此结合题意进行分析判断。
【解答】解:A、Hg的名称是“汞”,故选项说法错误。
B、该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应,故选项说法错误。
C、氧化汞是由两种元素组成的且有一种是氧元素的化合物,属于氧化物,故选项说法正
确。
D、氧化汞中氧元素显﹣2价,汞元素显+2价,故选项说法错误。
故选:C。
【点评】本题难度不大,化学方程式是最重要的化学用语之一,掌握化学方程式的含义(宏
观、微观、量的含义)、了解方化学程式的读法是正确解答此类题的关键。
9.(3分)一定质量的氧气液化成为液氧,此过程中发生改变的是( )
A.氧分子之间的间隔 B.氧分子的质量
C.氧元素的存在形态 D.氧气的化学性质
【分析】分子、原子和离子是构成物质的基本微粒,它们很小,之间有间隔,总是不断运动
的。
【解答】解:A、过程中氧分子间隔变小;
B、过程中氧分子质量不变;
C、过程中氧气都是以单质形式存在,因此氧元素始终处于游离态;
D、过程中氧气化学性质不变。
故选:A。
【点评】微观粒子之间有一定间隔,温度越高,间隔越大,温度越低,间隔越小。
10.(3分)铁丝在氧气中燃烧的化学方程式书写正确的是( )
A.4Fe+3O 2Fe O B.Fe+O Fe O
2 2 3 2 3 4
C.3Fe+2O Fe O D.3Fe+2O ═Fe O
2 3 4 2 3 4
【分析】根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式。
第10页(共23页)【解答】解:铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为:3Fe+2O
2
Fe O 。
3 4
故选:C。
【点评】书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循
质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”。
11.(3分)不能在试管中完成的实验是( )
A.溶解少量硝酸钾
B.量取10.0mL水
C.氢氧化钠溶液与硫酸铜溶液反应
D.加热氯酸钾固体
【分析】根据常见仪器的名称、用途等进行分析判断即可。
【解答】解:A、试管可用于溶剂少量固体物质,故选项错误;
B、试管不能用于量度液体的体积,应用量筒,故选项正确。
C、试管可用作少量试剂的反应容器,故选项错误。
D、试管可用作少量试剂的反应容器,故选项错误。
故选:B。
【点评】本题主要考查了常用仪器的名称和用途,要想解答好这类题目,就要熟记常用仪
器的名称和用途。
12.(3分)粗盐中含有少量可溶性杂质与泥沙,有关粗盐提纯的实验说法正确的是( )
A.步骤为溶解、蒸发
B.加热时需蒸发皿、石棉网、酒精灯、铁架台
C.有大量固体析出时停止加热,用余热蒸干
D.得到纯净的氯化钠
【分析】根据粗盐提纯是将粗盐中含有的泥沙等不溶物除去,结合实验注意事项进行分析
解答。
【解答】解:A、粗盐的主要成分是氯化钠,粗盐提纯是通过溶解(把不溶物与食盐初步分
离)、过滤(把不溶物彻底除去)、蒸发(食盐从溶液中分离出来而得到食盐的过程),故选
项说法错误。
B、蒸发操作需要使用蒸发皿、酒精灯、铁架台,无需使用石棉网,故选项说法错误。
C、蒸发时,有大量固体析出时停止加热,用余热蒸干,故选项说法正确。
第11页(共23页)D、得到的氯化钠中含有可溶性杂质,不能得到纯净的氯化钠,故选项说法错误。
故选:C。
【点评】本题难度不大,掌握粗盐提纯的原理、实验步骤(溶解、过滤、蒸发)、所需的仪器是
正确解答本题的关键。
13.(3分)符合启普发生器工作原理的装置是( )
A. B. C. D.
【分析】根据启普发生器具有随时可使反应发生或停止的特点,启普发生器之所以能控制
反应的进行与停止,就是因为它当将装置中的导气管关闭后,生成的气体使装置中的气压
增大,从而使固体和液体分离,使反应停止进行分析。
【解答】解:A、通过打开和关闭弹簧夹,能控制反应的发生和停止,具有启普发生器原理,
故A正确;
B、通过打开和关闭弹簧夹,不能控制反应的发生和停止,不具有启普发生器原理,故B错
误;
C、弹簧夹关闭后,气体将液体压回长颈漏斗,使固体和液体分离,符合启普发生器工作原
理,故C正确;
D、注射器只能添加液体,不能是固体和液体分离,不具有启普发生器原理,故D错误。
故选:AC。
【点评】启普发生器的原理就是:将生成的气体密封后,能使密封空间内的压强增大,从而
将液体压离固体,从而实现固液分离的目的。
14.(3分)计算一定质量的物质所含的微粒个数,必需用到的量是( )
A.摩尔质量 B.体积
C.密度 D.元素百分含量
【分析】用物质的质量×摩尔质量,计算出物质的量,再用物质的量×6.02×1023,计算出微粒
个数。
【解答】解:物质的质量×摩尔质量,计算出物质的量,再用物质的量×6.02×1023,计算出微
粒个数。
故选:A。
第12页(共23页)【点评】解答本题关键是熟悉物质的量与微粒个数的关系。
15.(3分)有关分子和原子的说法,错误的是( )
A.原子是化学变化中最小的微粒
B.分子的质量可能比原子的质量小
C.分子是保持物质化学性质的一种微粒
D.若原子的种类相同则构成的分子一定相同
【分析】化学变化中分子可分,原子不可分,因此原子是化学变化中的最小微粒;
原子种类相同时可以构成不同分子。
【解答】解:A、原子是化学变化中最小的微粒,该选项说法正确;
B、分子的质量可能比原子的质量小,例如水分子质量小于汞原子质量,该选项说法正确;
C、分子是保持物质化学性质的一种微粒,该选项说法正确;
D、原子的种类相同,构成的分子不一定相同,例如氢原子和氧原子可以构成水分子,也可
以构成过氧化氢分子,该选项说法不正确。
故选:D。
【点评】如果不知道原子、分子种类,不能比较大小。
16.(3分)一定含有多种元素的物质是( )
A.混合物 B.单质 C.纯净物 D.化合物
【分析】根据混合物、单质、纯净物、化合物的特点回答本题。
【解答】解:A、混合物是由不同物质组成,可以由一种元素组成,例如氧气和臭氧属于混合
物,故A错;
B、单质是由一种元素组成的纯净物,故B错;
C、纯净物是由一种物质组成,可以由一种元素组成,可以由多种元素组成,故C错;
D、化合物是由两种或两种以上元素组成,所以化合物一定含有多种元素,故D正确。
故选:D。
【点评】解答本题关键是熟悉物质的分类方法。
17.(3分)固体物质的溶解性与下列因素无关的是( )
A.温度的高低 B.溶质的性质 C.压力的大小 D.溶剂的性质
【分析】影响固体物质溶解性的因素有外因和内因,内因是指溶质的性质和溶剂的性质,
外因是温度;所以温度是影响溶解度大小的重要因素;气压对固体的溶解性几乎无影响。
【解答】解:A、温度的高低,影响固体物质的溶解性,故选项错误。
B、溶质的性质,影响固体物质的溶解性,是影响固体物质溶解性的内因,故选项错误。
第13页(共23页)C、气压对固体的溶解性几乎无影响,压力的大小,不影响固体物质的溶解性,故选项正确。
D、溶剂的性质,影响固体物质的溶解性,是影响固体物质溶解性的内因,故选项错误。
故选:C。
【点评】本题难度不大,了解固体物质的溶解性受到溶剂和溶质性质影响、还受到温度的
影响是正确解答本题的关键。
18.(3分)所含氧元素质量最多的物质是( )
A.2mol氧气 B.18mL水 C.3g臭氧 D.6.02×1023个二氧化碳分子
【分析】根据质量的计算方法考虑,质量=体积×密度。
【解答】解:
A、2mol氧气的质量=2×32g/mol=64g,所以氧元素质量是64g;
B、18mL水的质量=18mL×1g/ml=18g,氧元素质量=18g× =16g;
C、3g臭氧中氧元素质量是3g;
D、6.02×1023个二氧化碳分子,是1mol二氧化碳,质量为:1mol×44g/mol=44g,氧元素的
质量:44g× =32g。
故选:A。
【点评】解答本题关键是熟悉物质的量和质量的关系。
19.(3分)关于元素化合价的说法一定正确的是( )
A.单质中元素的化合价最低
B.非金属元素在化合物中显负价
C.同种元素在同一化合物里化合价相同
D.化合物中各元素化合价的代数和等于零
【分析】A.根据在化合物中非金属元素常显负价来分析;
B.根据氧化物中,非金属元素显正价来分析;
C.根据同种元素在同一化合物也会显示不同价态来分析;
D.根据化合物中各元素正负化合价的代数和为零来分析。
【解答】解:A.单质中元素的化合价为零,而在非金属氧化物中,非金属元素显负价,化合
价更低,故错误;
B.在化合物中,非金属元素不一定显负价,比如硫酸中氢元素和硫元素为正价,故错误;
C.同种元素在同种物质中化合价不一定相同,比如硝酸铵中氮元素为﹣3和+5价,故错
第14页(共23页)误;
D.在化合物中,各元素正负化合价的代数和为零,故正确。
故选:D。
【点评】本题考查学生对化合价知识的理解与掌握,并能通过举出反例的方法来验证观点
是否正确。
20.(3分)加热氯酸钾与二氧化锰的固体混合物,受热过程中图体质量的变化如图所示,有
关说法正确的是( )
A.参加反应的氯酸钾的履量为(a﹣b)g
B.m点时固体中钾元素的质量大于n点时固体中钾元素的质量
C.m→n的过程中,二氧化锰在固体中的质量分数增加
D.n点时固体中含有三种元素
【分析】根据氯酸钾在二氧化锰的催化作用下加热生成氯化钾和氧气,固体中的氧元素质
量逐渐减小,然后不变;生成的氧气质量逐渐增加,然后不变;二氧化锰是反应的催化剂,
质量不会改变;固体质量逐渐减小,钾元素的质量分数逐渐增加,然后不变进行分析。
【解答】解:A.由图象可知,反应中生成氧气的质量为(a﹣b)g,故错误;
B.反应过程中,固体所含钾元素的质量不变,而固体的质量在减小,所以m点时固体中钾
元素的质量等于n点时固体中钾元素的质量,故错误;
C.二氧化锰是该反应的催化剂,其质量保持不变,所以m→n的过程中,固体质量在减小,
所以二氧化锰在固体中的质量分数增加,故正确;
D.n点剩余固体是氯化钾和二氧化锰的混合物,含有钾元素、氯元素、锰元素与氧元素四
种元素,故错误。
故选:C。
【点评】本题主要考查了氯酸钾和二氧化锰混合加热后,各物质的质量变化,难度不大,需
要结合图象认真分析。
七、填空题(共22分)
21.(8分)以下是我们所学的部分化学物质,它们与生产、生括息思相关。
第15页(共23页)自然界中最坚硬的物质名称是 金刚石 :干冰的化学式是 CO :碳60的摩尔质
2
①量为 720g/mo l ;二氧化碳灭火是利用了二氧化碳 不燃烧、也不支持燃烧、且密度比
空气大 的性质。
写出图中I的化学方程式 CaCO CaO+CO ↑ 。氧化钙俗称为 生石灰 。
3 2
②
Ⅱ的转化过程中 放出 (选填“放出”或“吸收”)热量。
属于物理变化的过程是 Ⅲ (选填“I”、“II”、“Ⅲ”或“Ⅳ”)。
【分析】根据碳单质的性质与用途、干冰的组成、摩尔质量的计算方法、二氧化碳的性质与
用途、化学反应的原理、物质的名称与俗称、是否生成新物质来分析。
【解答】解: 金刚石是自然界中最坚硬的物质;干冰是固态二氧化碳的俗称,其化学式为
CO ;碳60的①摩尔质量为:12×60g/mol=720g/mol;二氧化碳不燃烧、也不支持燃烧、且密
2
度比空气大,所以可用来灭火;故填:金刚石;CO ;720g/mol;不燃烧、也不支持燃烧、且密
2
度比空气大;
图示Ⅰ的转化为碳酸钙在高温的条件下分解为氧化钙和二氧化碳,氧化钙俗称生石灰;
②图示Ⅱ的转化为:氧化钙与水反应生成氢氧化钙,此反应放出热量;Ⅲ中氢氧化钙溶于水
形成澄清的石灰水的过程中没有新物质生成,属于物理变化;图中的Ⅳ可以是二氧化碳与
氢氧化钙反应生成碳酸钙沉淀和水,属于化学变化;故填:CaCO CaO+CO ↑;生
3 2
石灰;放出;Ⅲ。
【点评】本题考查了碳及其化合物的性质、用途以及物质间的转化关系,难度不大。
22.(7分)宏观与微观是认识事物的两种基本角度。可以用“分”与“合”的思想设计实验
证明水的组成。( )
第16页(共23页)实验
装置
图
微观
示意
图
在方框中画出氢气燃烧的微观示意图。
实验 通直流电。 点燃氢气,伸入充满氧气的干燥集气瓶中。
步骤 切断电源,取出试管。将燃着的
木条伸入试管a中;用带火星的
木条伸入试管b中。
实验 一段时间后,试管a中气体的体 氢气燃烧、淡蓝色火焰,集气瓶内部有水雾出现
现象 积约为试管b中气体的体积的
2 倍。
试管a中的气体能燃烧,产生淡
蓝色火焰:试管b中的气体使带
火星的木条 复燃 。
结论 水由 氢、氧 元素组成。水分子中氢、氧原子的个数比为 2: 1 。
及解
释
【分析】根据水在通电的条件下生成氢气和氧气,正氧负氢,体积比是1:2,氢气和氧气在
点燃的条件下生成水进行分析。
【解答】解:水在通电的条件下生成氢气和氧气,正氧负氢,体积比是1:2,氢气和氧气在
点燃的条件下生成水,所以
实
验
装
置
图
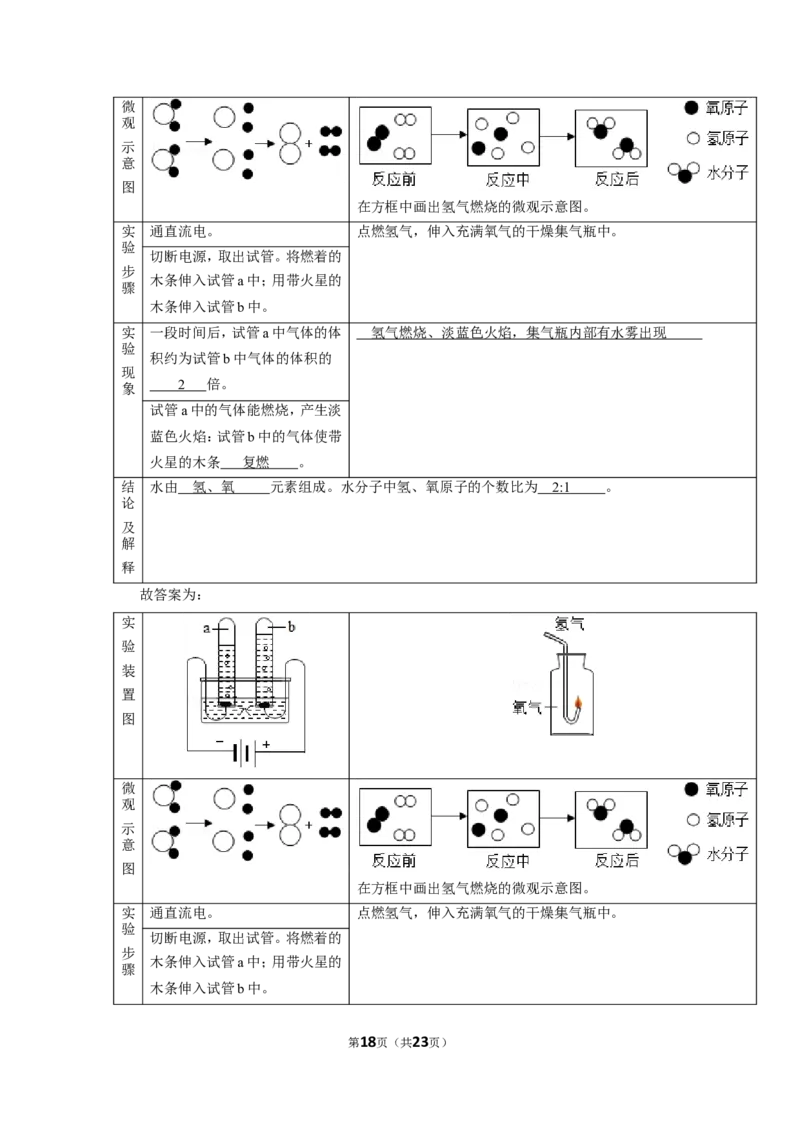
第17页(共23页)微
观
示
意
图
在方框中画出氢气燃烧的微观示意图。
实 通直流电。 点燃氢气,伸入充满氧气的干燥集气瓶中。
验
切断电源,取出试管。将燃着的
步
木条伸入试管a中;用带火星的
骤
木条伸入试管b中。
实 一段时间后,试管a中气体的体 氢气燃烧、淡蓝色火焰,集气瓶内部有水雾出现
验
积约为试管b中气体的体积的
现
象 2 倍。
试管a中的气体能燃烧,产生淡
蓝色火焰:试管b中的气体使带
火星的木条 复燃 。
结 水由 氢、氧 元素组成。水分子中氢、氧原子的个数比为 2: 1 。
论
及
解
释
故答案为:
实
验
装
置
图
微
观
示
意
图
在方框中画出氢气燃烧的微观示意图。
实 通直流电。 点燃氢气,伸入充满氧气的干燥集气瓶中。
验
切断电源,取出试管。将燃着的
步
木条伸入试管a中;用带火星的
骤
木条伸入试管b中。
第18页(共23页)实 一段时间后,试管a中气体的体 氢气燃烧、淡蓝色火焰,集气瓶内部有水雾出现
验
积约为试管b中气体的体积的
现
象 2 倍。
试管a中的气体能燃烧,产生淡
蓝色火焰:试管b中的气体使带
火星的木条 复燃 。
结 水由 氢、氧 元素组成。水分子中氢、氧原子的个数比为 2: 1 。
论
及
解
释
【点评】合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要
学会设计实验、进行实验、分析实验,为学好化学知识奠定基础。
23.(7分)硝酸钾的部分溶解度数据见下表。
温度(℃) 10 20 40 60
溶解度(g/100g水) 20.9 31.6 63.9 110
20℃时,称取100克硝酸钾固体加入到400克水中,用 玻璃棒 (写出仪器名称)搅
①拌,充分溶解后得到 不饱和 (选填“饱和”或“不饱和”)溶液。
将上述溶液升温至60℃,所得溶液的溶质质量分数为 20% 。
②将60℃的硝酸钾溶液进行如图所示操作。
③将溶液I降温,开始析出硝酸钾晶体的温度介于 C ℃(选填编号)之间。
A.40﹣60 B.20﹣40 C.10﹣20 D.低于10
为得到60℃时硝酸钾饱和溶液,将溶液Ⅱ恒温蒸发15克水,请分析该操作能否达到实验
目的并说明理由 不能,溶液 I I 恒温蒸发 15g 后溶剂质量为 185g ,此时最多可溶解
203.5g 的硝酸钾,而此时溶液中的溶质质量为 50g 。
第19页(共23页)【分析】根据固体的溶解度表可以: 查出某物质在一定温度下的溶解度,从而确定物质
的溶解性, 比较不同物质在同一温①度下的溶解度大小,从而判断饱和溶液中溶质的质
量分数的大②小, 判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还
是蒸发结晶的方法③达到提纯物质的目的。
【解答】解: 20℃时,硝酸钾的溶解度是31.6g,400g水中需要溶解度的硝酸钾为:
31.6g×4=126.①4g,所以称取100克硝酸钾固体加入到400克水中,用玻璃棒搅拌,充分溶
解后得到不饱和溶液;
将上述溶液升温至60℃,溶质和溶剂质量不变,所以所得溶液的溶质质量分数为:
②
×100%=20%;
20℃,硝酸钾的溶解度是20.9g,400g水中需要溶解度的硝酸钾为:20.9g×4=83.6g,所
③以将溶液I降温,开始析出硝酸钾晶体的温度介于10﹣20℃(选填编号)之间,故选:C;
为得到60℃时硝酸钾饱和溶液,将溶液Ⅱ恒温蒸发15克水,该操作不能达到实验目的,
理由是:溶液II恒温蒸发15g后溶剂质量为185g,此时最多可溶解203.5g的硝酸钾,而此
时溶液中的溶质质量为50g。
故答案为: 玻璃棒,不饱和;
20%; ①
②C;
③不能,溶液II恒温蒸发15g后溶剂质量为185g,此时最多可溶解203.5g的硝酸钾,而此时
溶液中的溶质质量为50g。
【点评】本题难度不是很大,主要考查了固体的溶解度表所表示的意义,及根据固体的溶
解度表来解决相关的问题,从而培养分析问题、解决问题的能力。
八、简答题(共18分)
24.(10分)气体的制取是初中化学常见的实验(装置气密性均良好)。
第20页(共23页)实验室制取二氧化碳。
①I如图1所示,仪器m的名称是 锥形瓶 。从长颈漏斗中加入的试剂名称是 稀盐酸 。
Ⅱ将二氧化碳通入紫色石蕊试液中,观察到石蕊变 红 色。
Ⅲ用 向上排空气 法收集一瓶二氧化碳。证明二氧化碳已经收集满的方法是 将燃着
的木条置于集气瓶口,木条熄灭则已收集满 。
实验室制取氧气
②I如图2所示,取用二氧化锰操作正确的是 A (选填编号)。
Ⅱ用3%左右的双氧水可平稳地制取氧气。现有100g 15%的双氧水,为稀释成3%的双氧
水,需加入 40 0 g水。
Ⅲ如需制取0.1摩尔的氧气,所需过氧化氢的质量至少为多少克?(根据化学方程式列式
计算) 6.8 g 。
【分析】 I、根据常用仪器的名称、用途和制取二氧化碳的药品分析回答。
Ⅱ、根据①二氧化碳能与水化合生成了碳酸分析。
Ⅲ、根据二氧化碳的性质分析回答。
Ⅰ、根据二氧化锰是粉末状的药品分析加入试管中的操作。
②Ⅱ、根据溶质质量不变原理分析计算。
Ⅲ、根据化学方程式列式由氧气的物质的量计算出所需过氧化氢的质量。
【解答】解: I由图示可知,仪器m的名称是锥形瓶;制取二氧化碳用的药品是大理石和
稀盐酸,从①长颈漏斗中加入的试剂是液体试剂,名称是稀盐酸。
Ⅱ、将二氧化碳通入紫色石蕊试液中,二氧化碳能与水化合生成了碳酸,所以观察到石蕊
变红色。
Ⅲ、由于二氧化碳的密度大于空气,用向上排空气法收集一瓶二氧化碳。证明二氧化碳已
经收集满的方法是将燃着的木条置于集气瓶口,木条熄灭则已收集满。
I、由于二氧化锰是粉末状的药品,操作正确的是A;
②Ⅱ、设需要加水的质量为x
100g×15%=(100g+x)×3% 解得:x=400g
Ⅲ设需要过氧化氢物质的量为y
2H O 2H O+O ↑;
2 2 2 2
2 1
y .1mol
第21页(共23页)解得:y=0.2mol
过氧化氢的质量是0.mol×34g/mol=6.8g
故答为: Ⅰ锥形瓶,稀盐酸;Ⅱ红;Ⅲ向上排空气,将燃着的木条置于集气瓶口,木条熄
灭则已收①集满。 ⅠA;Ⅱ400g;Ⅲ6.8g。
【点评】本题主要②考查了二氧化碳、氧气的之前和计算的知识,难度不大,根据已有的知识
分析解答即可。
25.(8分)用如图实验装置验证一氧化碳与氧化铜反应的产物(固定装置省略、装置气密性
良好)。
(1)A处玻璃管中反应的化学方程式是 C+CO 2CO 。
2
(2)B中固体由黑变 红 ,反应的化学方程式是 CuO+CO Cu+CO ,说明一
2
氧化碳有 还原 性。
(3)有关该实验说法正确的是 d (选填编号)。
a.A中消耗的碳粉的物质的量等于B中消耗的一氧化碳的物质的量
b.C的作用是收集剩余的一氧化碳
c.点燃e处,火焰呈淡蓝色
d.B处玻璃管中固体减少的质量等于消耗的氧化铜中氧元素的质量
(4)如图实验装置设计还不能完全证明一氧化碳与氧化铜反应的产物,请说明理由 能使
澄清石灰水变浑浊的也可能是 A 中过量的二氧化碳 。
【分析】高温条件下,二氧化碳和碳反应生成一氧化碳,一氧化碳和氧化铜反应生成铜和
二氧化碳,二氧化碳能使澄清石灰水变浑浊;
一氧化碳燃烧生成二氧化碳,产生蓝色火焰。
【解答】解:(1)A处玻璃管中碳和二氧化碳在高温条件下反应生成一氧化碳,反应的化学
第22页(共23页)方程式是:C+CO 2CO。
2
故填:C+CO 2CO。
2
(2)B中固体由黑变红色,是因为一氧化碳和氧化铜反应生成了铜和二氧化碳,反应的化
学方程式是:CuO+CO Cu+CO ,说明一氧化碳有还原性。
2
故填:红;CuO+CO Cu+CO ;还原。
2
(3)a.由C+CO 2CO、2CuO+2CO 2Cu+2CO 可知,A中消耗的碳粉的物
2 2
质的量等于B中消耗的一氧化碳的物质的量的二分之一,该选项说法不正确;
b.C的作用是防止D中的液体倒吸入B装置中,该选项说法不正确;
c.点燃e处,一氧化碳燃烧,火焰呈蓝色,该选项说法不正确;
d.由CuO+CO Cu+CO 可知,B处玻璃管中固体减少的质量等于消耗的氧化铜中
2
氧元素的质量,该选项说法正确。
故填:d。
(4)如图实验装置设计还不能完全证明一氧化碳与氧化铜反应的产物,理由:能使澄清石
灰水变浑浊的也可能是A中过量的二氧化碳。
故填:能使澄清石灰水变浑浊的也可能是A中过量的二氧化碳。
【点评】本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行
分析、判断,从而得出正确的结论。
第23页(共23页)