文档内容
哈师大附中2025级2025-2026学年度第一学期期中考试 C.同物质的量浓度同体积 溶液与NaOH溶液混合:
化学试题
D.碳酸氢钙与少量澄清石灰水溶液反应:
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Fe 56 Cu 64
一、选择题(本题共20小题,1-10题每题2分,11-20每题3分,每题只有一个选项符合题意,共50
8.已知反应:① ② ③
分)
1.分类是学习和研究化学的重要方法,下列分类不合理的是
A.KCO 属于钾盐、碳酸盐 B.NaOH属于可溶性强碱
2 3
C.液氯属于混合物 D.CaO属于碱性氧化物
下列说法错误的是
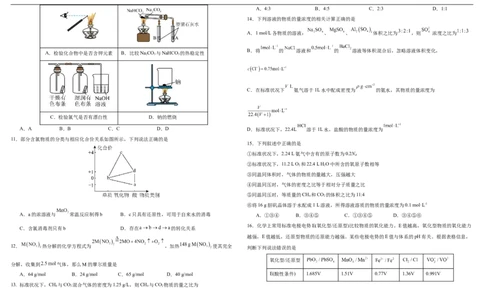
2.下列与实验室制备氢氧化铁胶体实验无关的图标是
A. 中 的化合价为 价
A. B. C. D. B.氧化性由强到弱的顺序为KBrO 3 >KClO 3 >Cl 2 >Br 2
C. 在①、③反应中均作氧化剂
3.下列物质中,属于电解质的是
A.熔融氯化钠 B.稀硫酸 C.乙醇 D.石墨 D.根据题中信息, 和 共存的溶液中加入 先发生反应
4.下列各组溶液澄清透明,且离子能大量共存的是
9.通过催化氧化可实现氯资源的再利用,其机理如下图所示,已知铜(Cu)元素的常见价态为0, 、
A.K+、Ag+、SO 、Cl- B.Cu2+、Mg2+、SO 、Cl- 。
C.H+、Na+、CO 、CHCOO- D.K+、Na+、HCO 、OH-
3
5.关于钠的化合物的用途,下列说法不正确的是
A.过氧化钠可作呼吸面具中的供氧剂 B.碳酸钠可用于治疗胃酸过多
C.氯化钠可作调味品 D.碳酸氢钠可作发酵粉
下列说法不正确的是
6.下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的是
A.催化循环中Cu的化合价只涉及 、 B.图中①~⑤有三个氧化还原反应
A.CuCl B.FeCl C.FeCl D.ZnCl
2 3 2 2
C.该方法中CuO可以循环利用 D.该转化的总反应
7.下列反应的离子方程式正确的是
10.实验是研究化学的基础,下图中所示的实验方法、装置或操作完全正确的是
A.向 中滴加少量溶液 :
B.向 溶液中通入少量 气体:A.4:3 B.4:5 C.2:3 D.1:1
14.下列溶液的物质的量浓度的相关计算正确的是
A.1 mol/L各物质的溶液: 、 、 体积之比为 ,则 浓度之比为
B.将 的 溶液和 的 溶液等体积混合后,忽略溶液体积变化,
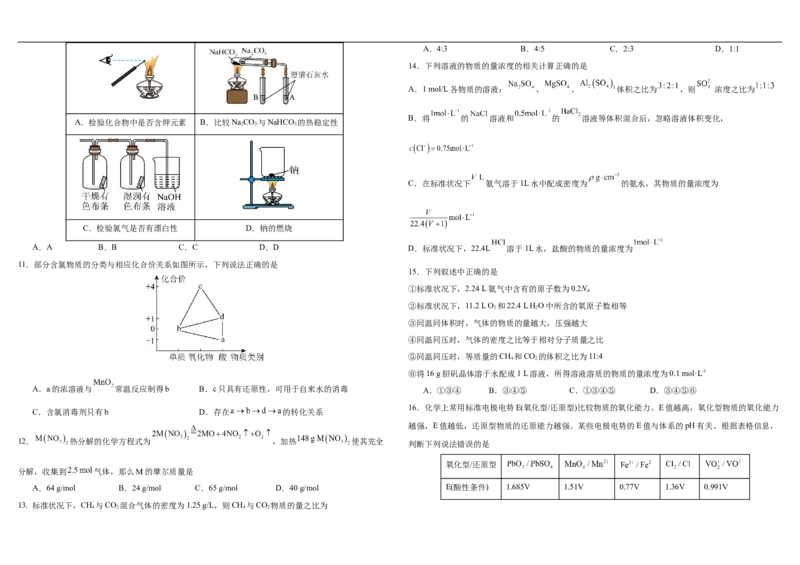
A.检验化合物中是否含钾元素 B.比较NaCO 与NaHCO 的热稳定性
2 3 3
C.在标准状况下 氨气溶于1L水中配成密度为 的氨水,其物质的量浓度为
C.检验氯气是否有漂白性 D.钠的燃烧
A.A B.B C.C D.D D.标准状况下,22.4L 溶于1L水,盐酸的物质的量浓度为
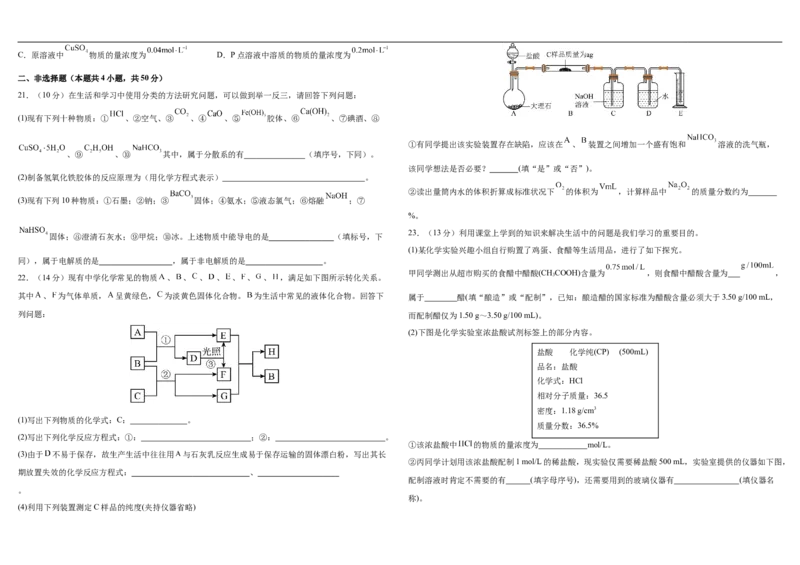
11.部分含氯物质的分类与相应化合价关系如图所示,下列说法正确的是
15.下列叙述中正确的是
①标准状况下,2.24 L氨气中含有的原子数为0.2N
A
②标准状况下,11.2 L O 和22.4 L H O中所含的氧原子数相等
2 2
③同温同体积时,气体的物质的量越大,压强越大
④同温同压时,气体的密度之比等于相对分子质量之比
⑤同温同压时,等质量的CH 和CO 的体积之比为11:4
4 2
⑥将16 g胆矾晶体溶于水配成1 L溶液,所得溶液溶质的物质的量浓度为0.1 mol·L-1
A.a的浓溶液与 常温反应制得b B.c只具有还原性,可用于自来水的消毒 A.①③④ B.③④⑤ C.①③④⑤ D.③④⑤⑥
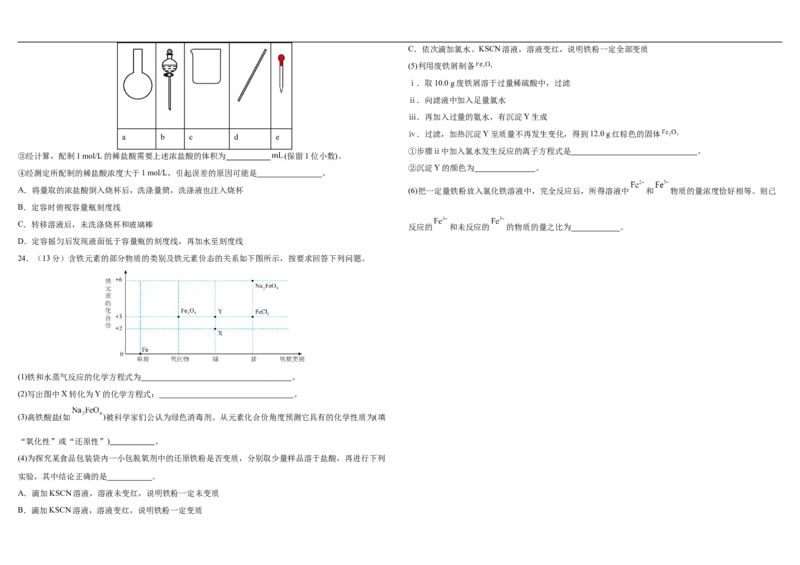
16.化学上常用标准电极电势E(氧化型/还原型)比较物质的氧化能力。E值越高,氧化型物质的氧化能力
C.含氯消毒剂只有b D.存在 的转化关系
越强,E值越低,还原型物质的还原能力越强。某些电极电势的E值与体系的pH有关。根据表格信息,
12. 热分解的化学方程式为 ,加热 使其完全
判断下列说法错误的是
氧化型/还原型
分解,收集到 气体,那么 的摩尔质量是
A.64 g/mol B.24 g/mol C.65 g/mol D.40 g/mol E(酸性条件) 1.685V 1.51V 0.77V 1.36V 0.991V
13. 标准状况下,CH 与CO 混合气体的密度为1.25 g/L,则CH 与CO 物质的量之比为
4 2 4 2A.实验室可用 与浓盐酸反应制备 B
B.酸性条件下,还原性强弱顺序为 C
C.向 酸化的含足量 的溶液中加入少量 ,可观察到黄绿色气体氯气产生 D
A.A B.B C.C D.D
D.该反应能发生:
19.向 500 mL 2.2 mol/L NaOH溶液中通入一定体积的CO 使其充分反应,再向所得溶液中逐滴滴加
2
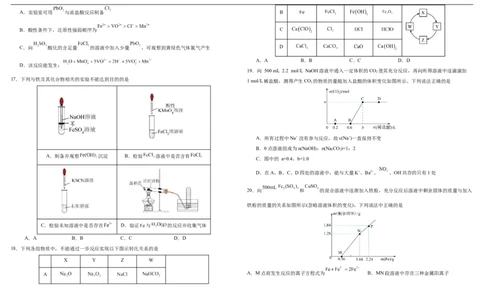
17.下列与铁及其化合物相关的实验不能达到目的的是
1 mol/L稀盐酸,测得产生CO 的物质的量随加入盐酸的体积变化如图所示。下列说法正确的是
2
A.所有过程中Na+ 没有参与反应,故c(Na+)一直保持不变
B.0点溶液组成为n(NaOH):n(Na CO)=1:2
2 3
A.制备并观察 沉淀 B.检验 溶液中是否含有
C.图中的 a=0.4,b=1.0
D.在A、B、C、D四处的溶液中,能与大量K+、Ba2+、 、OH-共存的只有1处
20.向 和 的混合溶液中逐渐加入铁粉,充分反应后溶液中剩余固体的质量与加入
铁粉的质量的关系如图所示(忽略溶液体积的变化)。下列说法中正确的是
C.检验未知溶液中是否存在 D.验证 与 的反应并收集气体
A.A B.B C.C D.D
18.下列各组物质中,不能通过一步反应实现以下图示转化关系的是
X Y Z W
A A.M点前发生反应的离子方程式为 B.MN段溶液中存在三种金属阳离子C.原溶液中 物质的量浓度为 D.P点溶液中溶质的物质的量浓度为
二、非选择题(本题共4小题,共50分)
21.(10分)在生活和学习中使用分类的方法研究问题,可以做到举一反三,请回答下列问题:
(1)现有下列十种物质:① 、②空气、③ 、④ 、⑤ 胶体、⑥ 、⑦碘酒、⑧
①有同学提出该实验装置存在缺陷,应该在 、 装置之间增加一个盛有饱和 溶液的洗气瓶,
、⑨ 、⑩ 其中,属于分散系的有 (填序号,下同)。
该同学想法是否必要? (填“是”或“否”)。
(2)制备氢氧化铁胶体的反应原理为(用化学方程式表示) 。
②读出量筒内水的体积折算成标准状况下 的体积为 ,计算样品中 的质量分数约为
(3)现有下列10种物质:①石墨;②钠;③ 固体;④氨水;⑤液态氯气;⑥熔融 ;⑦
%。
23.(13分)利用课堂上学到的知识来解决生活中的问题是我们学习的重要目的。
固体;⑧澄清石灰水;⑨甲烷;⑩冰。上述物质中能导电的是 (填标号,下
(1)某化学实验兴趣小组自行购置了鸡蛋、食醋等生活用品,进行了如下探究。
同),属于电解质的是 ,属于非电解质的是 。
甲同学测出从超市购买的食醋中醋酸(CHCOOH)含量为 ,则食醋中醋酸含量为 ,
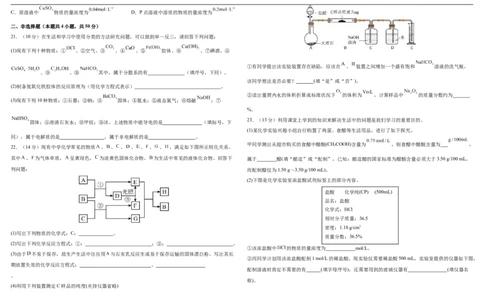
22.(14分)现有中学化学常见的物质 、 、 、 、 、 、 、 ,满足如下图所示转化关系。 3
其中 、 为气体单质, 呈黄绿色, 为淡黄色固体化合物。 为生活中常见的液体化合物。回答下 属于 醋(填“酿造”或“配制”,已知:酿造醋的国家标准为醋酸含量必须大于3.50 g/100 mL,
列问题: 而配制醋仅为1.50 g~3.50 g/100 mL)。
(2)下图是化学实验室浓盐酸试剂标签上的部分内容。
盐酸 化学纯(CP) (500mL)
品名:盐酸
化学式:HCl
相对分子质量:36.5
密度:1.18 g/cm3
(1)写出下列物质的化学式:C: 。
质量分数:36.5%
(2)写出下列化学反应方程式:①: ;②: 。
①该浓盐酸中 的物质的量浓度为 mol/L。
(3)由于 不易于保存,故生产生活中往往用 与石灰乳反应生成易于保存运输的固体漂白粉,写出其长
②丙同学计划用该浓盐酸配制1 mol/L的稀盐酸,现实验仅需要稀盐酸500 mL,实验室提供的仪器如下图,
期放置失效的化学反应方程式: 、
配制溶液时肯定不需要的有 (填字母序号),还需要用到的玻璃仪器有 (填仪器名
。
称)。
(4)利用下列装置测定C样品的纯度(夹持仪器省略)C.依次滴加氯水、KSCN溶液,溶液变红,说明铁粉一定全部变质
(5)利用废铁屑制备
ⅰ.取10.0 g废铁屑溶于过量稀硫酸中,过滤
ⅱ.向滤液中加入足量氯水
ⅲ.再加入过量的氨水,有沉淀Y生成
ⅳ.过滤,加热沉淀Y至质量不再发生变化,得到12.0 g红棕色的固体
a b c d e
①步骤ⅱ中加入氯水发生反应的离子方程式是 。
③经计算,配制1 mol/L的稀盐酸需要上述浓盐酸的体积为 (保留1位小数)。
②沉淀Y的颜色为 。
④经测定所配制的稀盐酸浓度大于1 mol/L,引起误差的原因可能是 。
A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入烧杯 (6)把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中 和 物质的量浓度恰好相等。则已
B.定容时俯视容量瓶刻度线
C.转移溶液后,未洗涤烧杯和玻璃棒
反应的 和未反应的 的物质的量之比为 。
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
24.(13分)含铁元素的部分物质的类别及铁元素价态的关系如下图所示,按要求回答下列问题。
(1)铁和水蒸气反应的化学方程式为 。
(2)写出图中X转化为Y的化学方程式: 。
(3)高铁酸盐(如 )被科学家们公认为绿色消毒剂。从元素化合价角度预测它具有的化学性质为(填
“氧化性”或“还原性”) 。
(4)为探究某食品包装袋内一小包脱氧剂中的还原铁粉是否变质,分别取少量样品溶于盐酸,再进行下列
实验,其中结论正确的是 。
A.滴加KSCN溶液,溶液未变红,说明铁粉一定未变质
B.滴加KSCN溶液,溶液变红,说明铁粉一定变质