文档内容
2024年上海市长宁区中考化学二模试卷
相对原子质量:H-1 O-16 N-14 S-32 Cu-64 Zn-65 Fe-56 Ba-137
一、选择题。(共20分)1~14每题均只有1个正确选项,每题1分;15~17每题均有1~2个正确选项,
每题2分。
1.(1分)Na O可用于制备钠的化合物。它属于( )
2
A.单质 B.氧化物 C.碱 D.盐
2.(1分)Na O中钠元素的化合价为( )
2
A.﹣2 B.+1 C.+2 D.+4
3.(1分)灼烧氯化钠,火焰呈( )
A.黄色 B.红色 C.绿色 D.紫色
4.(1分)氧化钠能与水反应,化学方程式为Na O+H O═2NaOH,该反应属于( )
2 2
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
5.(1分)氢氧化钠中所含原子团的名称是( )
A.氢氧根 B.氧氢根 C.氧钠根 D.氧化钠
6.(1分)氢氧化钠溶液的pH可能是( )
A.1 B.5 C.7 D.14
7.(1分)能与氢氧化钠溶液发生反应的是( )
A.Mg B.Fe O C.CuSO D.KCl
2 3 4
8.(1分)属于中和反应的是( )
A.2KOH+CO ═K CO +H O
2 2 3 2
B.Na O+2HCl═2NaCl+H O
2 2
C.2NaOH+H SO ═Na SO +2H O
2 4 2 4 2
D.K CO +2HCl═2KCl+H O+CO ↑
2 3 2 2
9.(1分)称量10.0g氢氧化钠固体必须用到的玻璃仪器是( )
A.烧杯 B.电子天平 C.称量纸 D.玻璃棒
10.(1分)属于氢氧化钠溶液性质的是( )
A.久置后会分层
B.上层溶液腐蚀性更强
C.不饱和的溶液一定是稀溶液
D.上下层溶液的浓度一致11.(1分)能利用氢氧化钠溶液制得的是( )
A.KOH B.K CO C.Na CO D.Ca(OH)
2 3 2 3 2
12.(1分)能表示两个氮气分子的是( )
A.2N B.N C.2N D.2N
2 2 3
13.(1分)能区分氮气和一氧化碳的方法是( )
A.闻气味 B.观察颜色
C.倒入澄清石灰水 D.通入灼热的氧化铜
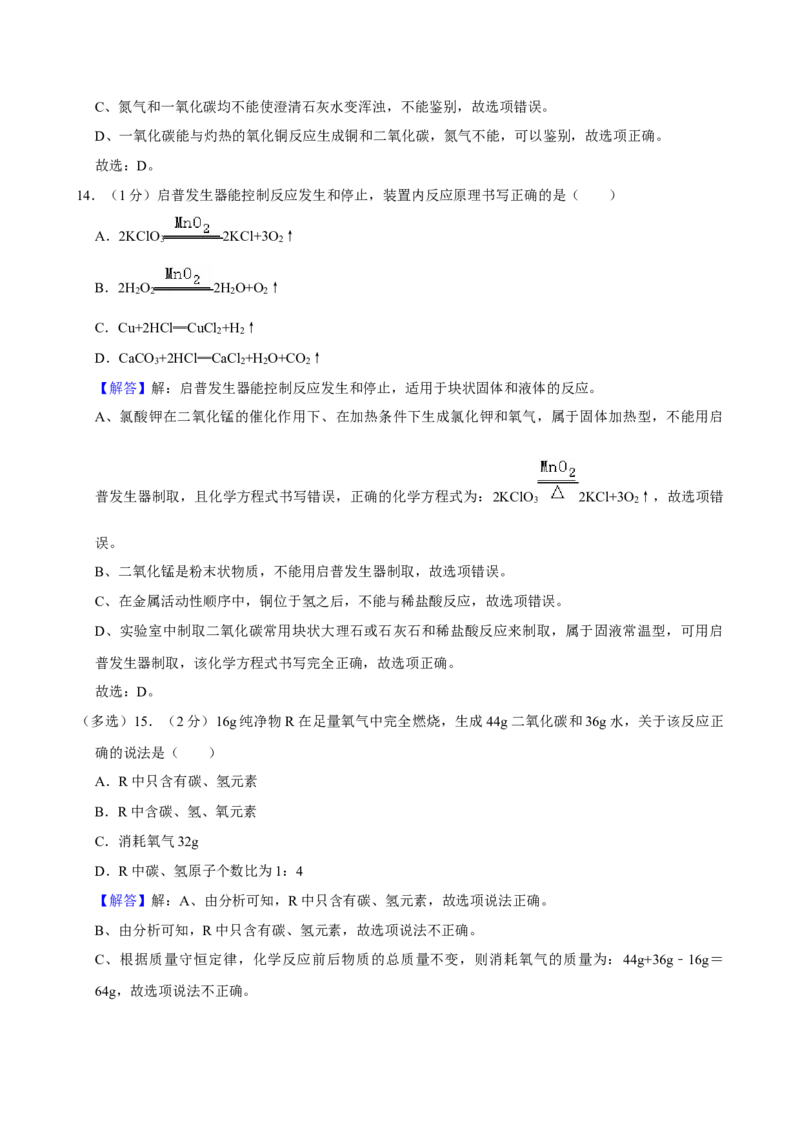
14.(1分)启普发生器能控制反应发生和停止,装置内反应原理书写正确的是( )
A.2KClO 2KCl+3O ↑
3 2
B.2H O 2H O+O ↑
2 2 2 2
C.Cu+2HCl═CuCl +H ↑
2 2
D.CaCO +2HCl═CaCl +H O+CO ↑
3 2 2 2
(多选)15.(2分)16g纯净物R在足量氧气中完全燃烧,生成44g二氧化碳和36g水,关于该反应正
确的说法是( )
A.R中只含有碳、氢元素
B.R中含碳、氢、氧元素
C.消耗氧气32g
D.R中碳、氢原子个数比为1:4
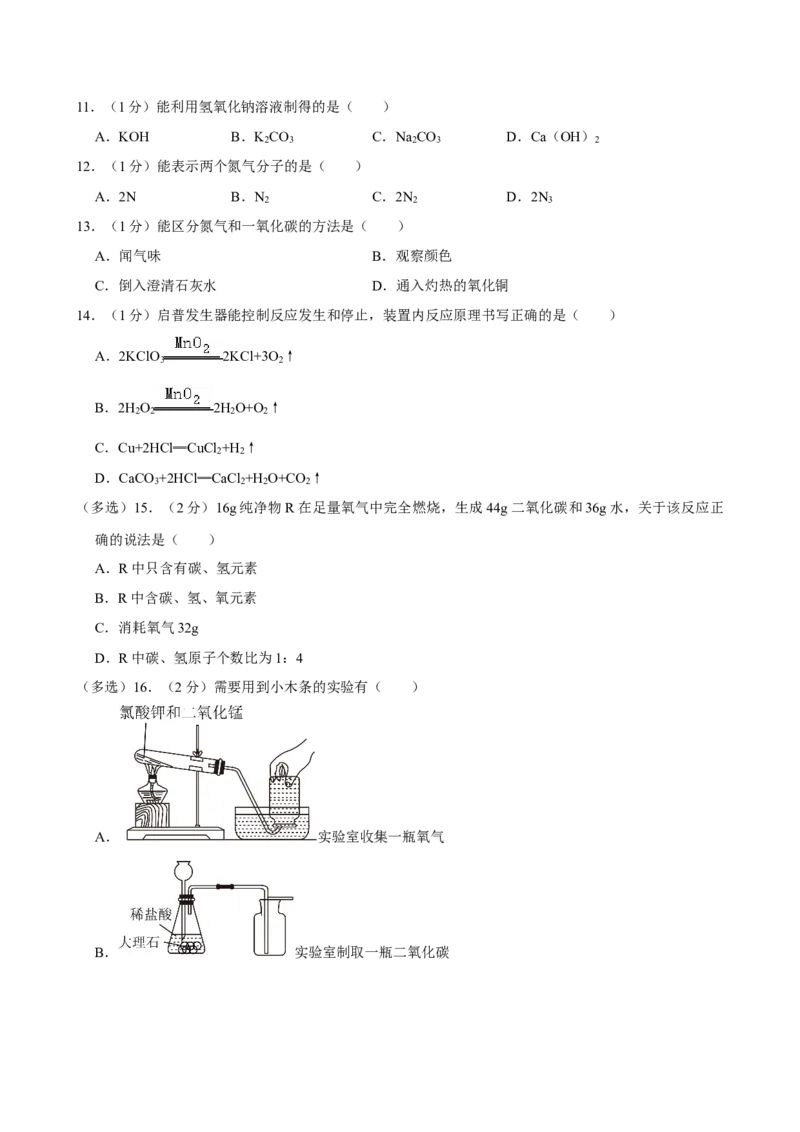
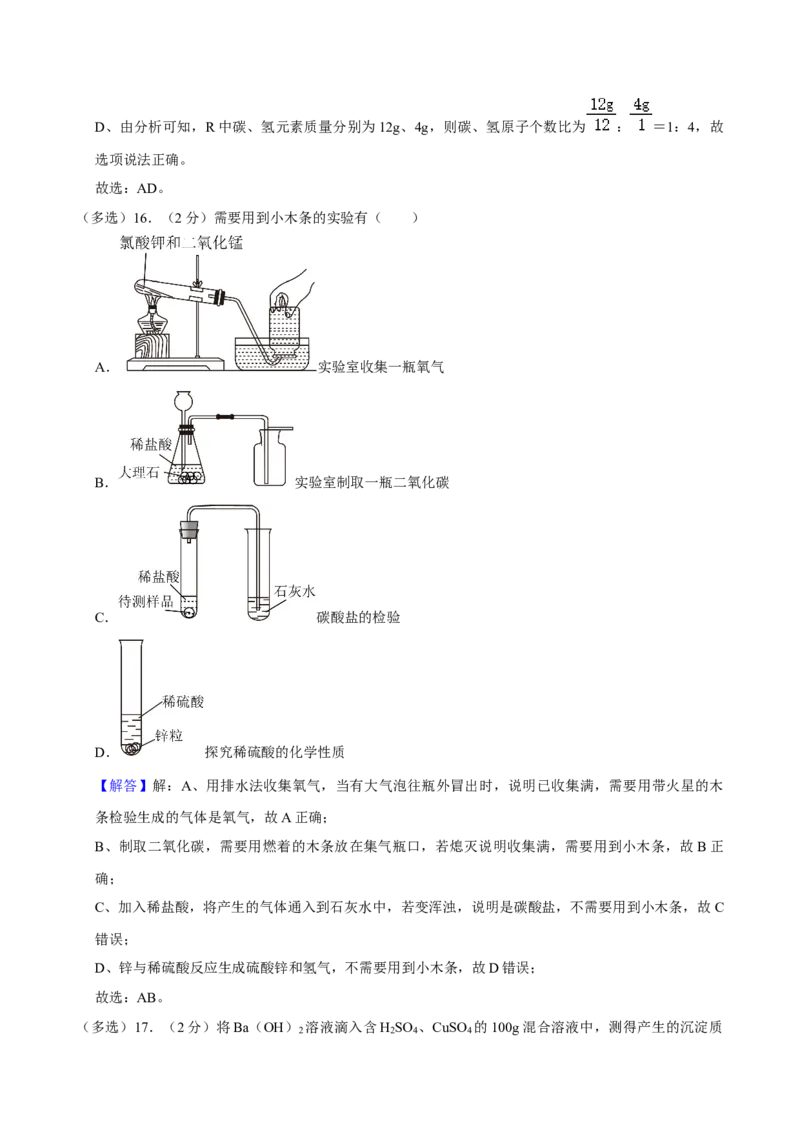
(多选)16.(2分)需要用到小木条的实验有( )
A. 实验室收集一瓶氧气
B. 实验室制取一瓶二氧化碳C. 碳酸盐的检验
D. 探究稀硫酸的化学性质
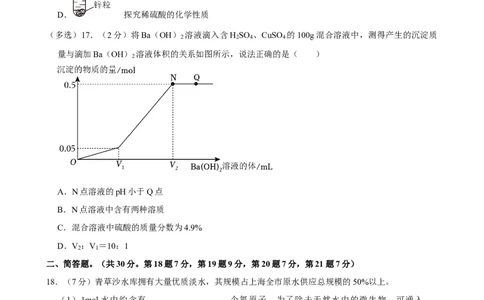
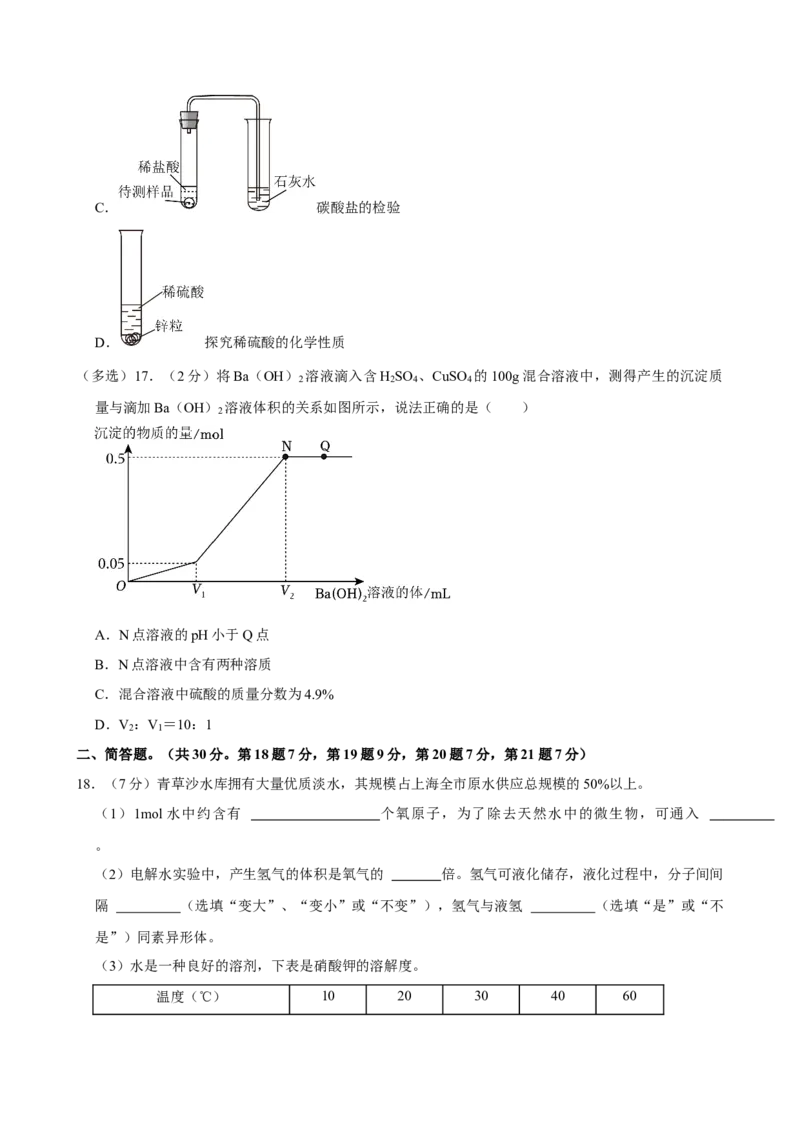
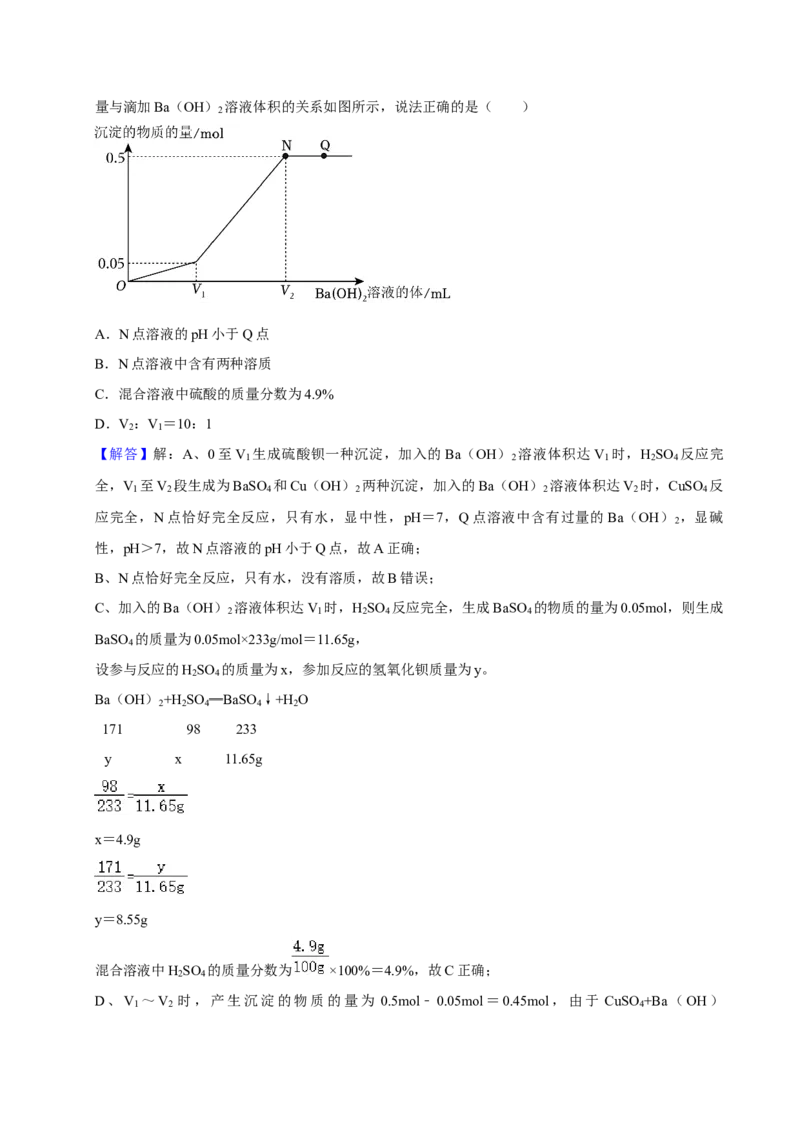
(多选)17.(2分)将Ba(OH) 溶液滴入含H SO 、CuSO 的100g混合溶液中,测得产生的沉淀质
2 2 4 4
量与滴加Ba(OH) 溶液体积的关系如图所示,说法正确的是( )
2
A.N点溶液的pH小于Q点
B.N点溶液中含有两种溶质
C.混合溶液中硫酸的质量分数为4.9%
D.V :V =10:1
2 1
二、简答题。(共30分。第18题7分,第19题9分,第20题7分,第21题7分)
18.(7分)青草沙水库拥有大量优质淡水,其规模占上海全市原水供应总规模的50%以上。
(1)1mol水中约含有 个氧原子,为了除去天然水中的微生物,可通入
。
(2)电解水实验中,产生氢气的体积是氧气的 倍。氢气可液化储存,液化过程中,分子间间
隔 (选填“变大”、“变小”或“不变”),氢气与液氢 (选填“是”或“不
是”)同素异形体。
(3)水是一种良好的溶剂,下表是硝酸钾的溶解度。
温度(℃) 10 20 30 40 60溶解度(g/100g水) 20.9 31.6 45.8 63.9 110
20℃时,在烧杯中加入50g硝酸钾固体和100mL水,充分溶解后得到的是硝酸钾的 (选
填“饱和”或“不饱和”)溶液,为了提升溶液的浓度,可进行的实验操作是 。
19.(9分)新中国成立70年来,我国化学工业得到长足发展。
(1)积极开发燃料酒精等石油替代品。酒精(C H O)属于 (选填“有机物”或“无机
2 6
物”),酒精燃烧属于 (选填“物理变化”或“化学变化”)。
(2)充分利用化石能源。对煤进行脱硫处理,避免燃烧产生二氧化硫,防止产生 。将煤进
行粉碎,并鼓入大量空气进行燃烧,其目的是 。
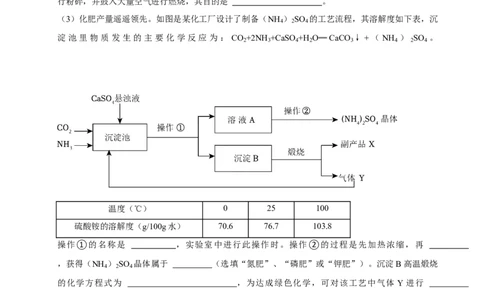
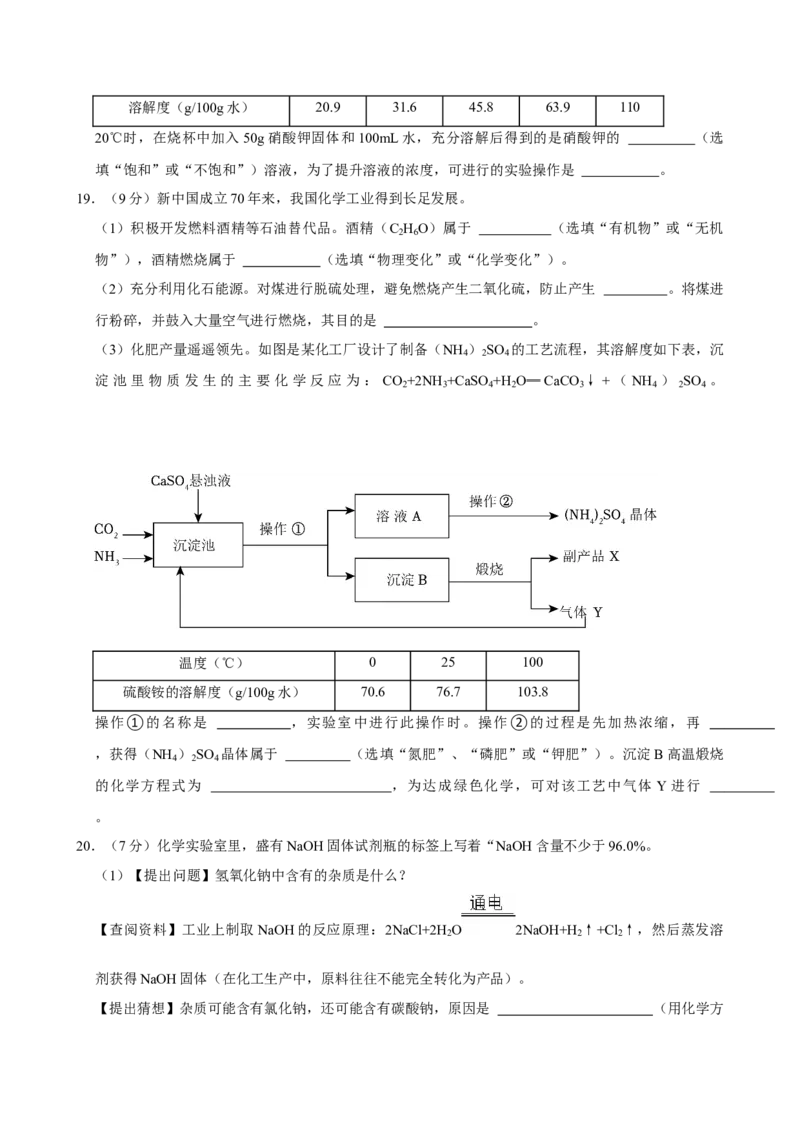
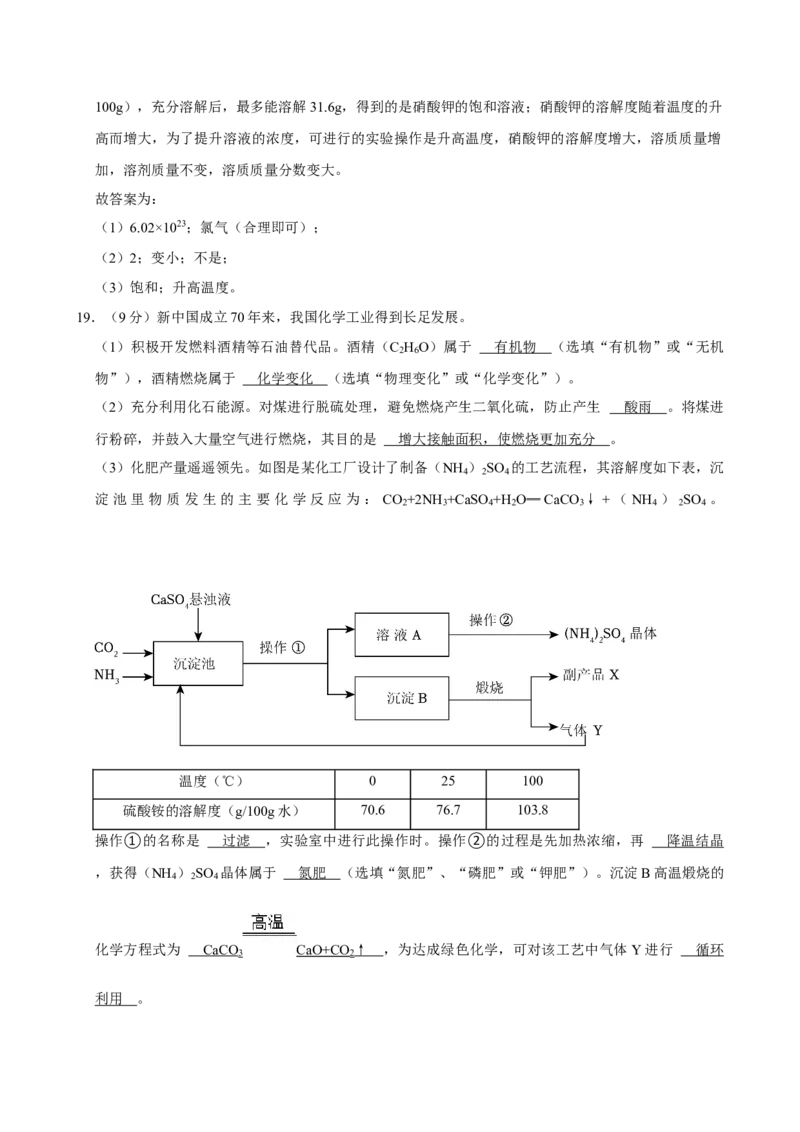
(3)化肥产量遥遥领先。如图是某化工厂设计了制备(NH ) SO 的工艺流程,其溶解度如下表,沉
4 2 4
淀池里物质发生的主要化学反应为: CO +2NH +CaSO +H O═CaCO ↓+(NH ) SO 。
2 3 4 2 3 4 2 4
温度(℃) 0 25 100
硫酸铵的溶解度(g/100g水) 70.6 76.7 103.8
操作①的名称是 ,实验室中进行此操作时。操作②的过程是先加热浓缩,再
,获得(NH ) SO 晶体属于 (选填“氮肥”、“磷肥”或“钾肥”)。沉淀B高温煅烧
4 2 4
的化学方程式为 ,为达成绿色化学,可对该工艺中气体 Y 进行
。
20.(7分)化学实验室里,盛有NaOH固体试剂瓶的标签上写着“NaOH含量不少于96.0%。
(1)【提出问题】氢氧化钠中含有的杂质是什么?
【查阅资料】工业上制取NaOH的反应原理:2NaCl+2H O 2NaOH+H ↑+Cl ↑,然后蒸发溶
2 2 2
剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
【提出猜想】杂质可能含有氯化钠,还可能含有碳酸钠,原因是 (用化学方程式表示)。
(2)【设计实验】取样溶于水,并分成两份。
步骤1:向一份溶液中滴加酚酞试液,溶液变 。
步骤2:向另一份溶液中滴加过量的稀硝酸,先无明显现象后产生气泡。
步骤3:向步骤2所得溶液中继续滴加 溶液,产生白色沉淀。
(3)【实验结论与反思】杂质中含有 。上述实验中步骤 (填序号)是没有
必要进行的。实验中,滴加稀硝酸至过量的目的是 。
21.(7分)镀锌铁片是指在铁上进行双面镀锌而制成的一种锌铁合金。
(1)对铁片镀锌的目的是为了防止铁被空气中的 (填写化学式)氧化生锈,针对日常生活
中的铁锈,可用 (填写化学式)来除锈。
(2)测量镀锌铁片表面镀锌层的厚度。
步骤1:剪下一块表面积为9.1cm2的镀锌铁片,称量,记录质量为17.6g。
步骤2:将镀锌铁片放入过量稀硫酸中,一开始能观察到大量气泡,此时反应的化学方程式为
。
步骤3:待镀锌铁片表面气泡明显减少后,用蒸馏水清洗,并擦干,称量,记录质量为16.3g。
假设上述反应只有一种金属参与,产生氢气 mol。通过锌的密度计算得到该镀锌铁片的单面
镀锌层厚度为0.01cm。该实验结果 (选填“大于”、“小于”或“等于”)实际镀锌铁片厚
度,理由是 。参考答案与试题解析
一、选择题。(共20分)1~14每题均只有1个正确选项,每题1分;15~17每题均有1~2个正确选项,
每题2分。
1.(1分)Na O可用于制备钠的化合物。它属于( )
2
A.单质 B.氧化物 C.碱 D.盐
【解答】解:Na O是由两种元素组成,且其中有一种元素是氧元素的化合物,因此,该物质属于氧化
2
物。
故选:B。
2.(1分)Na O中钠元素的化合价为( )
2
A.﹣2 B.+1 C.+2 D.+4
【解答】解:在化合物中正负化合价代数和为零,Na O中,氧元素显﹣2,设钠元素的化合价是x,
2
2x+(﹣2)=0,则x=+1。
故选:B。
3.(1分)灼烧氯化钠,火焰呈( )
A.黄色 B.红色 C.绿色 D.紫色
【解答】解:多种金属或它们的化合物在灼烧时,会使火焰呈现特殊的颜色,化学上叫焰色反应;氯
化钠中含有钠元素,属于钠盐,灼烧氯化钠时火焰的颜色呈黄色。
故选:A。
4.(1分)氧化钠能与水反应,化学方程式为Na O+H O═2NaOH,该反应属于( )
2 2
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
【解答】解:A、化合反应是有两种或两种以上的物质生成一种物质的化学反应,Na O+H O═2NaOH
2 2
属于化合反应;故选项正确;
B、分解反应是由一种物质生成两种或两种以上的物质的反应,故选项错误;
C、置换反应是一种单质和一种化合物反应生成另一种单质和另一种化合物的化学反应,故选项错
误;
D、复分解反应是两种化合物互相交换成分生成另外两种化合物的反应,故选项错误;故选:A。
5.(1分)氢氧化钠中所含原子团的名称是( )
A.氢氧根 B.氧氢根 C.氧钠根 D.氧化钠
【解答】解:氢氧化钠是离子化合物,由钠离子和氢氧根离子构成,其中氢氧根属于原子团。
故选:A。
6.(1分)氢氧化钠溶液的pH可能是( )
A.1 B.5 C.7 D.14
【解答】解:氢氧化钠是一种碱,其水溶液显碱性,pH大于7,氢氧化钠溶液的pH可能是14。
故选:D。
7.(1分)能与氢氧化钠溶液发生反应的是( )
A.Mg B.Fe O C.CuSO D.KCl
2 3 4
【解答】解:A、镁不能和氢氧化钠非国有,该选项不正确。
B、氧化铁不能和氢氧化钠反应,该选项不正确。
C、硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,该选项正确。
D、氯化钾不能和氢氧化钠反应,该选项不正确。
故选:C。
8.(1分)属于中和反应的是( )
A.2KOH+CO ═K CO +H O
2 2 3 2
B.Na O+2HCl═2NaCl+H O
2 2
C.2NaOH+H SO ═Na SO +2H O
2 4 2 4 2
D.K CO +2HCl═2KCl+H O+CO ↑
2 3 2 2
【解答】解:A、该反应的反应物是碱和非金属氧化物,不是酸与碱的反应,不属于中和反应,故选
项错误。
B、该反应的反应物是酸和金属氧化物,不是酸与碱的反应,不属于中和反应,故选项错误。
C、该反应的反应物是酸和碱,生成物是盐和水,属于中和反应,故选项正确。
D、该反应的反应物是酸和盐,不是酸与碱的反应,不属于中和反应,故选项错误。
故选:C。
9.(1分)称量10.0g氢氧化钠固体必须用到的玻璃仪器是( )
A.烧杯 B.电子天平 C.称量纸 D.玻璃棒
【解答】解:称量10.0g氢氧化钠固体需要的仪器:托盘天平(或电子天平)、药匙、烧杯(由于氢
氧化钠具有腐蚀性和吸水性,不能使用称量纸),其中烧杯属于玻璃仪器。故选:A。
10.(1分)属于氢氧化钠溶液性质的是( )
A.久置后会分层
B.上层溶液腐蚀性更强
C.不饱和的溶液一定是稀溶液
D.上下层溶液的浓度一致
【解答】解:A、溶液具有稳定性,久置后不会分层,故选项说法错误。
B、溶液具有均一性,上层、下层的溶液腐蚀性相同,故选项说法错误。
C、溶液是否饱和与溶液的浓稀没有必然联系,不饱和的溶液不一定是稀溶液,也可能是浓溶液,故
选项说法错误。
D、溶液具有均一性,下层溶液的浓度一致,故选项说法正确。
故选:D。
11.(1分)能利用氢氧化钠溶液制得的是( )
A.KOH B.K CO C.Na CO D.Ca(OH)
2 3 2 3 2
【解答】解:A、氢氧化钠不能和其它物质反应生成氢氧化钾,该选项不正确。
B、氢氧化钠不能和其它物质反应生成碳酸钾,该选项不正确。
C、氢氧化钠和二氧化碳反应生成碳酸钠和水,该选项正确。
D、氢氧化钠不能和其它物质反应生成氢氧化钙,该选项不正确。
故选:C。
12.(1分)能表示两个氮气分子的是( )
A.2N B.N C.2N D.2N
2 2 3
【解答】解:A.2N表示2个氮原子,故A错误;
B.N 表示一个氮气分子,故B错误;
2
C.2N 表示两个氮气分子,故C正确;
2
D.2N 不表示两个氮气分子,故D错误。
3
故选:C。
13.(1分)能区分氮气和一氧化碳的方法是( )
A.闻气味 B.观察颜色
C.倒入澄清石灰水 D.通入灼热的氧化铜
【解答】解:A、氮气和一氧化碳均没有气味,用闻气味的方法不能鉴别,故选项错误。
B、氮气和一氧化碳均没有颜色,用观察颜色的方法不能鉴别,故选项错误。C、氮气和一氧化碳均不能使澄清石灰水变浑浊,不能鉴别,故选项错误。
D、一氧化碳能与灼热的氧化铜反应生成铜和二氧化碳,氮气不能,可以鉴别,故选项正确。
故选:D。
14.(1分)启普发生器能控制反应发生和停止,装置内反应原理书写正确的是( )
A.2KClO 2KCl+3O ↑
3 2
B.2H O 2H O+O ↑
2 2 2 2
C.Cu+2HCl═CuCl +H ↑
2 2
D.CaCO +2HCl═CaCl +H O+CO ↑
3 2 2 2
【解答】解:启普发生器能控制反应发生和停止,适用于块状固体和液体的反应。
A、氯酸钾在二氧化锰的催化作用下、在加热条件下生成氯化钾和氧气,属于固体加热型,不能用启
普发生器制取,且化学方程式书写错误,正确的化学方程式为:2KClO 2KCl+3O ↑,故选项错
3 2
误。
B、二氧化锰是粉末状物质,不能用启普发生器制取,故选项错误。
C、在金属活动性顺序中,铜位于氢之后,不能与稀盐酸反应,故选项错误。
D、实验室中制取二氧化碳常用块状大理石或石灰石和稀盐酸反应来制取,属于固液常温型,可用启
普发生器制取,该化学方程式书写完全正确,故选项正确。
故选:D。
(多选)15.(2分)16g纯净物R在足量氧气中完全燃烧,生成44g二氧化碳和36g水,关于该反应正
确的说法是( )
A.R中只含有碳、氢元素
B.R中含碳、氢、氧元素
C.消耗氧气32g
D.R中碳、氢原子个数比为1:4
【解答】解:A、由分析可知,R中只含有碳、氢元素,故选项说法正确。
B、由分析可知,R中只含有碳、氢元素,故选项说法不正确。
C、根据质量守恒定律,化学反应前后物质的总质量不变,则消耗氧气的质量为:44g+36g﹣16g=
64g,故选项说法不正确。D、由分析可知,R中碳、氢元素质量分别为12g、4g,则碳、氢原子个数比为 : =1:4,故
选项说法正确。
故选:AD。
(多选)16.(2分)需要用到小木条的实验有( )
A. 实验室收集一瓶氧气
B. 实验室制取一瓶二氧化碳
C. 碳酸盐的检验
D. 探究稀硫酸的化学性质
【解答】解:A、用排水法收集氧气,当有大气泡往瓶外冒出时,说明已收集满,需要用带火星的木
条检验生成的气体是氧气,故A正确;
B、制取二氧化碳,需要用燃着的木条放在集气瓶口,若熄灭说明收集满,需要用到小木条,故B正
确;
C、加入稀盐酸,将产生的气体通入到石灰水中,若变浑浊,说明是碳酸盐,不需要用到小木条,故C
错误;
D、锌与稀硫酸反应生成硫酸锌和氢气,不需要用到小木条,故D错误;
故选:AB。
(多选)17.(2分)将Ba(OH) 溶液滴入含H SO 、CuSO 的100g混合溶液中,测得产生的沉淀质
2 2 4 4量与滴加Ba(OH) 溶液体积的关系如图所示,说法正确的是( )
2
A.N点溶液的pH小于Q点
B.N点溶液中含有两种溶质
C.混合溶液中硫酸的质量分数为4.9%
D.V :V =10:1
2 1
【解答】解:A、0至V 生成硫酸钡一种沉淀,加入的Ba(OH) 溶液体积达V 时,H SO 反应完
1 2 1 2 4
全,V 至V 段生成为BaSO 和Cu(OH) 两种沉淀,加入的Ba(OH) 溶液体积达V 时,CuSO 反
1 2 4 2 2 2 4
应完全,N点恰好完全反应,只有水,显中性,pH=7,Q点溶液中含有过量的Ba(OH) ,显碱
2
性,pH>7,故N点溶液的pH小于Q点,故A正确;
B、N点恰好完全反应,只有水,没有溶质,故B错误;
C、加入的Ba(OH) 溶液体积达V 时,H SO 反应完全,生成BaSO 的物质的量为0.05mol,则生成
2 1 2 4 4
BaSO 的质量为0.05mol×233g/mol=11.65g,
4
设参与反应的H SO 的质量为x,参加反应的氢氧化钡质量为y。
2 4
Ba(OH) +H SO ═BaSO ↓+H O
2 2 4 4 2
171 98 233
y x 11.65g
x=4.9g
y=8.55g
混合溶液中H SO 的质量分数为 ×100%=4.9%,故C正确;
2 4
D、V ~V 时,产生沉淀的物质的量为 0.5mol﹣0.05mol=0.45mol,由于 CuSO +Ba(OH)
1 2 4═BaSO ↓+Cu(OH) ↓,产生BaSO 和Cu(OH) 的物质的量为1:1,故BaSO 和Cu(OH) 的
2 4 2 4 2 4 2
物质的量均为 =0.225mol,生成BaSO 的质量为0.225mol×233g/mol=52.425g,
4
设参加反应的氢氧化钡的质量为z。
CuSO +Ba(OH) ═BaSO ↓+Cu(OH) ↓
4 2 4 2
171 233
z 52.425g
z=38.475g
所使用Ba(OH) 溶液相同,则V :V =(38.475g+8.55g):8.55g=11:2,故D错误;
2 2 1
故选:AC。
二、简答题。(共30分。第18题7分,第19题9分,第20题7分,第21题7分)
18.(7分)青草沙水库拥有大量优质淡水,其规模占上海全市原水供应总规模的50%以上。
(1)1mol水中约含有 6.02×1 0 2 3 个氧原子,为了除去天然水中的微生物,可通入 氯气(合理
即可) 。
(2)电解水实验中,产生氢气的体积是氧气的 2 倍。氢气可液化储存,液化过程中,分子间间隔
变小 (选填“变大”、“变小”或“不变”),氢气与液氢 不是 (选填“是”或“不是”)同
素异形体。
(3)水是一种良好的溶剂,下表是硝酸钾的溶解度。
温度(℃) 10 20 30 40 60
溶解度(g/100g水) 20.9 31.6 45.8 63.9 110
20℃时,在烧杯中加入50g硝酸钾固体和100mL水,充分溶解后得到的是硝酸钾的 饱和 (选
填“饱和”或“不饱和”)溶液,为了提升溶液的浓度,可进行的实验操作是 升高温度 。
【解答】解:(1)1mol水中约含有6.02×1023个水分子,一个水分子含有1个氧原子,故1mol水中约
含有6.02×1023个氢原子。为了除去天然水中的微生物,可通入氯气(合理即可)。
(2)电解水时,与电源负极相连的玻璃管内的气体体积多,是氢气;与电源正极相连的玻璃管内产生
的气体体积少,是氧气;且两者的体积之比大约是2:1,即产生氢气的体积是氧气的2倍;氢气可液
化储存,液化过程中,分子间间隔变小。
液氢是液态的氢气,与氢气是同一种物质,不是同素异形体。
(3)20℃时,硝酸钾的溶解度为 31.6g,20℃时,在烧杯中加入 50g硝酸钾固体和 100mL水(合100g),充分溶解后,最多能溶解31.6g,得到的是硝酸钾的饱和溶液;硝酸钾的溶解度随着温度的升
高而增大,为了提升溶液的浓度,可进行的实验操作是升高温度,硝酸钾的溶解度增大,溶质质量增
加,溶剂质量不变,溶质质量分数变大。
故答案为:
(1)6.02×1023;氯气(合理即可);
(2)2;变小;不是;
(3)饱和;升高温度。
19.(9分)新中国成立70年来,我国化学工业得到长足发展。
(1)积极开发燃料酒精等石油替代品。酒精(C H O)属于 有机物 (选填“有机物”或“无机
2 6
物”),酒精燃烧属于 化学变化 (选填“物理变化”或“化学变化”)。
(2)充分利用化石能源。对煤进行脱硫处理,避免燃烧产生二氧化硫,防止产生 酸雨 。将煤进
行粉碎,并鼓入大量空气进行燃烧,其目的是 增大接触面积,使燃烧更加充分 。
(3)化肥产量遥遥领先。如图是某化工厂设计了制备(NH ) SO 的工艺流程,其溶解度如下表,沉
4 2 4
淀池里物质发生的主要化学反应为: CO +2NH +CaSO +H O═CaCO ↓+(NH ) SO 。
2 3 4 2 3 4 2 4
温度(℃) 0 25 100
硫酸铵的溶解度(g/100g水) 70.6 76.7 103.8
操作①的名称是 过滤 ,实验室中进行此操作时。操作②的过程是先加热浓缩,再 降温结晶
,获得(NH ) SO 晶体属于 氮肥 (选填“氮肥”、“磷肥”或“钾肥”)。沉淀B高温煅烧的
4 2 4
化学方程式为 CaCO CaO+CO ↑ ,为达成绿色化学,可对该工艺中气体Y进行 循环
3 2
利用 。【解答】解:(1)含有碳元素的化合物为有机物,酒精(C H O)属于有机物;酒精燃烧产生二氧化
2 6
碳和水,有新物质产生,属于化学变化;
(2)充分利用化石能源。对煤进行脱硫处理,避免燃烧产生二氧化硫,防止产生酸雨。将煤进行粉
碎,并鼓入大量空气进行燃烧,其目的是增大接触面积,使燃烧更加充分;
(3)操作①是把溶液与沉淀分离开,故为过滤操作;操作②的过程是先加热浓缩,再降温结晶,获
得(NH ) SO 晶体;硫酸铵中含有氮元素,属于氮肥;沉淀池里物质发生的主要化学反应为:
4 2 4
CO +2NH +CaSO +H O═CaCO ↓+(NH ) SO 。因此沉淀 B 高温煅烧的化学方程式为 CaCO
2 3 4 2 3 4 2 4 3
CaO+CO ↑;Y为二氧化碳,二氧化碳直接排放,易引起温室效应;为达成绿色化学,可对
2
该工艺中气体Y进行循环利用。
故答案为:
(1)有机物;化学变化;
(2)酸雨;增大接触面积,使燃烧更加充分;
(3)过滤;降温结晶;氮肥;CaCO CaO+CO ↑;循环利用。
3 2
20.(7分)化学实验室里,盛有NaOH固体试剂瓶的标签上写着“NaOH含量不少于96.0%。
(1)【提出问题】氢氧化钠中含有的杂质是什么?
【查阅资料】工业上制取NaOH的反应原理:2NaCl+2H O 2NaOH+H ↑+Cl ↑,然后蒸发溶
2 2 2
剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
【提出猜想】杂质可能含有氯化钠,还可能含有碳酸钠,原因是 CO +2NaOH = Na CO +H O (用
2 2 3 2
化学方程式表示)。
(2)【设计实验】取样溶于水,并分成两份。
步骤1:向一份溶液中滴加酚酞试液,溶液变 红色 。
步骤2:向另一份溶液中滴加过量的稀硝酸,先无明显现象后产生气泡。
步骤3:向步骤2所得溶液中继续滴加 硝酸银 溶液,产生白色沉淀。
(3)【实验结论与反思】杂质中含有 氯化钠、碳酸钠 。上述实验中步骤 1 (填序号)是没
有必要进行的。实验中,滴加稀硝酸至过量的目的是 检验碳酸钠,并除尽氢氧化钠和碳酸钠,排除
对氯化钠检验的干扰 。【解答】解:(1)杂质可能含有氯化钠,还可能含有碳酸钠,原因是氢氧化钠会与空气中的二氧化碳
反应生成碳酸钠和水,反应的化学方程式为CO +2NaOH=Na CO +H O;
2 2 3 2
(2)步骤1:氢氧化钠溶液显碱性,能使无色酚酞试液变红,则向一份溶液中滴加酚酞试液,溶液变
红色;
步骤3:步骤2中滴加过量的稀硝酸除尽了氢氧化钠和碳酸钠,氯化钠与硝酸银溶液反应生成硝酸钠
和不溶于稀硝酸的白色沉淀氯化银,实验现象是产生白色沉淀,则向步骤2所得溶液中继续滴加硝酸
银溶液;
(3)碳酸钠和稀硝酸反应生成硝酸钠、水和二氧化碳,则另一份溶液中滴加过量的稀硝酸,先无明显
现象后产生气泡,说明杂质中含有碳酸钠,向步骤 2所得溶液中继续滴加硝酸银溶液,产生白色沉
淀,说明杂质中含有氯化钠,则杂质中含有氯化钠、碳酸钠,溶液中含有氢氧化钠,无论是否含有碳
酸钠,溶液都呈碱性,则上述实验中步骤1是没有必要进行的,实验中,滴加稀硝酸至过量的目的是
检验碳酸钠,并除尽氢氧化钠和碳酸钠,排除对氯化钠检验的干扰。
故答案为:(1)CO +2NaOH=Na CO +H O;
2 2 3 2
(2)步骤1:红色;
步骤3:硝酸银;
(3)氯化钠、碳酸钠;1;检验碳酸钠,并除尽氢氧化钠和碳酸钠,排除对氯化钠检验的干扰。
21.(7分)镀锌铁片是指在铁上进行双面镀锌而制成的一种锌铁合金。
(1)对铁片镀锌的目的是为了防止铁被空气中的 O (填写化学式)氧化生锈,针对日常生活中
2
的铁锈,可用 HC l 或 H SO (填写化学式)来除锈。
2 4
(2)测量镀锌铁片表面镀锌层的厚度。
步骤1:剪下一块表面积为9.1cm2的镀锌铁片,称量,记录质量为17.6g。
步骤2:将镀锌铁片放入过量稀硫酸中,一开始能观察到大量气泡,此时反应的化学方程式为
Zn+H SO = ZnSO +H ↑ 。
2 4 4 2
步骤3:待镀锌铁片表面气泡明显减少后,用蒸馏水清洗,并擦干,称量,记录质量为16.3g。
假设上述反应只有一种金属参与,产生氢气 0.02 mol。通过锌的密度计算得到该镀锌铁片的单面
镀锌层厚度为0.01cm。该实验结果 大于 (选填“大于”、“小于”或“等于”)实际镀锌铁片
厚度,理由是 铁会与过量的硫酸反应,导致失去的质量中包含铁,失去的质量偏大,测得厚度数值
偏大 。
【解答】解:(1)铁生锈是铁与空气中的氧气和水共同作用的结果,则对铁片镀锌的目的是为了防止
铁被空气中的O 氧化生锈,铁锈的主要成分是氧化铁,氧化铁能与盐酸或硫酸反应,则针对日常生活
2
中的铁锈,可用HCl或H SO 来除锈;
2 4(2)步骤2:将镀锌铁片放入过量稀硫酸中,一开始能观察到大量气泡,是因为锌和稀硫酸反应生成
硫酸锌和氢气,反应的化学方程式为Zn+H SO =ZnSO +H ↑;
2 4 4 2
步骤3:待镀锌铁片表面气泡明显减少后,用蒸馏水清洗,并擦干,称量,记录质量为16.3g,则锌的
质量为17.6g﹣16.3g=1.3g,
设产生氢气的质量为x,
Zn+H SO =ZnSO +H ↑
2 4 4 2
65 2
1.3g x
=
x=0.04g
则产生氢气的物质的量为0.04g÷2g/mol=0.02mol,通过锌的密度计算得到该镀锌铁片的单面镀锌层厚
度为0.01cm,该实验结果大于实际镀锌铁片厚度,理由是铁会与过量的硫酸反应,导致失去的质量中
包含铁,失去的质量偏大,测得厚度数值偏大。
故答案为:(1)O ;HCl或H SO ;
2 2 4
(2)步骤2:Zn+H SO =ZnSO +H ↑;
2 4 4 2
步骤3:0.02;大于;铁会与过量的硫酸反应,导致失去的质量中包含铁,失去的质量偏大,测得
厚度数值偏大。序