文档内容
化学部分
选择题未标注说明的,为单选,每题只能选一个选项;标注“不定项”的,每题应选一个或
多个选项。
相对原子质量:C-12 H-1 O-16
一、关于水的研究
科学家们通过一系列经典实验逐步揭开了水的组成之谜:
实验①:1783年,卡文迪许把氢气和氧气混合后盛在干燥、洁净的玻璃瓶中,当用电火花点火时发出爆鸣
声,且玻璃瓶内壁上出现了液滴,经检验是水。
实验②;1785年,拉瓦锡将水蒸气通过一根灼热的铁管,在出口处得到了氢气,铁管内壁生成黑色的四氧
化三铁。
实验③;1789年,德曼和特鲁斯维克通过静电装置发电首次将水电解成气体。
1. 铁的元素符号是___________。
A. Mg B. Ag C. Fe D. He
2. 保持水的化学性质的微观粒子是___________。
A. 水分子 B. 氢原子 C. 氢分子 D. 氧原子
3. 实验①~③涉及的各物质中,属于氧化物的是___________。(不定项)
A. 氧气 B. 水 C. 四氧化三铁 D. 氢气
4. 实验②涉及的化学反应属于___________。(填化学反应的基本类型)。
5. 如图是1864年一篇文献中所绘制的处于工作状态的电解水装置示意图。有关说法正确的是___________。
(不定项)
A. 电解水的化学方程式:2HO 2H↑+O ↑
2 2 2
B. 与b管电极相连的是电池的负极
第1页/共11页
学科网(北京)股份有限公司C. a与b管内收集到的气体质量比约为1∶2
D. a管中的气体能使带火星的木条复燃
自然界的水一般需要通过净化方可成为饮用水,生命吸管可以将自然界的水快速净化为饮用水,主要构造
如图所示。
6. 生命吸管中活性炭的主要作用是___________。
7. 海水中的主要成分是氯化钠,钠离子的直径约为0.2 nm,推测“生命吸管”能否淡化海水,请说明理由。
【答案】1. C 2. A 3. BC
4. 置换反应 5. ABD
6. 吸附水中的色素和异味
7. 不能;海水中钠离子的直径约为0.2 nm,而生命吸管中空纤维超滤膜的孔径为10 nm,10 nm远大于钠离
子的直径,钠离子无法被超滤膜截留,因此不能去除海水中的氯化钠,无法实现海水淡化
【解析】
【1题详解】
铁的元素符号是Fe,故选C。
【2题详解】
分子是保持物质化学性质的最小粒子,水是由水分子构成的,所以保持水化学性质的微观粒子是水分子,
故选A。
【3题详解】
氧化物是由两种元素组成,其中一种是氧元素的化合物。
A、氧气(O)只由一种元素组成,属于单质,不是氧化物,不符合题意。
2
B、水(HO)由氢和氧两种元素组成,属于氧化物,符合题意。
2
C、四氧化三铁(Fe O)由铁和氧两种元素组成,属于氧化物,符合题意。
3 4
D、氢气(H)只由一种元素组成,属于单质,不是氧化物,不符合题意。
2
第2页/共11页
学科网(北京)股份有限公司故选BC。
【4题详解】
实验②中水蒸气与铁在高温下反应生成氢气和四氧化三铁,该反应是一种单质和一种化合物反应生成另一
种单质和另一种化合物,属于置换反应。
【5题详解】
A、水通电分解,产生氢气和氧气,反应的化学方程式为 ,正确。
B、电解水时,与电源负极相连的电极产生氢气,与电源正极相连的电极产生氧气,氢气和氧气的体积比
约为2:1,b管内气体体积大,是氢气,所以与b管电极相连的是电池的负极,正确。
C、a管内是氧气,b管内是氢气,氢气和氧气的质量比为(16×2):(1×4)=8:1,不是1:2,错误。
D、a管内是氧气,氧气能使带火星的木条复燃,正确。
故选ABD。
【6题详解】
活性炭具有疏松多孔的结构,有吸附性,在生命吸管中主要作用是吸附水中的色素和异味。
【7题详解】
“生命吸管” 不能淡化海水,因为 海水中钠离子的直径约为0.2 nm,而生命吸管中空纤维超滤膜的孔径
为10 nm,10 nm远大于钠离子的直径,钠离子无法被超滤膜截留,因此不能去除海水中的氯化钠,无法
实现海水淡化。
二、芒硝制西瓜霜
8. 古人以天然盐卤水为原料,采用“滩田法”制取芒硝(硫酸钠晶体),制取流程如图1所示。表1是NaCl
和NaSO 的溶解度表。
2 4
图1
温度/℃ 10 20 30 40 50 60
36. 36.
NaCl 35.8 35.9 36.4 37.1
1 7
溶 解
度/g
40. 47.
NaSO 9.1 19.5 48.8 45.3
2 4 8 5
第3页/共11页
学科网(北京)股份有限公司表1
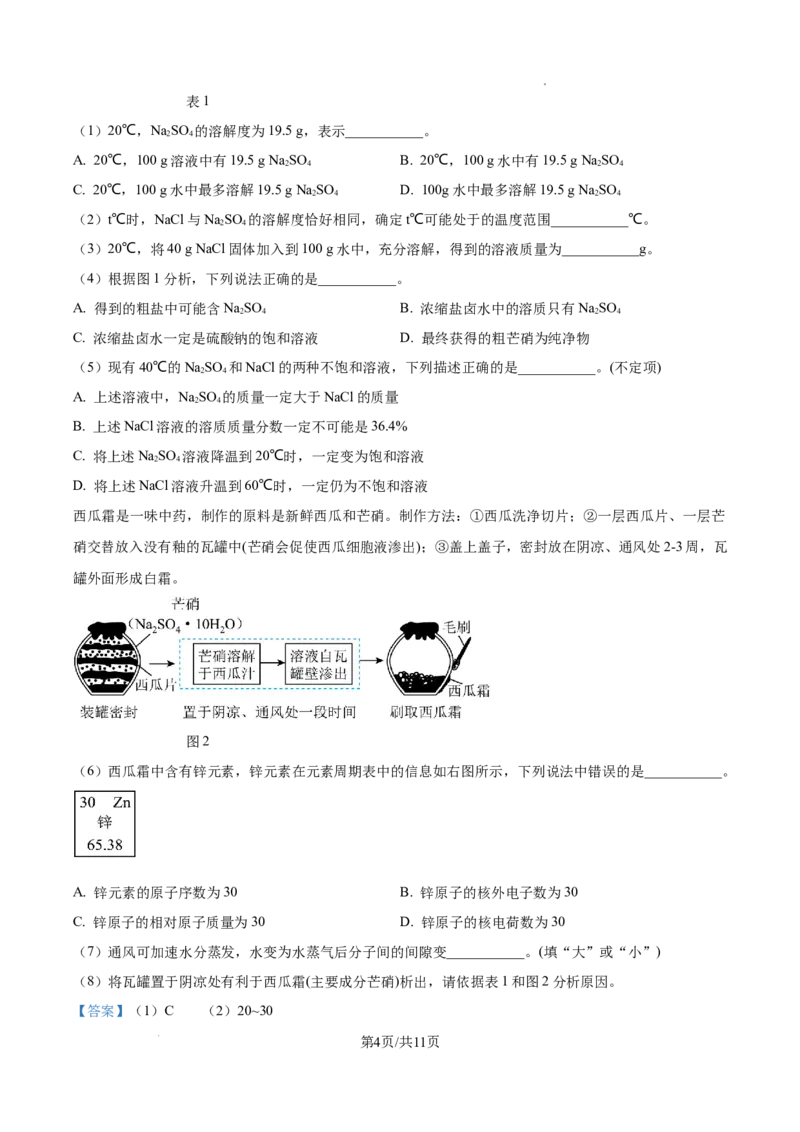
(1)20℃,NaSO 的溶解度为19.5 g,表示___________。
2 4
A. 20℃,100 g溶液中有19.5 g Na SO B. 20℃,100 g水中有19.5 g Na SO
2 4 2 4
C. 20℃,100 g水中最多溶解19.5 g Na SO D. 100g水中最多溶解19.5 g Na SO
2 4 2 4
(2)t℃时,NaCl与NaSO 的溶解度恰好相同,确定t℃可能处于的温度范围___________℃。
2 4
(3)20℃,将40 g NaCl固体加入到100 g水中,充分溶解,得到的溶液质量为___________g。
(4)根据图1分析,下列说法正确的是___________。
A. 得到的粗盐中可能含NaSO B. 浓缩盐卤水中的溶质只有NaSO
2 4 2 4
C. 浓缩盐卤水一定是硫酸钠的饱和溶液 D. 最终获得的粗芒硝为纯净物
(5)现有40℃的NaSO 和NaCl的两种不饱和溶液,下列描述正确的是___________。(不定项)
2 4
A. 上述溶液中,NaSO 的质量一定大于NaCl的质量
2 4
B. 上述NaCl溶液的溶质质量分数一定不可能是36.4%
C. 将上述NaSO 溶液降温到20℃时,一定变为饱和溶液
2 4
D. 将上述NaCl溶液升温到60℃时,一定仍为不饱和溶液
西瓜霜是一味中药,制作的原料是新鲜西瓜和芒硝。制作方法:①西瓜洗净切片;②一层西瓜片、一层芒
硝交替放入没有釉的瓦罐中(芒硝会促使西瓜细胞液渗出);③盖上盖子,密封放在阴凉、通风处2-3周,瓦
罐外面形成白霜。
图2
(6)西瓜霜中含有锌元素,锌元素在元素周期表中的信息如右图所示,下列说法中错误的是___________。
A. 锌元素的原子序数为30 B. 锌原子的核外电子数为30
C. 锌原子的相对原子质量为30 D. 锌原子的核电荷数为30
(7)通风可加速水分蒸发,水变为水蒸气后分子间的间隙变___________。(填“大”或“小”)
(8)将瓦罐置于阴凉处有利于西瓜霜(主要成分芒硝)析出,请依据表1和图2分析原因。
【答案】(1)C (2)20~30
第4页/共11页
学科网(北京)股份有限公司(3)135.9 (4)A (5)BD (6)C
(7)大 (8)由表1可知,硫酸钠溶解度随温度降低而减小,阴凉处温度低,可降低硫酸钠溶解度;
同时通风加速水分蒸发,可减少溶剂的含量,增大硫酸钠溶液浓度,二者共同促进芒硝析出
【解析】
【小问1详解】
A、20℃时,NaSO 的溶解度为19.5 g,表示20℃时,100g水中最多可溶解19.5g硫酸钠,即表示20℃时,
2 4
119.5g硫酸钠饱和溶液中溶质质量为19.5g,不符合题意;
B、20℃时,NaSO 的溶解度为19.5 g,表示20℃时,100g水中最多可溶解19.5g硫酸钠,不符合题意;
2 4
C、20℃时,NaSO 的溶解度为19.5 g,表示20℃时,100g水中最多可溶解19.5g硫酸钠,符合题意;
2 4
D、20℃时,NaSO 的溶解度为19.5 g,表示20℃时,100g水中最多可溶解19.5g硫酸钠,应指明温度,
2 4
不符合题意。
故选C;
【小问2详解】
20℃时,溶解度:氯化钠大于硫酸钠,30℃时,溶解度:氯化钠小于硫酸钠,则t℃时,NaCl与NaSO 的
2 4
溶解度恰好相同,t℃可能处于的温度范围为:20~30℃;
【小问3详解】
20℃时,氯化钠的溶解度为35.9g,即该温度下,100g水中最多可溶解35.9g氯化钠,则20℃,将40 g
NaCl固体加入到100 g水中,充分溶解,只能溶解35.9g,所得溶液的质量为:35.9g+100g=135.9g;
【小问4详解】
的
A、天然盐卤水中主要含氯化钠、硫酸钠等,氯化钠 溶解度受温度影响不大,则应采取蒸发结晶的方法
得到粗盐,蒸发过程中,硫酸钠也可能会结晶析出,故得到的粗盐中可能含硫酸钠,符合题意;
B、蒸发过程中,氯化钠结晶析出,但是氯化钠不能完全析出,故浓缩盐卤水中的溶质除了硫酸钠,还含
有氯化钠,不符合题意;
C、浓缩盐卤水是析出氯化钠后得到的,一定是氯化钠的饱和溶液,不一定是硫酸钠的饱和溶液,不符合
题意;
D、硫酸钠的溶解度受温度影响较大,故粗芒硝是通过降温结晶得到的,但是降温过程中,氯化钠也可能
析出,故得到的粗芒硝中可能含有氯化钠,可能为混合物,不符合题意。
故选A;
【小问5详解】
A、两种溶液的质量和溶质质量分数未知,上述溶液中硫酸钠和氯化钠的质量无法比较,不符合题意;
B、40℃时,氯化钠的溶解度为36.4g,则该温度下,氯化钠饱和溶液的溶质质量分数为:
第5页/共11页
学科网(北京)股份有限公司,该温度下,氯化钠不饱和溶液的溶质质量分数一定小于26.7%,故上述
NaCl溶液的溶质质量分数一定不可能是36.4%,符合题意;
的
C、将上述NaSO 溶液降温到20℃时,降温后,硫酸钠 溶解度减小,但是不一定变为饱和溶液,不符合
2 4
题意;
D、将上述NaCl溶液升温到60℃时,升温后,氯化钠的溶解度增加,仍然是不饱和溶液,符合题意。
故选BD;
【小问6详解】
A、在元素周期表中,元素名称左上角的数字表示原子序数,故锌元素的原子序数为30,不符合题意;
B、在原子中,原子序数=质子数=核外电子数,故锌原子的核外电子数为30,不符合题意;
C、在元素周期表中,元素名称下方的数字表示相对原子质量,相对原子质量是一个比值,单位为“1”,
常省略不写,故锌原子的相对原子质量为65.38,符合题意;
D、在原子中,核电荷数=原子序数=质子数,故锌原子的核电荷数为30,不符合题意。
故选C;
【小问7详解】
通风可加速水分蒸发,水变为水蒸气后,液态变为气态,分子间的间隙变大;
【小问8详解】
由图2可知,将瓦罐置于阴凉、通风处一段时间,得到西瓜霜,由表1可知,硫酸钠溶解度随温度降低而
减小,阴凉处温度低,可降低硫酸钠溶解度;同时通风加速水分蒸发,可减少溶剂的含量,增大硫酸钠溶
液浓度,二者共同促进芒硝析出。
三、认识二氧化碳
9. 二氧化碳在大气中的含量是相对稳定的,但随着全球经济的发展,含碳燃料的消耗激增,大气中二氧化
碳含量持续上升,导致温室效应加剧。为减缓全球变暖趋势,我国力争在2030年前实现碳达峰,2060年
前实现碳中和。
(1)CO 中碳元素的化合价为___________价。
2
A. +1 B. +2 C. +4 D. 4
(2)下列说法错误的是___________。
A. CO 能与水反应,可生产碳酸饮料 B. CO 参与光合作用,可用作气体肥料
2 2
C. 干冰升华会吸热,可用于人工降雨 D. CO 密度大于空气,可用于灭火
2
(3)要实现“碳达峰”“碳中和”的目标,可以从源头上减少CO 排放:请写出一条具体措施
2
第6页/共11页
学科网(北京)股份有限公司___________。
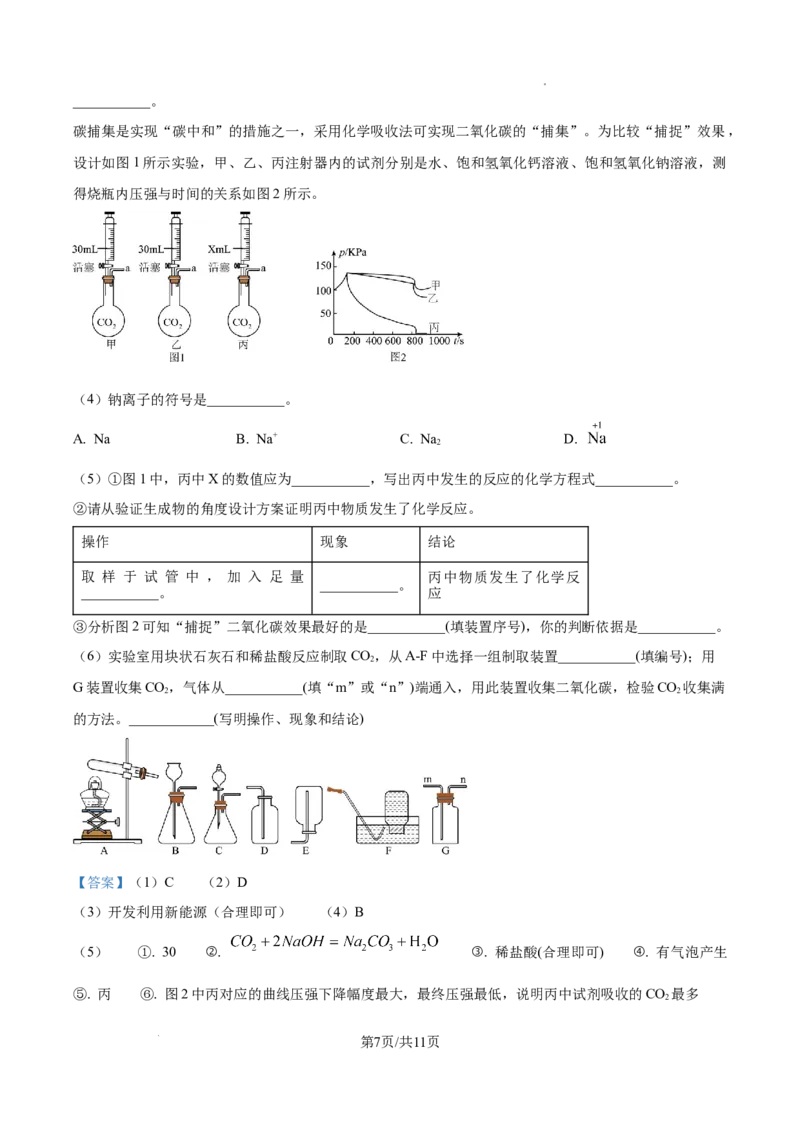
碳捕集是实现“碳中和”的措施之一,采用化学吸收法可实现二氧化碳的“捕集”。为比较“捕捉”效果,
设计如图1所示实验,甲、乙、丙注射器内的试剂分别是水、饱和氢氧化钙溶液、饱和氢氧化钠溶液,测
得烧瓶内压强与时间的关系如图2所示。
(4)钠离子的符号是___________。
A. Na B. Na+ C. Na D.
2
(5)①图1中,丙中X的数值应为___________,写出丙中发生的反应的化学方程式___________。
②请从验证生成物的角度设计方案证明丙中物质发生了化学反应。
操作 现象 结论
取 样 于 试 管 中 , 加 入 足 量 丙中物质发生了化学反
___________。
___________。 应
③分析图2可知“捕捉”二氧化碳效果最好的是___________(填装置序号),你的判断依据是___________。
(6)实验室用块状石灰石和稀盐酸反应制取CO,从A-F中选择一组制取装置___________(填编号);用
2
G装置收集CO,气体从___________(填“m”或“n”)端通入,用此装置收集二氧化碳,检验CO 收集满
2 2
的方法。____________(写明操作、现象和结论)
【答案】(1)C (2)D
(3)开发利用新能源(合理即可) (4)B
(5) ①. 30 ②. ③. 稀盐酸(合理即可) ④. 有气泡产生
⑤. 丙 ⑥. 图2中丙对应的曲线压强下降幅度最大,最终压强最低,说明丙中试剂吸收的CO 最多
2
第7页/共11页
学科网(北京)股份有限公司(6) ①. BD或CD ②. m ③. 将燃着的木条放在n端管口,若木条熄灭,则证明已收集满
【解析】
【小问1详解】
二氧化碳中氧元素显-2价,设碳元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:
,x=+4。
故选C;
【小问2详解】
A、二氧化碳能与水反应生成碳酸,可用于生产碳酸饮料,不符合题意;
B、二氧化碳是植物光合作用的原料,光合作用吸收二氧化碳,放出氧气,故二氧化碳可用作气体肥料,
不符合题意;
C、干冰升华吸热,能使周围温度降低,可用于人工降雨,不符合题意;
D、二氧化碳不燃烧、不支持燃烧,密度比空气大,可用于灭火,不只是因为二氧化碳的密度大于空气,
符合题意。
故选D;
【
小问3详解】
要实现“碳达峰”“碳中和”的目标,可以从源头上减少CO 排放,如开发利用新能源,减少化石燃料的
2
使用,减少二氧化碳的排放;
【小问4详解】
离子的表示方法:在该离子元素符号的右上角标上该离子所带的正负电荷数,数字在前,正负号在后,带
一个电荷时,1通常省略,多个离子,就是在元素符号前面加上相应的数字;每个钠离子带1个单位的正
电荷,故钠离子表示为:Na+。
故选B;
【小问5详解】
①该实验的目的是比较三种试剂的“捕捉”效果,根据控制变量法,三种试剂不同,其他因素相同,则丙
中X的数值应为30;
丙中发生反应为二氧化碳与氢氧化钠反应生成碳酸钠和水,该反应的化学方程式为:
;
②二氧化碳与氢氧化钠反应生成碳酸钠和水,碳酸钠能与稀盐酸反应生成氯化钠、二氧化碳和水,故取样
第8页/共11页
学科网(北京)股份有限公司于试管中,加入足量稀盐酸;有气泡产生,说明反应生成了碳酸钠,说明丙中物质发生了化学反应;
③图2中丙对应的曲线压强下降幅度最大,最终压强最低,说明丙中试剂吸收的CO 最多,则“捕捉”二
2
氧化碳效果最好的是丙;
【小问6详解】
实验室用块状石灰石和稀盐酸反应制取二氧化碳,属于固液不加热反应,发生装置可选B或C,二氧化碳
溶于水,密度比空气大,可用向上排空气法收集,收集装置可选D,故填:BD或CD;
用G装置收集CO,二氧化碳的密度比空气大,气体从m端通入;
2
二氧化碳不燃烧、不支持燃烧,二氧化碳验满:将燃着的木条放在n端管口,若木条熄灭,则证明已收集
满。
四、土壤酸碱性的调节
探究土壤酸碱性对不同植物生长的影响,为农业生产提供科学依据。以下为测定某地区土壤酸碱度的流程
图:
10. 几种植物生长适宜的pH范围如下表所示,其中适合在此土壤种植的是___________。
植物 小麦 棉花 茶树 甘草
5.0-
适宜范围(pH) 6.0-7.0 6.0-6.8 7.2-8.5
5.5
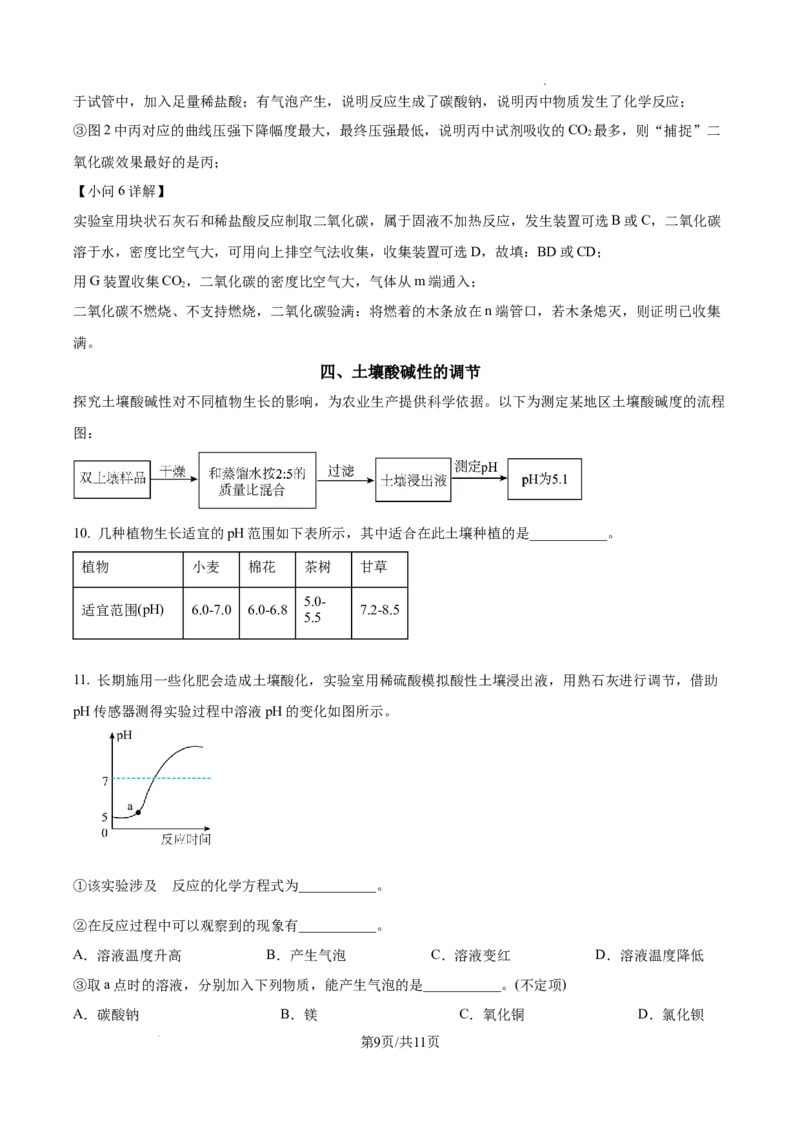
11. 长期施用一些化肥会造成土壤酸化,实验室用稀硫酸模拟酸性土壤浸出液,用熟石灰进行调节,借助
pH传感器测得实验过程中溶液pH的变化如图所示。
的
①该实验涉及 反应的化学方程式为___________。
②在反应过程中可以观察到的现象有___________。
A.溶液温度升高 B.产生气泡 C.溶液变红 D.溶液温度降低
③取a点时的溶液,分别加入下列物质,能产生气泡的是___________。(不定项)
A.碳酸钠 B.镁 C.氧化铜 D.氯化钡
第9页/共11页
学科网(北京)股份有限公司【答案】10. 茶树 11. ①. HSO +Ca(OH) =CaSO +2H O ②. A ③. AB
2 4 2 4 2
【解析】
【10题详解】
该土壤pH为5.1,则适合种植茶树。
【11题详解】
①熟石灰为氢氧化钙的俗称,氢氧化钙和硫酸反应生成硫酸钙和水,反应的化学方程式为:
。
②该反应为中和反应,反应放热,则溶液温度会升高,但不会有气泡产生,溶液也不变色,故选A。
③a点时溶液显酸性,说明此时溶液中的溶质为硫酸钙和硫酸。
A、碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,有气泡产生,该选项符合题意;
B、镁能和硫酸反应生成硫酸镁和氢气,有气泡产生,该选项符合题意;
C、氧化铜和硫酸反应生成硫酸铜和水,不会产生气泡,该选项不符合题意;
D、氯化钡能和硫酸根结合为硫酸钡沉淀,但不会产生气泡,该选项不符合题意。
故选AB。
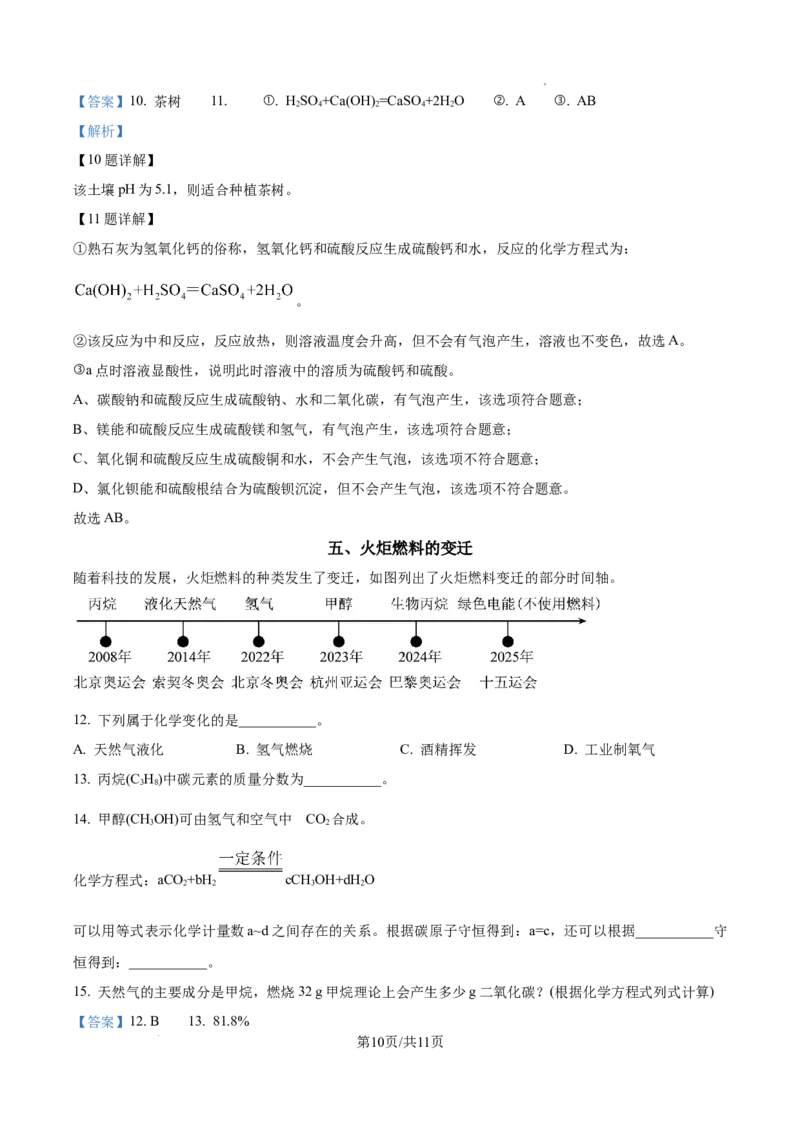
五、火炬燃料的变迁
随着科技的发展,火炬燃料的种类发生了变迁,如图列出了火炬燃料变迁的部分时间轴。
12. 下列属于化学变化的是___________。
A. 天然气液化 B. 氢气燃烧 C. 酒精挥发 D. 工业制氧气
13. 丙烷(C H)中碳元素的质量分数为___________。
3 8
的
14. 甲醇(CHOH)可由氢气和空气中 CO 合成。
3 2
化学方程式:aCO+bH cCHOH+dH O
2 2 3 2
可以用等式表示化学计量数a~d之间存在的关系。根据碳原子守恒得到:a=c,还可以根据___________守
恒得到:___________。
15. 天然气的主要成分是甲烷,燃烧32 g甲烷理论上会产生多少g二氧化碳?(根据化学方程式列式计算)
【答案】12. B 13. 81.8%
第10页/共11页
学科网(北京)股份有限公司14. ①. 氢原子(或氧原子) ②. 2b=4c+2d(或2a=c+d)
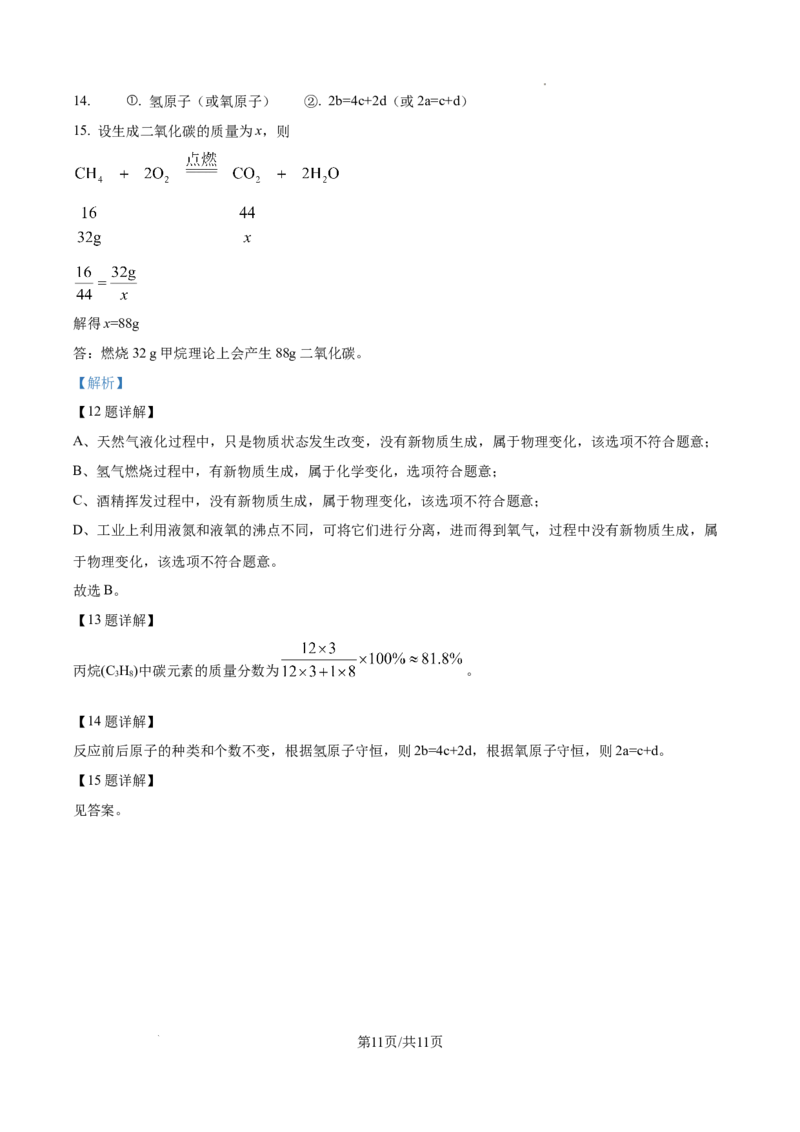
15. 设生成二氧化碳的质量为x,则
解得x=88g
答:燃烧32 g甲烷理论上会产生88g二氧化碳。
【解析】
【12题详解】
A、天然气液化过程中,只是物质状态发生改变,没有新物质生成,属于物理变化,该选项不符合题意;
B、氢气燃烧过程中,有新物质生成,属于化学变化,选项符合题意;
C、酒精挥发过程中,没有新物质生成,属于物理变化,该选项不符合题意;
D、工业上利用液氮和液氧的沸点不同,可将它们进行分离,进而得到氧气,过程中没有新物质生成,属
于物理变化,该选项不符合题意。
故选B。
【13题详解】
丙烷(C H)中碳元素的质量分数为 。
3 8
【14题详解】
反应前后原子的种类和个数不变,根据氢原子守恒,则2b=4c+2d,根据氧原子守恒,则2a=c+d。
【15题详解】
见答案。
第11页/共11页
学科网(北京)股份有限公司