文档内容
2021-2022学年上海市普陀区九年级(上)期末化学试卷(一
模)
答案与解析
一、选择题(共20分)1-14题只有一个正确选项
1.下列中国民俗文化活动中,涉及化学变化的是( )
A.贴春联 B.包粽子 C.画彩蛋 D.酿米酒
【分析】有新物质生成的变化叫化学变化;没有新物质生成的变化叫物理变化。化学变
化的特征是:有新物质生成。判断物理变化和化学变化的依据是:是否有新物质生成。
【解答】解:A、贴春联,没有新物质生成,属于物理变化,故A错误;
B、包粽子,没有新物质生成,属于物理变化,故B错误;
C、画彩蛋,没有新物质生成,属于物理变化,故C错误;
D、酿米酒,酒精是新物质,属于化学变化,故D正确;
故选:D。
2.空气中含量最多的元素是( )
A.氧元素 B.氮元素 C.碳元素 D.氢元素
【分析】根据空气中含量最多的气体是氮气,氮气是由氮元素组成的,进行分析解答。
【解答】解:空气中含量最多的气体是氮气,氮气是由氮元素组成的,所以空气中含量
最多的元素是氮元素。
故选:B。
3.下列建材中属于纯净物的是( )
A.水泥 B.环保涂料 C.复合木材 D.铜制电线
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成,水泥、环
保涂料、复合木材都属于混合物;纯净物是由一种物质组成。纯净物又分为单质和化合
物。由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫化合物。
【解答】解:A、水泥中有碳酸钙和其它杂质,属于混合物;故选项错误;
B、环保涂料中有多种成分,属于混合物;故选项错误;
C、复合木材中有木材和粘合剂等,属于混合物;故选项错误;
D、铜制电线,铜属于纯净物;故选项正确;
故选:D。4.N O中氮元素的化合价是( )
2
A.+1 B.+2 C.+3 D.+4
【分析】根据在化合物中正负化合价代数和为零,进行分析解答即可。
【解答】解:氧元素显﹣2价,设氮元素的化合价是x,根据在化合物中正负化合价代
数和为零,可得:2x+(﹣2)=0,则x=+1价。
故选:A。
5.属于化学性质的是( )
A.熔点 B.密度 C.硬度 D.可燃性
【分析】物质在化学变化中表现出来的性质叫化学性质,如可燃性、助燃性、氧化性、
还原性、酸碱性、稳定性、腐蚀性等;物质不需要发生化学变化就表现出来的性质,叫
物理性质;物理性质经常表现为:颜色、状态、气味、密度、硬度、熔点、沸点、导电
性、导热性、溶解性、挥发性、吸附性、延展性等。
【解答】解:A、熔点属于物理性质,故选项错误;
B、密度属于物理性质,故选项错误;
C、硬度属于物理性质,故选项错误;
D、可燃性属于化学性质,故选项正确;
故选:D。
6.Na SO 中的原子团名称是( )
2 4
A.硫酸根 B.碳酸根 C.硝酸根 D.氢氧根
【分析】根据化学式的含义、常见的原子团,进行分析判断。
【解答】解:Na SO 是硫酸钠的化学式,含有的原子团的名称是硫酸根。
2 4
故选:A。
7.自来水生产中,加入“氯气”的作用是( )
A.沉降颗粒物 B.吸附悬浮物 C.杀菌消毒 D.提高口感
【分析】根据净化水的方法与原理来分析。
【解答】解:加氯气,即向水中通入氯气,氯气遇水会产生次氯酸HClO,用于杀菌消
毒。
故选:C。
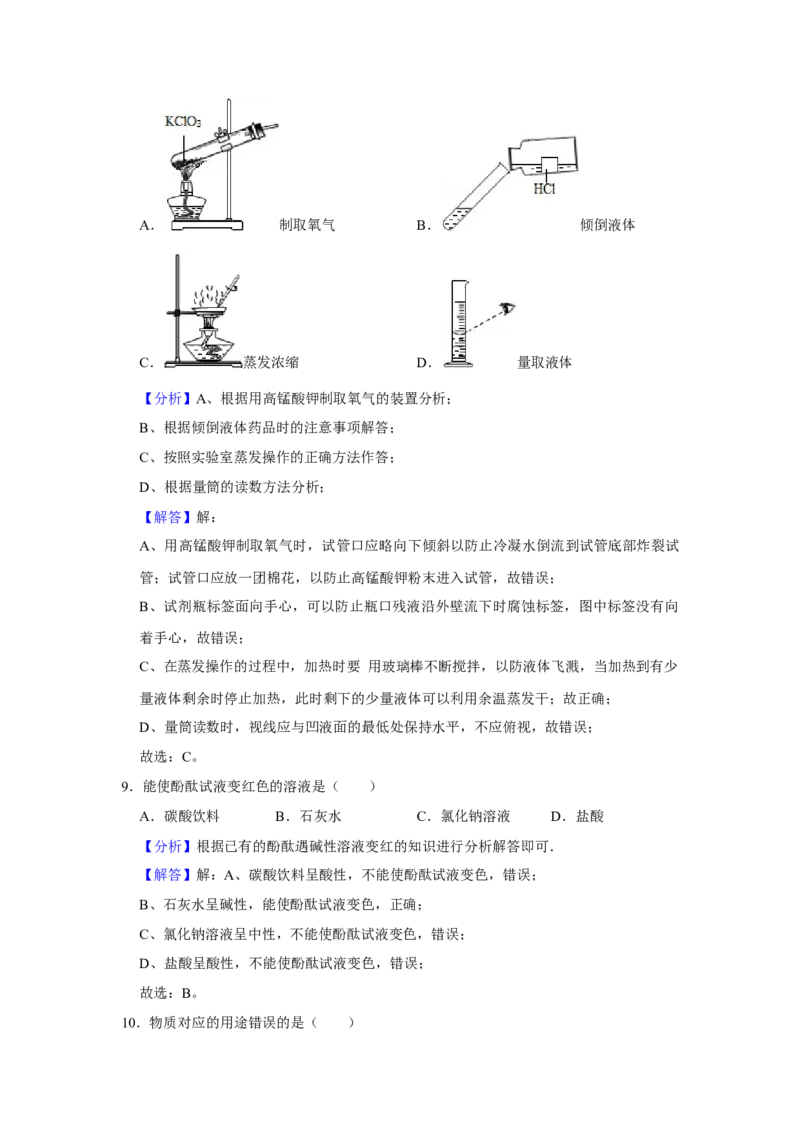
8.下列实验操作正确的是( )A. 制取氧气 B. 倾倒液体
C. 蒸发浓缩 D. 量取液体
【分析】A、根据用高锰酸钾制取氧气的装置分析;
B、根据倾倒液体药品时的注意事项解答;
C、按照实验室蒸发操作的正确方法作答;
D、根据量筒的读数方法分析;
【解答】解:
A、用高锰酸钾制取氧气时,试管口应略向下倾斜以防止冷凝水倒流到试管底部炸裂试
管;试管口应放一团棉花,以防止高锰酸钾粉末进入试管,故错误;
B、试剂瓶标签面向手心,可以防止瓶口残液沿外壁流下时腐蚀标签,图中标签没有向
着手心,故错误;
C、在蒸发操作的过程中,加热时要 用玻璃棒不断搅拌,以防液体飞溅,当加热到有少
量液体剩余时停止加热,此时剩下的少量液体可以利用余温蒸发干;故正确;
D、量筒读数时,视线应与凹液面的最低处保持水平,不应俯视,故错误;
故选:C。
9.能使酚酞试液变红色的溶液是( )
A.碳酸饮料 B.石灰水 C.氯化钠溶液 D.盐酸
【分析】根据已有的酚酞遇碱性溶液变红的知识进行分析解答即可.
【解答】解:A、碳酸饮料呈酸性,不能使酚酞试液变色,错误;
B、石灰水呈碱性,能使酚酞试液变色,正确;
C、氯化钠溶液呈中性,不能使酚酞试液变色,错误;
D、盐酸呈酸性,不能使酚酞试液变色,错误;
故选:B。
10.物质对应的用途错误的是( )A.氧气:高能燃料
B.稀有气体:多用途电光源
C.二氧化碳:灭火剂
D.金刚石:切割玻璃
【分析】根据物质的性质决定物质的用途,物质的用途反映物质的性质角度进行分析。
【解答】解:A、氧气具有助燃性,能支持其他物质燃烧,不能作燃料,故A错误;
B、稀有气体通电时会发出不同颜色的光,所以可以用作电光源,故B正确;
C、二氧化碳密度比空气大,不燃烧也不支持燃烧,所以可用作灭火剂,故C正确;
D、金刚石是自然界中硬度最大的物质,所以可用作切割玻璃,故D正确。
故选:A。
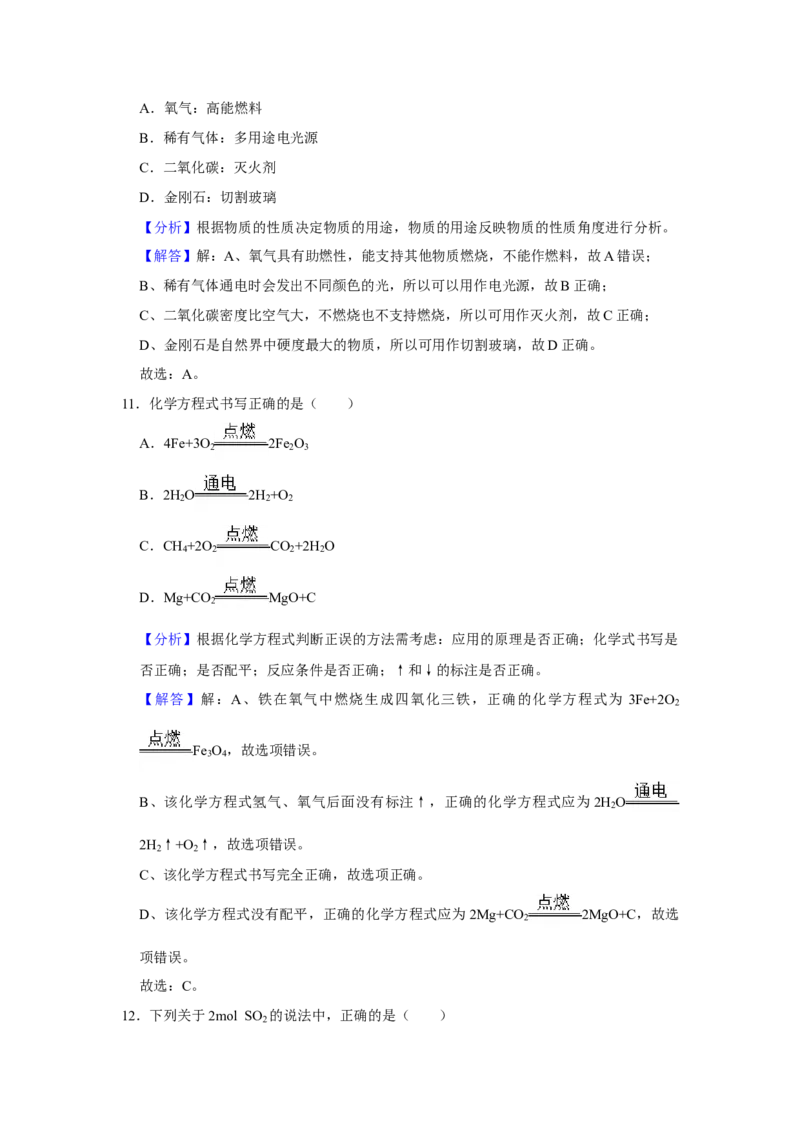
11.化学方程式书写正确的是( )
A.4Fe+3O 2Fe O
2 2 3
B.2H O 2H +O
2 2 2
C.CH +2O CO +2H O
4 2 2 2
D.Mg+CO MgO+C
2
【分析】根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是
否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确。
【解答】解:A、铁在氧气中燃烧生成四氧化三铁,正确的化学方程式为 3Fe+2O
2
Fe O ,故选项错误。
3 4
B、该化学方程式氢气、氧气后面没有标注↑,正确的化学方程式应为2H O
2
2H ↑+O ↑,故选项错误。
2 2
C、该化学方程式书写完全正确,故选项正确。
D、该化学方程式没有配平,正确的化学方程式应为2Mg+CO 2MgO+C,故选
2
项错误。
故选:C。
12.下列关于2mol SO 的说法中,正确的是( )
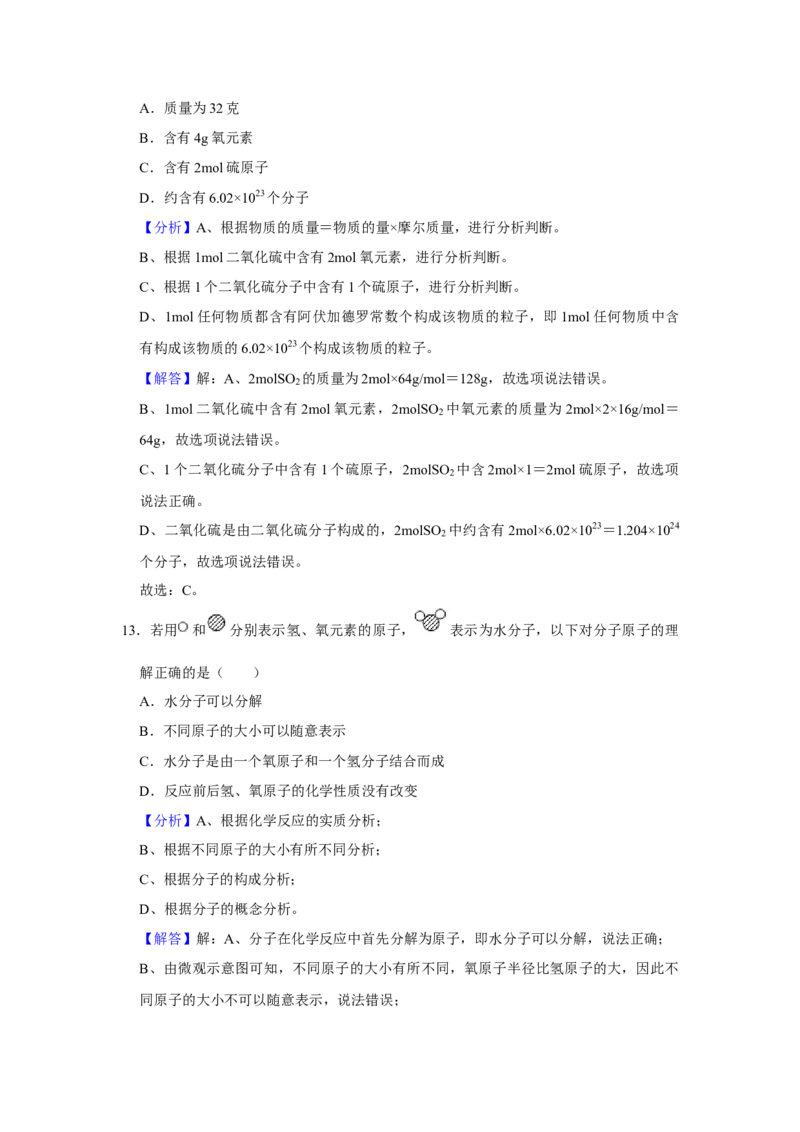
2A.质量为32克
B.含有4g氧元素
C.含有2mol硫原子
D.约含有6.02×1023个分子
【分析】A、根据物质的质量=物质的量×摩尔质量,进行分析判断。
B、根据1mol二氧化硫中含有2mol氧元素,进行分析判断。
C、根据1个二氧化硫分子中含有1个硫原子,进行分析判断。
D、1mol任何物质都含有阿伏加德罗常数个构成该物质的粒子,即1mol任何物质中含
有构成该物质的6.02×1023个构成该物质的粒子。
【解答】解:A、2molSO 的质量为2mol×64g/mol=128g,故选项说法错误。
2
B、1mol二氧化硫中含有2mol氧元素,2molSO 中氧元素的质量为2mol×2×16g/mol=
2
64g,故选项说法错误。
C、1个二氧化硫分子中含有1个硫原子,2molSO 中含2mol×1=2mol硫原子,故选项
2
说法正确。
D、二氧化硫是由二氧化硫分子构成的,2molSO 中约含有2mol×6.02×1023=1.204×1024
2
个分子,故选项说法错误。
故选:C。
13.若用 和 分别表示氢、氧元素的原子, 表示为水分子,以下对分子原子的理
解正确的是( )
A.水分子可以分解
B.不同原子的大小可以随意表示
C.水分子是由一个氧原子和一个氢分子结合而成
D.反应前后氢、氧原子的化学性质没有改变
【分析】A、根据化学反应的实质分析;
B、根据不同原子的大小有所不同分析;
C、根据分子的构成分析;
D、根据分子的概念分析。
【解答】解:A、分子在化学反应中首先分解为原子,即水分子可以分解,说法正确;
B、由微观示意图可知,不同原子的大小有所不同,氧原子半径比氢原子的大,因此不
同原子的大小不可以随意表示,说法错误;C、分子是由原子构成的,一个水分子由一个氧原子和两个氢原子结合而成,故说法错
误;
D、氢、氧原子结合成水分子后,氢、氧原子的化学性质改变了,故说法错误。
故选:A。
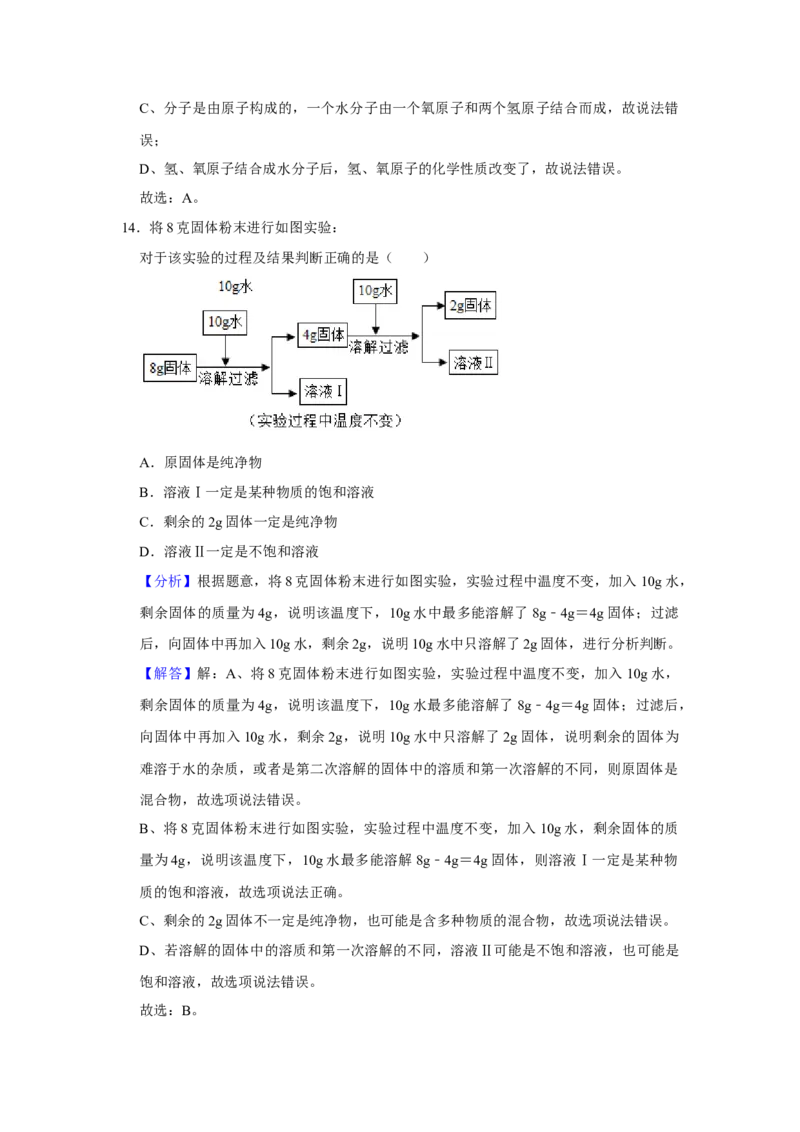
14.将8克固体粉末进行如图实验:
对于该实验的过程及结果判断正确的是( )
A.原固体是纯净物
B.溶液Ⅰ一定是某种物质的饱和溶液
C.剩余的2g固体一定是纯净物
D.溶液Ⅱ一定是不饱和溶液
【分析】根据题意,将8克固体粉末进行如图实验,实验过程中温度不变,加入10g水,
剩余固体的质量为4g,说明该温度下,10g水中最多能溶解了8g﹣4g=4g固体;过滤
后,向固体中再加入10g水,剩余2g,说明10g水中只溶解了2g固体,进行分析判断。
【解答】解:A、将8克固体粉末进行如图实验,实验过程中温度不变,加入10g水,
剩余固体的质量为4g,说明该温度下,10g水最多能溶解了8g﹣4g=4g固体;过滤后,
向固体中再加入10g水,剩余2g,说明10g水中只溶解了2g固体,说明剩余的固体为
难溶于水的杂质,或者是第二次溶解的固体中的溶质和第一次溶解的不同,则原固体是
混合物,故选项说法错误。
B、将8克固体粉末进行如图实验,实验过程中温度不变,加入 10g水,剩余固体的质
量为4g,说明该温度下,10g水最多能溶解8g﹣4g=4g固体,则溶液Ⅰ一定是某种物
质的饱和溶液,故选项说法正确。
C、剩余的2g固体不一定是纯净物,也可能是含多种物质的混合物,故选项说法错误。
D、若溶解的固体中的溶质和第一次溶解的不同,溶液Ⅱ可能是不饱和溶液,也可能是
饱和溶液,故选项说法错误。
故选:B。二.15-17题有1-2个正确选项
15.单质在氧气中发生燃烧时,有关说法正确的是( )
A.产物一般是氧化物
B.一定比在空气中更加剧烈
C.反应发生均需要点燃或加热
D.产物在常温下一定是气体或固体
【分析】A、根据单质在氧气中燃烧,发生氧化反应来分析;
B、根据氧气中氧气的浓度大于空气来分析;
C、根据单质在氧气中发生燃烧时,达到着火点即可,不一定需要点燃或加热来分析;
D、根据产物在常温下不一定是气体或固体来分析。
【解答】解:A、单质在氧气中燃烧,发生氧化反应,产物一定是氧化物,故A错误;
B、因为氧气中氧气的浓度大于空气,所以单质在氧气中燃烧比在空气中更加剧烈,故
B正确;
C、单质在氧气中发生燃烧时,达到着火点即可,不一定需要点燃或加热,例如铝在常
温下与空气中的氧气反应生成氧化铝,故C错误;
D、产物在常温下不一定是气体或固体,如氢气的燃烧产物水常温下是液体,故D错误;
故选:B。
16.关于“化合物”判断正确的是( )
A.化合反应的反应物是化合物
B.分解反应的反应物是化合物
C.化合反应的产物是化合物
D.分解反应的产物是化合物
【分析】根据化合物、单质、化合反应和分解反应的概念进行分析解答即可。
【解答】解:A、化合反应反应物不一定是化合物,比如氢气和氧气经化合反应生成水,
反应物都是单质,说法错误;
B、分解反应是一种物质生成两种或两种以上其他物质的化学反应,故分解反应的反应
物一定是化合物,说法正确;
C、化合反应是两种或两种以上物质生成一种物质的化学反应,故化合反应产物一定是
化合物,说法正确;
D、分解反应的产物不一定是化合物,比如水电解生成氢气和氧气,产物是单质,说法
错误。故选:BC。
17.某温度时,一定质量的固体M(不含结晶水)溶于水形成饱和溶液甲,有关说法正确
的是( )
A.甲溶液不能再溶解物质
B.降温,一定有固体M析出
C.该温度时,M形成的溶液中,甲溶液的溶质质量分数最大
D.该温度时,溶解等质量的M,形成甲溶液时所需水量最少
【分析】某温度时,一定质量的固体M(不含结晶水)溶于水形成饱和溶液甲,结合饱
和溶液的特征,进行分析判断。
【解答】解:A、某温度时,一定质量的固体M(不含结晶水)溶于水形成饱和溶液甲,
甲溶液不能再溶解M物质,但还能溶解其它的溶质,故选项说法错误。
B、无法确定M的溶解度受温度变化的影响趋势,降温,不一定有固体M析出,故选项
说法错误。
C、该温度时,M形成的溶液中,甲溶液为饱和溶液,则甲溶液的溶质质量分数最大,
故选项说法正确。
D、该温度时,溶解等质量的M,甲溶液为饱和溶液,形成甲溶液时所需水量最少,形
成不饱和溶液时所需的水的量比形成饱和溶液时多,故选项说法正确。
故选:CD。
二、简答题(共30分)
18.碳中和是通过植树造林、节能减排等形式,以抵消二氧化碳排放量,实现二氧化碳
“零排放”。
①自然界中有很多含“碳”的物质。其中金刚石属于 单质 (选填“单质”或“化
合物”),它的同素异形体有 石墨、 C 等 。
60
②含碳的矿石燃料,燃烧后均有CO 产生,大气中CO 含量过多的后果是 导致温室
2 2
效应 ,目前替代的清洁能源可以有 太阳能、水能等 。
③海水可以溶解吸收一部分的CO ,写出水与CO 反应的化学方程式 CO +H O =
2 2 2 2
H CO ;将CO 转化为固体含碳化合物,称之为“固碳”,写出一种“固碳”的化学
2 3 2
方程式 CO +Ca ( OH ) = CaCO ↓ +H O 。
2 2 3 2
④中国科学家将CO 转变成淀粉[化学式为(C H O ) ],转变的过程中,你认为还需
2 6 10 5 n
要的原料可能是 水 。
【分析】①根据单质和同素异形体的概念分析;②根据温室效应的成因,以及新能源的认知分析;
③根据二氧化碳的化学性质分析;
④根据质量守恒定律,并结合光合作用的原理分析。
【解答】解:①金刚石是由同种元素组成的纯净物,属于单质,同种元素组成的单质
属于同素异形体,金刚石的同素异形体有石墨、C 等;
60
②大气中CO 含量过多的后果是导致温室效应,目前替代矿石燃料的清洁能源可以有
2
太阳能、水能等;
③水与CO 反应生成碳酸,反应的化学方程式:CO +H O=H CO ;将CO 转化为固体
2 2 2 2 3 2
含碳化合物,称之为“固碳”,如二氧化碳与氢氧化钙反应生成碳酸钙,反应的化学方
程式:CO +Ca(OH) =CaCO ↓+H O;
2 2 3 2
④根据质量守恒定律,并结合光合作用的原理,可知将 CO 转变成淀粉[化学式为
2
(C H O ) ],转变的过程中,还需要的原料可能是水。
6 10 5 n
故答案为:①单质;石墨、C 等;②导致温室效应,目前替代矿石燃料的清洁能源可
60
以有太阳能、水能等;③CO +H O=H CO ;CO +Ca(OH) =CaCO ↓+H O;④水。
2 2 2 3 2 2 3 2
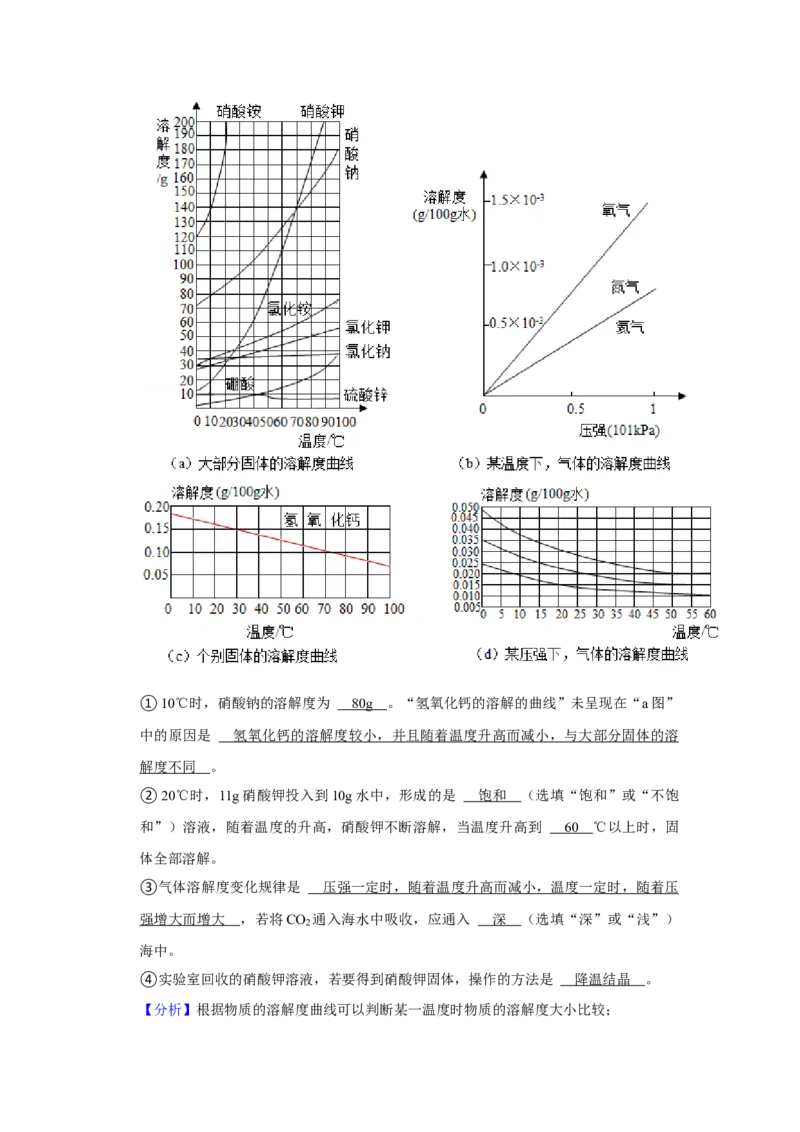
19.阅读下列溶解度曲线,并回答有关问题:①10℃时,硝酸钠的溶解度为 80 g 。“氢氧化钙的溶解的曲线”未呈现在“a图”
中的原因是 氢氧化钙的溶解度较小,并且随着温度升高而减小,与大部分固体的溶
解度不同 。
②20℃时,11g硝酸钾投入到10g水中,形成的是 饱和 (选填“饱和”或“不饱
和”)溶液,随着温度的升高,硝酸钾不断溶解,当温度升高到 60 ℃以上时,固
体全部溶解。
③气体溶解度变化规律是 压强一定时,随着温度升高而减小,温度一定时,随着压
强增大而增大 ,若将CO 通入海水中吸收,应通入 深 (选填“深”或“浅”)
2
海中。
④实验室回收的硝酸钾溶液,若要得到硝酸钾固体,操作的方法是 降温结晶 。
【分析】根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;根据物质的溶解度曲线可以判断随着温度的变化,物质的溶解度变化情况;
饱和溶液和不饱和溶液之间可以相互转化;
压强一定时,气体的溶解度随着温度升高而减小,温度一定时,气体的溶解度随着压强
增大而增大;
从溶液中结晶的方法有两种:蒸发结晶和降温结晶,物质的溶解度受温度变化影响较小
时,应该用蒸发结晶;物质的溶解度受温度变化影响较大时,应该用降温结晶.
【解答】解:①10℃时,硝酸钠的溶解度为80g;
“氢氧化钙的溶解的曲线”未呈现在“a图”中的原因是氢氧化钙的溶解度较小,并且
随着温度升高而减小,与大部分固体的溶解度不同。
故答案为:80g;氢氧化钙的溶解度较小,并且随着温度升高而减小,与大部分固体的
溶解度不同。
②20℃时硝酸钾溶解度是30g,11g硝酸钾投入到10g水中,能够溶解3g,形成的是饱
和溶液,随着温度的升高,硝酸钾不断溶解,当温度升高到60℃以上时,固体全部溶解,
是因为60℃时硝酸钾溶解度是110g,并且随着温度升高硝酸钾的溶解度增大。
故答案为:饱和;60。
③气体溶解度变化规律是压强一定时,随着温度升高而减小,温度一定时,随着压强
增大而增大,若将CO 通入海水中吸收,应通入深海中,是因为深海中的压强比浅海中
2
的压强大,更容易吸收二氧化碳。
故答案为:压强一定时,随着温度升高而减小,温度一定时,随着压强增大而增大;深。
④硝酸钾的溶解度受温度变化影响较大,实验室回收的硝酸钾溶液,若要得到硝酸钾
固体,操作的方法是降温结晶。
故答案为:降温结晶。
20.实验室常用氯酸钾和二氧化锰固体混合制取氧气。
①制取氧气发生反应的化学方程式是 2KClO 2KCl+3O ↑ 。若要制得0.96g
3 2
氧气,参加反应的氯酸钾应有 0.0 2 mol。
②实验过程中,二氧化锰起 催化 作用,为验证反应前后二氧化锰的质量没有变化,
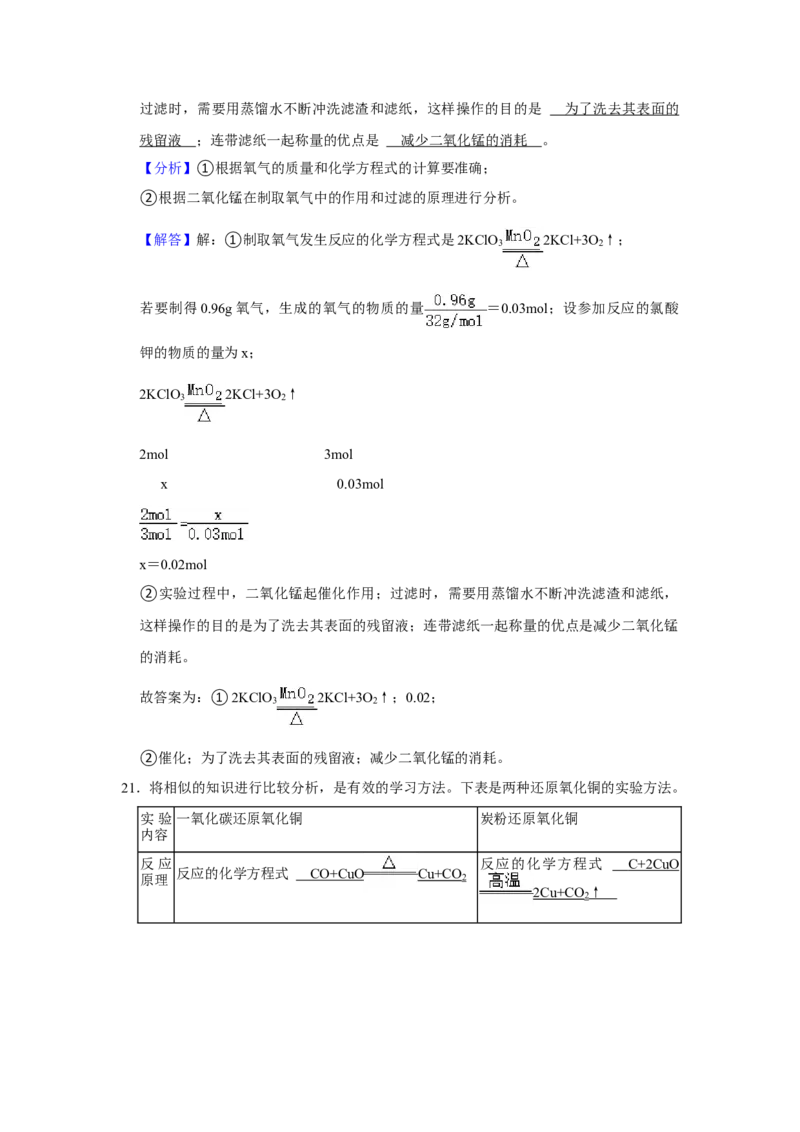
事先称量滤纸、二氧化锰的质量,制取氧气实验结束后,进行的实验操作流程如图。过滤时,需要用蒸馏水不断冲洗滤渣和滤纸,这样操作的目的是 为了洗去其表面的
残留液 ;连带滤纸一起称量的优点是 减少二氧化锰的消耗 。
【分析】①根据氧气的质量和化学方程式的计算要准确;
②根据二氧化锰在制取氧气中的作用和过滤的原理进行分析。
【解答】解:①制取氧气发生反应的化学方程式是2KClO 2KCl+3O ↑;
3 2
若要制得0.96g氧气,生成的氧气的物质的量 =0.03mol;设参加反应的氯酸
钾的物质的量为x;
2KClO 2KCl+3O ↑
3 2
2mol 3mol
x 0.03mol
x=0.02mol
②实验过程中,二氧化锰起催化作用;过滤时,需要用蒸馏水不断冲洗滤渣和滤纸,
这样操作的目的是为了洗去其表面的残留液;连带滤纸一起称量的优点是减少二氧化锰
的消耗。
故答案为:①2KClO 2KCl+3O ↑;0.02;
3 2
②催化;为了洗去其表面的残留液;减少二氧化锰的消耗。
21.将相似的知识进行比较分析,是有效的学习方法。下表是两种还原氧化铜的实验方法。
实验一氧化碳还原氧化铜 炭粉还原氧化铜
内容
反应 反应的化学方程式 C+2CuO
反应的化学方程式 CO+CuO Cu+CO
原理 2
2Cu+CO ↑
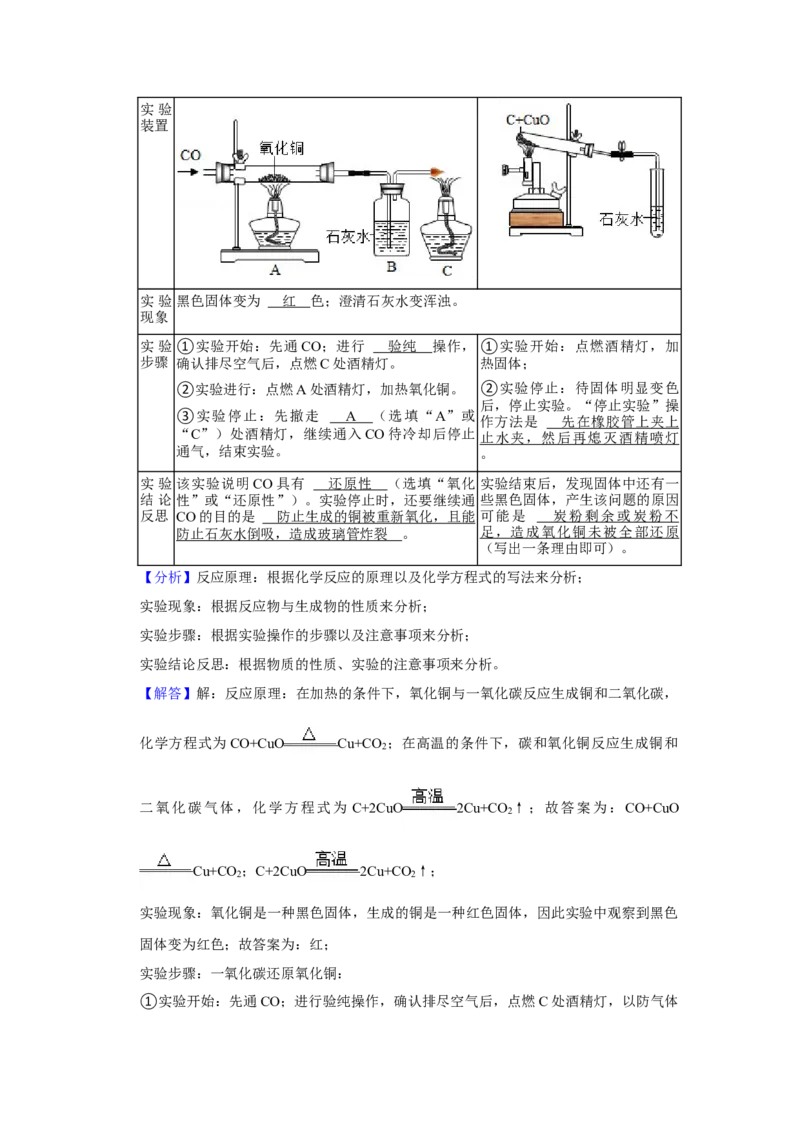
2实验
装置
实验黑色固体变为 红 色;澄清石灰水变浑浊。
现象
实验①实验开始:先通CO;进行 验纯 操作, ①实验开始:点燃酒精灯,加
步骤 确认排尽空气后,点燃C处酒精灯。 热固体;
②实验进行:点燃A处酒精灯,加热氧化铜。 ②实验停止:待固体明显变色
后,停止实验。“停止实验”操
③实验停止:先撤走 A (选填“A”或
作方法是 先在橡胶管上夹上
“C”)处酒精灯,继续通入CO待冷却后停止
止水夹,然后再熄灭酒精喷灯
通气,结束实验。 。
实验该实验说明CO具有 还原性 (选填“氧化 实验结束后,发现固体中还有一
结论性”或“还原性”)。实验停止时,还要继续通 些黑色固体,产生该问题的原因
反思 CO的目的是 防止生成的铜被重新氧化,且能 可能是 炭粉剩余或炭粉不
防止石灰水倒吸,造成玻璃管炸裂 。 足,造成氧化铜未被全部还原
(写出一条理由即可)。
【分析】反应原理:根据化学反应的原理以及化学方程式的写法来分析;
实验现象:根据反应物与生成物的性质来分析;
实验步骤:根据实验操作的步骤以及注意事项来分析;
实验结论反思:根据物质的性质、实验的注意事项来分析。
【解答】解:反应原理:在加热的条件下,氧化铜与一氧化碳反应生成铜和二氧化碳,
化学方程式为CO+CuO Cu+CO ;在高温的条件下,碳和氧化铜反应生成铜和
2
二氧化碳气体,化学方程式为 C+2CuO 2Cu+CO ↑;故答案为:CO+CuO
2
Cu+CO ;C+2CuO 2Cu+CO ↑;
2 2
实验现象:氧化铜是一种黑色固体,生成的铜是一种红色固体,因此实验中观察到黑色
固体变为红色;故答案为:红;
实验步骤:一氧化碳还原氧化铜:
①实验开始:先通CO;进行验纯操作,确认排尽空气后,点燃C处酒精灯,以防气体不纯,加热时发生爆炸。
②实验进行:点燃A处酒精灯,加热氧化铜。
③实验停止:先撤走A处酒精灯,继续通入CO待冷却后停止通气,结束实验。
故答案为:验纯;A;
炭粉还原氧化铜:
①实验开始:点燃酒精灯,加热固体;
②实验停止:待固体明显变色后,停止实验。“停止实验”操作方法是先在橡胶管上
夹上止水夹,然后再熄灭酒精喷灯,以防石灰水倒吸,造成试管炸裂;
故答案为:先在橡胶管上夹上止水夹,然后再熄灭酒精喷灯;
实验结论反思:一氧化碳还原氧化铜:
该实验中,一氧化碳能夺取氧化铜中的氧元素,说明 CO具有还原性。实验停止时,还
要继续通CO的目的是防止生成的铜被重新氧化,且能防止石灰水倒吸,造成玻璃管炸
裂;故答案为:还原性;防止生成的铜被重新氧化,且能防止石灰水倒吸,造成玻璃管
炸裂;
炭粉还原氧化铜:
实验结束后,发现固体中还有一些黑色固体,产生该问题的原因可能是炭粉剩余或碳粉
不足,造成氧化铜未被全部还原;故答案为:炭粉剩余或炭粉不足,造成氧化铜未被全
部还原。