文档内容
松江区 2021~2022 学年第一学期教学质量调研试卷
九年级理化(化学部分)答案解析版
相对原子质量:H-1 C-12 O-16 Na-23 Ca-40
五、选择题(共 20 分)
21-34 题每题均只有一个正确选项
1. 属于化学变化的是
A. 冰块熔化 B. 纸张燃烧 C. 海水晒盐 D. 黄瓜榨汁
【答案】B
【解析】
【详解】A、冰块熔化只是水的状态发生了变化,没有生成新物质,属于物理变化,选项错误;
B、纸张燃烧后生成了二氧化碳等物质,有新物质生成,属于化学变化,选项正确;
C、海水晒盐是将水与食盐进行分离的过程,没有生成新物质,属于物理变化,选项错误;
D、黄瓜榨汁只是黄瓜的形状法律变化,没有生成新物质,属于物理变化,选项错误,故选B。
2. 空气中含量最多的气体是
A. 氮气 B. 氧气 C. 稀有气体 D. 水蒸气
【答案】A
【解析】
【详解】空气的成分按体积分数计算,大约是:氮气 78%,氧气 21%,稀有气体 0.94%,二氧化碳
0.03%,其他气体和杂质0.03%,则空气中含量最多的气体是氮气;故选A。
3. 放入水中,能形成溶液的物质是
A. 面粉 B. 麻油 C. 食盐 D. 泥土
【答案】C
【解析】
【分析】
【详解】A、面粉不能溶解在水中,不能形成溶液,故选项A不符合题意;
B、麻油不能溶解在水中,不能形成溶液,故选项B不符合题意;
C、食盐能溶解在水中,能形成溶液,故选项C符合题意;
D、米兔不能溶解在水中,不能形成溶液,故选项D不符合题意。
故选:C。【点睛】
4. 能表示2个氮分子的是
A. N B. 2N C. 2N D. N
2 2 4
【答案】C
【解析】
【详解】A、 N 表示一个氮分子;一个氮分子中有两个氮原子,选项A不符合题意;
2
B、 2N 表示2个氮原子,选项B不符合题意;
C、2N 表示2个氮分子,选项C符合题意;
2
D、N 表示一个N 分子;一个N 分子中有四个氮原子,选项D不符合题意。
4 4 4
故选:C。
5. 玻璃成分中有二氧化硅(SiO),其中 Si 的化合价是
2
A. +2 B. +4 C. -1 D. -2
【答案】B
【解析】
【详解】根据化合物中各元素的化合价代数和为零原则和常见元素化合价可知,氧元素化合价为-2价,设
硅元素化合价为x,则有 ,解得 ,故二氧化硅中硅元素化合价为+4价,故选B。
6. 下列是一些食物的近似pH,其中酸性最强的是
食物 苹果 菠菜 牛奶 鸡蛋清
pH 2.9-3.3 5.1-5.7 6.3-6.6 7.6-8.0
A. 苹果 B. 菠菜 C. 牛奶 D. 鸡蛋清
【答案】A
【解析】
【分析】
【详解】对于酸性,pH<7,且数值越小,酸性越强,根据表格,苹果pH值最小,苹果的酸性最强。
故选A。
【点睛】
7. 物质在氧气中燃烧产生白烟的是
A. 硫 B. 木炭 C. 铁丝 D. 红磷【答案】D
【解析】
【详解】A、硫在氧气中燃烧,产生蓝紫色火焰,生成有刺激性气味的气体,不符合题意;
B、木炭在氧气中燃烧,发出白光,产生能使澄清石灰水变浑浊的气体,不符合题意;
C、铁丝在氧气中燃烧,火星四射,生成黑色固体,不符合题意;
D、红磷在空气中燃烧,产生大量白烟,符合题意;
故选D。
8. 自来水生产中其杀菌消毒作用的是
A. 明矾 B. 液氯 C. 活性炭 D. 氯化铁
【答案】B
【解析】
【分析】
【详解】自来水生产中其杀菌消毒作用的是液氯,具有杀菌消毒的作用;明矾具有净水的作用,活性炭具
有吸附性,出去颜色和异味,三氯化铁在污泥脱水中用作脱水剂,其效果极佳,也可用于无线电印刷电路
及不锈钢蚀刻行业做蚀刻剂等,故选:B。
【点睛】
9. 发生结晶现象的溶液,一定是
A. 浓溶液 B. 稀溶液 C. 饱和溶液 D. 不饱和溶液
【答案】C
【解析】
【详解】固体溶质从其饱和溶液中以晶体的形式析出的过程是结晶,所以发生结晶现象的溶液,一定是饱
和溶液,故选C。
10. 关于液氧的说法,正确的是
A. 含有水和氧气 B. 由氧分子构成
C. 具有可燃性 D. 与氧气互为同素异形体
【答案】B
【解析】
【分析】
【详解】液氧指液态的氧气,由氧分子构成,不可能含有水;氧气具有助燃性,没有可燃性。
故选B。
【点睛】11. 能表示混合物的微观示意图是
A. B. C. D.
【答案】C
【解析】
【分析】由一种元素组成的纯净物是单质,由两种或两种以上元素组成的纯净物为化合物;由一种物质组
成的为纯净物,多种物质组成的叫混合物;
【详解】A、只有一种元素,且是纯净物,该示意图为单质,故选项A不符合题意;
B、只有一种元素,且是纯净物,该示意图为单质,故选项B不符合题意;
C、图中有两种物质,故图示为混合物,故选项C符合题意;
D、图中只有一种物质,且由两种元素组成,图示为化合物,故选项D不符合题意。
故选:C。
【点睛】
12. 实验室用双氧水和二氧化锰制氧气的化学方程式正确的是
A. 2HO=2H O+O B. HO 2HO+O↑
2 2 2 2 2 2 2 2
C. HO H↑+O ↑ D. 2HO 2H O+O↑
2 2 2 2 2 2 2 2
【答案】D
【解析】
【分析】化学方程式书写时需要符合实验事实、正确使用化学符号标识、遵循质量守恒定律。涡阳化氢是
在二氧化锰作催化剂的条件下生成水和氧气,据此作答。
【详解】A、方程式缺少反应条件,故A错误;
B、方程式未配平,未遵守质量守恒定律,故B错误;
C、过氧化氢分解产生水和氧气,方程式不符合反应事实,故C错误;
D、方程式符合实验事实、正确使用化学符号标识、遵循质量守恒定律,故D正确;
故选D。
的
13. 将酒精灯 灯芯拨得松散些,可使火焰更旺,其原理是A. 减少空气中氧气含量 B. 减少二氧化碳的生成
C. 提高酒精的着火点 D. 增大酒精与空气的接触面积
【答案】D
【解析】
【详解】酒精灯火焰太小时,将灯芯拨得松散些,可使火焰更旺,是利用了增大可燃物与空气的接触面积
的原理,故选D。
的
【点睛】物质 着火点为其固有属性,不随外界环境的改变而改变。
14. 煤加工后产生的气体中含有CO、CH 和 H.取一定质量的该混合气体,完全燃烧产生 0.5mol 二氧化碳
4 2
和 1mol 水,则原混合气体中氢元素的物质的量是
A. 1.5mol B. 2mol C. 6mol D. 无法确定
【答案】B
【解析】
【详解】1个水分子中含有2个氢原子,则1mol 水中氢元素的物质的量是2mol,根据质量守恒定律可知,
原混合气体中氢元素的物质的量也是1mol,故选B。
35-37 每题均有 1~2 个正确选项
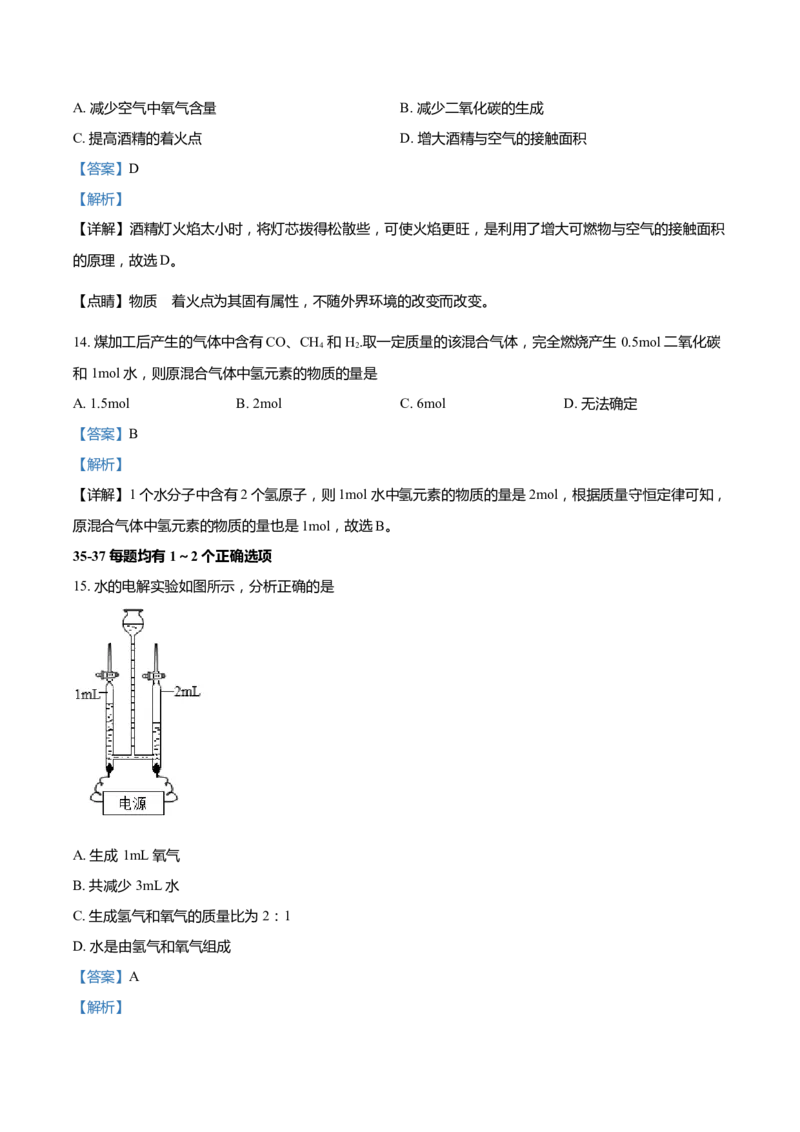
15. 水的电解实验如图所示,分析正确的是
A. 生成 1mL 氧气
B. 共减少 3mL 水
C. 生成氢气和氧气的质量比为 2:1
D. 水是由氢气和氧气组成
【答案】A
【解析】【分析】
【详解】A、根据图,左右玻璃管中产生气体的体积比为1:2,电解水实验中氧气和氢气的体积比为1:
2,故生成了1ml氧气,故选项A符合题意;
B、化学反应遵守质量守恒定律,没有体积的绝对关系,故选项B不符合题意;
C、电解水实验生成氢气和氧气的体积比为2:1,故选项C不符合题意;
D、电解水结论为:水是有氢元素和氧元素组成的,故选项D不符合题意;
故选:A。
【点睛】
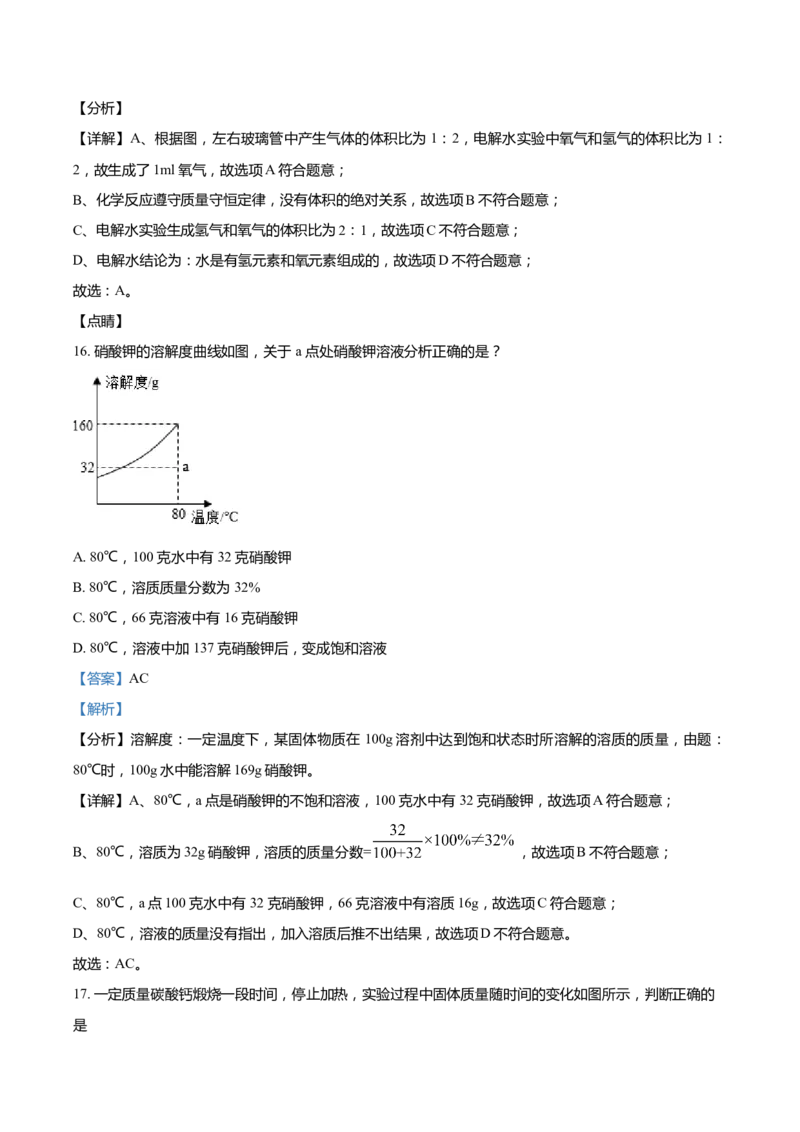
16. 硝酸钾的溶解度曲线如图,关于 a 点处硝酸钾溶液分析正确的是?
A. 80℃,100 克水中有 32 克硝酸钾
B. 80℃,溶质质量分数为 32%
C. 80℃,66 克溶液中有 16 克硝酸钾
D. 80℃,溶液中加 137 克硝酸钾后,变成饱和溶液
【答案】AC
【解析】
【分析】溶解度:一定温度下,某固体物质在 100g溶剂中达到饱和状态时所溶解的溶质的质量,由题:
80℃时,100g水中能溶解169g硝酸钾。
【详解】A、80℃,a点是硝酸钾的不饱和溶液,100 克水中有 32 克硝酸钾,故选项A符合题意;
B、80℃,溶质为32g硝酸钾,溶质的质量分数= ,故选项B不符合题意;
C、80℃,a点100 克水中有 32 克硝酸钾,66 克溶液中有溶质16g,故选项C符合题意;
D、80℃,溶液的质量没有指出,加入溶质后推不出结果,故选项D不符合题意。
故选:AC。
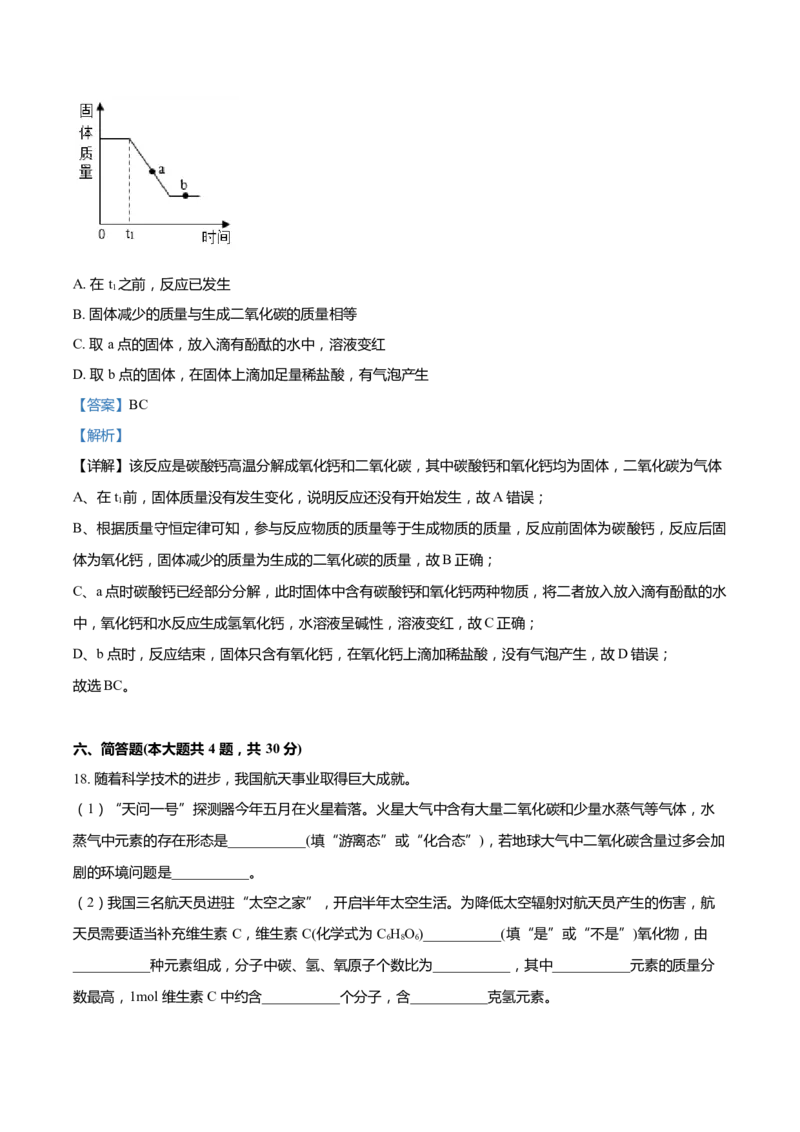
17. 一定质量碳酸钙煅烧一段时间,停止加热,实验过程中固体质量随时间的变化如图所示,判断正确的
是A. 在 t 之前,反应已发生
1
B. 固体减少的质量与生成二氧化碳的质量相等
C. 取 a 点的固体,放入滴有酚酞的水中,溶液变红
D. 取 b 点的固体,在固体上滴加足量稀盐酸,有气泡产生
【答案】BC
【解析】
【详解】该反应是碳酸钙高温分解成氧化钙和二氧化碳,其中碳酸钙和氧化钙均为固体,二氧化碳为气体
A、在t 前,固体质量没有发生变化,说明反应还没有开始发生,故A错误;
1
B、根据质量守恒定律可知,参与反应物质的质量等于生成物质的质量,反应前固体为碳酸钙,反应后固
体为氧化钙,固体减少的质量为生成的二氧化碳的质量,故B正确;
C、a点时碳酸钙已经部分分解,此时固体中含有碳酸钙和氧化钙两种物质,将二者放入放入滴有酚酞的水
中,氧化钙和水反应生成氢氧化钙,水溶液呈碱性,溶液变红,故C正确;
D、b点时,反应结束,固体只含有氧化钙,在氧化钙上滴加稀盐酸,没有气泡产生,故D错误;
故选BC。
六、简答题(本大题共 4 题,共 30 分)
18. 随着科学技术的进步,我国航天事业取得巨大成就。
(1)“天问一号”探测器今年五月在火星着落。火星大气中含有大量二氧化碳和少量水蒸气等气体,水
蒸气中元素的存在形态是___________(填“游离态”或“化合态”),若地球大气中二氧化碳含量过多会加
剧的环境问题是___________。
(2)我国三名航天员进驻“太空之家”,开启半年太空生活。为降低太空辐射对航天员产生的伤害,航
天员需要适当补充维生素 C,维生素 C(化学式为 C HO)___________(填“是”或“不是”)氧化物,由
6 8 6
___________种元素组成,分子中碳、氢、氧原子个数比为___________,其中___________元素的质量分
数最高,1mol 维生素C 中约含___________个分子,含___________克氢元素。【答案】(1) ①. 化合态 ②. 温室效应
(2) ①. 不是 ②. 三 ③. 6:8:6 ④. 氧 ⑤. 6.02×1023 ⑥. 8
【解析】
【小问1详解】
水蒸气就是气态的水,水在一种化合物,则水蒸气中元素的存在形态是化合态,故填化合态;
大气中二氧化碳含量过多会加剧的环境问题是温室效应,故填温室效应。
【小问2详解】
由化学式可知,维生素C由碳、氢、氧三种元素组成,不符合氧化物的特点,不属于氧化物,故填不是;
由化学式可知,维生素C由碳、氢、氧三种元素组成,故填三;
由化学式可知,维生素C的分子中碳、氢、氧原子个数比为6:8:6,故填6:8:6;
维生素C中,碳、氢、氧的质量比=(12×6):(1×8):(16×6)=9:1:12,则维生素C中氧元素的质
量分数最高,故填氧;
1mol 维生素C 中约含6.02×1023个维生素C分子,故填6.02×1023;
1mol 维生素C 中所含氢元素的质量=1mol×176g/mol× ×100%=8g,故填8。
19. 硝酸钾和氯化钠在不同温度下的溶解度如下表:
温度(℃) 10 20 30 40 60 80 100
硝酸钾 20.9 31.6 45.8 64 110 169 246
溶解度
(g/100g 水)
氯化钠 35.8 36.0 36.3 36.4 37 38.4 39.8
(1)10℃时,硝酸钾的溶解度___________(填“>”、“<”或“=”)氯化钠的溶解度。
(2)20℃时,20 克氯化钠固体放入 50 克水中,所得溶液___________(填“是”或“不是”)饱和溶液,
溶液的质量为___________克。
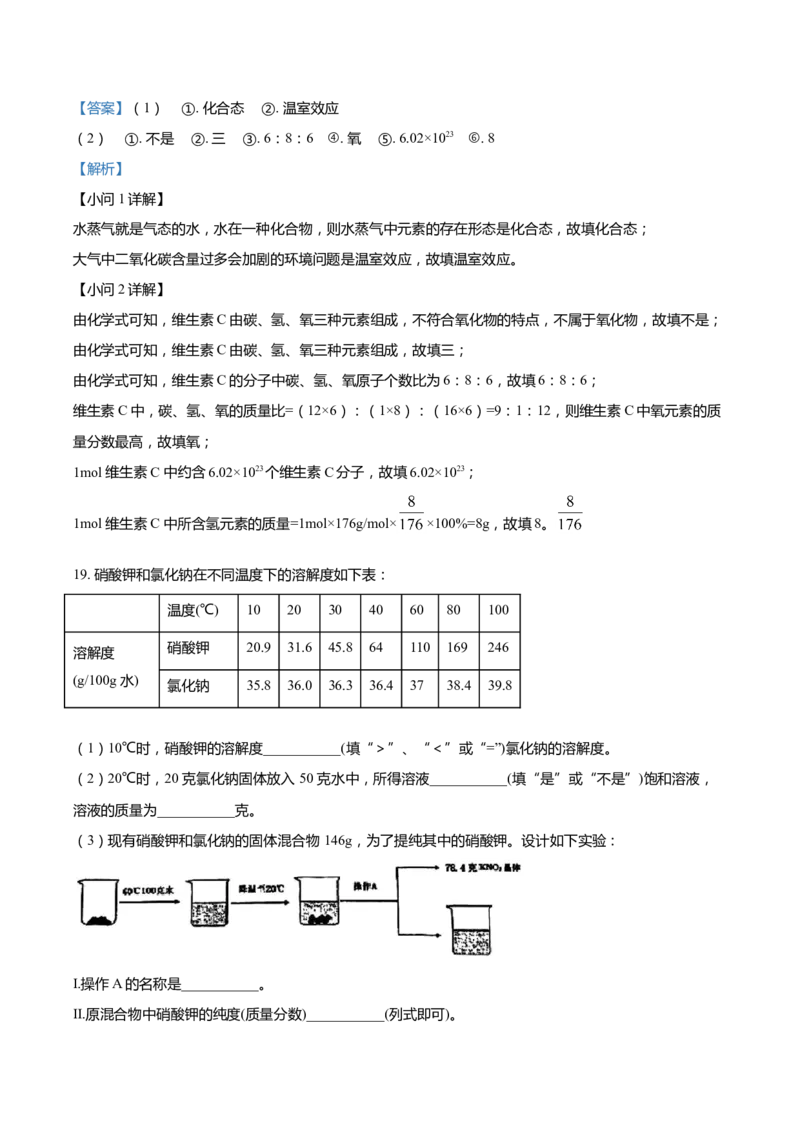
(3)现有硝酸钾和氯化钠的固体混合物 146g,为了提纯其中的硝酸钾。设计如下实验:
I.操作A 的名称是___________。
II.原混合物中硝酸钾的纯度(质量分数)___________(列式即可)。III.若降温到 10℃,能否得到纯净的硝酸钾?请结合相关数据分析说明。___________
【答案】(1)< (2) ①. 是 ②. 68
(3) ①. 过滤 ②. ×100% ③. 否,10℃时氯化钠的溶解度为35.8g,降温至10℃时,溶
液中36g氯化钠会有部分氯化钠与硝酸钾一起结晶析出,则得到的硝酸钾晶体中混有氯化钠
【解析】
【小问1详解】
由图可知,10℃时,硝酸钾的溶解度为20.9g,氯化钠的溶解度为35.8g,则10℃时,硝酸钾的溶解度<氯
化钠的溶解度,故填<。
【小问2详解】
由图可知,20℃时,氯化钠的溶解度为36.0g,则20℃时,20 克氯化钠固体放入 50 克水中,只能够溶解
18g氯化钠,所得溶液为氯化钠的饱和溶液,故填是;
20℃时,20 克氯化钠固体放入 50 克水中,只能够溶解18g氯化钠,所得溶液的质量=50g+18g=68g,故填
68。
【小问3详解】
I.操作A将硝酸钾晶体与溶液进行了分离,能够分离不再溶解的固体与液态的操作是过滤,即操作A的名
称是过滤,故填过滤。
II. 20℃时硝酸钾的溶解度为31.6g,溶液降温至20℃时,析出硝酸钾晶体的质量为78.4g,此时溶液为硝酸
钾的饱和溶液,溶剂水的质量为100g,则溶液中溶解的硝酸钾的质量为31.6g,则原混合物中硝酸钾的质
量=78.4g+31.6g,则原混合物中硝酸钾的纯度= ×100%,故填 ×100%。
III.原固体中氯化钠的质量=146g−78.4g−31.6g=36g,若降温到 10℃, 10℃时氯化钠的溶解度为35.8g,则
溶液中36g氯化钠会有部分氯化钠与硝酸钾一起结晶析出,则得到的硝酸钾晶体中混有氯化钠,故填否,
10℃时氯化钠的溶解度为35.8g,降温至10℃时,溶液中36g氯化钠会有部分氯化钠与硝酸钾一起结晶析
出,则得到的硝酸钾晶体中混有氯化钠。
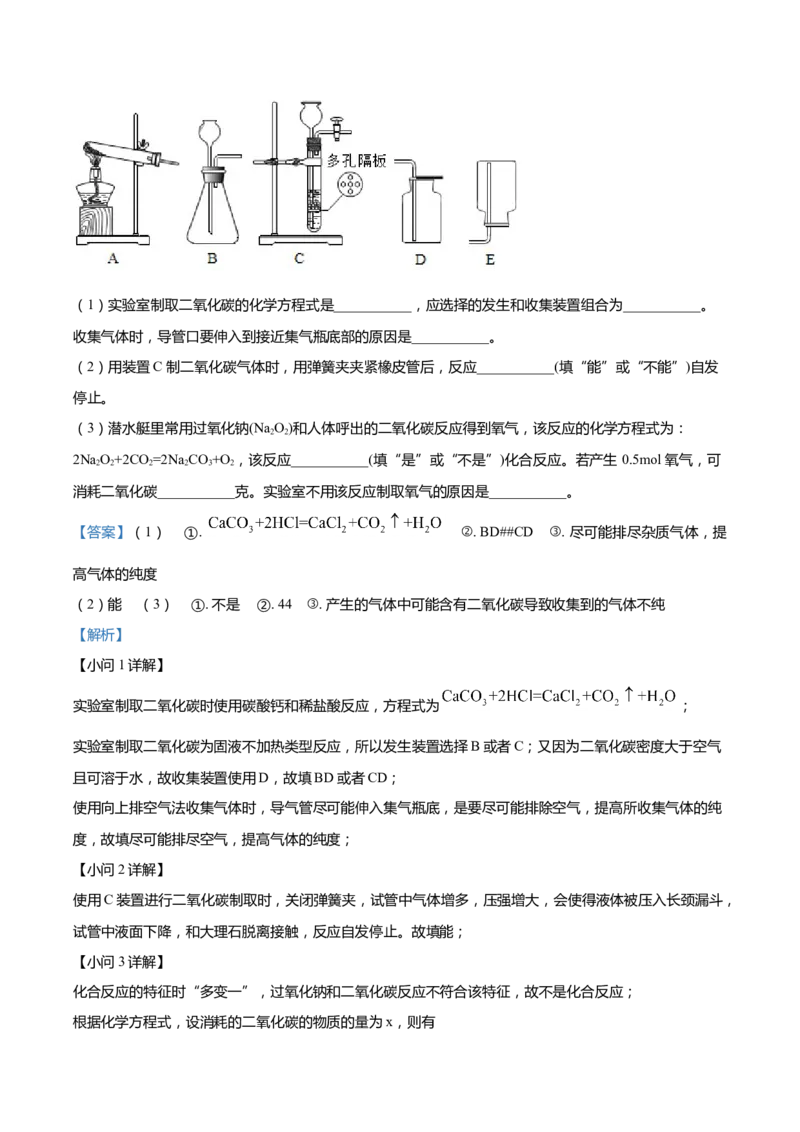
20. 根据如下实验装置,回答问题。(1)实验室制取二氧化碳的化学方程式是___________,应选择的发生和收集装置组合为___________。
收集气体时,导管口要伸入到接近集气瓶底部的原因是___________。
(2)用装置C 制二氧化碳气体时,用弹簧夹夹紧橡皮管后,反应___________(填“能”或“不能”)自发
停止。
(3)潜水艇里常用过氧化钠(Na O)和人体呼出的二氧化碳反应得到氧气,该反应的化学方程式为:
2 2
2NaO+2CO =2Na CO+O ,该反应___________(填“是”或“不是”)化合反应。若产生 0.5mol 氧气,可
2 2 2 2 3 2
消耗二氧化碳___________克。实验室不用该反应制取氧气的原因是___________。
【答案】(1) ①. ②. BD##CD ③. 尽可能排尽杂质气体,提
高气体的纯度
(2)能 (3) ①. 不是 ②. 44 ③. 产生的气体中可能含有二氧化碳导致收集到的气体不纯
【解析】
【小问1详解】
实验室制取二氧化碳时使用碳酸钙和稀盐酸反应,方程式为 ;
实验室制取二氧化碳为固液不加热类型反应,所以发生装置选择B或者C;又因为二氧化碳密度大于空气
且可溶于水,故收集装置使用D,故填BD或者CD;
使用向上排空气法收集气体时,导气管尽可能伸入集气瓶底,是要尽可能排除空气,提高所收集气体的纯
度,故填尽可能排尽空气,提高气体的纯度;
【小问2详解】
使用C装置进行二氧化碳制取时,关闭弹簧夹,试管中气体增多,压强增大,会使得液体被压入长颈漏斗,
试管中液面下降,和大理石脱离接触,反应自发停止。故填能;
【小问3详解】
化合反应的特征时“多变一”,过氧化钠和二氧化碳反应不符合该特征,故不是化合反应;
根据化学方程式,设消耗的二氧化碳的物质的量为x,则有解得 ,故二氧化碳的质量为 ,故填44;
二氧化碳和过氧化钠制取氧气时,二氧化碳反应不充分时会和氧气混在一起,导致收集到的氧气不纯净,
故填产生的气体中可能含有二氧化碳导致收集到的气体不纯
的
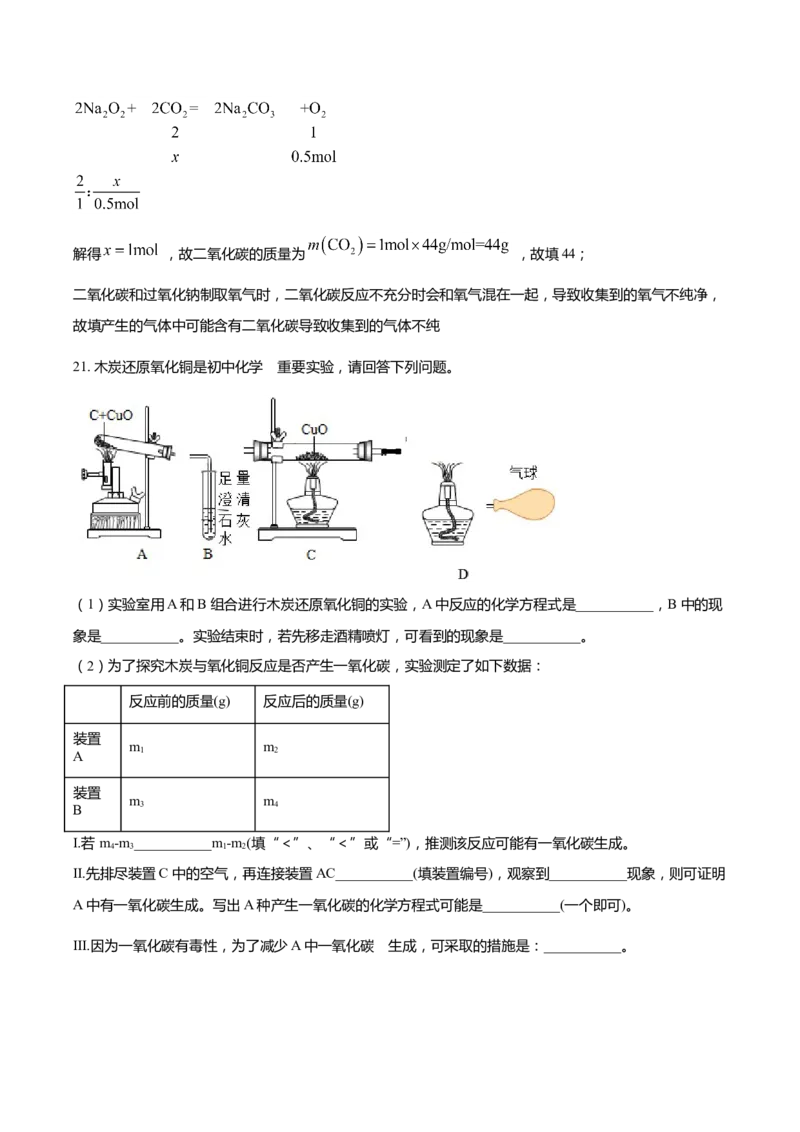
21. 木炭还原氧化铜是初中化学 重要实验,请回答下列问题。
(1)实验室用A 和B 组合进行木炭还原氧化铜的实验,A 中反应的化学方程式是___________,B 中的现
象是___________。实验结束时,若先移走酒精喷灯,可看到的现象是___________。
(2)为了探究木炭与氧化铜反应是否产生一氧化碳,实验测定了如下数据:
反应前的质量(g) 反应后的质量(g)
装置
m m
A 1 2
装置
m m
B 3 4
I.若 m-m ___________m-m (填“<”、“<”或“=”),推测该反应可能有一氧化碳生成。
4 3 1 2
II.先排尽装置C 中的空气,再连接装置AC___________(填装置编号),观察到___________现象,则可证明
A 中有一氧化碳生成。写出A 种产生一氧化碳的化学方程式可能是___________(一个即可)。
的
III.因为一氧化碳有毒性,为了减少A 中一氧化碳 生成,可采取的措施是:___________。【答案】(1) ①. ②. 澄清石灰水变浑浊 ③. 石灰水被倒吸入试管使试
管炸裂
(2) ①. < ②. D ③. C中黑色固体变红色 ④. ⑤. 使用足量氧化铜
【解析】
【小问1详解】
木炭在高温下还原氧化铜,生成铜和二氧化碳,方程式为 ;
B中是将含有二氧化碳的气体通入澄清石灰水,现象为澄清石灰水变浑浊;
【小问2详解】
表示石灰水增重的质量,也即混合气体中二氧化碳的质量; 表示A中生成气体的质量,
若二氧化碳质量小于生成气体的质量,则证明生成气体中含有一氧化碳,故填<;
一氧化碳还原氧化铜时产生铜单质,可以看到C装置中黑色固体变为红色;
A中碳和二氧化碳在高温情况下生成一氧化碳,方程式为 ;
A中产生一氧化碳的原因为在反应过程中产生大量二氧化碳能和碳单质反应产生一氧化碳,为减少一氧化
碳生成,可使用足量的氧化铜,使得生成的CO再被氧化铜消耗掉。故填使用足量的氧化铜。