文档内容
2021 学年九年级第二学期模拟练习
综合学科
相对原子质量:H-1 C-12 O-16 Cl-35.5 Ca-40
一、选择题(共20分,1~14题为单项选择)
1. 空气中含量较多且化学性质比较活泼的气体是 ( )
A. 氧气 B. 氮气 C. 二氧化碳 D. 氦气
【答案】A
【解析】
【详解】A、化学性质较活泼,在一定条件下,可以和多种物质发生化学反应,同时放出热量;具有助燃
性和氧化性,占空气总体积的体积分数大约为21%,故A正确;
B、氮气化学性质稳定,常温下不和其他物质反应,占空气总体积的体积分数大约为78%,故B不正确;
C、二氧化碳化学性质稳定,常温下不和其他物质反应,占空气总体积的体积分数大约为0.03%,故C不
正确;
D、氦气为稀有气体,化学性质稳定,故D不正确。故选A。
2. 自来水生产流程为:取水→沉降→过滤→吸附→杀菌消毒。涉及化学反应的步骤是
A. 取水 B. 过滤 C. 吸附 D. 杀菌消毒
【答案】D
【解析】
【详解】A、取水过程中,没有新物质生成,属于物理变化,故不符合题意;
B、过滤过程中,将不溶性杂质去除,没有新物质生成,属于物理变化,故不符合题意;
C、吸附过程中,吸附色素和异味,没有新物质生成,属于物理变化,故不符合题意;
D、杀菌消毒过程中,杀死水中微生物,有新物质生成,属于化学变化,发生化学反应,故符合题意;
故选D。
3. 中国争取 2060年前实现碳中和,“碳中和”中的“碳”指的是
A. 碳原子 B. 二氧化碳 C. 一氧化碳 D. 活性炭
【答案】B
【解析】
【详解】“碳中和”是指通过二氧化碳去除手段抵消部分碳排放,达到“净零排放”目的。“碳达峰”、
“碳中和”中的碳指的是二氧化碳。
故选B。
4. 不属于氧化物的是A. 干冰 B. 生石灰 C. 水银 D. 二氧化锰
【答案】C
【解析】
【分析】氧化物是由两种元素组成的化合物,且其中一种元素是氧元素的。
【详解】A、干冰是二氧化碳,是由氧元素和碳元素两种元素组成的,属于氧化物;
的
B、生石灰是氧化钙,是由钙、氧、两种元素组成 ,属于氧化物;
C、水银是汞单质,只有一种元素,不属于氧化物;
D、二氧化锰是由锰、氧两种元素组成的,属于氧化物;
故选C。
5. 草木灰的主要成分是碳酸钾(K CO),它属于化学肥料中的
2 3
A. 氮肥 B. 磷肥 C. 钾肥 D. 复合肥
【答案】C
【解析】
【详解】草木灰的主要成分是碳酸钾,含钾元素,属于钾肥。
故选C。
的
6. 属于溶液 是
A. 矿泉水 B. 酒精 C. 蒸馏水 D. 冰
【答案】A
【解析】
【分析】溶液的概念:一种或几种物质分散到另一种物质里形成的均一的、稳定的混合物;
【详解】A、矿泉水含有矿物质,是均一稳定的混合物,属于溶液,正确;
B、酒精是纯净物,不是溶液,错误;
C、蒸馏水只有一种物质,是纯净物,不是溶液,错误;
D、冰只有一种物质,是纯净物,不是溶液,错误;
故选A。
7. 灼烧时,火焰呈黄色的是
A. KCl B. Ca(NO ) C. CuCl D. NaNO
3 2 2 3
【答案】D
【解析】
【分析】含钠元素的化合物灼烧时,火焰呈黄色。【详解】A、KCl中不含有Na,而含有K,焰色反应为紫色,错误;
B、Ca(NO ) 中不含有Na,错误;
3 2
C、CuCl 中不含Na,而含Cu,焰色反应为绿色,错误;
2
D、硝酸钠中含有Na,焰色反应为黄色,正确;
故选D。
8. 化学用语表达正确的是
A. Fe(OH) :氢氧化铁 B. HNO:硝酸氢
2 3
C. 2个氧分子:2O D. SO :三氧化硫
3
【答案】D
【解析】
【详解】A、氢氧化铁中铁元素显+3价,氢氧根离子显-1价,化学式为:Fe(OH) ,Fe(OH) 是氢氧化亚铁
3 2
的化学式,不符合题意;
B、HNO 的名称是硝酸,不是硝酸氢,不符合题意;
3
C、分子用化学式表达,多个分子就是在化学式前面加上相应的数字,故2个氧分子表示为:2O,不符合
2
题意;
D、每个三氧化硫分子由1个硫原子和3个氧原子构成,化学式为:SO ,符合题意。
3
故选D。
9. 在pH=10的肥皂水中滴加紫色石蕊试液,溶液变
A. 无色 B. 红色 C. 蓝色 D. 紫色
【答案】C
【解析】
【详解】pH=10的肥皂水显碱性,紫色石蕊试液遇到碱性物质显蓝色,故选C项。
10. 物质的用途正确的是
A. 胆矾:检验水 B. 熟石灰:中和胃酸过多
C. 盐酸:除铁锈 D. 氧气:作燃料
【答案】C
【解析】
【详解】A、胆矾是硫酸铜晶体,呈蓝色,遇水仍然呈蓝色,不能用来检验水,硫酸铜粉末呈白色,遇水
变为蓝色,可用来检验水,不符合题意;
B、熟石灰是氢氧化钙的俗称,氢氧化钙虽然能中和胃酸,但具有腐蚀性,因此不能用来治疗胃酸过多,
不符合题意;
C、铁锈的主要成分是氧化铁,盐酸能和氧化铁反应生成氯化铁和水,因此盐酸能用来除铁锈,符合题意;
D、氧气没有可燃性,不能用作燃料,不符合题意。故选C。
11. 物质在氧气中燃烧的现象叙述错误的是
A. 硫粉:淡蓝色火焰 B. 木炭:发出白光 C. 红磷:大量白烟
D. 铁丝:火星四射
【答案】A
【解析】
【详解】A、硫粉在氧气中燃烧,发出明亮的蓝紫色火焰,故选项说法错误;B、木炭在氧气中燃烧,发出
白光,故选项说法正确;C、红磷在氧气中燃烧,产生大量的白烟,故选项说法正确;D、铁丝在氧气中剧
烈燃烧,火星四射,故选项说法正确。故选A。
12. 有关燃烧与灭火说法正确的是
A. 可燃物与氧气接触就会燃烧
B. 隔绝氧气可以灭火
C. 水灭火的原理是降低可燃物着火点
D. 温度达可燃物着火点就能燃烧
【答案】B
【解析】
【分析】
【详解】 燃烧需要同时满足三个条件:可燃物;与氧气或空气接触; 达到燃烧所需的最低温度即着火
点,可燃物接触氧气,温度达不到着火点不会发生燃烧,故错误;
B.因为燃烧必须同时具备三个条件,所以隔绝氧气能够灭火,故正确;
C.水灭火的原理是降低温度至可燃物着火点以下,物质的着火点一般不变,故错误;
D.燃烧需要同时满足三个条件:可燃物;与氧气或空气接触; 达到燃烧所需的最低温度即着火点,温度
达可燃物着火点不一定燃烧,故错误。
故选:B。
13. 关于金刚石与石墨涉及的学科观点错误的是
A. 元素观:金刚石与石墨是由碳元素组成的同素异形体
的
B. 微粒观:1 g金刚石和1 g石墨所含 碳原子数相同
C. 结构观:金刚石和石墨中碳原子排列方式不同,化学性质也不同
D. 守恒观:在一定条件下,1g金刚石能生成1g石墨
【答案】C
【解析】
【详解】A、金刚石与石墨是由碳元素组成的同素异形体,说法正确,不符合题意;B、金刚石和石墨都是由碳原子构成,同等质量金刚石和石墨所含的碳原子数相同,说法正确,不符合题
意;
C、金刚石和石墨中碳原子排列方式不同,决定其物理性质不同,但碳原子结构相同,化学性质基本相同,
说法错误,符合题意;
D、在一定条件下,1g金刚石能生成1g石墨,符合质量守恒定律,说法正确,不符合题意;
故选C。
14. 若用表达式“HSO +X→盐+Y”归纳总结稀硫酸的化学性质,观点正确的是
2 4
选项 X的物质类别 稀硫酸的性质描述
A 金属 若X为Cu,则Y一定为H
2
B 金属氧化物 若X为Fe O,则盐一定为FeSO
2 3 4
C 碱 Y一定为HO
2
D 盐 生成的盐一定为白色沉淀
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A、若X为Cu,铜的金属活动性排在氢的后面,不能与稀硫酸反应,故A错误;
B、氧化铁和硫酸反应生成硫酸铁和水,所以X为氧化铁,则盐为硫酸铁,而不是硫酸亚铁,故B错误;
为
C、若X 碱,而硫酸属于酸,酸碱中和产生盐和水,故C正确;
D、若X为盐,可以为碳酸钠,碳酸钠与硫酸反应生成硫酸钠和碳酸,碳酸不稳定分解生成二氧化碳和水,
而生成的盐为硫酸钠,易溶于水,故D错误。
故选C。
二、选择题(15~17每题均有1~2个正确选项)
15. 通过下列反应,无法得到单质的是
A. 分解反应 B. 置换反应 C. 化合反应 D. 复分解反应
【答案】CD
【解析】
【详解】A.分解反应可能生成单质,例如电解水可以得到氢气和氧气,氢气和氧气都属于单质;
B.置换反应是指由一种单质和一种化合物反应,生成另外一种单质和一种化合物的反应,生成物中含有单
质;C.化合反应是由两种或两种以上的物质反应生成的一种物质,生成物一定属于化合物;
D.复分解反应是两种化合物交换成分生成另外两种化合物的反应,反应物和生成物都是化合物。
故选CD。
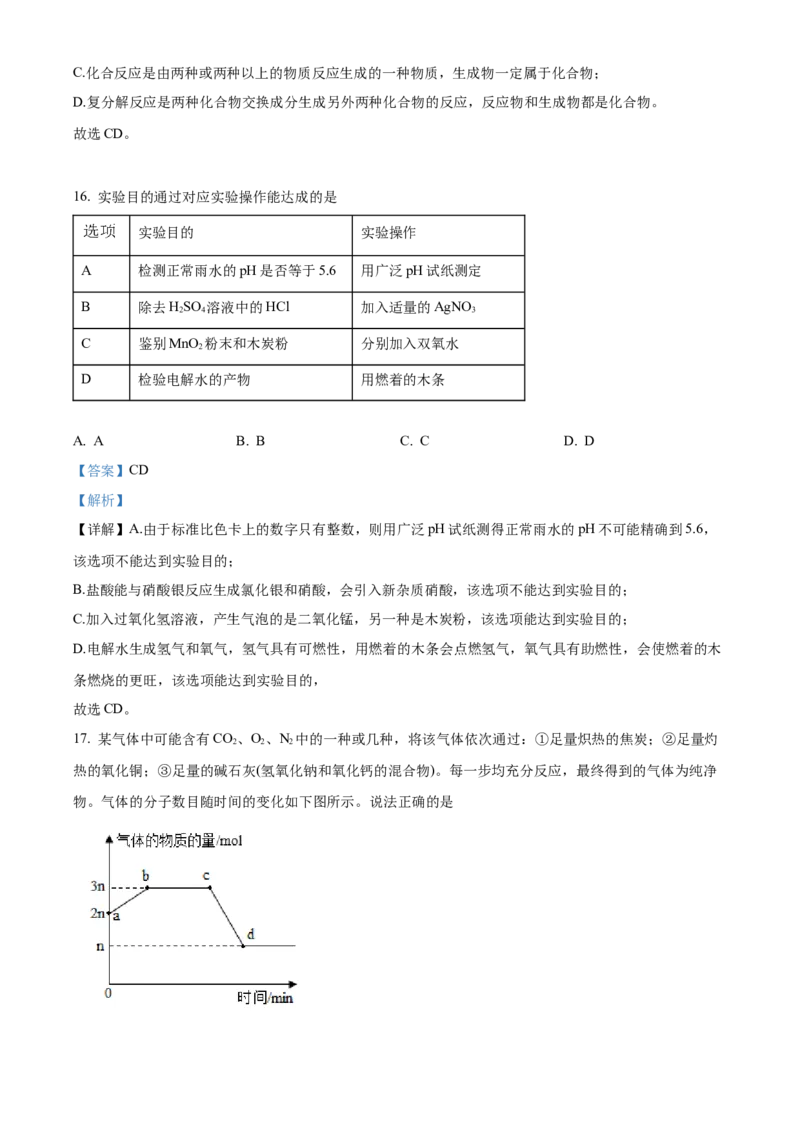
16. 实验目的通过对应实验操作能达成的是
实验目的 实验操作
A 检测正常雨水的pH是否等于5.6 用广泛pH试纸测定
B 除去HSO 溶液中的HCl 加入适量的AgNO
2 4 3
C 鉴别MnO 粉末和木炭粉 分别加入双氧水
2
D 检验电解水的产物 用燃着的木条
A. A B. B C. C D. D
【答案】CD
【解析】
【详解】A.由于标准比色卡上的数字只有整数,则用广泛pH试纸测得正常雨水的pH不可能精确到5.6,
该选项不能达到实验目的;
B.盐酸能与硝酸银反应生成氯化银和硝酸,会引入新杂质硝酸,该选项不能达到实验目的;
C.加入过氧化氢溶液,产生气泡的是二氧化锰,另一种是木炭粉,该选项能达到实验目的;
D.电解水生成氢气和氧气,氢气具有可燃性,用燃着的木条会点燃氢气,氧气具有助燃性,会使燃着的木
条燃烧的更旺,该选项能达到实验目的,
故选CD。
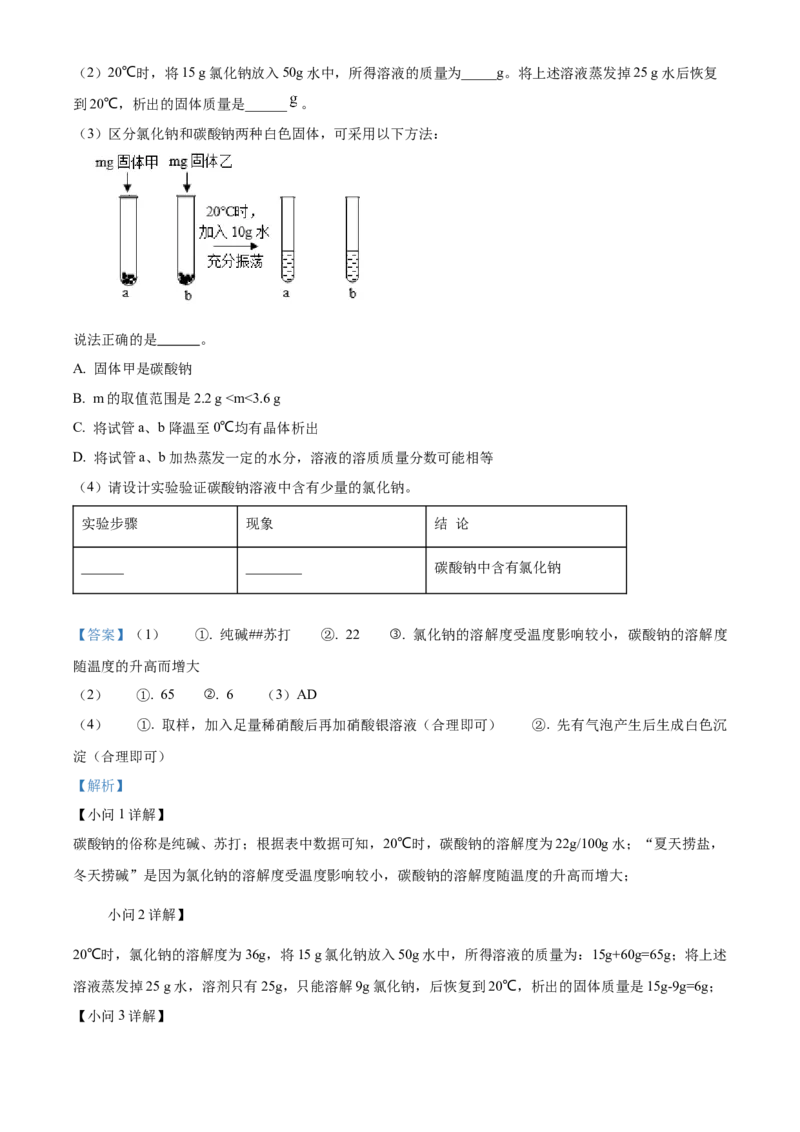
17. 某气体中可能含有CO、O、N 中的一种或几种,将该气体依次通过:①足量炽热的焦炭;②足量灼
2 2 2
热的氧化铜;③足量的碱石灰(氢氧化钠和氧化钙的混合物)。每一步均充分反应,最终得到的气体为纯净
物。气体的分子数目随时间的变化如下图所示。说法正确的是A. a点气体中一定含有N,可能含有O 或CO
2 2 2
B. b点气体中CO和N 的分子数目比为2∶1
2
C. b点气体可能由三种分子构成
D. c→d点过程中发生了复分解反应
【答案】AB
【解析】
【分析】①通过足量炽热的焦炭,可能发生反应:碳和氧气完全燃烧生成二氧化碳 ,二
氧化碳和碳高温下生成一氧化碳, ,反应后,分子数增加 ;
②通过足量灼热的氧化铜:一氧化碳和氧化铜在加热下生成铜和二氧化碳, ,反应
后气体分子数不变;
③通过足量的碱石灰(氢氧化钠和氧化钙的混合物):氢氧化钠和二氧化碳反应生成碳酸钠和水:
;如果气体中不含氮气,则最后气体的分子数为0,由图可知,最后分子
数为n,且得到的气体为纯净物,则剩余气体为氮气,分子数为n;ab段分子数增加n,说明ab反应后气
体中存在一氧化碳气体,则混合气中含有氧气或二氧化碳或两者都有;bc段分子数不变,cd段分子数减小,
是因为一氧化碳和氧化铜反应生成了二氧化碳,二氧化碳被碱石灰吸收;
【详解】A、由分析可知,a点气体中一定含有N,同时含CO 和O 中的至少一种,符合题意;
2 2 2
B、由分析可知,ab段二氧化碳和氧气都完全转化为了一氧化碳,故b点气体为一氧化碳和氮气的混合物,
氮气的分子数为n,则一氧化碳的分子数为2n,故b点气体中CO和N 的分子数目比为2∶1,符合题意;
2
C、由分析可知,b点气体为一氧化碳和氮气的混合物,不符合题意;
D、c→d点过程中二氧化碳和氢氧化钠反应生成碳酸钠和水,不属于基本反应类型,不符合题意。
故选AB。
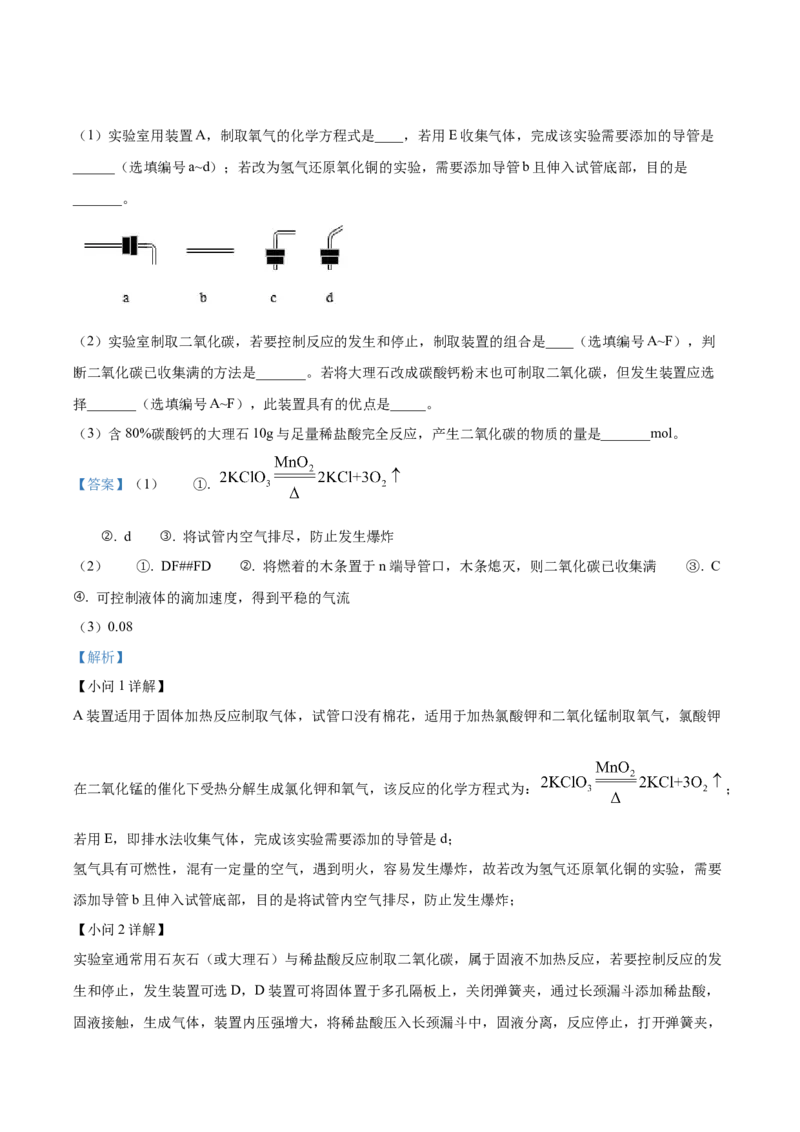
三、简答题(共30分)
18. 2022年2月在北京成功举办了第24届冬季奥运会,体现了“绿色冬奥”的理念。
(1)冬奥会国家速滑馆“冰丝带”的制冰过程采用了二氧化碳跨临界直冷技术,固体的二氧化碳称为
______(填名称);二氧化碳气体转变成固体的过程,从微观角度看,发生改变的是________。
(2)冬奥会采用“氢能点燃火炬,微火照亮世界”,真正实现碳的“零排放”。用氢气作为燃料的原因是____(用化学方程式表示),采用“微火”的原因是______。
(3)冬奥场馆提供的直饮水经过二氧化氯(ClO )消毒处理。ClO 中氯元素的化合价是____;ClO 的摩
2 2 2
尔质量是__,1 mol的ClO 中约含氯原子__个,含氧元素的质量是____g。
2
【答案】(1) ①. 干冰 ②. 分子间的间隙
(2) ①.
②. 节约能源
(3) ①. +4 ②. 67.5g/mol ③. 6.02×1023 ④. 32
【解析】
【小问1详解】
固体的二氧化碳称为干冰;
二氧化碳气体转变成固体的过程,分子之间的间隔发生了改变,分子的大小不变;
【小问2详解】
氢气具有可燃性,氢气燃烧生成水,故可用氢气作为燃料,该反应的化学方程式为:
;
采用“微火”,可以节约能源;
【小问3详解】
二氧化氯中氧元素显-2价,设氯元素的化合价为x,根据化合物中,正、负化合价的代数和为零,可得:
x+(-2)×2=0,x=+4;
ClO 的相对原子质量是:35.5+16×2=67.5,摩尔质量是67.5g/mol;
2
1 mol的ClO 中约含氯原子:1mol×1×6.02×1023=6.02×1023个;
2
含氧元素的质量是:1mol×2×16g/mol=32g。
19. 氯化钠和碳酸钠在不同温度下的溶解度见下表:
温度(℃) 0 10 20 30 40
氯化钠 35.7 35.8 36 36.3 36.6
溶解度
(g/100g水)
碳酸钠 7 12.5 22 40 48.8
(1)碳酸钠的俗称是_____;20℃时,碳酸钠的溶解度为______g/100g水。我国北方许多盐湖中溶有氯化
钠和碳酸钠,在这里有“夏天捞盐,冬天捞碱”的说法,试解释产生这种现象的原因______。(2)20℃时,将15 g氯化钠放入50g水中,所得溶液的质量为_____g。将上述溶液蒸发掉25 g水后恢复
到20℃,析出的固体质量是______ 。
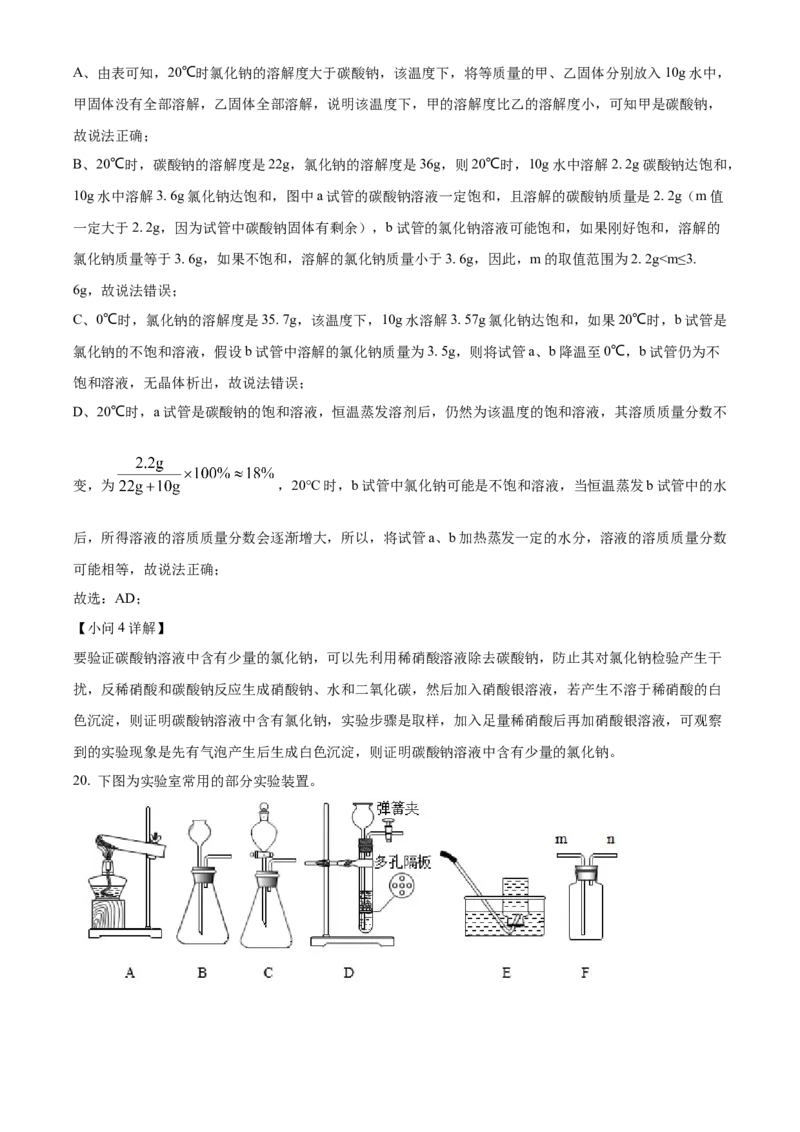
(3)区分氯化钠和碳酸钠两种白色固体,可采用以下方法:
说法正确的是 。
A. 固体甲是碳酸钠
B. m的取值范围是2.2 g Cu的过程是________(填①-⑤)。
(6)溶液丙能否直接排放?请说明理由________
【答案】(1)(2)将铁完全转化为FeCl
2
(3)FeCl 、NaCl
2
(4)HO (5)①②
2
(6)不能直接排放,溶液丙中含氢氧化钠,会污染环境
【解析】
【分析】废液中含有氯化钠、氯化铜和氯化亚铁,由于目的是获得铜和铁红,所以需要在过程中铜离子转
化为铜单质,根据流程可以看成铜应该出现在固体甲中,所以A就是转化铜离子用的铁粉,为使铜离子彻
底转化,所以应该加入过量的铁粉,这样导致固体甲为生成的铜和剩余的铁粉,当加入过量盐酸时,使铁
粉完全从铜粉中除掉,所以固体乙是纯净的铜粉,溶液乙为生成的氯化亚铁和剩余的盐酸,而溶液甲为氯
化钠和氯化亚铁,溶液甲和乙加入过量的B后生成氢氧化亚铁,说明B为氢氧化钠等可溶性碱。
【小问1详解】
由分析可知,加入过量的A是铁与氯化铜反应生成铜和氯化亚铁,化学方程式为:
;
【小问2详解】
当加入过量盐酸时,使铁粉完全从铜粉中除掉,过量盐酸的作用是将铁完全转化为FeCl ;
2
【小问3详解】
根据分析可知,溶液甲的溶质为FeCl 、NaCl;
2
【小问4详解】
由 可知,反应前后铁原子都是4个,反应后氢原子是12个,反应前应该是
12个,其中4个包含在2X,反应后氧原子是12个,反应前应该是12个,其中2个包含在2X中,则X的
化学式为HO;
2
【小问5详解】
过程①发生的是铁与氯化铜反应生成氯化亚铁和铜,可证明铁的活动性大于铜,过程②是固体铁和铜与稀
盐酸反应,只有铁与稀盐酸反应生成氯化亚铁和氢气,可证明铁的活动性大于铜的活动性,过程③中发生
两个反应;氯化亚铁和氢氧化钠反应;盐酸和氢氧化钠反应,无法证明铁与铜的金属活动性强弱,过程④
是氢氧化亚铁氧化为氢氧化铁的反应,无法证明铁与铜的金属活动强弱,过程⑤是氢氧化铁分解生成氧化
铁的反应,无法证明铁与铜的金属活动性强弱,则能证明金属活动性Fe>Cu的过程是①②;
【小问6详解】
溶液丙中含有过量的氢氧化钠,所以溶液丙不能直接排放,溶液丙中含氢氧化钠,会污染环境。