文档内容
化学部分
相对原子质量:H-1 O-16 C-12 Fe-56
一、选择题(共20分)
1. 北京冬奥会主场馆“冰丝带”采用二氧化碳直冷技术制冰,二氧化碳属于
A. 氧化物 B. 酸 C. 碱 D. 盐
【答案】A
【解析】
【详解】A、氧化物是由两种元素组成,且其中一种元素为氧元素的化合物,二氧化碳是由氧元素和碳元
素组成的化合物,所以为氧化物,故符合题意;
B、在水溶液中解离出的阳离子全部为氢离子的化合物是酸,故不符合题意;
C、在水溶液中解离出的阴离子全部为氢氧根离子的化合物是碱,故不符合题意;
D、盐是由金属离子或铵根离子与酸根离子构成的化合物,故不符合题意。
故选A。
2. 铝元素符号书写正确的是
A. Lv B. Lu C. Al D. Ar
【答案】C
【解析】
【详解】铝元素的元素符号为Al;
故选C。
3. 属于有机物的是
A. 食盐 B. 蒸馏水 C. 碳酸 D. 乙醇
【答案】D
【解析】
【分析】有机物是含碳化合物(一氧化碳、二氧化碳、碳酸、碳酸盐、碳酸氢盐、金属碳化物、氰化物、
硫氰化物等物质除外)或碳氢化合物及其衍生物的总称。
【详解】A、食盐是NaCl,属于化合物;
B、蒸馏水为HO,属于无机物;
2
C、碳酸为HCO,属于无机物;
2 3
D、乙醇为C HO,属于有机物;
2 6
故选D。
4. MnO 中锰元素的化合价是
2
A. +1 B. +2 C. +3 D. +4【答案】D
【解析】
【详解】MnO 中氧元素化合价为-2价,设锰元素化合价为x,根据化合物中正负化合价代数为0,则有
2
x+(-2)×2=0,得x=+4价,故选D。
5. 焰色反应时火焰呈黄色的物质是
A. 氯化铁 B. 氯酸钾 C. 氯化铵 D. 氢氧化钠
【答案】D
【解析】
【详解】焰色反应是物理变化。它并未生成新物质。
焰色反应 :钠黄锂紫红,钾紫铷浅紫, 钙砖红锶洋红,铜绿钡黄绿。
并不是所有的元素都有特殊的颜色。镁、铝还有铁、铂、镍等金属无焰色。
A、氯化铁无焰色反应。
B、氯酸钾焰色反应时火焰呈紫色。
C、氯化铵无焰色反应。
D、氢氧化钠色反应时火焰呈黄色。
综上所述:选择D。
6. 属于悬浊液的是
A. 自来水 B. 纯净水 C. 粗盐水 D. 矿泉水
【答案】C
【解析】
【分析】悬浊液是难溶性固体与液体形成的不均一、不稳定的混合物;乳浊液是小液滴分散到液体里而形
成的不均一、不稳定的混合物;溶液是可溶性固体和液体形成的均一、稳定的混合物。
的
【详解】A、自来水是可溶性钙、镁化合物等溶于水形成 均一、稳定的混合物,属于溶液,故选项错误;
B、纯净水中只含有一种物质水,属于纯净物,故选项错误;
C、粗盐中含有难溶于水的杂质,可以形成悬浊液,故选项正确;
D、矿泉水是均一、稳定的混合物,属于溶液,故选项错误。
故选:C。
7. NaSO 与NaHSO 都属于
2 4 4
A. 硫酸 B. 钠盐 C. 正盐 D. 酸式盐
【答案】B
【解析】【详解】A、硫酸为HSO ,故选项不符合题意;
2 4
B、NaSO 电离产生Na+与 ,NaHSO 电离产生Na+、H+与 ,两物质电离都产生Na+,则两物质
2 4 4
都属于钠盐,故选项符合题意;
C、正盐是指既不能电离出氢离子,也不能电离出氢氧根离子的盐,NaHSO 电离产生H+,则不属于正盐,
4
故选项不符合题意;
D、酸式盐为可电离出氢离子的盐,NaHSO 电离产生Na+、H+与 ,属于酸式盐;NaSO 电离不产生
4 2 4
H+,不属于酸式盐,故选项不符合题意;
故选B。
的
8. 互为同素异形体 是
A. 石灰水与石灰浆 B. 金刚石与石墨
C. 二氧化碳与一氧化碳 D. 氧气与液氧
【答案】B
【解析】
【分析】由同种元素形成的不同种单质互为同素异形体,即互为同素异形体的物质要满足:同种元素组成;
不同单质。
【详解】A、石灰水与石灰浆主要成分都是氢氧化钙,不属于同素异形体,故A错误;
的
B、金刚石与石墨都是由碳元素形成 不同物质,都是单质,互为同素异形体,故B正确;
C、二氧化碳与一氧化碳是两种不同的化合物,不是单质,故不属于同素异形体,故C错误;
D、氧气和液氧都是同一种单质的不同状态,是同一种单质,不属于同素异形体,故D错误;
故选B。
9. 空气的成分中氧元素以游离态存在的是
A. 氧气 B. 氮气 C. 二氧化碳 D. 水蒸气
【答案】A
【解析】
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成;纯净物是由一种物质组成。
纯净物又分为单质和化合物。由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物叫
化合物。氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素。元素以单质形式存在叫游离态,
元素以化合物的形式存在叫化合态。
【详解】A、氧气中氧元素只以游离态存在,故选项正确;
B、氮气中氮元素只以游离态存在,故选项错误;C、二氧化碳中氧元素只以化合态存在,故选项错误;
D、水蒸气中氧元素只以化合态存在,故选项错误。
故选:A。
10. 不能与石灰水反应的物质是
A. 氧化铜 B. 二氧化碳 C. 稀盐酸 D. 硫酸铜溶液
【答案】A
【解析】
【详解】A、石灰水主要成分是氢氧化钙,氧化铜不能与氢氧化钙反应,故A符合题意;
B、二氧化碳能和氢氧化钙反应生成碳酸钙沉淀和水,故B不符合题意;
C、稀盐酸能和氢氧化钙反应生成氯化钙和水,故C不符合题意;
D、硫酸铜能和氢氧化钙反应生成沉淀氢氧化铜和硫酸钙,故D不符合题意。
故选A。
11. 将“嫦娥五号”探测器送入预定轨道的“遥五运载火箭”,使用液氢、液氧作为推进剂,不属于氢能
的优势是
A. 相同质量的氢气燃烧产生的热量是汽油的三倍
B. 氢气的燃烧速度是汽油的十倍以上
C. 制氢气的原料丰富,比如各类活泼金属与酸
D. 氢气燃烧后生成水
【答案】C
【解析】
【详解】A、氢气的热值大约是汽油热值的3倍,则相同质量的氢气燃烧产生的热量是汽油的三倍,故属
于氢能源的优势;
B、氢气为气体燃料,汽油为液体燃料,气体燃料燃烧时与氧气接触面积较大,氢气的燃烧速度是汽油的
十倍以上,故属于氢能源的优势;
C、制氢气的原料丰富,比如各类活泼金属与酸,但此种生产氢气的方式成本较高,故不属于氢能源的优
势;
D、氢气与氧气燃烧产物为水,无污染,故属于氢能源的优势;
故选C。
12. 属于复分解反应的是
A. 加热氧化铜与木炭 B. 加热氧化铜与稀盐酸
C. 加热胆矾 D. 加热氯酸钾与二氧化锰
【答案】B
【解析】【详解】A、加热氧化铜与木炭,反应的化学方程式为: ,根据化学方程式可
知该反应为单质与化合物反应生成另一种单质和另一种化合物的反应,属于置换反应,不符合题意;
B、加热氧化铜与稀盐酸,反应的化学方程式为: ,根据化学方程式可知该反
应是两种化合物彼此交换成分,生成了另外两种化合物的反应,属于复分解反应,符合题意;
C、加热胆矾会分解为无水硫酸铜和水,属于分解反应,不符合题意;
D、加热氯酸钾与二氧化锰,反应的化学方程式为: ,根据化学方程式可知
该反应由一种物质生成了两种物质,属于分解反应,不符合题意。故选B。
【点睛】本题重在考查四种基本反应类型的区分。化合反应是多变一,分解反应是一变多,置换反应是一
换一,复分解反应是双交换,价不变。
13. 实验室试剂取用方法正确的是
A. 用镊子取少量无水硫酸铜粉末至试管中
B. 用纸槽取少量氢氧化钠固体至试管中
C. 用倾倒法取少量酚酞试液至试管中
D. 用胶头滴管取少量硝酸银溶液至试管中
【答案】D
【解析】
【详解】A.块状固体药品可以用镊子取用,无水硫酸铜粉末可用药匙或纸槽装入试管中,故说法错误,不
符合题意;
B.氢氧化钠固体易潮解且有腐蚀性,不可用纸槽装入试管中,故说法错误,不符合题意;
C.酚酞试液是指示剂,少量取用即可,少量取用液体药品用胶头滴管,倾倒法一般取用大量液体药品,故
说法错误,不符合题意;
D.少量取用液体药品用胶头滴管,用胶头滴管取少量硝酸银溶液至试管中,故说法正确,符合题意。
故选D。
14. 下图是测定空气中氧气体积分数的实验装置,从微观角度对该实验分析正确的是A. 反应前后,原子的种类和个数都发生了改变
B. 反应前后,分子的种类和个数都发生了改变
C. 反应结束后,打开弹簧夹前后,集气瓶中气体分子种类明显增多
D. 反应结束后,打开弹簧夹前后,集气瓶中气体分子数明显减少
【答案】B
【解析】
【详解】A、化学反应遵循质量守恒定律,反应前后原子的种类和个数都不变,故A错误;
B、该实验中发生的反应为: ,反应前后分子种类发生了改变,分子个数由5个变2
个,故分子个数也发生了改变,故反应前后,分子的种类和个数都发生了改变,故B正确;
C、反应结束后,打开弹簧夹前,空气中的氧气被反应掉,打开弹簧夹后,水倒流到集气瓶内,剩余气体
成分依然未改变,故集气瓶中气体分子种类不变,故C错误;
D、由C选项分析可知:集气瓶中气体分子种类不变,故D错误;
故选B。
15. 1956年中国首次人工合成结晶牛胰岛素,说法正确的是
A. 晶体都带有结晶水
B. 晶体具有规则的几何形状
C. 形成晶体的过程称为蒸发
D. 从不饱和溶液中析出晶体,一般需要消耗能量
【答案】BD
【解析】
【详解】A、晶体不一定都带有结晶水,如明矾为五水硫酸铜,带有结晶水;氯化钠晶体,不带结晶水,故A错误;
B、晶体具有规则的几何形状,故B正确;
C、形成晶体的过程称为结晶,故C错误;
D、从不饱和溶液中析出晶体,一般需要蒸发溶剂或降低温度,一般需要消耗能量,故D正确;
故选BD。
16. 生锈的铁钉与过量稀硫酸在试管中反应,现象描述错误的是
A. 产生气泡 B. 反应结束后,铁钉质量减少
C. 溶液变黄,溶液溶质为硫酸铁 D. 待冷却至室温后,反应停止
【答案】CD
【解析】
【分析】生锈的铁钉表面会有铁锈覆盖,铁锈的主要成分为氧化铁,氧化铁与稀硫酸反应生成硫酸铁与水,
硫酸铁的溶液呈黄色;当铁锈反应结束后铁与稀硫酸反应生成硫酸亚铁与氢气,硫酸亚铁的溶液呈浅绿色。
【详解】A、当铁锈反应完后,铁与稀硫酸反应生成氢气,实验现象中会有气泡产生,故选项说法正确;
B、生锈的铁钉中铁锈与铁反应中都被消耗,则反应后铁钉的质量减少,故选项说法正确;
C、反应中有硫酸铁产生,则实验现象中观察到溶液变黄,但溶液溶质为硫酸铁不属于实验现象,故选项
说法错误;
D、待冷却至室温后,反应停止不属于实验现象的描述,故选项说法错误;
故选CD。
17. 实验室用60 g 3%H O 水溶液制取氧气,平均分三次加入,每次加入时,发生装置内的反应液已完全反
2 2
应,说法正确的是
A. 三次制取氧气的量一样 B. 三次反应的剧烈程度一样
C. 第三次加入后,溶质质量分数最大为1.02% D. 第三次加入后,溶质质量分数最大为1%
【答案】AC
【解析】
【详解】A、60g3%的过氧化氢溶液,平均分成三等分,每等分的过氧化氢溶液中的溶质质量相等,每一
等分完全反应制取的氧气质量相等,所以,三次制取氧气的量一样,故选项说法正确;
B、影响化学反应剧烈程度的因素之一是反应物的浓度,其他条件相同时,溶液浓度越大,反应越剧烈;
第一次加入的过氧化氢溶液浓度是3%,过氧化氢在二氧化锰催化下分解为水和氧气,完全反应后容器中
剩余水和二氧化锰,第二次加入20g3%的过氧化氢溶液时,过氧化氢溶液被水稀释,所得溶液浓度小于
3%,反应剧烈程度降低,过氧化氢溶液完全反应后,容器中剩余水量增多,第三次加入20g3%的过氧化氢
溶液时,过氧化氢溶液继续被稀释,所得溶液浓度更小,反应更慢,故选项说法错误;
C、设第二次加入20g3%的过氧化氢溶液完全反应后,生成氧气的总质量为x,则x≈0.56g
由质量守恒定律可知,第二次加入20g3%过氧化氢溶液完全反应后,容器中水的质量为40g-0.
56g-0.56g=38.88g,第三次加入20g3%的过氧化氢溶液,过氧化氢未分解时溶液浓度最大,其最大值为
,故选项说法正确;
D、由上述C选项计算可知,第三次加入后,溶质质量分数最大约为1.02%,而不是最大为1%,故选项说
法错误。
故选:AC。
二、简答题(共30分)
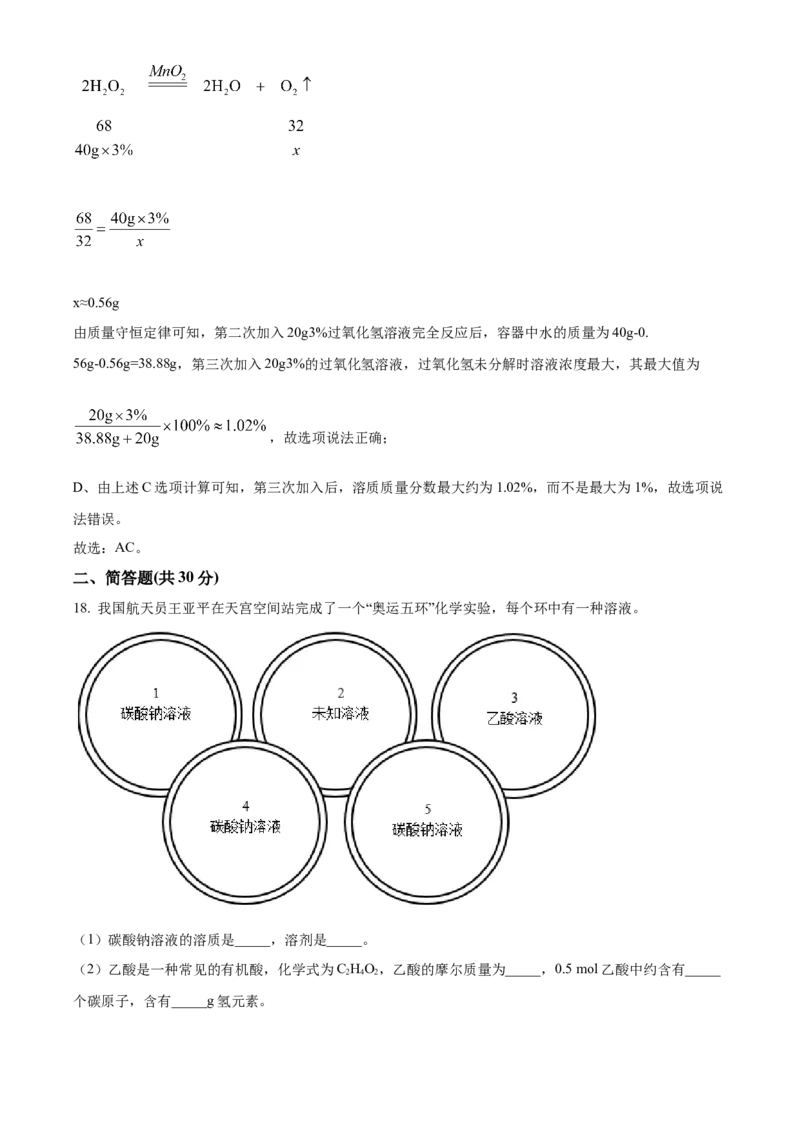
18. 我国航天员王亚平在天宫空间站完成了一个“奥运五环”化学实验,每个环中有一种溶液。
(1)碳酸钠溶液的溶质是_____,溶剂是_____。
(2)乙酸是一种常见的有机酸,化学式为C HO,乙酸的摩尔质量为_____,0.5 mol乙酸中约含有_____
2 4 2
个碳原子,含有_____g氢元素。(3)为使五环变色,分别向1号环和3号环中滴加几滴紫色石蕊溶液并混合均匀,分别观察到1号环由无
色变为蓝色,3号环由无色变为_____,向4号环中滴加几滴甲基橙溶液并混合均匀,观察到4号环由无色
变为黄色,说明甲基橙溶液遇_____(选填“酸性”、“碱性”或“中性”)溶液变黄色。向5号环滴加几滴紫色石
蕊和甲基橙并混合均匀后,观察到溶液由无色变绿色。
(4)向2号环中先滴加几滴淀粉溶液,再滴加几滴稀硫酸,发生以下反应,生成的碘遇淀粉变深蓝色。请
补全以下化学方程式。5KI+KIO +3H SO =3K SO +3I +3_____
3 2 4 2 4 2
【答案】(1) ①. 碳酸钠 ②. 水
(2) ①. 60g/mol ②. 6.02×1023 ③. 2
(3) ①. 红 ②. 碱性
(4)HO
2
【解析】
【小问1详解】
碳酸钠溶液的溶质是碳酸钠,溶剂是水;
【小问2详解】
乙酸化学式是C HO,其相对分子质量为12×2+4+16×2=60,所以摩尔质量为60g/mol;1mol乙酸中含有
2 4 2
6.02×1023个醋酸分子,一个乙酸分子中含有2个碳原子,故0.5mol 乙酸中含有6.02×1023个碳原子;含有
氢元素的质量为0.5mol×60g/mol× ×100%=2g;
【小问3详解】
为使五环变色,分别向1号环和3号环中滴加几滴紫色石蕊溶液并混合均匀,分别观察到1号环由无色变
为蓝色,3号环为乙酸(紫色石蕊溶液遇酸变红色)由无色变为红色,向4号环为碳酸钠(溶液显碱性)
中滴加几滴甲基橙溶液并混合均匀,观察到4号环由无色变为黄色,说明甲基橙溶液遇碱性溶液变黄色。
【小问4详解】
根据质量守恒定律,反应前:6K、6I、6H、3S、15O,反应后:6K、6I、3S、12O,故3个分子中有6H、
3O,化学式为HO。
2
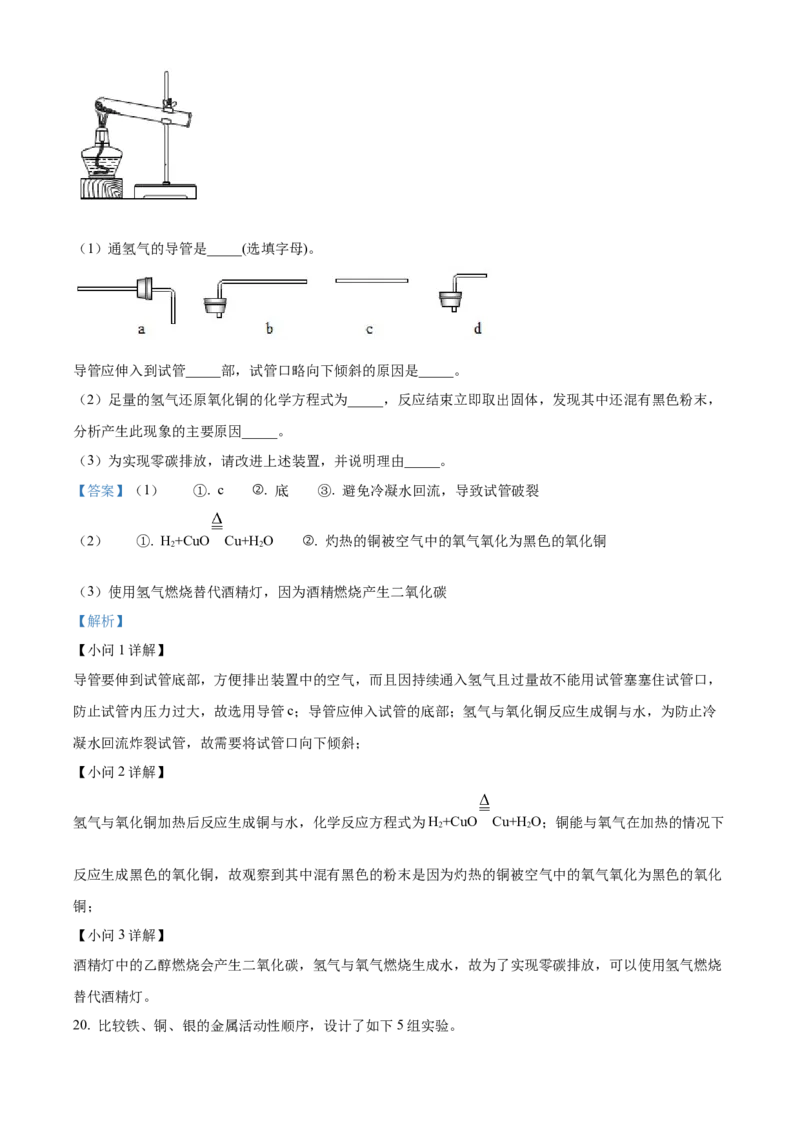
19. 氢冶金是指使用氢气替代煤炭冶炼金属,实现零碳排放。我们在化学实验室,可以用氢气还原氧化铜
制得少量金属铜。(1)通氢气的导管是_____(选填字母)。
导管应伸入到试管_____部,试管口略向下倾斜的原因是_____。
(2)足量的氢气还原氧化铜的化学方程式为_____,反应结束立即取出固体,发现其中还混有黑色粉末,
分析产生此现象的主要原因_____。
(3)为实现零碳排放,请改进上述装置,并说明理由_____。
【答案】(1) ①. c ②. 底 ③. 避免冷凝水回流,导致试管破裂
(2) ①. H+CuO Cu+H O ②. 灼热的铜被空气中的氧气氧化为黑色的氧化铜
2 2
(3)使用氢气燃烧替代酒精灯,因为酒精燃烧产生二氧化碳
【解析】
【小问1详解】
导管要伸到试管底部,方便排出装置中的空气,而且因持续通入氢气且过量故不能用试管塞塞住试管口,
防止试管内压力过大,故选用导管c;导管应伸入试管的底部;氢气与氧化铜反应生成铜与水,为防止冷
凝水回流炸裂试管,故需要将试管口向下倾斜;
【小问2详解】
氢气与氧化铜加热后反应生成铜与水,化学反应方程式为H+CuO Cu+H O;铜能与氧气在加热的情况下
2 2
反应生成黑色的氧化铜,故观察到其中混有黑色的粉末是因为灼热的铜被空气中的氧气氧化为黑色的氧化
铜;
【小问3详解】
酒精灯中的乙醇燃烧会产生二氧化碳,氢气与氧气燃烧生成水,故为了实现零碳排放,可以使用氢气燃烧
替代酒精灯。
20. 比较铁、铜、银的金属活动性顺序,设计了如下5组实验。实验编号 金属丝(直径1 mm) 溶液
A 0.056g铁丝 5mL5%稀盐酸
B 0.056g铜丝 5mL5%稀盐酸
C 0.056g银丝 5mL5%稀盐酸
.
D 0056g铁丝 5mL5%硫酸铜溶液
E
(1)铁、铜、银中金属活动性最强的是_____,A组反应的化学方程式是_____。
(2)D组反应的现象是_____,请补全E组实验试剂_____ _____。
(3)实验结束后,发现D组中0.056g铁丝已完全反应,求消耗多少mol硫酸铜?_____(请根据化学方程
式列式计算)
(4)回收未完全反应的金属丝,收集A、B、C、D组实验的废液,放置一段时间后得到含盐酸、氯化铁、
硫酸铁和硫酸铜的混合溶液,向其中逐滴滴加氢氧化钠溶液,直至溶液变为中性,此时溶液中的溶质是
_____ (硫酸铁、氯化铁、硫酸铜溶液均显酸性)。
.
【答案】(1) ① 铁##Fe ②.
(2) ①. 铁丝表面析出红色固体 ②. 0.056g铜丝(或0.056g银丝) ③. 5mL 5%硝酸银溶液
(或5mL 5%硫酸铜溶液)
(3)解:设消耗硫酸铜的质量为x
x=0.16g
故消耗硫酸铜的物质的量为:0.16g÷160g/mol=0.001mol
答:消耗硫酸铜的物质的量为0.001mol
(4)硫酸钠、氯化钠
【解析】【小问1详解】
铁能与稀盐酸反应生成氯化亚铁和氢气,产生气泡,说明在金属活动性顺序里,铁排在氢前,铜、银与稀
盐酸不反应,无明显现象,说明在金属活动性顺序里,铜、银排在氢后,故铁、铜、银中金属活动性最强
的是铁;
A组反应为铁和稀盐酸反应生成氯化亚铁和氢气,该反应的化学方程式为: ;
【小问2详解】
D组铁和硫酸铜反应生成硫酸亚铁和铜,故现象是:铁丝表面析出红色固体;
铁能与稀盐酸反应生成氯化亚铁和氢气,产生气泡,说明在金属活动性顺序里,铁排在氢前,铜、银与稀
盐酸不反应,无明显现象,说明在金属活动性顺序里,铜、银排在氢后,故A、B、C可得出铁比铜、银
活泼;D组中,铁与硫酸铜反应生成硫酸亚铁和铜,有红色固体析出,说明铁比铜活泼,故还需验证铜和
银的金属活动性顺序,故E组实验可以是:0.056g铜丝,5mL 5%硝酸银溶液,铜能与硝酸银反应生成硝酸
铜和银,有银白色固体析出,说明铜比银活泼,或0.056g银丝,5mL 5%硫酸铜溶液,银与硫酸铜不反应,
无明显现象,说明铜比银活泼;
【小问3详解】
见答案;
【小问4详解】
逐滴滴加氢氧化钠溶液,氢氧化钠先与稀盐酸反应生成氯化钠和水,待稀盐酸完全反应后,氢氧化钠和硫
酸铜反应生成氢氧化铜和硫酸钠,氢氧化钠和氯化铁反应生成氢氧化铁和氯化钠,氢氧化钠和硫酸铁反应
生成氢氧化铁和硫酸钠,恰好完全反应时,溶液为中性,此时溶液中的溶质是:硫酸钠、氯化钠。
21. 我国化工专家吴蕴初创办了天原化工厂,以食盐为原料,生产烧碱、盐酸等化工原料。下表是氯化钠
与氢氧化钠的部分溶解度。
温度(℃) 20 40 60 80
氯化钠 35.9 36.4 37.1 38.0
溶解度
(g/100g
水) 氢氧化钠 109 129 174 314
(1)由上表可知,20℃时,氯化钠的溶解度是___,80℃时,溶解度相对较大的物质是___。
(2)20℃时,化工厂电解饱和食盐水后最终可得40%的氢氧化钠溶液,该溶液是氢氧化钠的_____(选填
“饱和”或“不饱和”)溶液。请结合氢氧化钠的性质,分析化工厂能否利用如下流程生产氢氧化钠固体。
_____【答案】(1) ①. 35.9g/100g ②. 氢氧化钠
(2) ①. 不饱和 ②. 否,蒸发浓缩氢氧化钠溶液时,易吸收空气中二氧化碳,产生杂质,得到产
品不纯或降温结晶时,易吸收溶液中的水分,无法得到纯净的固体
【解析】
【小问1详解】
由表可知,20℃时,氯化钠的溶解度是35.9g/100g;80℃时,氢氧化钠的溶解度为314g/100g,氯化钠的溶
解度为38.0g/100g,则氢氧化钠的溶解度相对较大。
【小问2详解】
20℃时,氢氧化钠的溶解度为109g/100g,则该温度下氢氧化钠的饱和溶液的溶质质量分数为
,大于40%,说明40%的氢氧化钠溶液为不饱和溶液;
由于氢氧化钠溶液能与空气中的二氧化碳反应生成碳酸钠,且氢氧化钠易潮解,降温时会吸收水分,则无
法利用该流程生产氢氧化钠固体。