文档内容
化学部分
相对原子质量:H-1 C-12 O-16 Cl-35.5 Ca-40 Cu-64
五、选择题(共20分)21~34题均只有一个正确选项
的
1. 属于纯净物 是
A. 奶粉 B. 大理石 C. 蒸馏水 D. 植物油
2. 与金刚石互为同素异形体的是
A. 焦炭 B. 石墨 C. CO D. C H
2 4
3. 健康人体中一些体液pH值如下所示,其中酸性最强的是
A. 胆液:6.8-7.4 B. 唾液:6.5-7.5 C. 胃液 0.8-1.5 D. 血液:7.35-7.45
4. 属于钾肥的是
A. CO(NH ) B. KCO C. Ca(HPO ) D. NH HCO
2 2 2 3 2 4 2 4 3
5. SiO 中Si的化合价是
2
.
A -4 B. -2 C. +2 D. +4
6. 氧元素以游离态存在的是
A. 臭氧 B. 双氧水 C. 二氧化锰 D. 食盐水
7. 汞的元素符号是
A. Ag B. Hg C. hg D. He
8. 在水中能形成溶液的是
A. 硝酸铜 B. 氢氧化铁 C. 氢氧化铜 D. 氧化铁
.
9 化学变化Mg+HSO =MgSO +H↑属于
2 4 4 2
A. 化合反应 B. 分解反应 C. 复分解反应 D. 置换反应
10. 能鉴别碳酸钠、硫酸钠两种溶液的是
A. 酚酞试剂 B. 氯化钡溶液 C. 焰色反应 D. 硝酸银溶液
11. 物质的用途正确的是
A. 胆矾:检验水
B. 熟石灰:干燥剂
C. 氦气:填充飞艇
D. 稀硫酸:与块状大理石反应制取CO
2
12. 一定可以增大二氧化碳溶解度的方法是
A. 升温加压 B. 升温降压 C. 降温降压 D. 降温加压
13. 与下列实验相关的化学方程式,正确的是A. 比较铜和银的金属活动性:Cu+2AgCl=CuCl +2Ag
2
B. 实验室制取氧气:
C. 稀盐酸除去铁锈:6HCl+Fe O=2FeCl +3H O
2 3 2 2
D. 煅烧石灰石生产生石灰:
14. 氢气还原氧化铜的实验装置如图所示,相关分析正确的是
A. 为充分利用氢气,应先加热再通入氢气
B. 实验中固体由黑色变为红色,试管口有小液滴
C. 实验中固体减少的质量等于生成水的质量
D. 生成的水的物质的量等于通入的氢气的物质的量
35~37题每题均有1~2个正确选项
15. 关于分子、原子的说法正确的是
A. 都是构成物质的微粒
B. 化学变化中都可再分
C. 都是保持物质性质的微粒
D. 都可用物质的量计量
16. 关于一氧化碳的说法正确的是
A. 是一种酸性氧化物
B. 1mol一氧化碳的质量是28g/mol
.
C 一个分子由一个碳原子和一个氧原子构成
D. 可用点燃后观察火焰颜色的方法进行检验
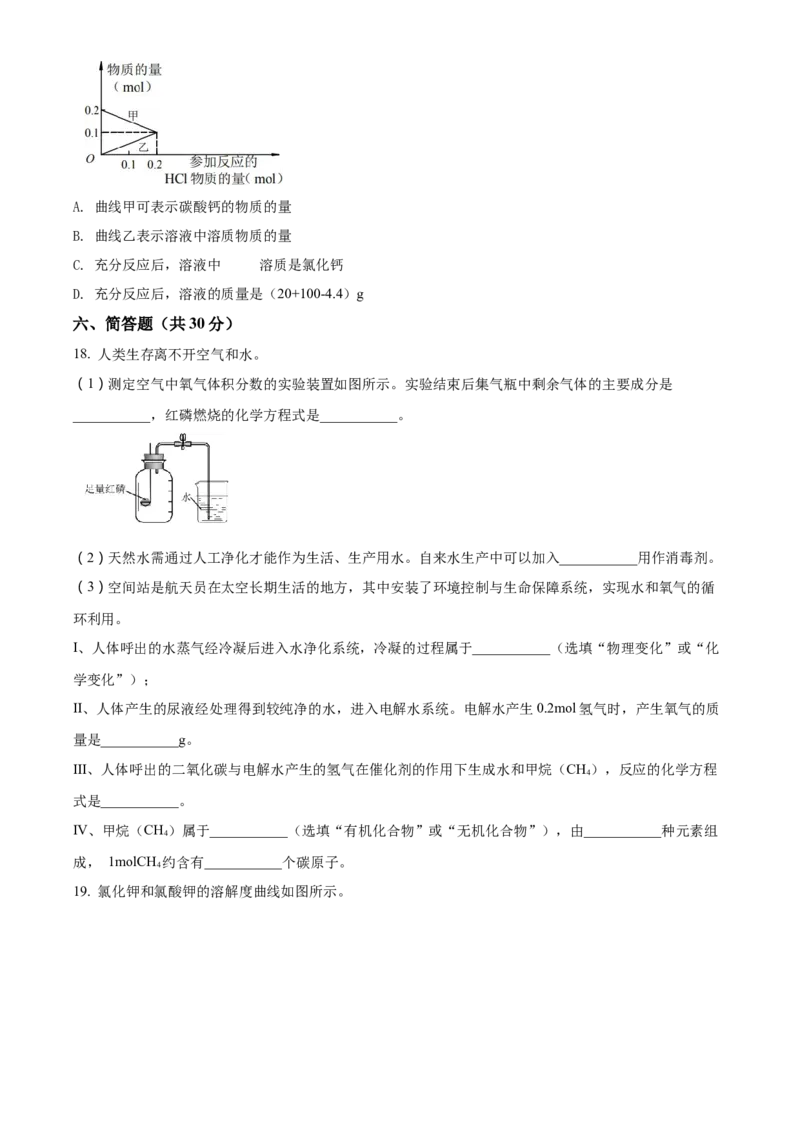
17. 20g碳酸钙粉末与100g含溶质0.2mol的稀盐酸混合(假设二氧化碳全部逸出),某些量的关系如图所
示。相关分析正确的是A. 曲线甲可表示碳酸钙的物质的量
B. 曲线乙表示溶液中溶质物质的量
C. 充分反应后,溶液中 的溶质是氯化钙
D. 充分反应后,溶液的质量是(20+100-4.4)g
六、简答题(共30分)
18. 人类生存离不开空气和水。
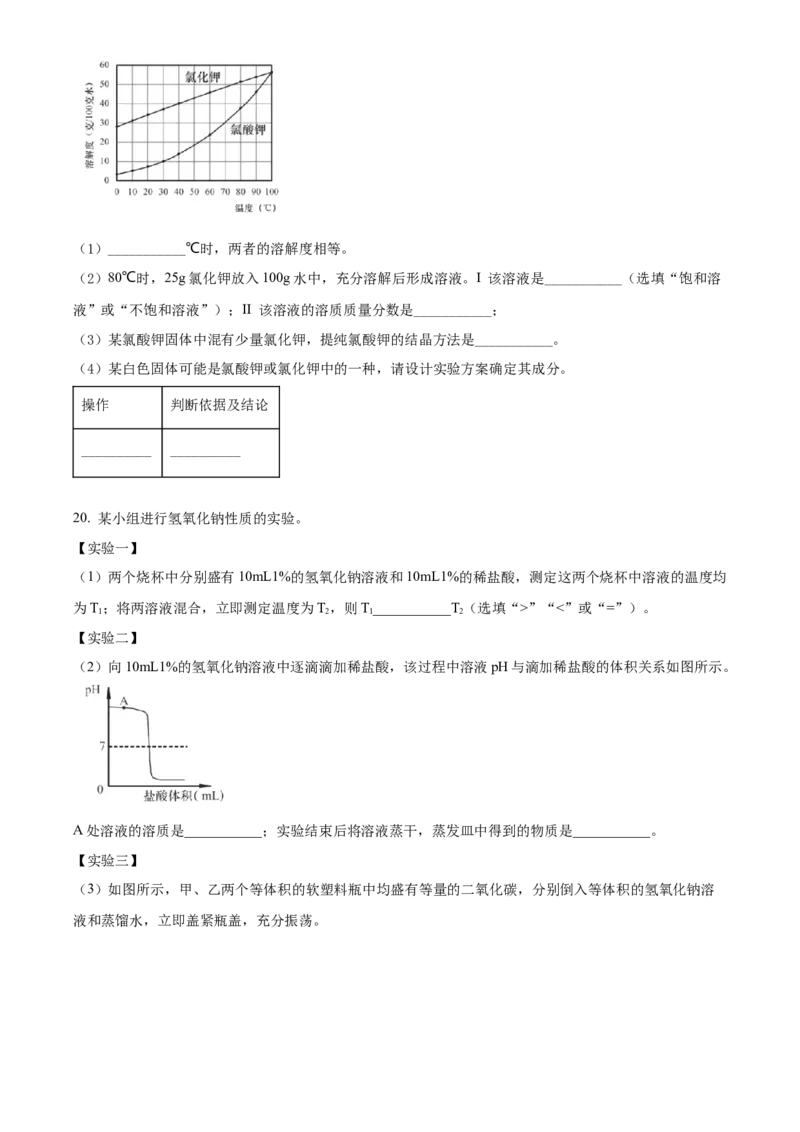
(1)测定空气中氧气体积分数的实验装置如图所示。实验结束后集气瓶中剩余气体的主要成分是
___________,红磷燃烧的化学方程式是___________。
(2)天然水需通过人工净化才能作为生活、生产用水。自来水生产中可以加入___________用作消毒剂。
(3)空间站是航天员在太空长期生活的地方,其中安装了环境控制与生命保障系统,实现水和氧气的循
环利用。
I、人体呼出的水蒸气经冷凝后进入水净化系统,冷凝的过程属于___________(选填“物理变化”或“化
学变化”);
II、人体产生的尿液经处理得到较纯净的水,进入电解水系统。电解水产生0.2mol氢气时,产生氧气的质
量是___________g。
III、人体呼出的二氧化碳与电解水产生的氢气在催化剂的作用下生成水和甲烷(CH),反应的化学方程
4
式是___________。
IV、甲烷(CH)属于___________(选填“有机化合物”或“无机化合物”),由___________种元素组
4
成, 1molCH 约含有___________个碳原子。
4
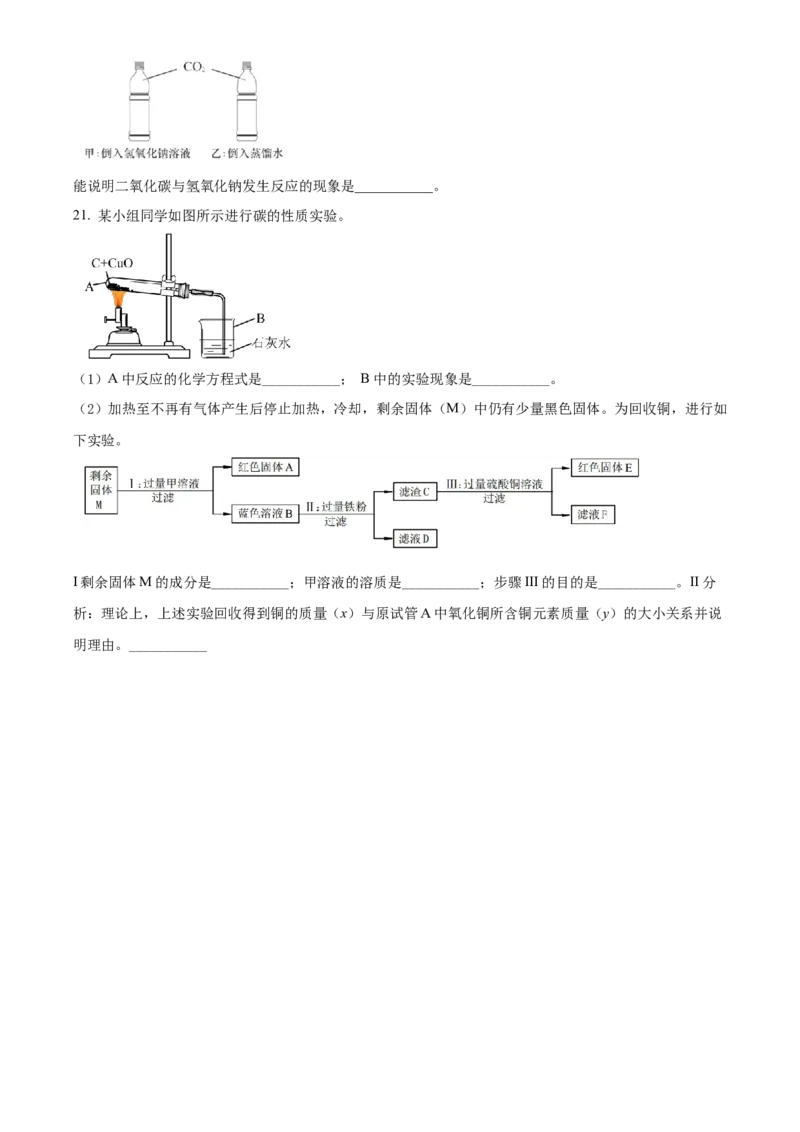
19. 氯化钾和氯酸钾的溶解度曲线如图所示。(1)___________℃时,两者的溶解度相等。
(2)80℃时,25g氯化钾放入100g水中,充分溶解后形成溶液。I 该溶液是___________(选填“饱和溶
液”或“不饱和溶液”);II 该溶液的溶质质量分数是___________;
(3)某氯酸钾固体中混有少量氯化钾,提纯氯酸钾的结晶方法是___________。
(4)某白色固体可能是氯酸钾或氯化钾中的一种,请设计实验方案确定其成分。
操作 判断依据及结论
__________ __________
20. 某小组进行氢氧化钠性质的实验。
【实验一】
(1)两个烧杯中分别盛有10mL1%的氢氧化钠溶液和10mL1%的稀盐酸,测定这两个烧杯中溶液的温度均
为T;将两溶液混合,立即测定温度为T,则T___________T(选填“>”“<”或“=”)。
1 2 1 2
【实验二】
(2)向10mL1%的氢氧化钠溶液中逐滴滴加稀盐酸,该过程中溶液pH与滴加稀盐酸的体积关系如图所示。
A处溶液的溶质是___________;实验结束后将溶液蒸干,蒸发皿中得到的物质是___________。
【实验三】
(3)如图所示,甲、乙两个等体积的软塑料瓶中均盛有等量的二氧化碳,分别倒入等体积的氢氧化钠溶
液和蒸馏水,立即盖紧瓶盖,充分振荡。能说明二氧化碳与氢氧化钠发生反应的现象是___________。
21. 某小组同学如图所示进行碳的性质实验。
(1)A中反应的化学方程式是___________; B中的实验现象是___________。
(2)加热至不再有气体产生后停止加热,冷却,剩余固体(M)中仍有少量黑色固体。为回收铜,进行如
下实验。
I剩余固体M的成分是___________;甲溶液的溶质是___________;步骤III的目的是___________。II分
析:理论上,上述实验回收得到铜的质量(x)与原试管A中氧化铜所含铜元素质量(y)的大小关系并说
明理由。___________