文档内容
杨浦区 2021 学年度第二学期中考适应性训练(一)
综合测试试卷化学部分
2022.6
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5 K-39 Ca-40 Ag-108
五、选择题(共 20 分)
21~34 题均只有一个正确选项
1. 空气成分中,体积分数最大的是
A. 氧气 B. 稀有气体 C. 二氧化碳 D. 氮气
2. 下列属于非金属元素的是
A. Mg B. Zn C. S D. Ag
3. 属于氮肥的是
A. FeSO B. KCO C. Ca(HPO ) D. NH NO
4 2 3 2 4 2 4 3
4. 焰色反应呈黄色的物质是
A. KCl B. NaCl C. CaCl D. CuCl
2 2
5. 下列物质分别加入适量水中,充分搅拌,能够得到溶液的是
A. 蔗糖 B. 花生油 C. 面粉 D. 冰块
6. 关于化学方程式: ,说法错误的是
A. 还原剂:CO B. 反应类型:置换反应
C. 反应条件:高温 D. 反应物类别:氧化物
的
7. 属于同素异形体 一组物质是
A. 水和冰 B. 石墨和金刚石
C. 烧碱和纯碱 D. 水和双氧水
8. 测得一些物质的pH如下,其中酸性最强的是
A. 肥皂水:pH=10.2 B. 唾液:pH=6.8 C. 柠檬汁:pH=2.5 D. 洗涤剂:pH=12.2
9. 化学式书写错误的是
A. 生石灰:CaO B. 胆矾:CuSO
4
C. 烧碱:NaOH D. 熟石灰:Ca(OH)
2
10. 在氧气中燃烧,能产生蓝紫色火焰的是
A. 木炭 B. 红磷 C. 甲烷 D. 硫粉11. 鉴别稀盐酸和稀硫酸可选用的试剂是
A. 氯化钡溶液 B. 硝酸银溶液 C. 紫色石蕊试液 D. 碳酸钠溶液
12. 将洁净的铁丝浸入AgNO 和Zn(NO ) 的混合液中,一段时间后,铁丝表面覆盖了一层固体,这层固体
3 3 2
是( )
A. Zn B. Zn和Ag C. Zn和Fe D. Ag
13. 下列实验方法能够达到实验目的是
选项 实验目的 实验方法
A 除去二氧化碳中混有的少量一氧化碳 将混合气体点燃
B 除去生石灰中混有的少量碳酸钙 加足量水,过滤
C 除去氢氧化钠溶液混有的少量碳酸钠 加过量氢氧化钙溶液,过滤
D 提纯含有少量氯化钠的硝酸钾固体 高温溶解,降温结晶,过滤
A. A B. B C. C D. D
14. 回收含铜废料中的铜(杂质不溶于水,也不溶于酸),实验流程如下、有关说法错误的是
A. “灼烧”的主要目的是将 Cu 转变为CuO
B. “还原”过程中气泡不再生成时,说明铁屑足量
C. 滤液 X 中的溶质为 FeSO 、HSO
4 2 4
D. 将 Cu、Fe 混合物加入足量稀硫酸中充分反应后,过滤可以得到 Cu
35~37 题每题均有 1~2 个正确选项
15. 在空气中敞口久置,质量增加的是
A. 食盐 B. 生石灰 C. 稀硫酸 D. 烧碱
16. 有关酸的说法正确的是
A. 酸的组成中一定含有氢元素
B. 使石蕊试液变红的溶液一定是酸溶液C. 金属氧化物一定能和酸溶液反应
D. 酸与碱反应一定没有沉淀生成
17. 等物质的量的CO和CO 含有相同的
2
A. 分子个数
B. 原子总数
.
C 摩尔质量
D. 质量
六、简答题
18. 北京冬奥会使用了多项新技术、新材料。
的
(1)“二氧化碳跨临界直冷制冰”以二氧化碳为原料,在冰面下直接蒸发进行制冰。固态 二氧化碳
称为______(填写名称):使用膜分离法把二氧化碳从空气中分离出来,该过程发生的是______(选填
“物理”或“化学”)变化。
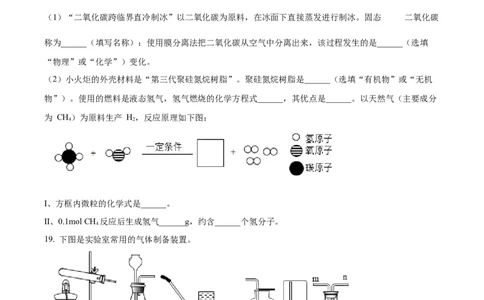
(2)小火炬的外壳材料是“第三代聚硅氮烷树脂”。聚硅氮烷树脂是______(选填“有机物”或“无机
物”)。使用的燃料是液态氢气,氢气燃烧的化学方程式______,其优点是______。以天然气(主要成分
为 CH)为原料生产 H,反应原理如下图:
4 2
I、方框内微粒的化学式是______。
II、0.1mol CH 反应后生成氢气______g,约含______个氢分子。
4
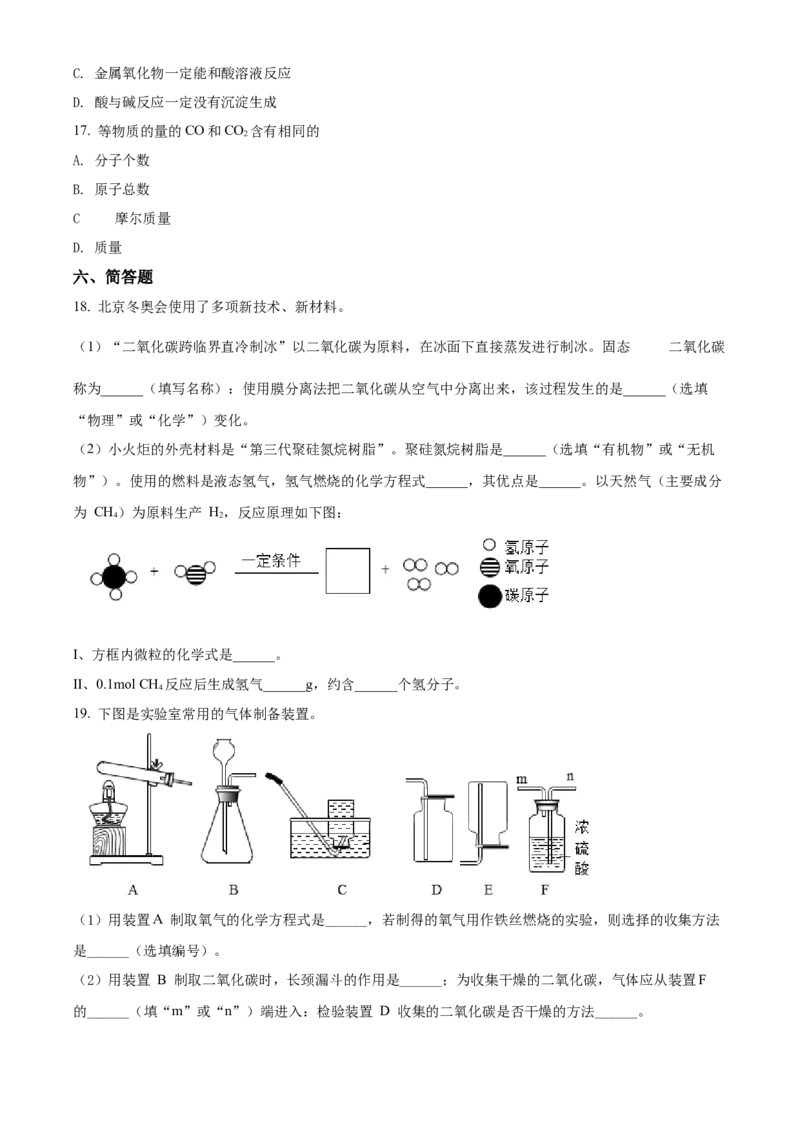
19. 下图是实验室常用的气体制备装置。
(1)用装置A 制取氧气的化学方程式是______,若制得的氧气用作铁丝燃烧的实验,则选择的收集方法
是______(选填编号)。
(2)用装置 B 制取二氧化碳时,长颈漏斗的作用是______;为收集干燥的二氧化碳,气体应从装置F
的______(填“m”或“n”)端进入:检验装置 D 收集的二氧化碳是否干燥的方法______。的
(3)实验室用装置A、F 进行碳还原氧化铜 实验,为了检验反应的产物,装置F 中应盛放的试剂
是______,能说明碳与氧化铜已发生反应的现象是______。
20. 下表是碳酸钠、氯化钠的部分溶解度数据。
温度/℃ 20 30 40 50 60 80 100
碳酸钠 21.8 39.7 48.8 47.3 46.4 45.1 44.7
溶解度
(g/100g
36.
水) 氯化钠 36.0 36.3 37.0 37.3 38.4 39.8
6
(1)40℃时,碳酸钠的溶解度是______。
(2)碳酸钠与氯化钠的溶解度相等的温度范围是______。
A. 20℃~30℃ B. 30℃~40℃ C. 40℃~50℃ D. 60℃~80℃
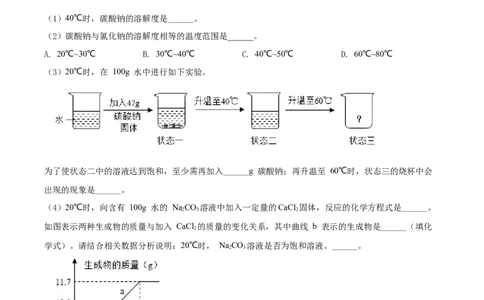
(3)20℃时,在 100g 水中进行如下实验。
为了使状态二中的溶液达到饱和,至少需再加入______g 碳酸钠;再升温至 60℃时,状态三的烧杯中会
出现的现象是______。
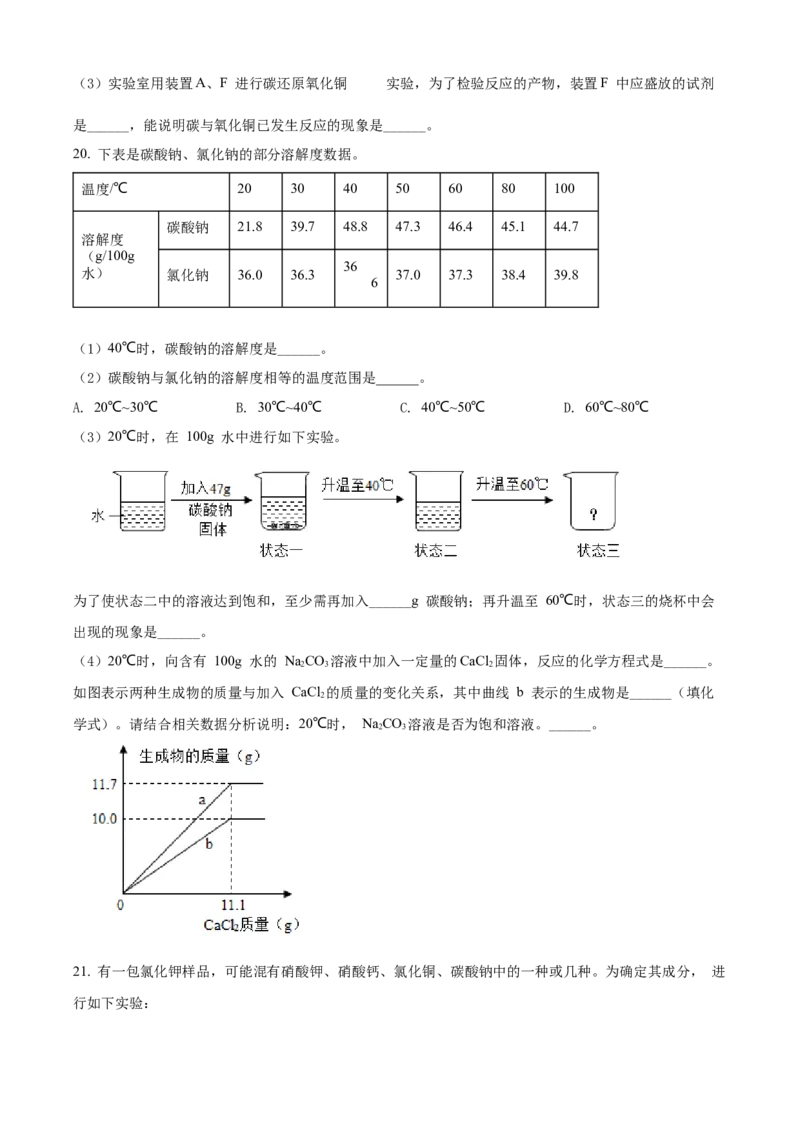
(4)20℃时,向含有 100g 水的 NaCO 溶液中加入一定量的CaCl 固体,反应的化学方程式是______。
2 3 2
如图表示两种生成物的质量与加入 CaCl 的质量的变化关系,其中曲线 b 表示的生成物是______(填化
2
学式)。请结合相关数据分析说明:20℃时, NaCO 溶液是否为饱和溶液。______。
2 3
21. 有一包氯化钾样品,可能混有硝酸钾、硝酸钙、氯化铜、碳酸钠中的一种或几种。为确定其成分, 进
行如下实验:(1)由步骤 I 可知,样品中一定没有______。
(2)步骤 II 中发生的化学反应类型是______。
(3)无色溶液B 中的溶质一定有______。
(4)写出白色沉淀的化学式______。
(5)该样品中的一定含有的杂质是______。
(6)为了确定可能存在的物质,还应该测量的数据是______。