文档内容
杨浦区 2021 学年度第二学期中考适应性训练(一)
综合测试试卷化学部分
2022.6
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Cl-35.5 K-39 Ca-40 Ag-108
五、选择题(共 20 分)
21~34 题均只有一个正确选项
1. 空气成分中,体积分数最大的是
A. 氧气 B. 稀有气体 C. 二氧化碳 D. 氮气
【答案】D
【解析】
【详解】空气的成分按体积分数计算大约是:大约是氮气占(78%),氧气占(21%),稀有气体占
(0.94%),二氧化碳占(0.03%),其它气体和杂质占(0.03%)。所以其中体积分数最大的是氮气。故
选D。
2. 下列属于非金属元素的是
A. Mg B. Zn C. S D. Ag
【答案】C
【解析】
【详解】A、Mg是镁元素的元素符号,带“钅”字旁,属于金属元素,故选项错误。
B、Zn是锌元素的元素符号,带“钅”字旁,属于金属元素,故选项错误。
C、S是硫元素的元素符号,带“石”字旁,属于固态非金属元素,故选项正确。
D、Ag是银元素的元素符号,带“钅”字旁,属于金属元素,故选项错误。
故选:C。
【点睛】金属元素名称一般有“钅”字旁,固态非金属元素名称有“石”字旁,气态非金属元素名称有
“气”字头,据此进行分析解答即可。
3. 属于氮肥的是
A. FeSO B. KCO C. Ca(HPO ) D. NH NO
4 2 3 2 4 2 4 3
【答案】D
【解析】
【详解】A、FeSO 不含氮元素,不属于氮肥;
4
B、KCO 含有钾元素,属于钾肥;
2 3
C、Ca(HPO ) 含有磷元素,属于磷肥;
2 4 2D、NH NO 含有氮元素,属于氮肥;
4 3
答案:D。
4. 焰色反应呈黄色的物质是
A. KCl B. NaCl C. CaCl D. CuCl
2 2
【答案】B
【解析】
【详解】试题分析:A、钾的焰色反应是紫色(透过蓝色的钴玻璃),错误;B、钠的焰色反应是黄色,正
确;C、钙的焰色反应是砖红色,错误;D、铜的焰色反应是绿色,错误。故选B
考点:焰色反应
的
5. 下列物质分别加入适量水中,充分搅拌,能够得到溶液 是
A. 蔗糖 B. 花生油 C. 面粉 D. 冰块
【答案】A
【解析】
【详解】A、蔗糖易溶于水,形成均一、稳定的混合物,属于溶液,正确;B、花生油不溶于水,与水混合
形成乳浊液,错误;C、面粉不溶于水,与水混合形成悬浊液,错误;D、冰块与水混合属于纯净物,不属
于溶液,错误。故选A。
6. 关于化学方程式: ,说法错误的是
A. 还原剂:CO B. 反应类型:置换反应
C. 反应条件:高温 D. 反应物类别:氧化物
【答案】B
【解析】
【详解】A、由化学方程式可知,一氧化碳得到氧,为还原剂,故A正确;
B、反应不符合一种单质和一种化合物生成另一种单质和另一种化合物,不属于置换反应,故B不正确;
C、由化学方程式可知,反应条件为高温,故C正确;
D、反应物均是由两种元素组成,其中一种元素为氧元素,均属于氧化物,故D正确。
故选B。
7. 属于同素异形体的一组物质是
A. 水和冰 B. 石墨和金刚石
C. 烧碱和纯碱 D. 水和双氧水
【答案】B
【解析】【分析】同素异形体是由同种元素组成的不同单质。
【详解】A、水和冰是同种物质,此选项不符合题意;
B.、石墨和金刚石是由碳元素组成的不同单质,此选项符合题意;
C.、烧碱是氢氧化钠的俗称,由钠元素、氢元素、氧元素组成的化合物,纯碱是碳酸钠的俗称,由钠元素、
氧元素、碳元素组成的化合物,此选项不符合题意;
D. 水和双氧水都是由氧元素和氢元素组成的化合物,不属于单质,此选项不符合题意。故选B。
8. 测得一些物质的pH如下,其中酸性最强的是
A. 肥皂水:pH=10.2 B. 唾液:pH=6.8 C. 柠檬汁:pH=2.5 D. 洗涤剂:pH=12.2
【答案】C
【解析】
【分析】
【详解】pH>7,溶液显碱性,pH越大,碱性越强;pH<7,溶液显酸性,pH越小,酸性越强,pH=7,溶
液显中性;
答案:C。
9. 化学式书写错误的是
A. 生石灰:CaO B. 胆矾:CuSO
4
C. 烧碱:NaOH D. 熟石灰:Ca(OH)
2
【答案】B
【解析】
【详解】A、氧化钙俗称生石灰,化学式为CaO,化学式书写正确;
B、五水硫酸铜俗称胆矾,化学式为CuSO ·5HO,化学式书写错误;
4 2
C、氢氧化钠俗称烧碱,化学式NaOH,化学式书写正确;
D、氢氧化钙俗称熟石灰,化学式Ca(OH) ,化学式书写正确;
2
故选:B。
10. 在氧气中燃烧,能产生蓝紫色火焰的是
A. 木炭 B. 红磷 C. 甲烷 D. 硫粉
【答案】D
【解析】
【详解】A、木炭在氧气燃烧发出白光,不符合题意;
B、红磷在氧气中燃烧放出大量的白烟,不符合题意;
C、甲烷在氧气中燃烧产生蓝色的火焰,不符合题意;
D、硫粉在氧气中燃烧产生蓝紫色的火焰,符合题意;
故选D。11. 鉴别稀盐酸和稀硫酸可选用的试剂是
A. 氯化钡溶液 B. 硝酸银溶液 C. 紫色石蕊试液 D. 碳酸钠溶液
【答案】A
【解析】
【详解】A、稀盐酸和氯化钡不反应,稀硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,可以鉴别,故A正确;
B、稀盐酸和硝酸银生成氯化银沉淀和硝酸,稀硫酸和硝酸银反应生成硫酸银沉淀和硝酸,不能鉴别,故
B不正确;
C、 稀盐酸和稀硫酸均显酸性,均能使紫色石蕊试液变红色,不能鉴别,故C不正确;
D、稀盐酸和稀硫酸均与碳酸钠反应生成二氧化碳气体,生成溶液无明显现象,不能鉴别,故D不正确。
故选A。
12. 将洁净的铁丝浸入AgNO 和Zn(NO ) 的混合液中,一段时间后,铁丝表面覆盖了一层固体,这层固体
3 3 2
是( )
A. Zn B. Zn和Ag C. Zn和Fe D. Ag
【答案】D
【解析】
【详解】根据金属的活动性顺序可知Zn>Fe>Ag,所以将洁净的铁丝浸入含有Zn(NO ) 和AgNO 的混
3 2 3
合液中,铁排在锌的后面,所以铁和Zn(NO ) 溶液不反应;而铁排在银的前面,一定发生铁和AgNO
3 2 3
溶液的反应,铁丝表面覆盖了一层银。
故选D。
13. 下列实验方法能够达到实验目的是
选项 实验目的 实验方法
A 除去二氧化碳中混有的少量一氧化碳 将混合气体点燃
B 除去生石灰中混有的少量碳酸钙 加足量水,过滤
C 除去氢氧化钠溶液混有的少量碳酸钠 加过量氢氧化钙溶液,过滤
D 提纯含有少量氯化钠 的硝酸钾固体 高温溶解,降温结晶,过滤
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A、二氧化碳不能燃烧也不支持燃烧,二氧化碳中的一氧化碳不能被点燃,该选项不能达到实验
目的,不符合题意;B、CaO能与水反应生成氢氧化钙,碳酸钙难溶于水,反而会把原物质除去,不符合除杂原则,故选项所
采取的方法错误,不符合题意;
C、氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,由于加入过量的氢氧化钙溶液,除去碳酸钠带入
氢氧化钙,该选项不能达到实验目的,不符合题意;
D、氯化钠中含有少量的硝酸钾,氯化钠的溶解度受温度影响变化不大,硝酸钾的溶解度受温度影响较大,
可以采用高温溶解,降温结晶,过滤的方法进行分离,故选项所采取的方法正确,符合题意。
故选D。
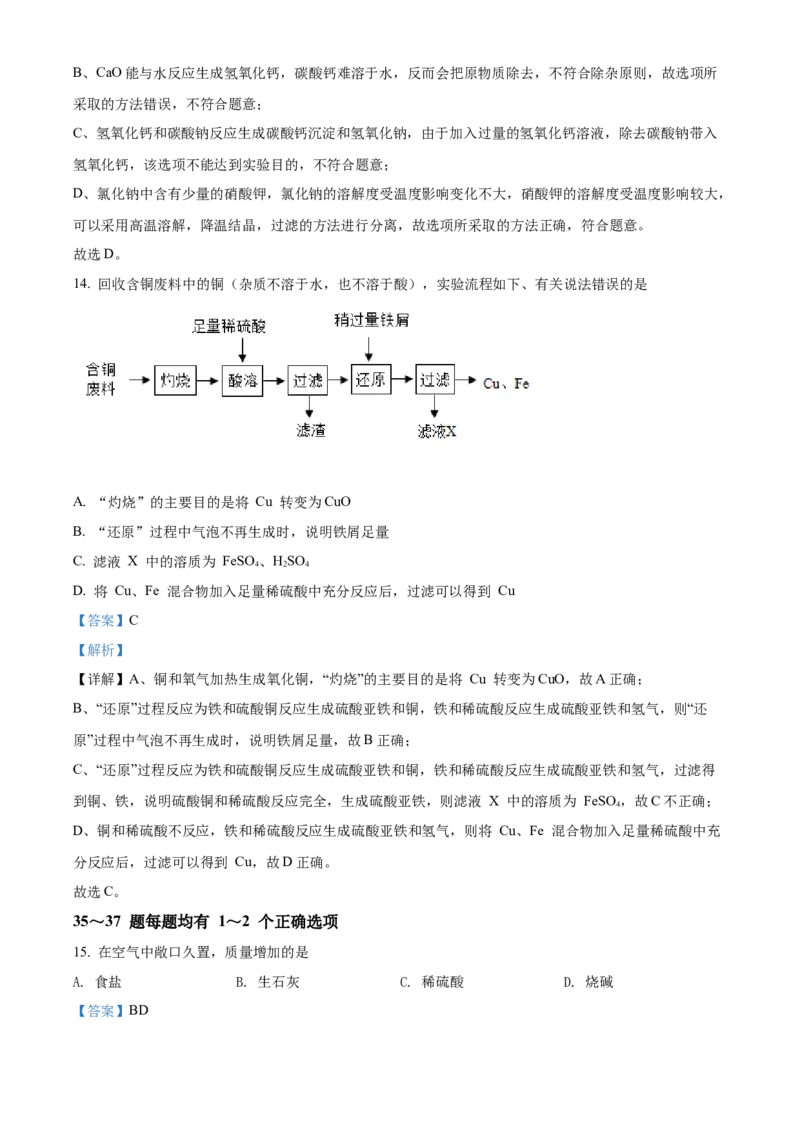
14. 回收含铜废料中的铜(杂质不溶于水,也不溶于酸),实验流程如下、有关说法错误的是
A. “灼烧”的主要目的是将 Cu 转变为CuO
B. “还原”过程中气泡不再生成时,说明铁屑足量
C. 滤液 X 中的溶质为 FeSO 、HSO
4 2 4
D. 将 Cu、Fe 混合物加入足量稀硫酸中充分反应后,过滤可以得到 Cu
【答案】C
【解析】
【详解】A、铜和氧气加热生成氧化铜,“灼烧”的主要目的是将 Cu 转变为CuO,故A正确;
B、“还原”过程反应为铁和硫酸铜反应生成硫酸亚铁和铜,铁和稀硫酸反应生成硫酸亚铁和氢气,则“还
原”过程中气泡不再生成时,说明铁屑足量,故B正确;
C、“还原”过程反应为铁和硫酸铜反应生成硫酸亚铁和铜,铁和稀硫酸反应生成硫酸亚铁和氢气,过滤得
到铜、铁,说明硫酸铜和稀硫酸反应完全,生成硫酸亚铁,则滤液 X 中的溶质为 FeSO ,故C不正确;
4
D、铜和稀硫酸不反应,铁和稀硫酸反应生成硫酸亚铁和氢气,则将 Cu、Fe 混合物加入足量稀硫酸中充
分反应后,过滤可以得到 Cu,故D正确。
故选C。
35~37 题每题均有 1~2 个正确选项
15. 在空气中敞口久置,质量增加的是
A. 食盐 B. 生石灰 C. 稀硫酸 D. 烧碱
【答案】BD【解析】
【详解】A、食盐难挥发,且不与空气中的物质发生反应,在空气中敞口久置,质量保持不变;
B、生石灰与空气中的水蒸气反应生成氢氧化钙,在空气中敞口久置,质量增加;
C、稀硫酸不具有吸水性,在空气中敞口久置水会部分挥发,质量减少;
D、烧碱与空气中的二氧化碳反应生成碳酸钠,在空气中敞口久置,质量增加;
故选:BD。
16. 有关酸的说法正确的是
A. 酸的组成中一定含有氢元素
B. 使石蕊试液变红的溶液一定是酸溶液
C. 金属氧化物一定能和酸溶液反应
D. 酸与碱反应一定没有沉淀生成
【答案】A
【解析】
【详解】A、酸是指在电离时产生的阳离子全部是氢离子的化合物,故酸的组成中一定含有氢元素,选项
说法正确,符合题意;
B、酸性溶液能使紫色石蕊试液变红,但能使紫色石蕊试液变红的溶液不一定是酸溶液,也可能是硫酸氢
钠等盐溶液,故选项说法错误,不符合题意。
C、有的金属氧化物是酸性氧化物,比如MnO、PbO ,它们不能与酸反应,只溶于强碱,故选项说法错
2 7 2
误,不符合题意;
D、酸与碱反应可以有沉淀生成,比如硫酸与氢氧化钡反应生成水和硫酸钡,故选项说法错误,不符合题
意。
故选A。
17. 等物质的量的CO和CO 含有相同的
2
A. 分子个数
B. 原子总数
C. 摩尔质量
D. 质量
【答案】A
【解析】
【详解】A、等物质的量的一氧化碳与二氧化碳,含有相同的分子个数,选项A正确;
B、1分子的一氧化碳含有两个原子,1分子的二氧化碳含有3个原子,所以等物质的量的一氧化碳与二氧
化碳含有的原子总数不同,选项B错误;
C、一氧化碳摩尔质量为28g/mol,二氧化碳为44g/mol,选项C错误;D、质量=物质的量×摩尔质量,由于一氧化碳与二氧化碳摩尔质量不同,所以质量也不同,选项D错误。
故选A。
六、简答题
18. 北京冬奥会使用了多项新技术、新材料。
(1)“二氧化碳跨临界直冷制冰”以二氧化碳为原料,在冰面下直接蒸发进行制冰。固态的二氧化碳称
为______(填写名称):使用膜分离法把二氧化碳从空气中分离出来,该过程发生的是______(选填“物
理”或“化学”)变化。
(2)小火炬的外壳材料是“第三代聚硅氮烷树脂”。聚硅氮烷树脂是______(选填“有机物”或“无机
物”)。使用的燃料是液态氢气,氢气燃烧的化学方程式______,其优点是______。以天然气(主要成分
为 CH)为原料生产 H,反应原理如下图:
4 2
I、方框内微粒的化学式是______。
II、0.1mol CH 反应后生成氢气______g,约含______个氢分子。
4
【答案】(1) ①. 干冰 ②. 物理
(2) ①. 有机物 ②.
③. 清洁、无污染(多写不扣) ④. CO ⑤. 0.6 ⑥. 1.806×1023
【解析】
【小问1详解】
固态的二氧化碳称为干冰,使用膜分离法把二氧化碳从空气中分离出来,该过程没有新的物质生成,属于
物理变化。
【小问2详解】
聚硅氮烷树脂是有机物,氢气与氧气燃烧生成水,其化学方程式为 ,氢气燃烧的优
点为清洁、无污染,根据中信息并结合质量守恒定律可得:一个甲烷分子与一个水分子在一定条件下转化
为三个氢气分子和一个一氧化碳分子,其化学方程式为 ,故方框内微粒的化学式是CO,根据方程式可得0.1mol CH 反应后生成氢气的物质的量为0.3mol,0.3mol氢气的质量为
4
,约含的氢分子为
。
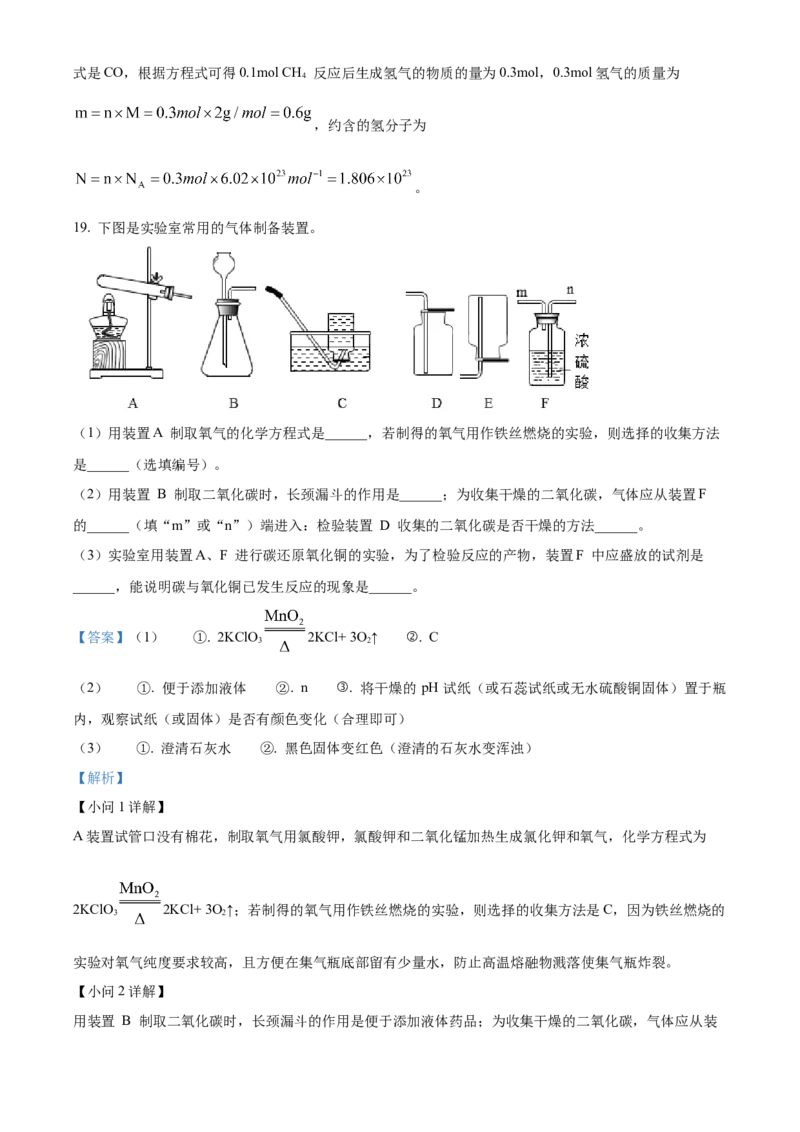
19. 下图是实验室常用的气体制备装置。
(1)用装置A 制取氧气的化学方程式是______,若制得的氧气用作铁丝燃烧的实验,则选择的收集方法
是______(选填编号)。
(2)用装置 B 制取二氧化碳时,长颈漏斗的作用是______;为收集干燥的二氧化碳,气体应从装置F
的______(填“m”或“n”)端进入:检验装置 D 收集的二氧化碳是否干燥的方法______。
(3)实验室用装置A、F 进行碳还原氧化铜的实验,为了检验反应的产物,装置F 中应盛放的试剂是
______,能说明碳与氧化铜已发生反应的现象是______。
【答案】(1) ①. 2KClO 2KCl+ 3O↑ ②. C
3 2
(2) ①. 便于添加液体 ②. n ③. 将干燥的 pH 试纸(或石蕊试纸或无水硫酸铜固体)置于瓶
内,观察试纸(或固体)是否有颜色变化(合理即可)
(3) ①. 澄清石灰水 ②. 黑色固体变红色(澄清的石灰水变浑浊)
【解析】
【小问1详解】
A装置试管口没有棉花,制取氧气用氯酸钾,氯酸钾和二氧化锰加热生成氯化钾和氧气,化学方程式为
2KClO 2KCl+ 3O ↑;若制得的氧气用作铁丝燃烧的实验,则选择的收集方法是C,因为铁丝燃烧的
3 2
实验对氧气纯度要求较高,且方便在集气瓶底部留有少量水,防止高温熔融物溅落使集气瓶炸裂。
【小问2详解】
用装置 B 制取二氧化碳时,长颈漏斗的作用是便于添加液体药品;为收集干燥的二氧化碳,气体应从装置F 的n端进入,让二氧化碳从浓硫酸经过,才能起到干燥的作用;检验装置 D 收集的二氧化碳是否干
燥?可以用干燥的pH试纸、石蕊试纸或无水硫酸铜固体,具体方法是将干燥的pH试纸(或石蕊试纸或
无水硫酸铜固体)置于瓶内,观察试纸(或固体)是否有颜色变化。
【小问3详解】
碳还原氧化铜的产物为铜和二氧化碳, F装置用来检验二氧化碳,因此装置F 中应盛放的试剂是澄清石
灰水;能说明碳与氧化铜已发生反应的现象是黑色固体变红色或澄清的石灰水变浑浊。
20. 下表是碳酸钠、氯化钠的部分溶解度数据。
温度/℃ 20 30 40 50 60 80 100
碳酸钠 21.8 39.7 48.8 47.3 46.4 45.1 44.7
溶解度
(g/100g
水) 氯化钠 36.0 36.3 36.6 37.0 37.3 38.4 39.8
(1)40℃时,碳酸钠的溶解度是______。
(2)碳酸钠与氯化钠的溶解度相等的温度范围是______。
A. 20℃~30℃ B. 30℃~40℃ C. 40℃~50℃ D. 60℃~80℃
在
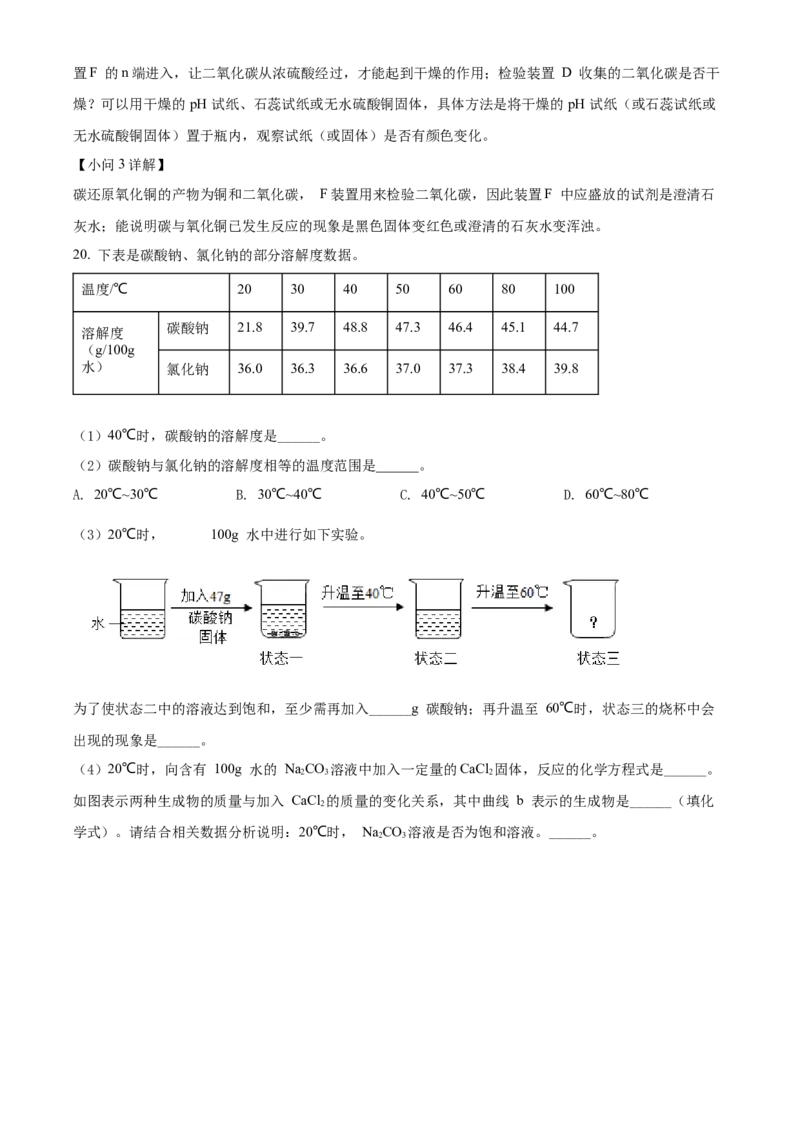
(3)20℃时, 100g 水中进行如下实验。
为了使状态二中的溶液达到饱和,至少需再加入______g 碳酸钠;再升温至 60℃时,状态三的烧杯中会
出现的现象是______。
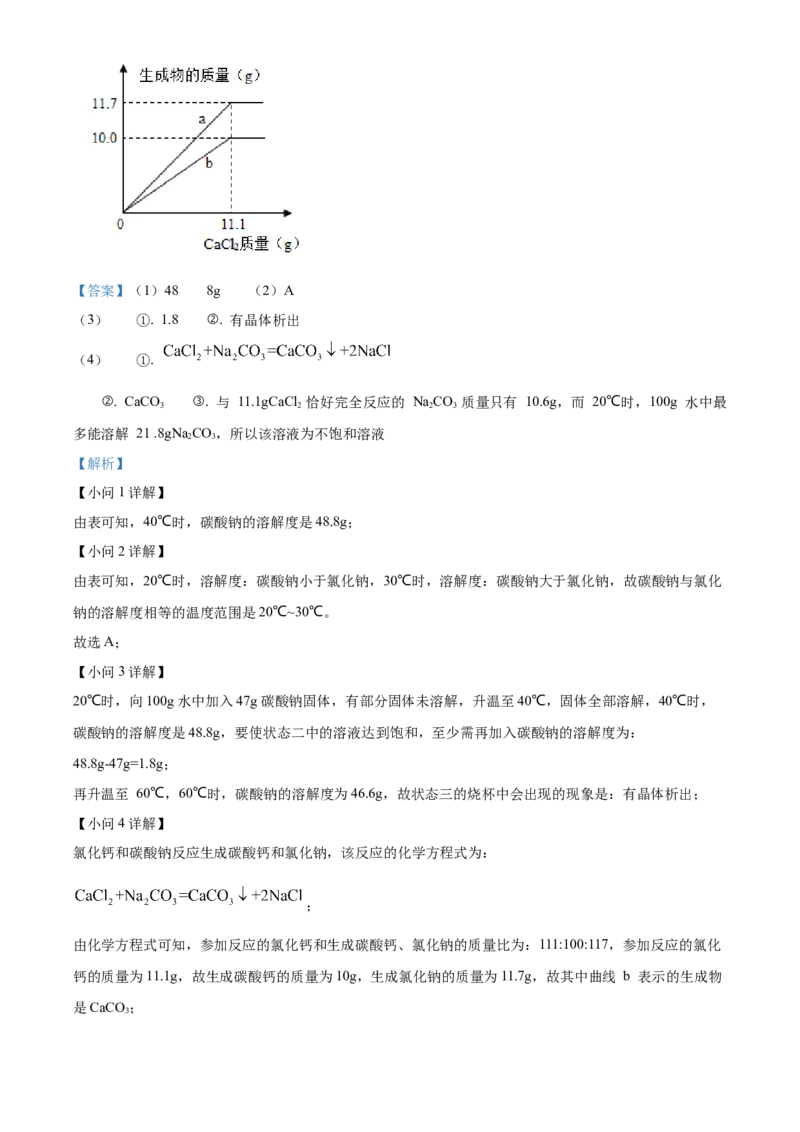
(4)20℃时,向含有 100g 水的 NaCO 溶液中加入一定量的CaCl 固体,反应的化学方程式是______。
2 3 2
如图表示两种生成物的质量与加入 CaCl 的质量的变化关系,其中曲线 b 表示的生成物是______(填化
2
学式)。请结合相关数据分析说明:20℃时, NaCO 溶液是否为饱和溶液。______。
2 3.
【答案】(1)48 8g (2)A
(3) ①. 1.8 ②. 有晶体析出
(4) ①.
②. CaCO ③. 与 11.1gCaCl 恰好完全反应的 NaCO 质量只有 10.6g,而 20℃时,100g 水中最
3 2 2 3
多能溶解 21 .8gNa CO,所以该溶液为不饱和溶液
2 3
【解析】
【小问1详解】
由表可知,40℃时,碳酸钠的溶解度是48.8g;
【小问2详解】
由表可知,20℃时,溶解度:碳酸钠小于氯化钠,30℃时,溶解度:碳酸钠大于氯化钠,故碳酸钠与氯化
钠的溶解度相等的温度范围是20℃~30℃。
故选A;
【小问3详解】
20℃时,向100g水中加入47g碳酸钠固体,有部分固体未溶解,升温至40℃,固体全部溶解,40℃时,
碳酸钠的溶解度是48.8g,要使状态二中的溶液达到饱和,至少需再加入碳酸钠的溶解度为:
48.8g-47g=1.8g;
再升温至 60℃,60℃时,碳酸钠的溶解度为46.6g,故状态三的烧杯中会出现的现象是:有晶体析出;
【小问4详解】
氯化钙和碳酸钠反应生成碳酸钙和氯化钠,该反应的化学方程式为:
;
由化学方程式可知,参加反应的氯化钙和生成碳酸钙、氯化钠的质量比为:111:100:117,参加反应的氯化
钙的质量为11.1g,故生成碳酸钙的质量为10g,生成氯化钠的质量为11.7g,故其中曲线 b 表示的生成物
是CaCO ;
3由化学方程式可知, 参加反应的氯化钙和碳酸钠的质量比为111:106,加入氯化钙的质量为11.1g时,碳
酸钠恰好完全反应,则参加反应的碳酸钠的质量为10.6g,而 20℃时,100g 水中最多能溶解 21
.8gNa CO,所以该溶液为不饱和溶液。
2 3
21. 有一包氯化钾样品,可能混有硝酸钾、硝酸钙、氯化铜、碳酸钠中的一种或几种。为确定其成分, 进
行如下实验:
(1)由步骤 I 可知,样品中一定没有______。
(2)步骤 II 中发生的化学反应类型是______。
(3)无色溶液B 中的溶质一定有______。
(4)写出白色沉淀的化学式______。
(5)该样品中的一定含有的杂质是______。
(6)为了确定可能存在的物质,还应该测量的数据是______。
【答案】(1)氯化铜##CuCl
2
(2)复分解反应 (3)NaNO 、KNO、HNO、AgNO
3 3 3 3
(4)AgCl (5)碳酸钠##NaCO
2 3
(6)生成的气体质量
【解析】
【小问1详解】
氯化铜溶液显蓝色,样品溶于水形成无色溶液A,说明不含氯化铜,故由步骤 I 可知,样品中一定没有氯
化铜或CuCl 。
2
【
小问2详解】
步骤 II 中发生的化学反应为稀硝酸和碳酸钠生成硝酸钠、水和二氧化碳,硝酸银和氯化钾生成氯化银沉
淀和硝酸钾,反应均符合两种化合物相互交换成分生成另两种化合物,故步骤 II 中发生的化学反应类型
是复分解反应。
【小问3详解】
步骤 II稀硝酸和碳酸钠生成硝酸钠、水和二氧化碳,硝酸银和氯化钾生成氯化银沉淀和硝酸钾,则无色溶
液B 中的溶质一定有生成的硝酸钠、硝酸钾,过量的稀硝酸、硝酸银,化学式为NaNO 、KNO、HNO、
3 3 3AgNO。
3
【小问4详解】
硝酸银和氯化钾生成氯化银沉淀和硝酸钾,故白色沉淀的化学式为AgCl。
【小问5详解】
由步骤 II反应稀硝酸和碳酸钠生成硝酸钠、水和二氧化碳,产生气泡,说明含有碳酸钠,故该样品中的一
定含有的杂质是NaCO。
2 3
【小问6详解】
由步骤 I 可知,不含氯化铜,步骤 II可知样品中含有碳酸钠,则不含硝酸钙,可能含有硝酸钾,白色沉
淀氯化银的质量为28.7g,则由化学方程式 计算出氯化钾的质量,则为
了确定可能存在的物质,还需要计算碳酸钠的质量,故还应该测量的数据是生成的气体质量。