文档内容
2021 学年第二学期九年级化学学科阶段练习综合测试
化学部分
考生注意:
1.本化学试卷满分50分。考试时间40分钟。
2.按要求在答题纸上规定的位置作答,在试卷、草稿纸上答题一律无效。
相对原子质量:H-1 C-12 O -16 K-39 Cl-35.5 Fe-56 Cu-64 Ag-108
六、选择题(共20分)
请将正确选项的代号用2B铅笔填涂在答题纸的相应位置上,更改答案时,用橡皮擦去,重新
填涂。21~34题只有一个正确选项
1. 属于化学变化的是
A. 纸张燃烧 B. 花香四溢 C. 灯泡发光 D. 滴水成冰
2. 酒精(C HOH)属于
2 5
A. 单质 B. 有机物 C. 氧化物 D. 盐
3. 互为同素异形体的一组物质是
A. 活性炭、石墨
B. 氧气、臭氧
C. 液氮、氮气
D. 水、双氧水
4. 某同学测定了生活中常见物质的pH,部分数据如下,其中酸性最强的是
A. 洁厕剂:1 B. 白醋:3 C. 牙膏:9 D. 洗发水:10
5. 下列属于复合肥的是
A. CO(NH ) B. NH HCO C. NH NO D. KNO
2 2 4 3 4 3 3
6. 二氧化钛(TiO)可做水分解的光催化剂,TiO 中Ti的化合价是
2 2
A. +2 B. +3 C. +4 D. +6
7. 还原 的反应中, 体现出的性质是( )
A. 可燃性 B. 毒性 C. 还原性 D. 不溶于水
8. 药物“胃舒平”治疗胃酸过多的原理为 ,该反应属于
.
A 复分解反应 B. 分解反应 C. 置换反应 D. 化合反应9. 某有机物燃烧的化学方程式:X+5O 3CO+4H O,有机物X的化学式是
2 2 2
A. C H B. C H C. C HO D. C HO
3 8 3 6 3 8 2 3 6
10. 物质的用途错误的是
A. 氯气:自来水杀菌消毒
B. 干冰:冷藏食品
C. 氧气:高能燃料
D. 氦气:制多用途电光源
11. 仅通过下列操作就能达到提纯目的的是(括号内为杂质)
A. CaO(CaCO )放入适量稀盐酸
3
B. CO(HCl)通过足量氢氧化钠固体
2
C. N(O)通过足量红热的木炭
2 2
D. CO(CO)通过足量灼热氧化铜
2
12. 关于电解水实验的说法正确的是
A. 该实验证明水由氢气和氧气组成
B. 水中存在大量的氢分子和氧原子
C. 正、负电极产生气体的体积比是1:2
D. 负极产生的气体能使带火星的木条复燃
13. 如图是物质的分类及部分转化关系图,有关说法不正确的是( )
A. 转化b一定是化学变化 B. 转化a一定是化学变化
C. 转化b中一定有元素的存在形态发生改变 D. 分离液态空气制取氧气属于转化c
14. 在氯化钡溶液中滴入某种液体,生成白色沉淀。有关说法正确的是
A. 滴入的一定是某种盐溶液
.
B 反应后溶液一定呈中性
.
C 白色沉淀一定不溶于盐酸D. 该反应一定是复分解反应
35~37有1-2个答案
15. 镧(La)的金属活动性比锌强,La在化合物中通常显正3价,La(OH) 难溶于水,LaCl、La
3 3
(NO ) 都可溶于水。由此推断能直接反应制取LaCl 的是
3 3 3
A. La(NO ) 和稀盐酸
3 3
.
B La(NO ) 和KCl溶液
3 3
C. La(OH) 和稀盐酸
3
D. La(OH) 和KCl溶液
3
16. 下列各组物质反应,所得溶液能使酚酞溶液变红的是
A. 一定量的稀盐酸与适量的氢氧化钠溶液恰好完全反应
B. 相同质量、相同溶质质量分数的氢氧化钾溶液与盐酸相混合
C. 将硫酸钾溶液滴入氢氧化钡溶液中恰好完全反应
D. 将二氧化碳气体通入氢氧化钠溶液中得到碳酸钠溶液
17. 在硝酸银、硝酸铜的混合溶液中加入一定量的锌粉,反应停止后,滤液仍为蓝色,有关判断正确的是
A. 滤渣中一定有银,没有铜和锌
.
B 滤渣中一定有银和铜,可能有锌
C. 滤液中一定有硝酸锌、硝酸铜、硝酸银
D. 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
七、简答题(共30分)请根据要求在答题纸的相应位置作答。
18. 碳元素的存在让我们的世界绚丽多彩,请根据所学知识回答问题:
(1)防毒面具中使用了活性炭,这是利用了活性炭的______________________作用。
(2)草木灰是重要的化肥,其主要成分是碳酸钾,检验碳酸钾中的钾元素的方法是_________________。
(3)甲烷在自然界的分布很广,在空气中燃烧后,其反应的微观示意图如下:
Ⅰ、甲烷的摩尔质量为________________,2mol甲烷分子中约含有_________________个分子。
Ⅱ、反应过程中的甲烷和氧气的物质的量之比为___________________。
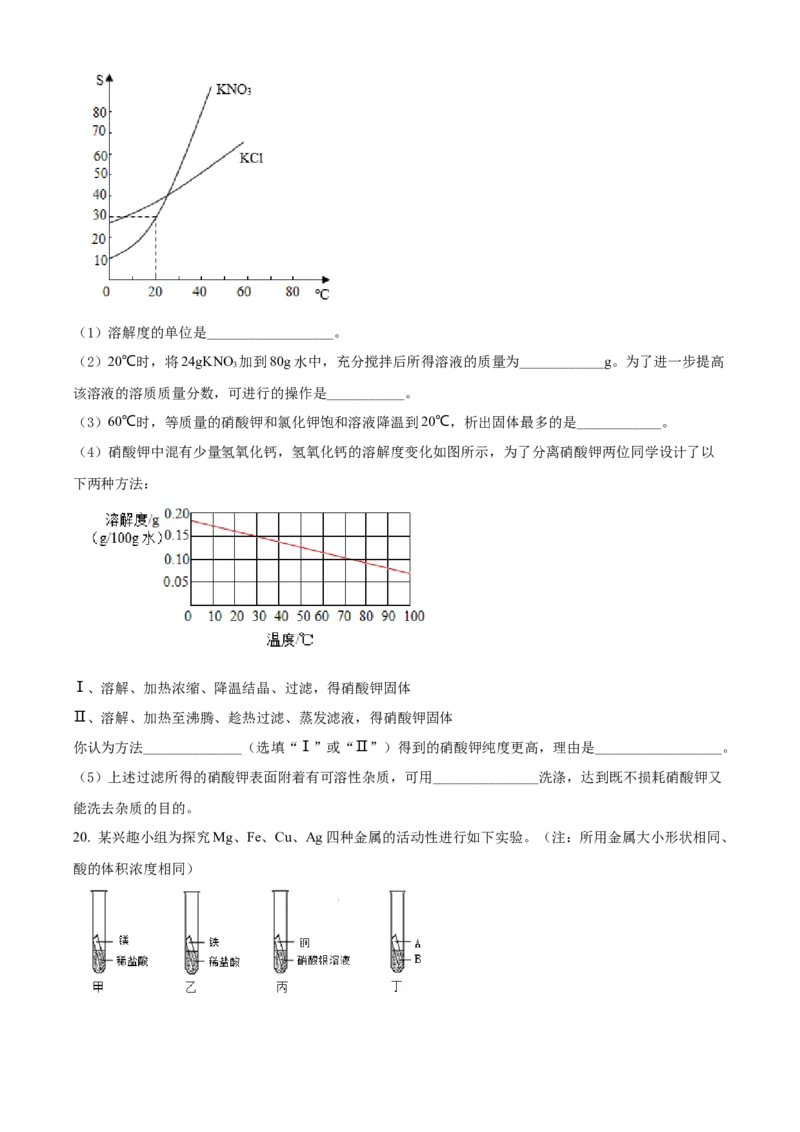
19. 根据溶解度曲线,请回答下列问题:(1)溶解度的单位是__________________。
(2)20℃时,将24gKNO 加到80g水中,充分搅拌后所得溶液的质量为____________g。为了进一步提高
3
该溶液的溶质质量分数,可进行的操作是___________。
(3)60℃时,等质量的硝酸钾和氯化钾饱和溶液降温到20℃,析出固体最多的是____________。
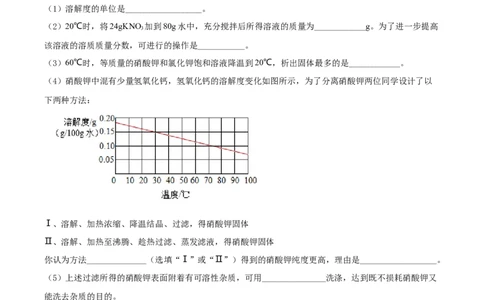
(4)硝酸钾中混有少量氢氧化钙,氢氧化钙的溶解度变化如图所示,为了分离硝酸钾两位同学设计了以
下两种方法:
Ⅰ、溶解、加热浓缩、降温结晶、过滤,得硝酸钾固体
Ⅱ、溶解、加热至沸腾、趁热过滤、蒸发滤液,得硝酸钾固体
你认为方法______________(选填“Ⅰ”或“Ⅱ”)得到的硝酸钾纯度更高,理由是__________________。
(5)上述过滤所得的硝酸钾表面附着有可溶性杂质,可用_______________洗涤,达到既不损耗硝酸钾又
能洗去杂质的目的。
20. 某兴趣小组为探究Mg、Fe、Cu、Ag四种金属的活动性进行如下实验。(注:所用金属大小形状相同、
酸的体积浓度相同)(1)乙试管中的发生的反应方程式为________________,依据甲乙试管冒气泡速率的差异,可知活动性
Mg___________Fe(填“>”、“=”或“<”);
(2)根据丙中现象___________,可知活动性Cu>Ag;
(3)小组同学发现该实验无法得出四种金属的活动性顺序,请你帮助他们在上述实验的基础上,设计一
个补充实验来实现探究目的,若按照图丁所示进行实验探究,你决定推荐他们用的试剂是:金属A是
_____________;溶液B是_______________。(要求写出化学式)
(4)为了减少环境污染,小组同学将乙中剩余的铁加入丙溶液中回收丙溶液溶质中的金属,至t时间后固
体质量不再变化,根据如图所示溶液中固体质量变化情况,分析最后所得固体成分是_________________。
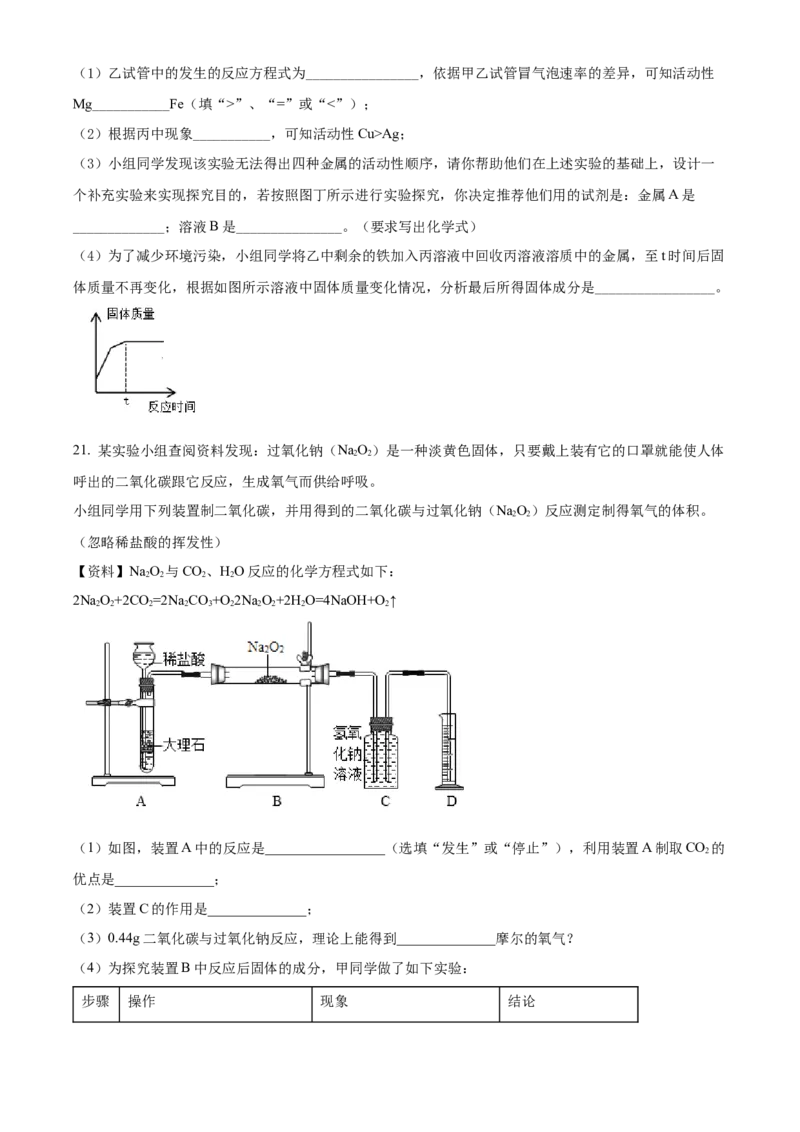
21. 某实验小组查阅资料发现:过氧化钠(NaO)是一种淡黄色固体,只要戴上装有它的口罩就能使人体
2 2
呼出的二氧化碳跟它反应,生成氧气而供给呼吸。
小组同学用下列装置制二氧化碳,并用得到的二氧化碳与过氧化钠(NaO)反应测定制得氧气的体积。
2 2
(忽略稀盐酸的挥发性)
【资料】NaO 与CO、HO反应的化学方程式如下:
2 2 2 2
2NaO+2CO =2Na CO+O 2NaO+2H O=4NaOH+O ↑
2 2 2 2 3 2 2 2 2 2
(1)如图,装置A中的反应是_________________(选填“发生”或“停止”),利用装置A制取CO 的
2
优点是______________;
(2)装置C的作用是______________;
(3)0.44g二氧化碳与过氧化钠反应,理论上能得到______________摩尔的氧气?
(4)为探究装置B中反应后固体的成分,甲同学做了如下实验:
步骤 操作 现象 结论I 取反应后的固体,加水 固体全部溶解,无气泡产生 固体中没有_______
向步骤I溶液中加过量稀盐
II _______________ 固体中有碳酸钠
酸
Ⅲ _________________ ____________ 固体中有氢氧化钠
(5)加入稀盐酸的体积对测定生成氧气的体积__________________(选填“有”或“无”)影响。