文档内容
2024 年松江区初中毕业生学业模拟考试试卷
九年级 综合测试
(满分135分,完卷时间120分钟)
考生注意:
1. 试卷第 1~20 题为物理部分,第 21~41 题为化学部分,第 42 题开始为跨学科案例分析
部分。
2. 试卷满分 135 分。考试时间 120 分钟。
3. 按要求在答题纸规定的位置上作答,在试卷、草稿纸上答题一律无效。
化 学 部 分
考生注意:
1. 本练习化学部分含两个大题。
2. 答题时,考生务必按答题要求在答题纸规定的位置上作答,在草稿纸、本试卷上答题一律
无效。
相对原子质量: H-1 C-12 O-16 Na-23 S-32 Ca-40 Cu-64
一、选择题,每题均只有一个正确选项
1. 属于化学变化的是
A. 切割玻璃 B. 湿衣晒干 C. 钢铁生锈 D. 水结成冰
【答案】C
【解析】
【详解】A、切割玻璃,只是形状的改变,无新物质生成,属于物理变化;
B、湿衣晾干,只是水的状态的改变,无新物质生成,属于物理变化;
C、钢铁生锈,有铁锈等新物质生成,属于化学变化;
D、水结成冰,只是状态的改变,无新物质生成,属于物理变化。
故选C。
2. 属于溶液的是
A. 矿泉水 B. 蒸馏水 C. 牛奶 D. 石灰乳
【答案】A
【解析】
【分析】溶液是一种或几种物质分散到另一种物质中,形成均一、稳定的混合物;
【详解】A、矿泉水是均一稳定的混合物,属于溶液,故符合题意;
B、蒸馏水是纯净物,不是溶液,故不符合题意;C、牛奶属于乳浊液,不均一稳定,不是溶液,故不符合题意;
D、石灰乳属于悬浊液,不均一稳定,不是溶液,故不符合题意;
故选A。
3. 五氧化二钒(V O)广泛用于化工行业。其中钒元素的化合价是
2 5
A. +2 B. +5 C. -1 D. -5
【答案】B
【解析】
【详解】五氧化二钒中氧元素显-2价,设钒元素的化合价为x,根据化合物中,正、负化合价的代数和为
零,可得: ,x=+5。
故选B。
4. 属于有机物的是
A. C B. HCO C. CH D. CO
60 2 3 4 2
【答案】C
【解析】
【详解】A、C 虽然含碳元素,但是属于无机物,不符合题意;
60
B、碳酸虽然含碳元素,但是属于无机物,不符合题意;
C、甲烷含碳元素,属于有机物,符合题意;
D、二氧化碳虽然含碳元素,但是属于无机物,不符合题意。
故选C。
5. 属于钾肥的是
A. B. CaCl C. KCO D. NaNO
2 2 3 3
【答案】C
【解析】
【详解】A、硫酸铵含N、P、K中的N元素,属于氮肥,不符合题意;
B、氯化钙不含N、P、K元素,不属于化肥,不符合题意;
C、碳酸钾含N、P、K中的K元素,属于钾肥,符合题意;
D、硝酸钠含N、P、K中的N元素,属于氮肥,不符合题意。
故选C。
6. 实验室用氯酸钾和二氧化锰制氧气,化学方程式书写正确的是
A. B.C. D.
【答案】D
【解析】
【详解】氯酸钾在二氧化锰的催化下加热分解生成氯化钾和氧气,化学方程式为:
;
故选:D。
7. 胃酸能帮助消化,但过多的胃酸会危害健康。可用于治疗胃酸过多的物质是
A. KCl B. CaO C. Al(OH) D. NaOH
3
【答案】C
【解析】
【详解】A、氯化钾和盐酸不反应,不能用于治疗胃酸过多,不符合题意;
B、氧化钙能与盐酸反应生成氯化钙和水,但是氧化钙遇水放出大量的热,不能用于治疗胃酸过多,不符
合题意;
C、氢氧化铝和盐酸反应生成氯化铝和水,可用于治疗胃酸过多,符合题意;
D、氢氧化钠和盐酸反应生成氯化钠和水,但是氢氧化钠具有腐蚀性,不能用于治疗胃酸过多,不符合题
意。
故选C。
8. 关于原子、分子叙述正确的是
A. 加热可使分子或原子体积变大 B. 相同原子可以构成不同分子
C. 分子质量大,原子质量小 D. 化学变化中分子数目不变
【答案】B
【解析】
【详解】A、加热可以使分子的运动速率变快,分子间隔变大,不能改变分子或原子体积,选项错误;
B、相同原子可能构成不同的分子。如:氧原子即可以构成氧气分子也可以构成臭氧分子。选项正确;
C、分子质量不一定大于原子质量。如氦原子的质量(相对原子质量为4)就大于氢分子的质量(相对分子
质量为2)。选项错误;
D、化学变化中分子数目可能变化。如:氢气在空气中燃烧:2H+O 2HO 反应前分子数目是3个,
2 2 2反应后变为2个,分子数目发生了改变;氢气在氯气中燃烧:H+Cl 2HCl 反应前分子数目是2个,
2 2
反应后仍为2个,分子数目没有改变。选项错误。
故选B。
9. 双氧水分解的微观示意图如下,方框内应是
A. B.
.
C D.
【答案】B
【解析】
【详解】由质量守恒定律反应前后原子的种类及数目不变可知,2个双氧水分子分解生成了两个水分子和
一个氧分子,所以方框内应应填入的是: ,所以B正确。
故选B 。
10. 有关叙述正确的是
A. 水中含氢分子 B. 二氧化碳中含有2个氧原子
C. 1mol物质约含( 个分子) D. 1molH 和1molO 所含原子个数相等
2 2
【答案】D
【解析】
【详解】A、水由水分子构成,不含氢分子,不符合题意;
B、二氧化碳由二氧化碳分子构成,每个二氧化碳分子中含2个氧原子,不符合题意;
C、物质不都是由分子构成,还可能由原子、离子构成,不符合题意;
D、1molH 所含氢原子的个数为: ,1molO 所含原子个数为:
2 2
,故1molH 和1molO 所含原子个数相等,符合题意。
2 2
故选D。的
11. 物质 性质决定其用途。有关物质的用途正确的是
A. 食盐水清洗伤口 B. 胆矾检验水 C. 石墨作钻头 D. 氧气作火箭燃料
【答案】A
【解析】
【详解】A、食盐水具有杀菌消毒的作用,可用于清洗伤口,符合题意;
B、无水硫酸铜遇水变蓝,可用无水硫酸铜检验水,不能用胆矾,不符合题意;
C、金刚石是天然存在的最硬的物质,可用作钻头,石墨质软,不能用作钻头,不符合题意;
D、氧气具有助燃性,不具有可燃性,不能作燃料,不符合题意。
故选A。
12. 用如图装置进行实验,充分反应后,U型管内水面没有明显变化的是
A. 氢氧化钠溶液和二氧化碳 B. 稀盐酸和石灰石 C. 水和氧化钙 D. 稀硫
酸和氯化钡溶液
【答案】D
【解析】
【详解】A、氢氧化钠和二氧化碳反应生成碳酸钠和水,二氧化碳被消耗,装置内气体减少,压强减小,
U型管中液面左高右低,不符合题意;
B、石灰石的主要成分碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,装置内气体增多,压强增大,U
型管中液面左低右高,不符合题意;
C、氧化钙和水反应生成氢氧化钙,放出大量的热,装置内气体受热膨胀,压强增大,U型管中液面左低
右高,不符合题意;
D、稀硫酸和氯化钡反应生成硫酸钡和盐酸,装置内压强变化不大,U型管内水面没有明显变化,符合题
意。
故选D。
13. 下列实验方法能达到实验目的的是
选项 实验目的 实验方法
A 除去氧化钙中的碳酸钙 放入适量稀盐酸
B 除去粗盐中的泥沙 溶解、过滤、蒸发C 除去 CO 中 CO 点燃该混合气体
2
除去 NaCl 溶液中的 加入过量的NaSO 溶液,过
D 2 4
BaCl 滤
2
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A、放入适量稀盐酸,氧化钙和稀盐酸反应生成氯化钙和水,碳酸钙和稀盐酸反应生成氯化钙、
二氧化碳和水,不但除去了杂质,也除去了原物质,不符合题意;
B、除去粗盐中的泥沙,泥沙难溶于水,可通过溶解、过滤,除去泥沙,然后蒸发,得到精盐,符合题意;
C、二氧化碳不燃烧、不支持燃烧,二氧化碳中混有少量一氧化碳,无法被点燃,不符合题意;
D、加入过量的硫酸钠溶液,硫酸钠和氯化钡反应生成硫酸钡和氯化钠,过滤,除去硫酸钠,虽然除去了
杂质,但是引入了新的杂质硫酸钠,不符合题意。
故选B。
14. 在含 1mol NaOH 的氢氧化钠溶液中加入下列酸,恰好完全反应的是
A. 1mL 的稀盐酸 B. 40 克稀盐酸
C. 含 1molH SO 的稀硫酸 D. 含49 克 HSO 的稀硫酸
2 4 2 4
【答案】D
【解析】
【详解】A、稀盐酸的密度和溶质质量分数未知,是否恰好完全反应,无法确定, 不符合题意;
B、氢氧化钠和稀盐酸反应生成氯化钠和水,即 ,参加反应的氢氧化钠和HCl的
质量比为:40:36.5,1mol氢氧化钠的质量为: ,40g氢氧化钠与36.5gHCl恰好完
全反应,加入40g稀盐酸,稀盐酸的溶质质量分数未知,无法确定是否完全反应,不符合题意;
C、氢氧化钠和稀硫酸反应生成硫酸钠和水,即 ,则参加反应的氢氧化
钠和硫酸的物质的量之比为:2:1,则 1mol NaOH与0.5mol硫酸恰好完全反应,不符合题意;
D、氢氧化钠和稀硫酸反应生成硫酸钠和水,即 ,参加反应的氢氧化钠
和硫酸的质量比为:80:98,1mol氢氧化钠的质量为40g,故40g氢氧化钠与49g硫酸恰好完全反应,符合
题意。故选D。
15-17 每题均有1~2个正确选项
15. 乳酸钙是常用的补钙剂之一。乳酸钙的组成元素为Ca、C、H、O,且钙、碳、氢和氧四种元素质量比
为20:36:5:48。下列结论正确的是
A. 乳酸钙的式量是20+36+5+48 B. 乳酸钙属于氧化物
C. 乳酸钙分子中H、O的原子个数比为5:3 D. 乳酸钙中钙元素的质量分数最高
【答案】C
【解析】
【分析】乳酸钙的组成元素为Ca、C、H、O,且钙、碳、氢和氧四种元素质量比为20:36:5:48,则乳
酸钙中Ca、C、H、O元素的原子个数比为: ,故乳酸钙的化学式为:
C H OCa。
6 10 6
【详解】A、乳酸钙的式量是: ,不符合题意;
B、氧化物是由两种元素组成,其中一种元素是氧元素的化合物,乳酸钙由Ca、C、H、O四种元素组成,
不属于氧化物,不符合题意;
C、由化学式可知,乳酸钙分子中H、O的原子个数比为:10:6=5:3,符合题意;
D、乳酸钙的组成元素为Ca、C、H、O,且钙、碳、氢和氧四种元素质量比为20:36:5:48,故乳酸钙
中氧元素的质量分数最高,不符合题意。
故选C。
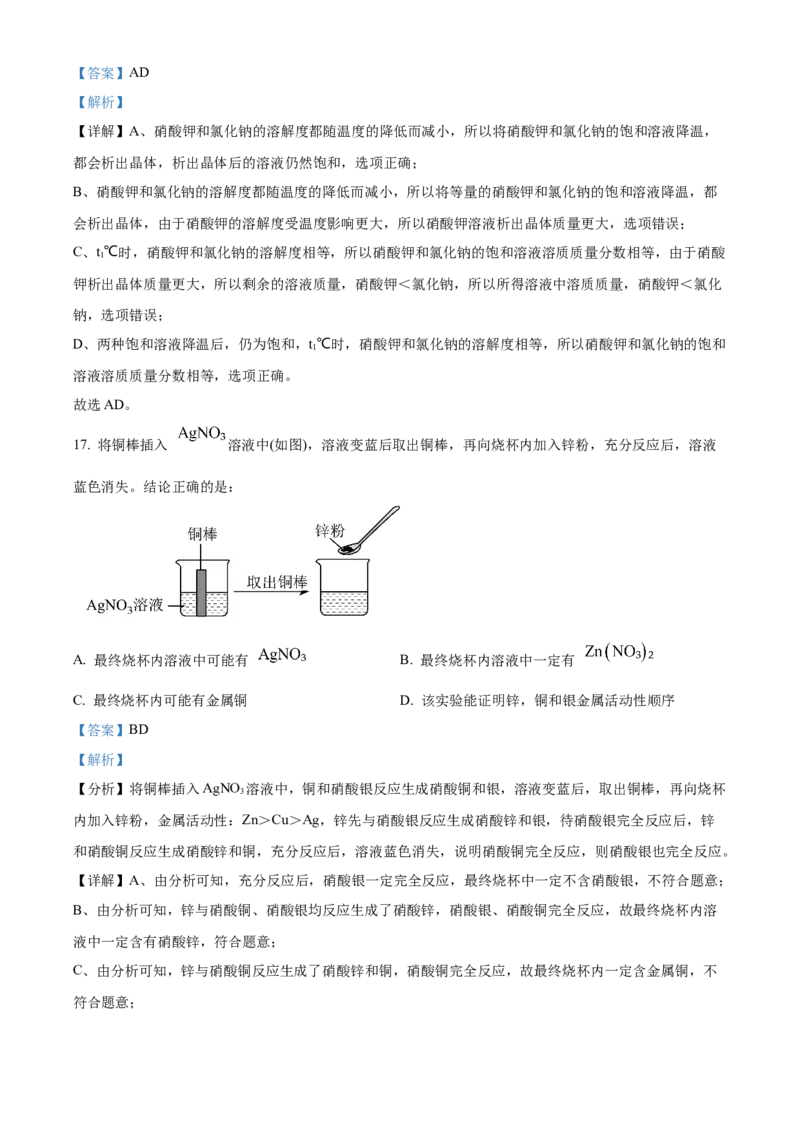
16. 硝酸钾和氯化钠的溶解度曲线如图所示。将 等质量的硝酸钾饱和溶液、氯化钠饱和溶液,分别
降温到 ,下列说法正确的是
A. 所得溶液都饱和 B. 析出晶体质量相等
C. 所得溶液中溶质质量相等 D. 所得溶液溶质质量分数相等【答案】AD
【解析】
【详解】A、硝酸钾和氯化钠的溶解度都随温度的降低而减小,所以将硝酸钾和氯化钠的饱和溶液降温,
都会析出晶体,析出晶体后的溶液仍然饱和,选项正确;
B、硝酸钾和氯化钠的溶解度都随温度的降低而减小,所以将等量的硝酸钾和氯化钠的饱和溶液降温,都
会析出晶体,由于硝酸钾的溶解度受温度影响更大,所以硝酸钾溶液析出晶体质量更大,选项错误;
C、t℃时,硝酸钾和氯化钠的溶解度相等,所以硝酸钾和氯化钠的饱和溶液溶质质量分数相等,由于硝酸
1
钾析出晶体质量更大,所以剩余的溶液质量,硝酸钾<氯化钠,所以所得溶液中溶质质量,硝酸钾<氯化
钠,选项错误;
D、两种饱和溶液降温后,仍为饱和,t℃时,硝酸钾和氯化钠的溶解度相等,所以硝酸钾和氯化钠的饱和
1
溶液溶质质量分数相等,选项正确。
故选AD。
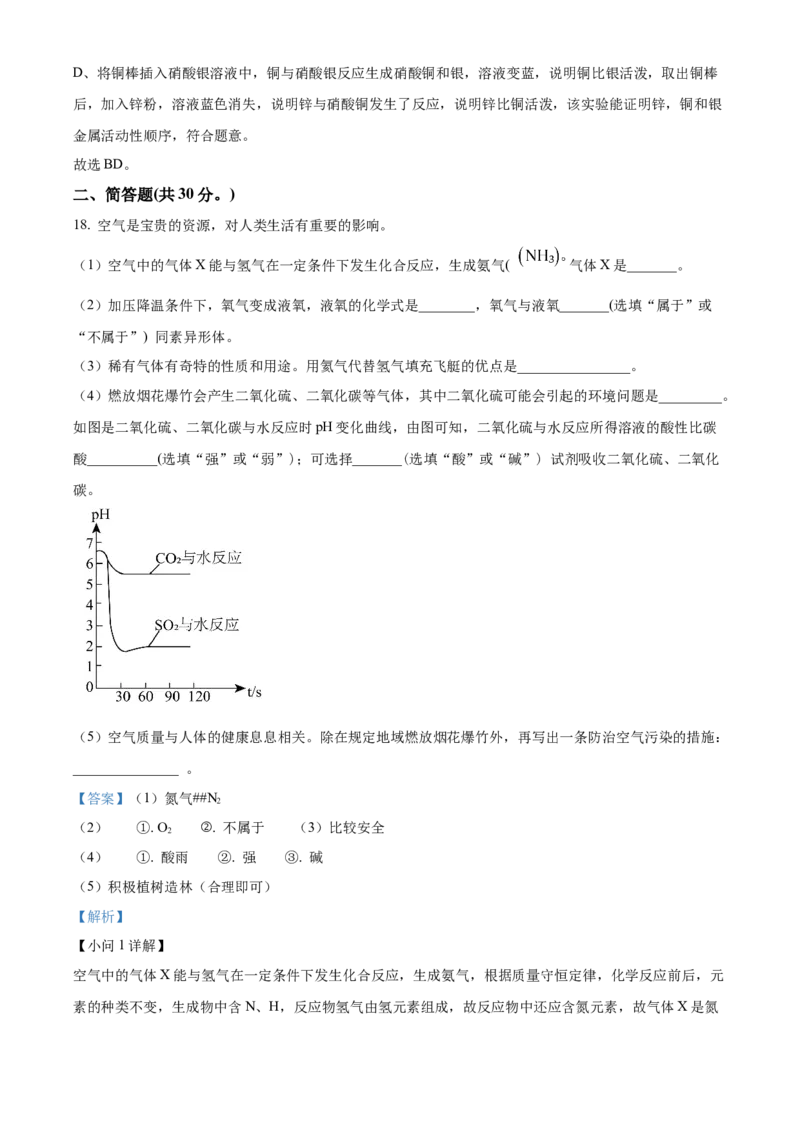
17. 将铜棒插入 溶液中(如图),溶液变蓝后取出铜棒,再向烧杯内加入锌粉,充分反应后,溶液
蓝色消失。结论正确的是:
A. 最终烧杯内溶液中可能有 B. 最终烧杯内溶液中一定有
C. 最终烧杯内可能有金属铜 D. 该实验能证明锌,铜和银金属活动性顺序
【答案】BD
【解析】
【分析】将铜棒插入AgNO 溶液中,铜和硝酸银反应生成硝酸铜和银,溶液变蓝后,取出铜棒,再向烧杯
3
内加入锌粉,金属活动性:Zn>Cu>Ag,锌先与硝酸银反应生成硝酸锌和银,待硝酸银完全反应后,锌
和硝酸铜反应生成硝酸锌和铜,充分反应后,溶液蓝色消失,说明硝酸铜完全反应,则硝酸银也完全反应。
【详解】A、由分析可知,充分反应后,硝酸银一定完全反应,最终烧杯中一定不含硝酸银,不符合题意;
B、由分析可知,锌与硝酸铜、硝酸银均反应生成了硝酸锌,硝酸银、硝酸铜完全反应,故最终烧杯内溶
液中一定含有硝酸锌,符合题意;
C、由分析可知,锌与硝酸铜反应生成了硝酸锌和铜,硝酸铜完全反应,故最终烧杯内一定含金属铜,不
符合题意;D、将铜棒插入硝酸银溶液中,铜与硝酸银反应生成硝酸铜和银,溶液变蓝,说明铜比银活泼,取出铜棒
后,加入锌粉,溶液蓝色消失,说明锌与硝酸铜发生了反应,说明锌比铜活泼,该实验能证明锌,铜和银
金属活动性顺序,符合题意。
故选BD。
二、简答题(共30分。)
18. 空气是宝贵的资源,对人类生活有重要的影响。
(1)空气中的气体X能与氢气在一定条件下发生化合反应,生成氨气( 气体X是_______。
(2)加压降温条件下,氧气变成液氧,液氧的化学式是________,氧气与液氧_______(选填“属于”或
“不属于”) 同素异形体。
(3)稀有气体有奇特的性质和用途。用氦气代替氢气填充飞艇的优点是________________。
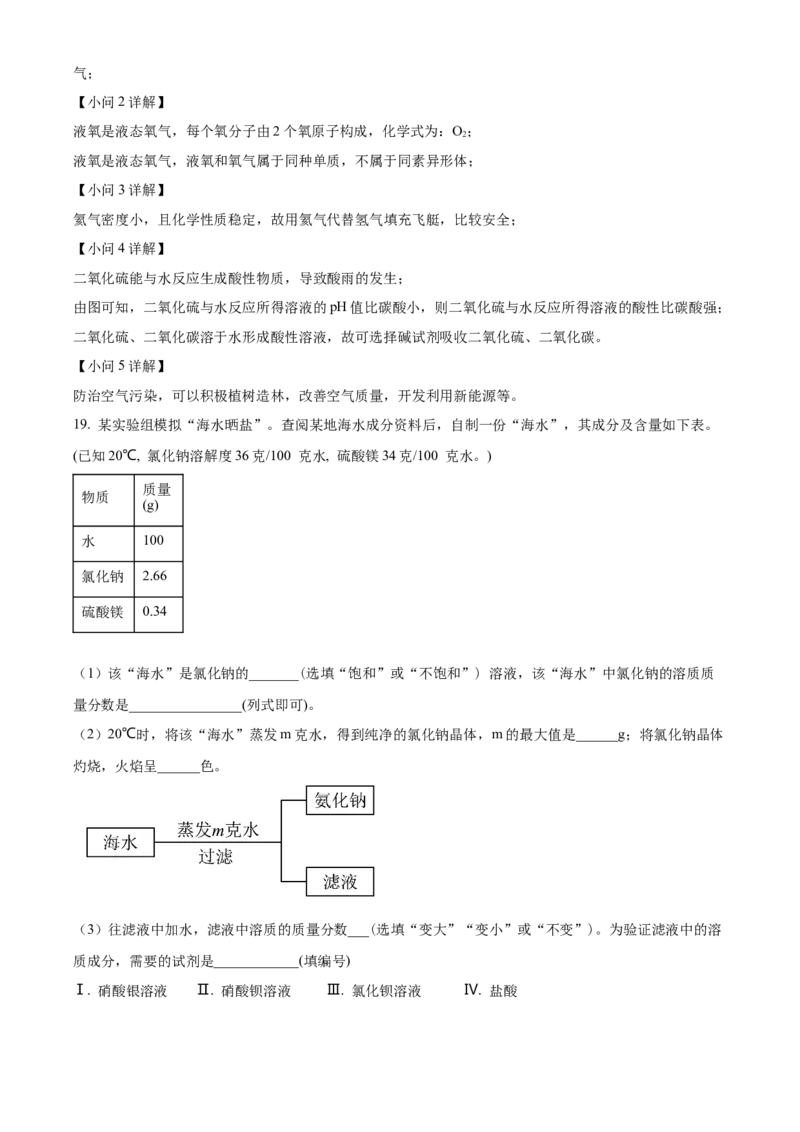
(4)燃放烟花爆竹会产生二氧化硫、二氧化碳等气体,其中二氧化硫可能会引起的环境问题是_________。
如图是二氧化硫、二氧化碳与水反应时pH变化曲线,由图可知,二氧化硫与水反应所得溶液的酸性比碳
酸__________(选填“强”或“弱”);可选择_______(选填“酸”或“碱”) 试剂吸收二氧化硫、二氧化
碳。
(5)空气质量与人体的健康息息相关。除在规定地域燃放烟花爆竹外,再写出一条防治空气污染的措施:
_______________ 。
【答案】(1)氮气##N
2
(2) ①. O ②. 不属于 (3)比较安全
2
(4) ①. 酸雨 ②. 强 ③. 碱
(5)积极植树造林(合理即可)
【解析】
【小问1详解】
空气中的气体X能与氢气在一定条件下发生化合反应,生成氨气,根据质量守恒定律,化学反应前后,元
素的种类不变,生成物中含N、H,反应物氢气由氢元素组成,故反应物中还应含氮元素,故气体X是氮气;
【小问2详解】
液氧是液态氧气,每个氧分子由2个氧原子构成,化学式为:O;
2
液氧是液态氧气,液氧和氧气属于同种单质,不属于同素异形体;
【小问3详解】
氦气密度小,且化学性质稳定,故用氦气代替氢气填充飞艇,比较安全;
【小问4详解】
二氧化硫能与水反应生成酸性物质,导致酸雨的发生;
由图可知,二氧化硫与水反应所得溶液的pH值比碳酸小,则二氧化硫与水反应所得溶液的酸性比碳酸强;
二氧化硫、二氧化碳溶于水形成酸性溶液,故可选择碱试剂吸收二氧化硫、二氧化碳。
【小问5详解】
防治空气污染,可以积极植树造林,改善空气质量,开发利用新能源等。
19. 某实验组模拟“海水晒盐”。查阅某地海水成分资料后,自制一份“海水”,其成分及含量如下表。
(已知20℃, 氯化钠溶解度36克/100 克水, 硫酸镁34克/100 克水。)
质量
物质
(g)
水 100
氯化钠 2.66
硫酸镁 0.34
(1)该“海水”是氯化钠的_______(选填“饱和”或“不饱和”) 溶液,该“海水”中氯化钠的溶质质
量分数是________________(列式即可)。
(2)20℃时,将该“海水”蒸发m克水,得到纯净的氯化钠晶体,m的最大值是______g;将氯化钠晶体
灼烧,火焰呈______色。
(3)往滤液中加水,滤液中溶质的质量分数___(选填“变大”“变小”或“不变”)。为验证滤液中的溶
质成分,需要的试剂是____________(填编号)
Ⅰ. 硝酸银溶液 Ⅱ. 硝酸钡溶液 Ⅲ. 氯化钡溶液 Ⅳ. 盐酸【答案】(1) ①. 不饱和 ②.
(2) ①. 99 ②. 黄
(3) ①. 变小 ②. Ⅰ、 Ⅱ
【解析】
【小问1详解】
20℃时,氯化钠的溶解度为36克/100 克水,即该温度下,100g水中最多可溶解36g氯化钠,该“海水”
中水的质量为100g,氯化钠的质量为2.66g,则该“海水”是氯化钠的不饱和溶液;
该“海水”中氯化钠的溶质质量分数是: ;
【小问2详解】
的
20℃时,氯化钠 溶解度为36克/100 克水,硫酸镁的溶解度为34克/100 克水,设溶解2.66g氯化钠,
至少需要水的质量为x,则 ,x≈7.4g,设溶解0.34g硫酸镁,至少需要水的质量为y,则
,y=1g,故m的最大值为100g-1g=99g,此时氯化钠结晶析出,硫酸镁还未析出;
氯化钠晶体中含钠元素,故将氯化钠晶体灼烧,火焰呈黄色;
【小问3详解】
往滤液中加水,溶剂质量变大,溶质质量不变,则滤液中溶质的质量分数变小;
硫酸镁能与硝酸钡反应生成硫酸钡和硝酸镁,产生白色沉淀,说明含硝酸镁,可加入过量的硝酸钡溶液检
验硫酸镁,且将硫酸镁除尽,不能选择氯化钡溶液,是因为加入氯化钡,引入了氯离子,会对氯化钠的检
验产生干扰,硝酸银能与氯化钠反应生成氯化银和硝酸钠,故可用硝酸银溶液检验氯化钠,故为验证滤液
中的溶质成分,需要的试剂是:Ⅰ、 Ⅱ。
20. 碳酸钠是一种重要的化工原料,常用于生成玻璃、造纸和日用化工。
(1)探究碳酸钠溶液的酸碱性。
碳酸钠溶液中滴加酚酞试液,溶液显红色,说明碳酸钠溶液呈_____性。
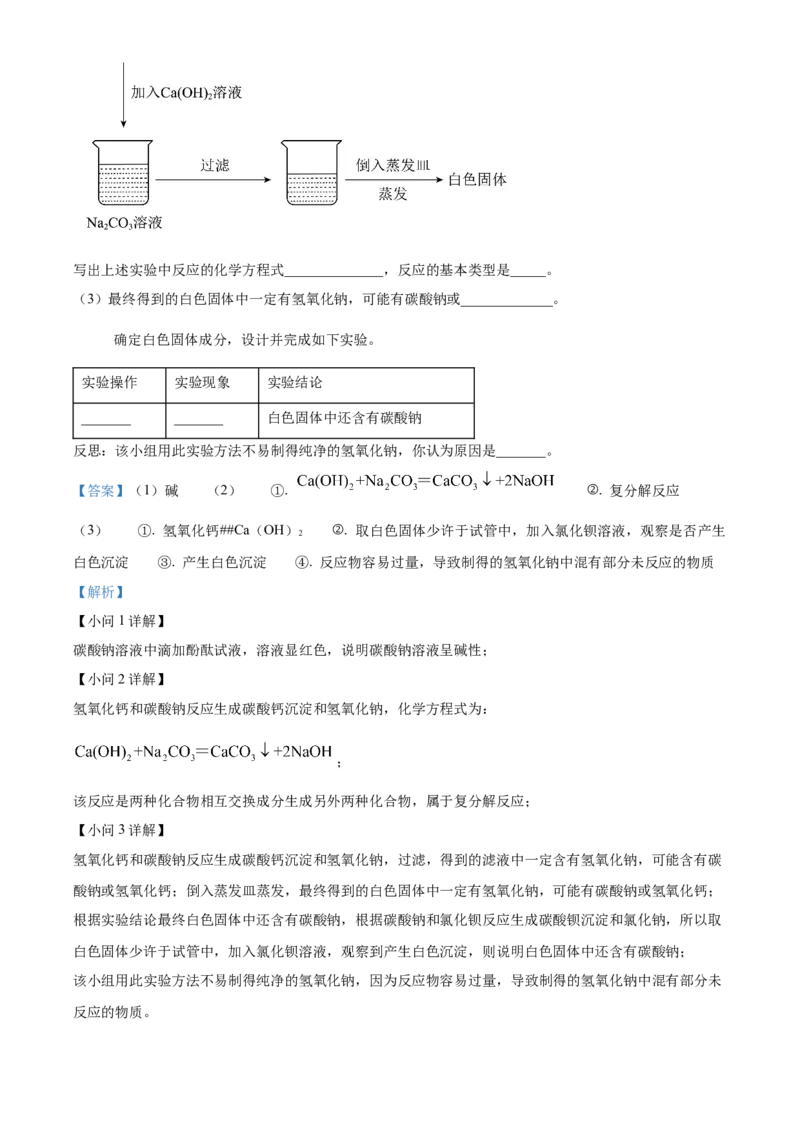
(2)实验室里,某实验小组用碳酸钠制取氢氧化钠。实验过程如下图。写出上述实验中反应的化学方程式______________,反应的基本类型是_____。
(3)最终得到的白色固体中一定有氢氧化钠,可能有碳酸钠或_____________。
为
确定白色固体成分,设计并完成如下实验。
实验操作 实验现象 实验结论
_______ _______ 白色固体中还含有碳酸钠
反思:该小组用此实验方法不易制得纯净的氢氧化钠,你认为原因是_______。
【答案】(1)碱 (2) ①. ②. 复分解反应
(3) ①. 氢氧化钙##Ca(OH) ②. 取白色固体少许于试管中,加入氯化钡溶液,观察是否产生
2
白色沉淀 ③. 产生白色沉淀 ④. 反应物容易过量,导致制得的氢氧化钠中混有部分未反应的物质
【解析】
【小问1详解】
碳酸钠溶液中滴加酚酞试液,溶液显红色,说明碳酸钠溶液呈碱性;
【小问2详解】
氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:
;
该反应是两种化合物相互交换成分生成另外两种化合物,属于复分解反应;
【小问3详解】
氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,过滤,得到的滤液中一定含有氢氧化钠,可能含有碳
酸钠或氢氧化钙;倒入蒸发皿蒸发,最终得到的白色固体中一定有氢氧化钠,可能有碳酸钠或氢氧化钙;
根据实验结论最终白色固体中还含有碳酸钠,根据碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,所以取
白色固体少许于试管中,加入氯化钡溶液,观察到产生白色沉淀,则说明白色固体中还含有碳酸钠;
该小组用此实验方法不易制得纯净的氢氧化钠,因为反应物容易过量,导致制得的氢氧化钠中混有部分未
反应的物质。21. 铜是人类最早使用的金属之一,我国商代就有了璀璨的青铜文明。
(1)古代工匠以孔雀石 和木炭为原料进行火法炼铜。加热时,孔雀石可分解生成氧化
铜和水、二氧化碳。配平反应的化学方程式为: ____CuO+___HO+___CO ;
2 2
↑
(2)木炭和生成的氧化铜反应炼出铜,写出反应的化学方程式_____________________,反应中碳和氧化
铜物质的量之比为________________。古籍《采铜炼铜记》记载,“……用碳八九千斤,不过得铜五六百
斤”,发现消耗掉碳物质的量大于氧化铜物质的量,写出可能的原因:__________________________。(用
化学方程式表示)
【答案】(1) ①. 2 ②. 1 ③. 1
(2) ①. ②. 1:2 ③. (合理即可)
【解析】
【小问1详解】
根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含2个Cu,生成物中也应含2个
Cu,故氧化铜的化学计量数为2,反应物中含2个H,生成物中也应含2个H,故水的化学计量数为1,反
应物中含1个C,生成物中也应含1个C,故二氧化碳的化学计量数为1,观察,配平后,化学反应前后,
氧原子的个数相等,故填:2、1、1;
【小问2详解】
木炭和氧化铜在高温下反应生成铜和二氧化碳,该反应的化学方程式为: ;
由化学方程式可知,反应中碳和氧化铜的物质的量之比为:1:2;
高温下,碳能燃烧生成二氧化碳,故消耗掉碳物质的量大于氧化铜物质的量,该反应的化学方程式为:
。