文档内容
2025—2026学年度第一学期期末学业水平监测
高 一 化 学
注意事项:
1本试卷满分100分,考试时间75分钟。
2作答题时务必将答案写在答题卡上。写在本卷及草稿纸上无效。
3可能用到的相对原子量:H1 C12 N14 O16 Na23 S32 Cl355 Ca40
一、选择题(每题只有一个选项符合题意,每小题3分,共48分)
1生活中处处有化学。下列说法中错误的是
ASO 是一种食品添加剂
2
B84消毒液的有效成分是NaClO
C激光打印机的墨粉中含有FeO
3 4
DNaCl是食品膨松剂的主要成分
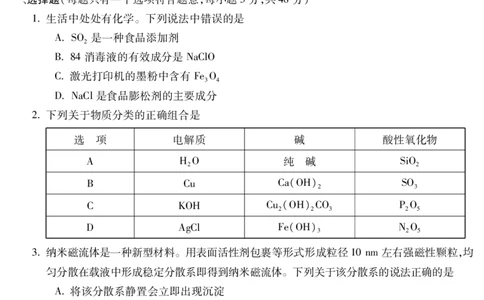
2下列关于物质分类的正确组合是
选 项 电解质 碱 酸性氧化物
A HO 纯 碱 SiO
2 2
B Cu Ca(OH) SO
2 3
C KOH Cu(OH)CO PO
2 2 3 2 5
D AgCl Fe(OH) NO
3 2 5
3纳米磁流体是一种新型材料。用表面活性剂包裹等形式形成粒径10nm左右强磁性颗粒,均
匀分散在载液中形成稳定分散系即得到纳米磁流体。下列关于该分散系的说法正确的是
A将该分散系静置会立即出现沉淀
B纳米颗粒直径较小,可以透过半透膜
C利用丁达尔效应可以区分氯化钠溶液和该分散系
D可以用过滤的方法将溶液与纳米材料分离
4下列说法正确的是
AH 的摩尔质量是2g
2
B1molO 含有氧原子数为2N
2 A
C标准状况下,1mol任何物质的体积都约为224L
D从100mL1mol·L-1的硫酸钠溶液中取出50mL溶液,c(Na+)=1mol·L-1
高一化学试卷第1页(共6页)
{#{QQABYYQ04gAwgsTACJ4KRQ0YCkgYkJGgLAgEAQAauAQKgYNIBIA=}#}
书书书5物质类别和元素价态是认识物质性质及其转化的重要角度,下图为含氯元素的物质的
“价—类”二维图。下列说法不正确的是
獉
A由甲转化为乙,需要加氧化剂 B戊的酸性强于碳酸
C庚与甲在一定条件下反应可制得乙 D丙可用于自来水消毒
6下列氯化物中,既能由金属和氯气直接化合制得,又能由金属和盐酸反应制得的是
AFeCl BNaCl CFeCl DCuCl
2 3 2
7氢化钠(氢元素为-1价)作为生氢剂的原理为 NaH+HONaOH+H↑。设 N 为阿
2 2 A
伏加德罗常数的值。下列说法正确的是
A若生成112LH,含氢原子数为N
2 A
B消耗1molNaH转移的电子数为2N
A
C18gHO中含有质子数为N
2 A
D010mol·L-1NaOH溶液中含有Na+的数目为01N
A
8在给定的反应物和反应条件下,下列物质间的转化正确的是
HO Cl
2 2
ACaO→Ca(OH)→Ca(ClO)
2 2
稀盐酸 Na
BCu(OH)→CuCl→Cu
2 2
Cl 2 NaOH溶液
CFe→FeCl→Fe(OH)
加热 2 2
CO 2 加热
DNaCl溶液→NaHCO →NaCO
3 2 3
9有一瓶NaSO 溶液,它可能部分被氧化。某同学取少量该溶液,滴加BaCl溶液,产生白色
2 3 2
沉淀;再加入足量稀硫酸,充分振荡后仍有白色沉淀。下列结论中正确的是
ANaSO 已部分被空气中的氧气氧化
2 3
B加入BaCl溶液后,产生的沉淀中一定含硫酸钡
2
C加入稀硫酸后,不溶的沉淀一定是硫酸钡
D取少量该溶液,加入足量稀盐酸,若生成能使品红褪色的气体,则NaSO 部分被氧化
2 3
高一化学试卷第2页(共6页)
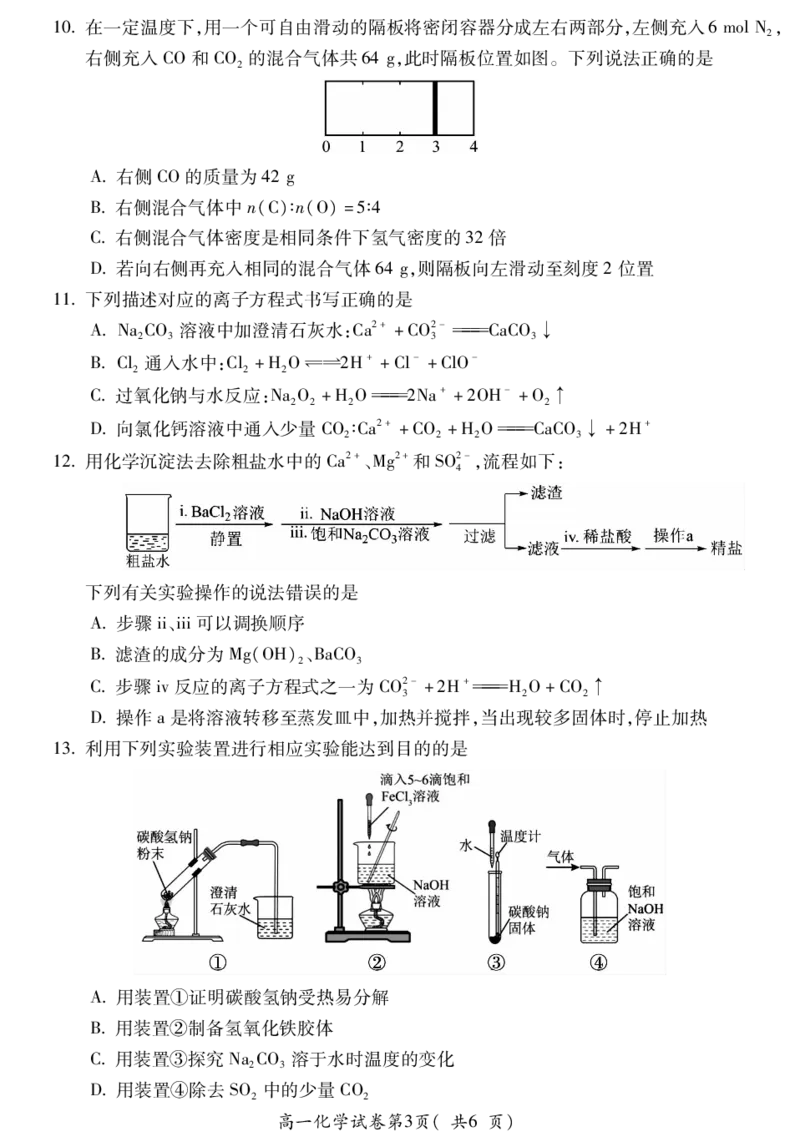
{#{QQABYYQ04gAwgsTACJ4KRQ0YCkgYkJGgLAgEAQAauAQKgYNIBIA=}#}10在一定温度下,用一个可自由滑动的隔板将密闭容器分成左右两部分,左侧充入6molN,
2
右侧充入CO和CO 的混合气体共64g,此时隔板位置如图。下列说法正确的是
2
A右侧CO的质量为42g
B右侧混合气体中n(C)∶n(O)=5∶4
C右侧混合气体密度是相同条件下氢气密度的32倍
D若向右侧再充入相同的混合气体64g,则隔板向左滑动至刻度2位置
11下列描述对应的离子方程式书写正确的是
ANaCO 溶液中加澄清石灰水:Ca2++CO2-CaCO↓
2 3 3 3
BCl通入水中:Cl+HO幑幐2H++Cl-+ClO-
2 2 2
C过氧化钠与水反应:NaO +HO2Na++2OH-+O↑
2 2 2 2
D向氯化钙溶液中通入少量CO∶Ca2++CO +HOCaCO↓+2H+
2 2 2 3
12用化学沉淀法去除粗盐水中的Ca2+、Mg2+和SO2-,流程如下:
4
下列有关实验操作的说法错误的是
A步骤ii、iii可以调换顺序
B滤渣的成分为Mg(OH)、BaCO
2 3
C步骤iv反应的离子方程式之一为CO2-+2H+HO+CO↑
3 2 2
D操作a是将溶液转移至蒸发皿中,加热并搅拌,当出现较多固体时,停止加热
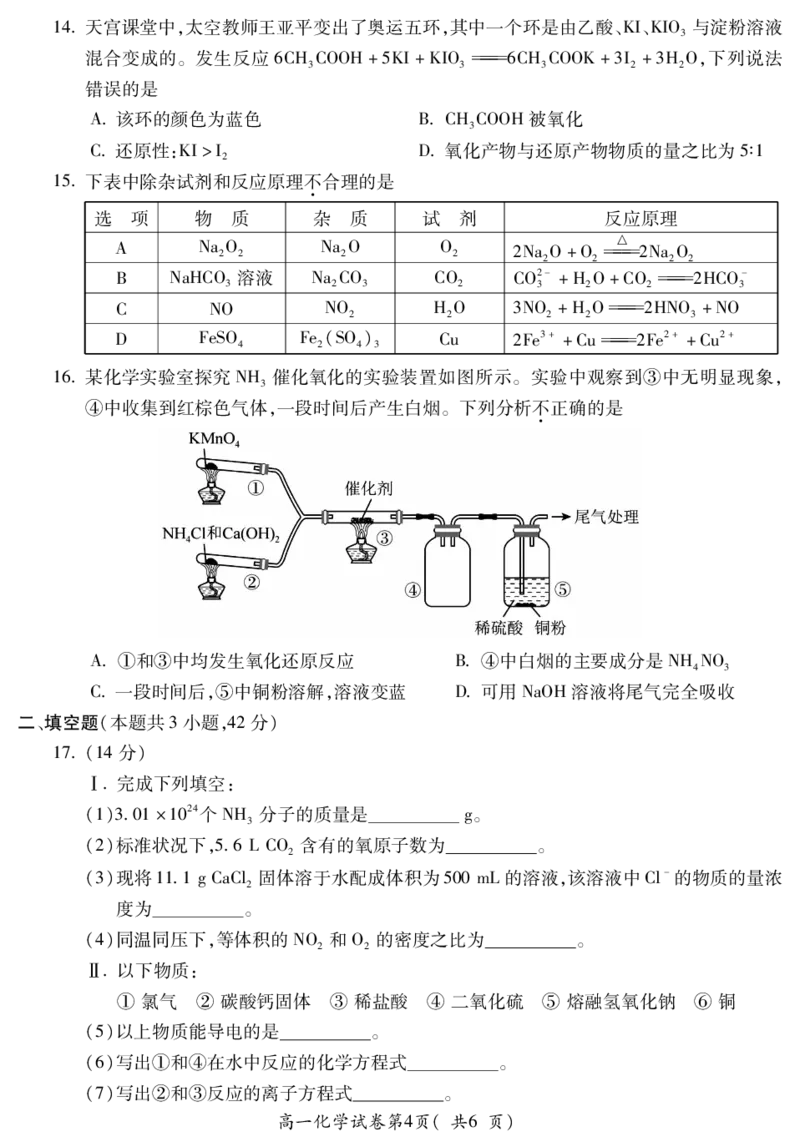
13利用下列实验装置进行相应实验能达到目的的是
A用装置①证明碳酸氢钠受热易分解
B用装置②制备氢氧化铁胶体
C用装置③探究NaCO 溶于水时温度的变化
2 3
D用装置④除去SO 中的少量CO
2 2
高一化学试卷第3页(共6页)
{#{QQABYYQ04gAwgsTACJ4KRQ0YCkgYkJGgLAgEAQAauAQKgYNIBIA=}#}14天宫课堂中,太空教师王亚平变出了奥运五环,其中一个环是由乙酸、KI、KIO 与淀粉溶液
3
混合变成的。发生反应6CHCOOH+5KI+KIO 6CHCOOK+3I+3HO,下列说法
3 3 3 2 2
错误的是
A该环的颜色为蓝色 BCHCOOH被氧化
3
C还原性:KI>I D氧化产物与还原产物物质的量之比为5∶1
2
15下表中除杂试剂和反应原理不合理的是
獉
选 项 物 质 杂 质 试 剂 反应原理
A Na 2 O 2 Na 2 O O 2 2Na 2 O+O 2 △ 2Na 2 O 2
B NaHCO 溶液 NaCO CO CO2-+HO+CO 2HCO-
3 2 3 2 3 2 2 3
C NO NO HO 3NO +HO2HNO +NO
2 2 2 2 3
D FeSO Fe(SO) Cu 2Fe3++Cu2Fe2++Cu2+
4 2 4 3
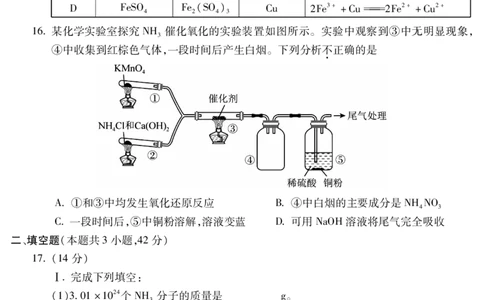
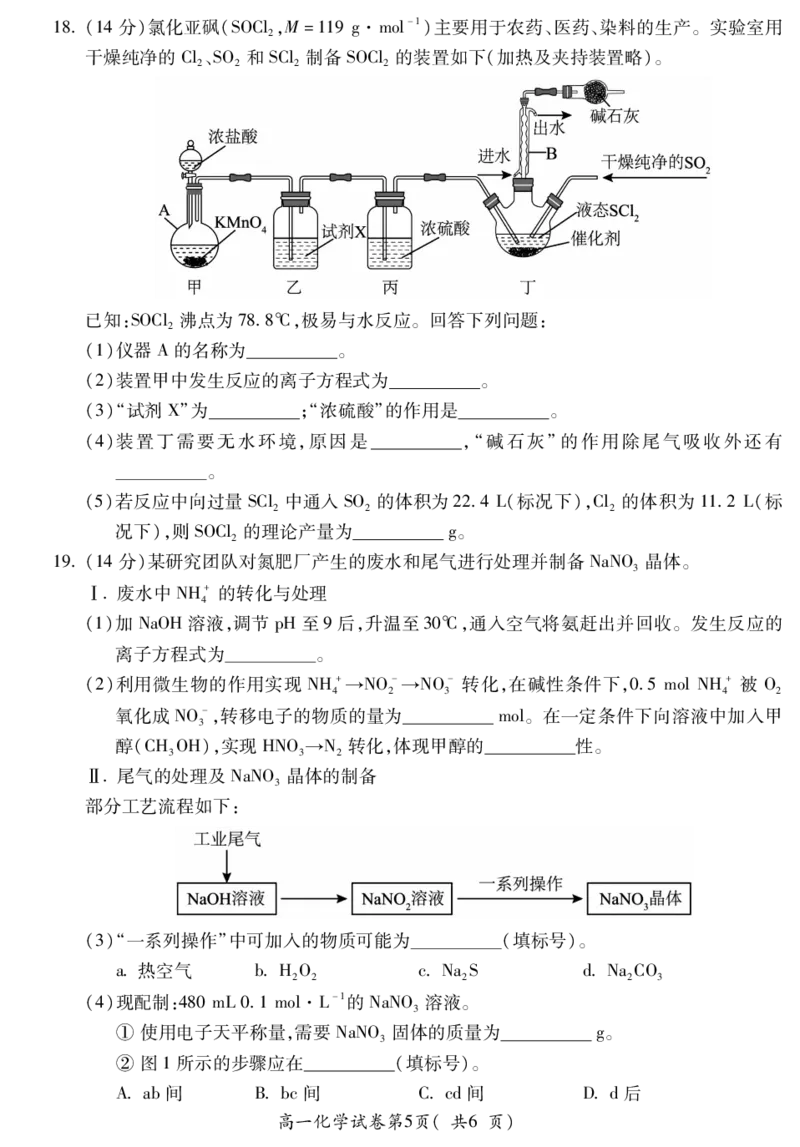
16某化学实验室探究NH 催化氧化的实验装置如图所示。实验中观察到③中无明显现象,
3
④中收集到红棕色气体,一段时间后产生白烟。下列分析不正确的是
獉
A①和③中均发生氧化还原反应 B④中白烟的主要成分是NHNO
4 3
C一段时间后,⑤中铜粉溶解,溶液变蓝 D可用NaOH溶液将尾气完全吸收
二、填空题(本题共3小题,42分)
17(14分)
Ⅰ完成下列填空:
(1)301×1024个NH 分子的质量是 g。
3
(2)标准状况下,56LCO 含有的氧原子数为 。
2
(3)现将111gCaCl固体溶于水配成体积为500mL的溶液,该溶液中Cl-的物质的量浓
2
度为 。
(4)同温同压下,等体积的NO 和O 的密度之比为 。
2 2
Ⅱ以下物质:
① 氯气 ② 碳酸钙固体 ③ 稀盐酸 ④ 二氧化硫 ⑤ 熔融氢氧化钠 ⑥ 铜
(5)以上物质能导电的是 。
(6)写出①和④在水中反应的化学方程式 。
(7)写出②和③反应的离子方程式 。
高一化学试卷第4页(共6页)
{#{QQABYYQ04gAwgsTACJ4KRQ0YCkgYkJGgLAgEAQAauAQKgYNIBIA=}#}18(14分)氯化亚砜(SOCl,M=119g·mol-1)主要用于农药、医药、染料的生产。实验室用
2
干燥纯净的Cl、SO 和SCl制备SOCl的装置如下(加热及夹持装置略)。
2 2 2 2
已知:SOCl沸点为788℃,极易与水反应。回答下列问题:
2
(1)仪器A的名称为 。
(2)装置甲中发生反应的离子方程式为 。
(3)“试剂X”为 ;“浓硫酸”的作用是 。
(4)装置丁需要无水环境,原因是 ,“碱石灰”的作用除尾气吸收外还有
。
(5)若反应中向过量SCl中通入SO 的体积为224L(标况下),Cl的体积为112L(标
2 2 2
况下),则SOCl的理论产量为 g。
2
19(14分)某研究团队对氮肥厂产生的废水和尾气进行处理并制备NaNO 晶体。
3
Ⅰ废水中NH+的转化与处理
4
(1)加NaOH溶液,调节pH至9后,升温至30℃,通入空气将氨赶出并回收。发生反应的
离子方程式为 。
(2)利用微生物的作用实现 NH+→NO-→NO-转化,在碱性条件下,05molNH+被 O
4 2 3 4 2
氧化成NO-,转移电子的物质的量为 mol。在一定条件下向溶液中加入甲
3
醇(CHOH),实现HNO→N 转化,体现甲醇的 性。
3 3 2
Ⅱ尾气的处理及NaNO 晶体的制备
3
部分工艺流程如下:
(3)“一系列操作”中可加入的物质可能为 (填标号)。
a热空气 bHO cNaS dNaCO
2 2 2 2 3
(4)现配制:480mL01mol·L-1的NaNO 溶液。
3
① 使用电子天平称量,需要NaNO 固体的质量为 g。
3
② 图1所示的步骤应在 (填标号)。
Aab间 Bbc间 Ccd间 Dd后
高一化学试卷第5页(共6页)
{#{QQABYYQ04gAwgsTACJ4KRQ0YCkgYkJGgLAgEAQAauAQKgYNIBIA=}#}③ 溶液配制时会导致NaNO 溶液浓度偏大的情况是 (填标号)。
3
A容量瓶在使用前未干燥
B定容时俯视液面
C称量后将固体转入烧杯中不小心洒落
D烧杯内溶液转入容量瓶中后未洗涤烧杯和玻璃棒
三、计算题(10分。写出计算过程)
20在500mL某混合溶液中,HSO、FeSO、Fe(SO)物质的量浓度相等,其中 Fe2+的物质
2 4 4 2 4 3
的量浓度为1mol·L-1。回答下列问题:
(1)该混合溶液中SO2-的物质的量浓度是多少?
4
(2)加入足量铁粉充分反应后,产生的氢气在标准状况下的体积是多少?溶液中 Fe2+的
物质的量浓度变为多少?(假设溶液体积不变)
高一化学试卷第6页(共6页)
{#{QQABYYQ04gAwgsTACJ4KRQ0YCkgYkJGgLAgEAQAauAQKgYNIBIA=}#}