文档内容
4.胶体化学的发展促使了纳米材料的广泛应用。对如下流程的分析与应用不合理的是 ( )
Cl 试剂①
高一化学试卷(二) Fe→ 2 FeCl→Fe(OH)胶体
Ⅰ 3 Ⅱ 3
(本试卷满分100分,考试时间75分钟) A.铁能够与Cl反应,液氯不能用干燥钢瓶保存
2
注意事项:1.答题前,考生务必用黑色字迹的签字笔或钢笔将自己的姓名、准考证号分别填写 B.试剂①是沸水,生成红褐色液体
在试卷和答题卡规定的位置上。 C.氢氧化铁胶体的分散质粒子直径在1~100nm范围内
2.答选择题时,选出每小题答案后,用2B铅笔把答题卡对应题目的答案涂黑,如需 D.可以通过改变材料的粒径大小从而改变其性能
改动,用橡皮擦干净后,再涂其它答案。非选择题的答案必须用黑色字迹的签字 5.下列有关新制氯水的说法不正确的是 ( )
笔或钢笔写在答题卡上相应的区域内,写在本试卷上无效。 A.新制氯水呈黄绿色,是因为氯水中含有Cl
2
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 B.新制氯水滴到NaCO 溶液中,有气泡产生,说明氯水中呈酸性
2 3
一 、选 择 题 : 本 题 共 15 小 题 ,每 小 题 3分 , 共 4 5分 。 在 每 小 题 给 出 的 四 个选项中,只有一项符 C.新制氯水滴到硝酸银溶液中,能产生白色沉淀
合题目要求。 D.新制氯水光照一段时间,酸性会减弱
1.我国历史悠久,劳动人民创造了丰富的物质财富。下列古代生产和生活过程中没有涉及氧 6.在酸性溶液中离子还原性强弱顺序为 SO >I->Fe2+>HO >Cl-,则下列反应不可能发
2 2 2
化还原反应的是 ( ) 生的是 ( )
A.冶铁和炼钢 B.制作笔、砚 C.酿制酒、醋 D.烧煤取暖 A.2Fe3++2HO+SO 2Fe2++SO2-+4H+
2 2 4
2.学习化学要善于从化学的视角分析问题,下列说法正确的是 ( ) B.2Fe2++Cl2Fe3++2Cl-
2
A.NaHSO、HNO 在水中均能电离出氢离子,都属于酸 C.I+SO +2HOHSO +2HI
4 3 2 2 2 2 4
B.CO 水溶液导电,实际是HCO 导电,所以 CO 是非电解质,NaO 溶于水导电,实际是 D.HO +HSO SO↑+O↑+2HO
2 2 3 2 2 2 2 2 2 4 2 2 2
NaOH导电,所以NaO 也是非电解质 7.下列反应的离子方程式书写正确的是 ( )
2 2
C.CuSO·5HO、液氨、碱石灰,漂白粉,都属于纯净物 A.氯化铁溶液与氢氧化钠溶液反应:Fe3++3OH-Fe(OH)↓
4 2 3
D.NaO 中阳离子和阴离子个数之比为2∶1 B.向硝酸银溶液中加盐酸:AgNO +Cl-AgCl↓+NO-
2 2 3 3
3.酸式盐是盐的一种,可看作是多元酸未被完全中和所得到的盐。常见的酸式盐有 NaHCO
3
、 C.碳酸钙与稀盐酸反应:CO2
3
-+2H+CO
2
↑+H
2
O
NaHSO
4
、KH
2
PO
4
、K
2
HPO
4
等。已知 H
3
PO
2
与足量的 KOH反应只能生成一种盐 KH
2
PO
2
。 D.铁与稀盐酸反应:2Fe+6H+2Fe3++3H↑
2
下列说法中,正确的是 ( )
8.生活离不开化学,下列说法不正确的是 ( )
A.KH 2 PO 2 属于正盐 A.放映机到银幕间光柱的形成是丁达尔效应,它可被用来区分胶体和溶液
B.KHPO 溶液一定为酸性 B.碳酸钠可用作制作糕点的膨松剂,是因为加热能分解出二氧化碳
2 2
C.HPO 属于三元酸 C.过氧化钠既可用作呼吸面具中氧气的来源,又可漂白织物
3 2
D.KHPO 可以与KOH反应生成KPO D.节日燃放的五彩缤纷的烟花所呈现的艳丽色彩是金属元素的焰色
2 2 3 2
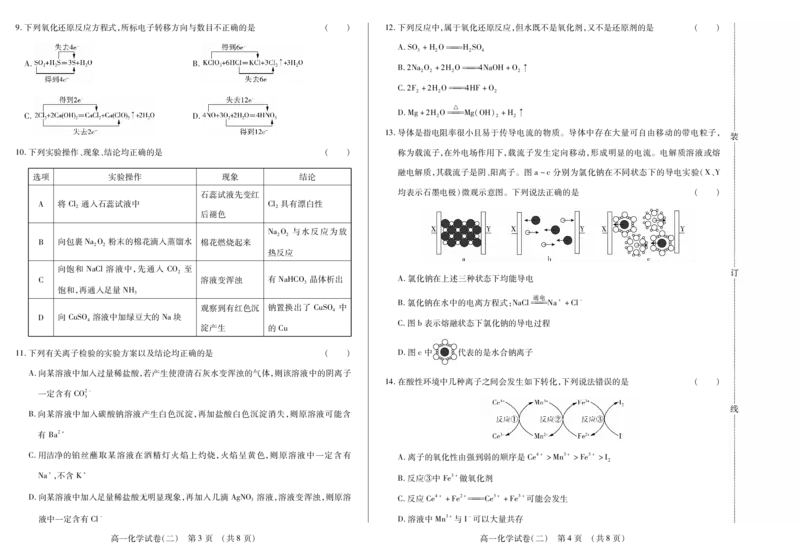
高一化学试卷(二) 第1页 (共8页) 高一化学试卷(二) 第2页 (共8页)9.下列氧化还原反应方程式,所标电子转移方向与数目不正确的是 ( ) 12.下列反应中,属于氧化还原反应,但水既不是氧化剂,又不是还原剂的是 ( )
A.SO +HOHSO
3 2 2 4
A. B.
B.2NaO +2HO4NaOH+O↑
2 2 2 2
C.2F+2HO4HF+O
2 2 2
△
D.Mg+2HOMg(OH)+H↑
C. D. 2 2 2
13.导体是指电阻率很小且易于传导电流的物质。导体中存在大量可自由移动的带电粒子,
10.下列实验操作、现象、结论均正确的是 ( ) 称为载流子,在外电场作用下,载流子发生定向移动,形成明显的电流。电解质溶液或熔
融电解质,其载流子是阴、阳离子。图a~c分别为氯化钠在不同状态下的导电实验(X、Y
选项 实验操作 现象 结论
石蕊试液先变红 均表示石墨电极)微观示意图。下列说法正确的是 ( )
A 将Cl通入石蕊试液中 Cl具有漂白性
2 2
后褪色
NaO 与水反应为放
2 2
B 向包裹NaO 粉末的棉花滴入蒸馏水 棉花燃烧起来
2 2
热反应
向饱和 NaCl溶液中,先通入 CO 至
2
C 溶液变浑浊 有NaHCO 晶体析出 A.氯化钠在上述三种状态下均能导电
3
饱和,再通入足量NH
3
通电
B.氯化钠在水中的电离方程式:NaClNa++Cl-
观察到有红色沉 钠置换出了 CuSO 中
4
D 向CuSO 溶液中加绿豆大的Na块
4 C.图b表示熔融状态下氯化钠的导电过程
淀产生 的Cu
11.下列有关离子检验的实验方案以及结论均正确的是 ( ) D.图c中 代表的是水合钠离子
A.向某溶液中加入过量稀盐酸,若产生使澄清石灰水变浑浊的气体,则该溶液中的阴离子
14.在酸性环境中几种离子之间会发生如下转化,下列说法错误的是 ( )
一定含有CO2-
3
B.向某溶液中加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,则原溶液可能含
有 Ba2+
C.用洁净的铂丝蘸取某溶液在酒精灯火焰上灼烧,火焰呈黄色,则原溶液中一定含有 A.离子的氧化性由强到弱的顺序是Ce4+>Mn3+>Fe3+>I
2
Na+,不含K+
B.反应③中Fe3+做氧化剂
D.向某溶液中加入足量稀盐酸无明显现象,再加入几滴 AgNO 溶液,溶液变浑浊,则原溶 C.反应Ce4++Fe2+Ce3++Fe3+可能会发生
3
液中一定含有Cl- D.溶液中Mn3+与I-可以大量共存
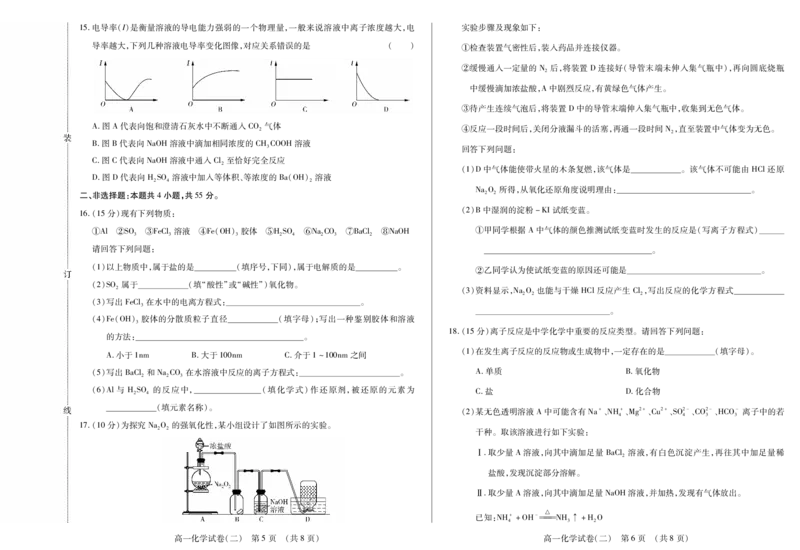
高一化学试卷(二) 第3页 (共8页) 高一化学试卷(二) 第4页 (共8页)15.电导率(I)是衡量溶液的导电能力强弱的一个物理量,一般来说溶液中离子浓度越大,电 实验步骤及现象如下:
导率越大,下列几种溶液电导率变化图像,对应关系错误的是 ( ) ①检查装置气密性后,装入药品并连接仪器。
②缓慢通入一定量的N 后,将装置D连接好(导管末端未伸入集气瓶中),再向圆底烧瓶
2
中缓慢滴加浓盐酸,A中剧烈反应,有黄绿色气体产生。
③待产生连续气泡后,将装置D中的导管末端伸入集气瓶中,收集到无色气体。
A.图A代表向饱和澄清石灰水中不断通入CO 气体
2 ④反应一段时间后,关闭分液漏斗的活塞,再通一段时间N,直至装置中气体变为无色。
2
B.图B代表向NaOH溶液中滴加相同浓度的CHCOOH溶液
3 回答下列问题:
C.图C代表向NaOH溶液中通入Cl至恰好完全反应
2
(1)D中气体能使带火星的木条复燃,该气体是 。该气体不可能由 HCl还原
D.图D代表向HSO 溶液中加入等体积、等浓度的Ba(OH)溶液
2 4 2
NaO 所得,从氧化还原角度说明理由: 。
二、非选择题:本题共4小题,共55分。 2 2
(2)B中湿润的淀粉-KI试纸变蓝。
16.(15分)现有下列物质:
①Al ②SO ③FeCl溶液 ④Fe(OH)胶体 ⑤HSO ⑥NaCO ⑦BaCl ⑧NaOH ①甲同学根据A中气体的颜色推测试纸变蓝时发生的反应是(写离子方程式)
3 3 3 2 4 2 3 2
请回答下列问题: 。
(1)以上物质中,属于盐的是 (填序号,下同),属于电解质的是 。
②乙同学认为使试纸变蓝的原因还可能是 。
(2)SO 属于 (填“酸性”或“碱性”)氧化物。
2 (3)资料显示,NaO 也能与干燥HCl反应产生 Cl,写出反应的化学方程式
2 2 2
(3)写出FeCl在水中的电离方程式: 。
3
。
(4)Fe(OH)胶体的分散质粒子直径 (填字母);写出一种鉴别胶体和溶液
3
18.(15分)离子反应是中学化学中重要的反应类型。请回答下列问题:
的方法: 。
(1)在发生离子反应的反应物或生成物中,一定存在的是 (填字母)。
A.小于1nm B.大于100nm C.介于1~100nm之间
(5)写出BaCl和NaCO 在水溶液中反应的离子方程式: 。 A.单质 B.氧化物
2 2 3
(6)Al与 HSO 的反应中, (填化学式)作还原剂,被还原的元素为 C.盐 D.化合物
2 4
(填元素名称)。
(2)某无色透明溶液A中可能含有Na+、NH+、Mg2+、Cu2+、SO2-、CO2-、HCO-离子中的若
4 4 3 3
17.(10分)为探究NaO 的强氧化性,某小组设计了如图所示的实验。
2 2 干种。取该溶液进行如下实验:
Ⅰ.取少量A溶液,向其中滴加足量 BaCl溶液,有白色沉淀产生,再往其中加足量稀
2
盐酸,发现沉淀部分溶解。
Ⅱ.取少量A溶液,向其中滴加足量NaOH溶液,并加热,发现有气体放出。
△
已知:NH++OH-NH↑+HO
4 3 2
高一化学试卷(二) 第5页 (共8页) 高一化学试卷(二) 第6页 (共8页)根据上述信息,回答下列问题: (6)某酸性反应体系中发生的一个氧化还原的离子反应,反应物和生成物共六种微粒:
①不做任何实验就可以肯定A溶液中不存在的离子是 。 Fe3+、Mn2+、MnO-、HO、Fe2+、H+,则写出反应的离子方程式并用双线桥法表示出电
4 2
②通过实验Ⅰ可以确定存在的离子是: ,不存在的离子是 。 子转移的方向和数目 。
③实验Ⅰ不能确定某阴离子是否存在,为此,补做实验Ⅲ:取少量无色溶液 A,向其中 Ⅲ.已知下列四种氧化剂(氧化KI后)对应的还原产物情况如表。
滴加足量BaCl溶液,静置,取上层清液,再滴加 溶液,产生白色沉淀,
2 氧化剂 KMnO KIO HO HNO
4 3 2 2 3
从而确定溶液A中存在阴离子: 。 还原产物 Mn2+ I HO NO
2 2
④实验Ⅰ、Ⅱ不能确定是否存在的阳离子,可以通过 来
(7)个数相等的四种氧化剂分别与足量KI作用,得到I最多的是 。
2
确定它是否存在。
(8)根据信息“氧化性:Cl>Br>HNO >I”思考:对于含 I-、Br-的混合溶液,若控制氧
2 2 3 2
⑤往无色溶液A中加入一定量的NaO,离子数目减少的是 。
2 2 化I-而不氧化Br-,请提出两种合理的氧化方案:①加入 ;
19.(15分)Ⅰ.氧化还原反应在工农业生产和日常生活中有广泛的应用,回答下列问题:
②加入 。
(1)罐头厂在装食品罐头时,通常要添加一些对人体无害的防腐剂。防止食物被空气中的
氧气氧化而变质,此类食物防腐剂应具有 (填“氧化性”或“还原性”)。
(2)氯气是一种重要的工业原料,且 HCl遇 NH 会产生 NHCl,NHCl为白色固体。工业
3 4 4
上利用反应3Cl+2NH N +6HCl检查氯气管道是否漏气。下列说法错误的是
2 3 2
。(填字母)
A.若管道漏气遇NH 就会产生白烟
3
B.该反应利用了Cl的强氧化性
2
C.该反应属于复分解反应
D.生成1个N 有6个电子转移
2
Ⅱ.按要求填写相关量。
(3)2NaO +2HO4NaOH+O↑反应中,每生成1个O 分子转移 个电子。
2 2 2 2 2
△
(4)2NaHCO NaCO +HO+CO↑反应中,每消耗168gNaHCO,生成 g
3 2 3 2 2 3
CO。
2
(5)Cl+HOHCl+HClO反应中,每消耗10个Cl分子,转移 个电子。
2 2 2
高一化学试卷(二) 第7页 (共8页) 高一化学试卷(二) 第8页 (共8页)