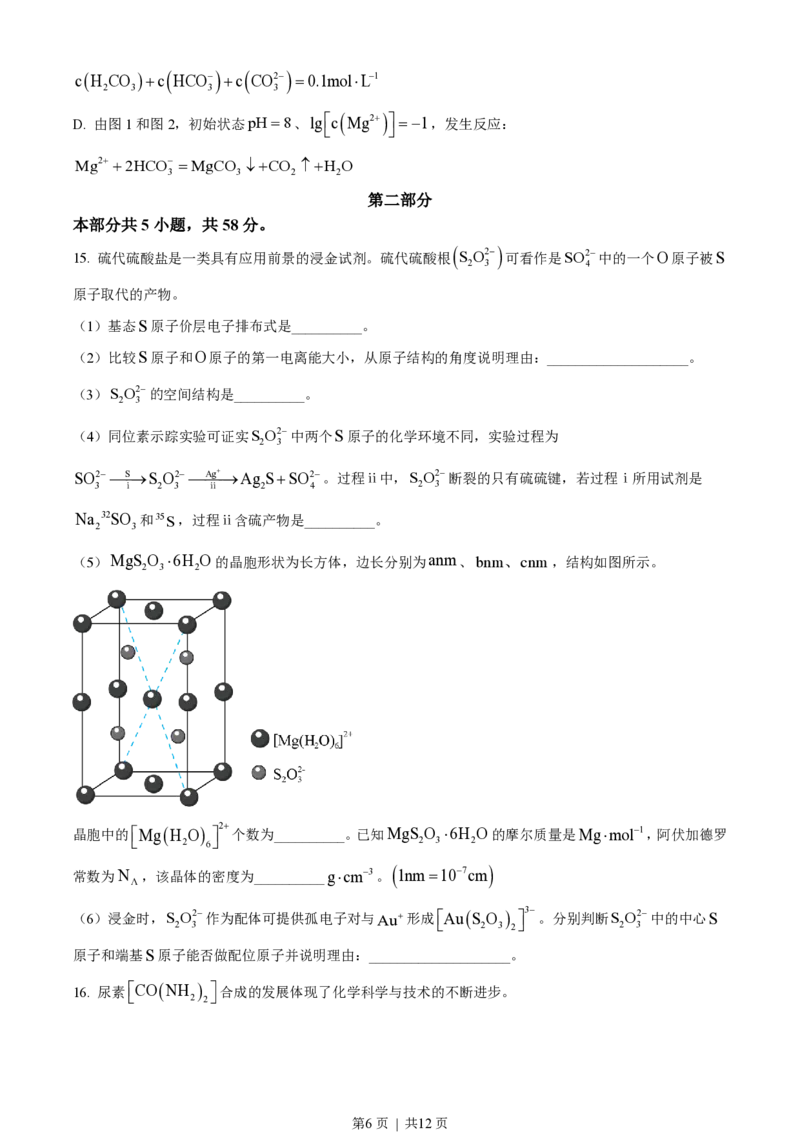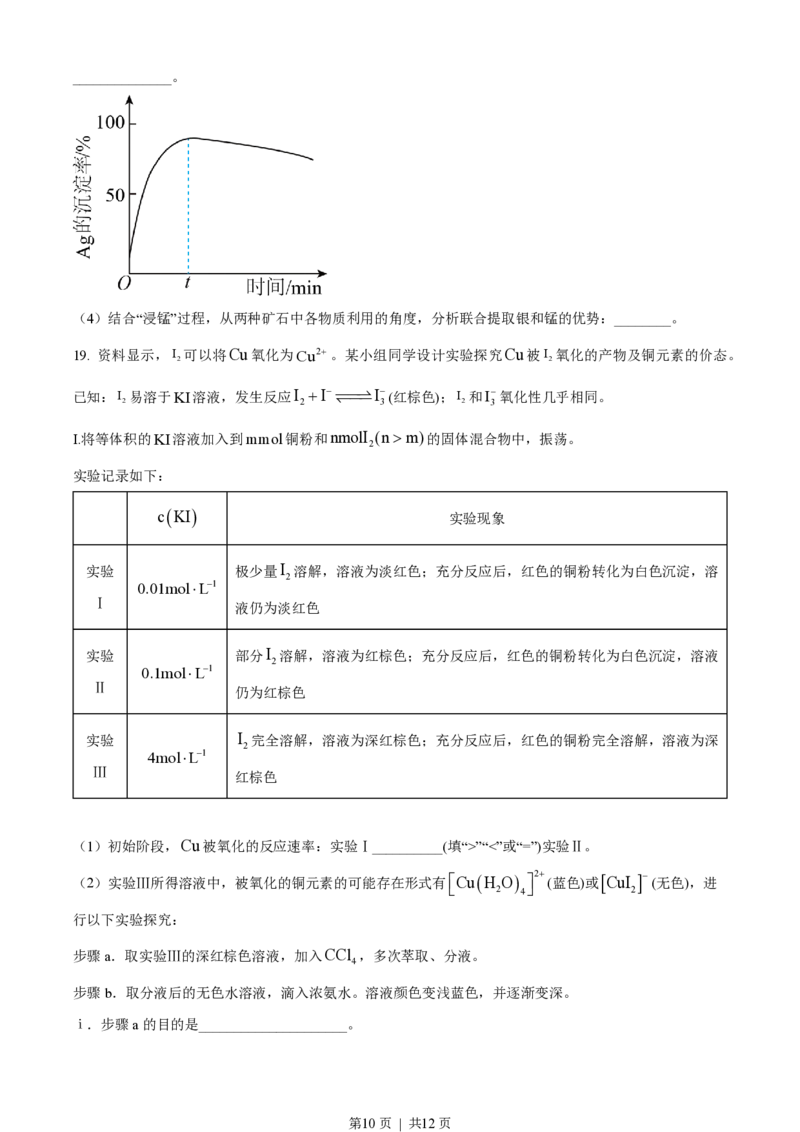文档内容
2023 年普通高中学业水平等级性考试
(北京卷)
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 S-32
第一部分
本部分共 14 小题,每题 3 分,共 42 分。在每题列出的四个选项中,选出最符合题目要求的
一项。
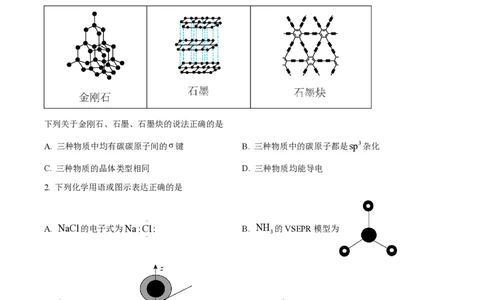
1. 中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是
A. 三种物质中均有碳碳原子间的σ键 B. 三种物质中的碳原子都是sp3杂化
C. 三种物质的晶体类型相同 D. 三种物质均能导电
2. 下列化学用语或图示表达正确的是
··
A. NaCl的电子式为Na:Cl: B. NH 的VSEPR模型为
3
··
C. 2p 电子云图为 D. 基态 Cr原子的价层电子轨道表示式为
z 24
3. 下列过程与水解反应无关的是
A. 热的纯碱溶液去除油脂
第1页 | 共12页B. 重油在高温、高压和催化剂作用下转化为小分子烃
C. 蛋白质在酶的作用下转化为氨基酸
D. 向沸水中滴入饱和FeCl 溶液制备Fe(OH) 胶体
3 3
4. 下列事实能用平衡移动原理解释的是
A. H O 溶液中加入少量MnO 固体,促进H O 分解
2 2 2 2 2
B. 密闭烧瓶内的NO 和N O 的混合气体,受热后颜色加深
2 2 4
C. 铁钉放入浓HNO 中,待不再变化后,加热能产生大量红棕色气体
3
D. 锌片与稀H SO 反应过程中,加入少量CuSO 固体,促进H 的产生
2 4 4 2
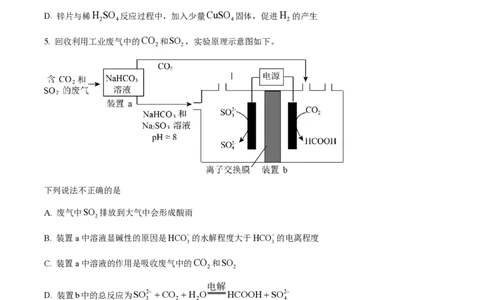
5. 回收利用工业废气中的CO 和SO ,实验原理示意图如下。
2 2
下列说法不正确的是
A. 废气中SO 排放到大气中会形成酸雨
2
B. 装置a中溶液显碱性的原因是HCO-的水解程度大于HCO-的电离程度
3 3
C. 装置a中溶液的作用是吸收废气中的CO 和SO
2 2
电解
D. 装置b中的总反应为SO2- +CO +H O HCOOH+SO2-
3 2 2 4
6. 下列离子方程式与所给事实不相符的是
A. Cl 制备84消毒液(主要成分是NaClO):Cl +2OH- =Cl- +ClO- +H O
2 2 2
B. 食醋去除水垢中的CaCO :CaCO +2H+ =Ca2+ +H O+CO
3 3 2 2
C. 利用覆铜板制作印刷电路板:2Fe3+ +Cu =2Fe2+ +Cu2+
D. Na S去除废水中的Hg2+:Hg2+ +S2- =HgS¯
2
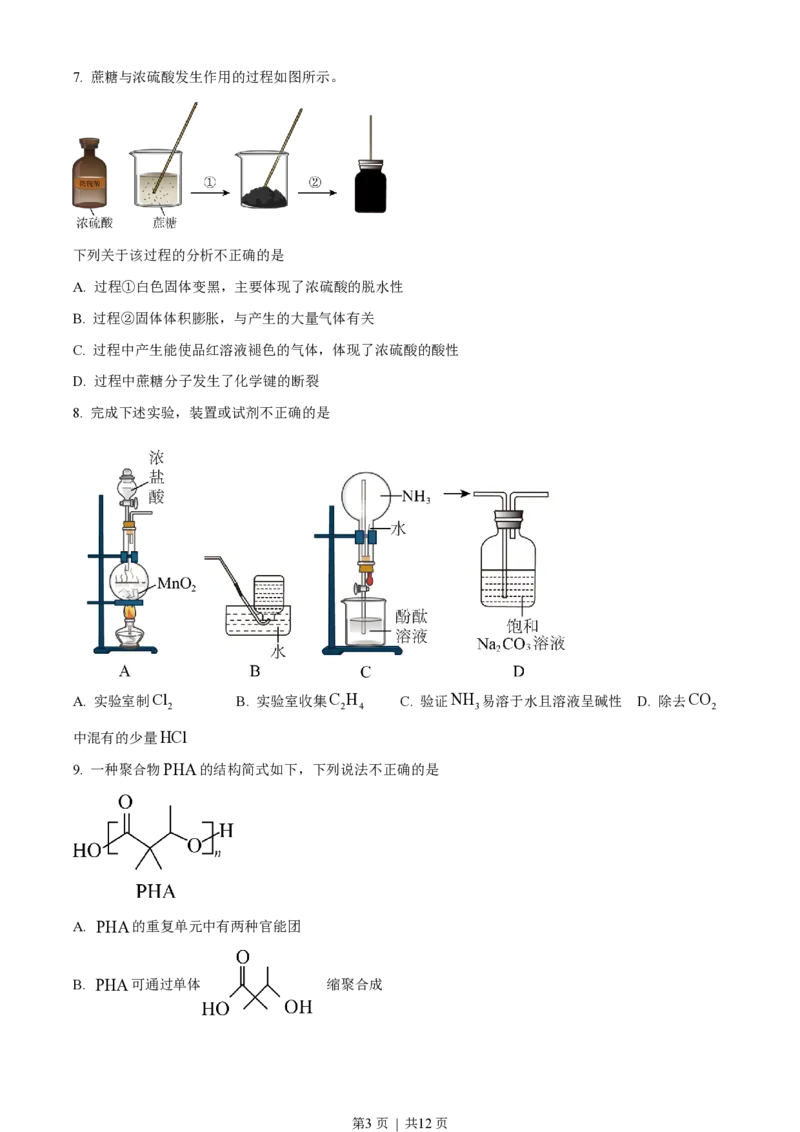
第2页 | 共12页7. 蔗糖与浓硫酸发生作用的过程如图所示。
下列关于该过程的分析不正确的是
A. 过程①白色固体变黑,主要体现了浓硫酸的脱水性
B. 过程②固体体积膨胀,与产生的大量气体有关
C. 过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D. 过程中蔗糖分子发生了化学键的断裂
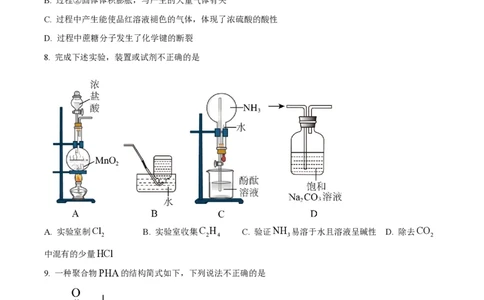
8. 完成下述实验,装置或试剂不正确的是
A. 实验室制Cl B. 实验室收集C H C. 验证NH 易溶于水且溶液呈碱性 D. 除去CO
2 2 4 3 2
中混有的少量HCl
9. 一种聚合物PHA的结构简式如下,下列说法不正确的是
A. PHA的重复单元中有两种官能团
B. PHA可通过单体 缩聚合成
第3页 | 共12页C. PHA在碱性条件下可发生降解
D. PHA中存在手性碳原子
10. 下列事实不能通过比较氟元素和氯元素的电负性进行解释的是
A. F-F键的键能小于Cl-Cl键的键能
B. 三氟乙酸的K 大于三氯乙酸的K
a a
C. 氟化氢分子的极性强于氯化氢分子的极性
D. 气态氟化氢中存在(HF) ,而气态氯化氢中是HCl分子
2
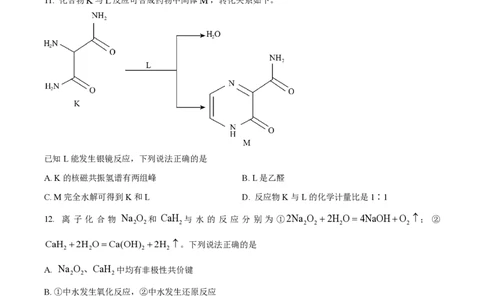
11. 化合物K与L反应可合成药物中间体M,转化关系如下。
已知L能发生银镜反应,下列说法正确的是
A. K的核磁共振氢谱有两组峰 B. L是乙醛
C. M完全水解可得到K和L D. 反应物K与L的化学计量比是1∶1
12. 离 子 化 合 物 Na O 和 CaH 与 水 的 反 应 分 别 为 ①2Na O +2H O=4NaOH+O ; ②
2 2 2 2 2 2 2
CaH +2H O=Ca(OH) +2H 。下列说法正确的是
2 2 2 2
A. Na O 、CaH 中均有非极性共价键
2 2 2
B. ①中水发生氧化反应,②中水发生还原反应
C. Na O 中阴、阳离子个数比为1:2,CaH 中阴、阳离子个数比为2:1
2 2 2
D. 当反应①和②中转移的电子数相同时,产生的O 和H 的物质的量相同
2 2
13.
一种分解氯化铵实现产物分离的物质转化关系如下,其中b、d代表MgO或MgOHCl中的一种。
下列说法正确的是
第4页 | 共12页A. a、c分别是HCl、NH
3
B.
d既可以是MgO,也可以是MgOHCl
C. 已知MgCl 为副产物,则通入水蒸气可减少MgCl 的产生
2 2
D. 等压条件下,反应①、②的反应热之和,小于氯化铵直接分解的反应热
14. 利用平衡移动原理,分析一定温度下Mg2+在不同pH的Na CO 体系中的可能产物。
2 3
已知:i.图1中曲线表示Na CO 体系中各含碳粒子的物质的量分数与pH的关系。
2 3
ii.2 中曲线Ⅰ的离子浓度关系符合c Mg2+ ×c2 OH- =K Mg(OH) ;曲线Ⅱ的离子浓度关系符合
sp 2
c Mg2+ ×c CO2- = K MgCO [注:起始cNa CO =0.1mol×L-1,不同pH下c CO2- 由图1得
3 sp 3 2 3 3
到]。
下列说法不正确的是
A. 由图1,pH =10.25,c
HCO-
=c
CO2-
3 3
B. 由图2,初始状态pH =11、lgéc Mg2+ù = -6,无沉淀生成
ë û
C. 由图2,初始状态pH =9、lgéc Mg2+ù = -2,平衡后溶液中存在
ë û
第5页 | 共12页cH CO +c HCO- +c CO2- =0.1mol×L-1
2 3 3 3
D. 由图1和图2,初始状态pH=8、lgéc Mg2+ù =-1,发生反应:
ë û
Mg2+ +2HCO- =MgCO ¯+CO +H O
3 3 2 2
第二部分
本部分共 5小题,共 58分。
15. 硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根
S
O2-
可看作是SO2-中的一个O原子被S
2 3 4
原子取代的产物。
(1)基态S原子价层电子排布式是__________。
(2)比较S原子和O原子的第一电离能大小,从原子结构的角度说明理由:____________________。
(3)S O2- 的空间结构是__________。
2 3
(4)同位素示踪实验可证实S O2-中两个S原子的化学环境不同,实验过程为
2 3
SO2- ¾S¾®S O2- ¾A¾g+ ¾®Ag S+SO2-。过程ⅱ中,S O2-断裂的只有硫硫键,若过程ⅰ所用试剂是
3 ⅰ 2 3 ⅱ 2 4 2 3
Na 32SO 和35S,过程ⅱ含硫产物是__________。
2 3
(5)MgS O ×6H O的晶胞形状为长方体,边长分别为anm、bnm、cnm,结构如图所示。
2 3 2
晶胞中的éMgH O ù 2+ 个数为__________。已知MgS O ×6H O的摩尔质量是Mg×mol-1,阿伏加德罗
ë 2 6 û 2 3 2
常数为N ,该晶体的密度为__________g×cm-3。 1nm=10-7cm
Λ
(6)浸金时,S O2-作为配体可提供孤电子对与Au+形成éAuS O ù 3- 。分别判断S O2-中的中心S
2 3 ë 2 3 2 û 2 3
原子和端基S原子能否做配位原子并说明理由:____________________。
16. 尿素é ë CONH 2 2 ù û 合成的发展体现了化学科学与技术的不断进步。
第6页 | 共12页(1)十九世纪初,用氰酸银 AgOCN 与NH Cl在一定条件下反应制得CONH ,实现了由无机物
4 2 2
到有机物的合成。该反应的化学方程式是____________________。
(2)二十世纪初,工业上以CO 和NH 为原料在一定温度和压强下合成尿素。反应分两步:
2 3
ⅰ.CO 和NH 生成NH COONH ;
2 3 2 4
ⅱ.NH COONH 分解生成尿素。
2 4
结合反应过程中能量变化示意图,下列说法正确的是__________(填序号)。
a.活化能:反应ⅰ<反应ⅱ
b.ⅰ为放热反应,ⅱ为吸热反应
c.CO l+2NH l=CONH l+H OlΔH=E -E
2 3 2 2 2 1 4
(3)近年研究发现,电催化CO 和含氮物质(NO-等)在常温常压下合成尿素,有助于实现碳中和及解决
2 3
含氮废水污染问题。向一定浓度的KNO 溶液通CO 至饱和,在电极上反应生成CONH ,电解原理
3 2 2 2
如图所示。
①电极b是电解池的__________极。
②电解过程中生成尿素的电极反应式是_____________。
(4)尿素样品含氮量的测定方法如下。
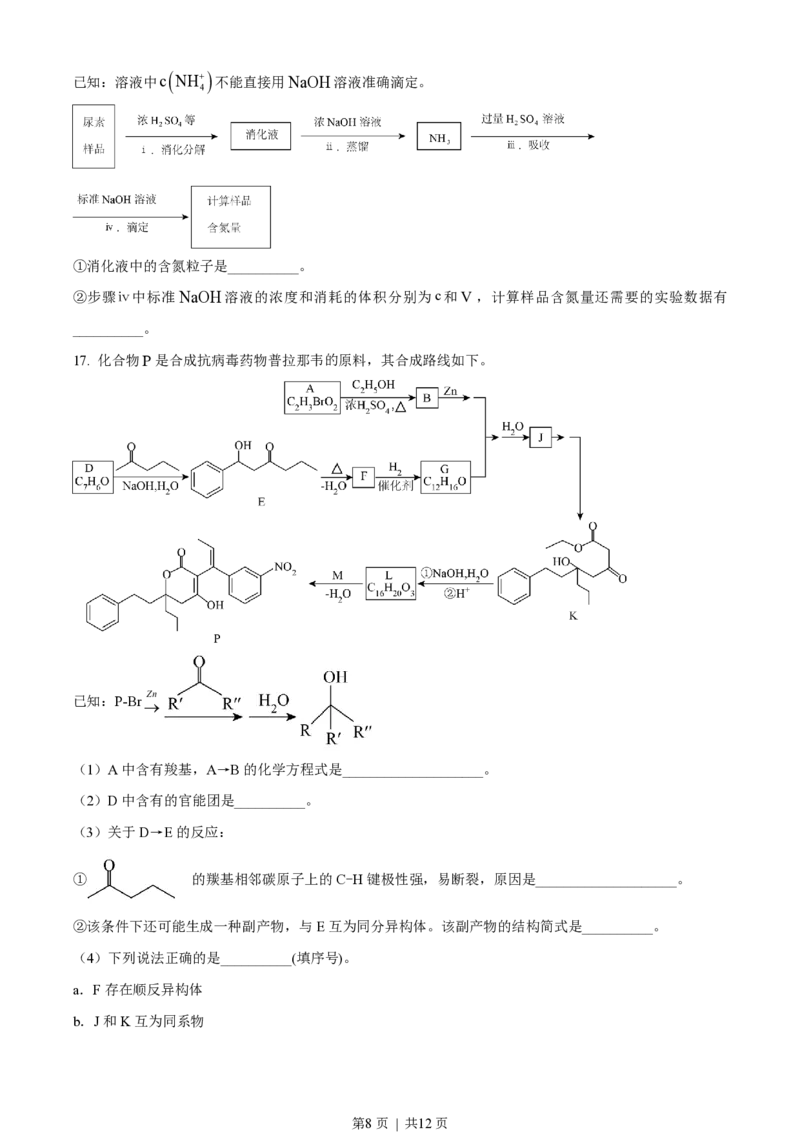
第7页 | 共12页已知:溶液中c
NH+
不能直接用NaOH溶液准确滴定。
4
①消化液中的含氮粒子是__________。
②步骤ⅳ中标准NaOH溶液的浓度和消耗的体积分别为c和V ,计算样品含氮量还需要的实验数据有
__________。
17. 化合物P是合成抗病毒药物普拉那韦的原料,其合成路线如下。
Zn
已知:P-Br
®
(1)A中含有羧基,A→B的化学方程式是____________________。
(2)D中含有的官能团是__________。
(3)关于D→E的反应:
① 的羰基相邻碳原子上的C-H键极性强,易断裂,原因是____________________。
②该条件下还可能生成一种副产物,与E互为同分异构体。该副产物的结构简式是__________。
(4)下列说法正确的是__________(填序号)。
a.F存在顺反异构体
b.J和K互为同系物
第8页 | 共12页c.在加热和Cu催化条件下,J不能被O 氧化
2
(5)L分子中含有两个六元环。L的结构简式是__________。
(6)已知: ,依据D®E的原理,L和M反应得到了
P。M的结构简式是__________。
18. 以银锰精矿(主要含Ag S、MnS、FeS )和氧化锰矿(主要含MnO )为原料联合提取银和锰的一种流
2 2 2
程示意图如下。
已知:酸性条件下,MnO 的氧化性强于Fe3+。
2
(1) “浸锰”过程是在H SO 溶液中使矿石中的锰元素浸出,同时去除FeS ,有利于后续银的浸出:矿
2 4 2
石中的银以Ag S的形式残留于浸锰渣中。
2
①“浸锰”过程中,发生反应MnS+2H+ =Mn2+ +H S,则可推断:K MnS __________(填“>”或“<”)
2 sp
K Ag S 。
sp 2
②在H SO 溶液中,银锰精矿中的FeS 和氧化锰矿中的MnO 发生反应,则浸锰液中主要的金属阳离子
2 4 2 2
有__________。
(2) “浸银”时,使用过量FeCl、HCl和CaCl 的混合液作为浸出剂,将Ag S中的银以AgCl - 形式
3 2 2 2
浸出。
①将“浸银”反应的离子方程式补充完整:__________。
□Fe3+ +Ag S+□_____ˆˆ† □_____+2AgCl - +S
2 ‡ˆˆ 2
②结合平衡移动原理,解释浸出剂中Cl-、H+的作用:____________________。
(3) “沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有______________________________。
②一定温度下,Ag的沉淀率随反应时间的变化如图所示。解释t分钟后Ag的沉淀率逐渐减小的原因:
第9页 | 共12页______________。
(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势:________。
19. 资料显示,I 可以将Cu氧化为Cu2+。某小组同学设计实验探究Cu被I 氧化的产物及铜元素的价态。
2 2
已知:I 易溶于KI溶液,发生反应I +I- ˆˆ†I- (红棕色);I 和I-氧化性几乎相同。
2 2 ‡ˆˆ 3 2 3
I.将等体积的KI溶液加入到mmol铜粉和nmolI (n>m)的固体混合物中,振荡。
2
实验记录如下:
cKI
实验现象
实验 极少量I 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶
2
0.01mol×L-1
Ⅰ
液仍为淡红色
实验 部分I 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液
2
0.1mol×L-1
Ⅱ
仍为红棕色
实验 I 完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深
2
4mol×L-1
Ⅲ
红棕色
(1)初始阶段,Cu被氧化的反应速率:实验Ⅰ__________(填“>”“<”或“=”)实验Ⅱ。
(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有éCuH O ù 2+ (蓝色)或CuI - (无色),进
ë 2 4 û 2
行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入CCl ,多次萃取、分液。
4
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
ⅰ.步骤a的目的是_____________________。
第10页 | 共12页ⅱ.查阅资料,2Cu2+ +4I- =2CuI¯+I ,éCuNH ù + (无色)容易被空气氧化。用离子方程式解释步
2 ë 3 2 û
骤b的溶液中发生的变化:______________。
(3)结合实验Ⅲ,推测实验Ⅰ和Ⅱ中的白色沉淀可能是CuI,实验Ⅰ中铜被氧化的化学方程式是
____________________。分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入浓KI溶液,
__________(填实验现象),观察到少量红色的铜。分析铜未完全反应的原因是____________________。
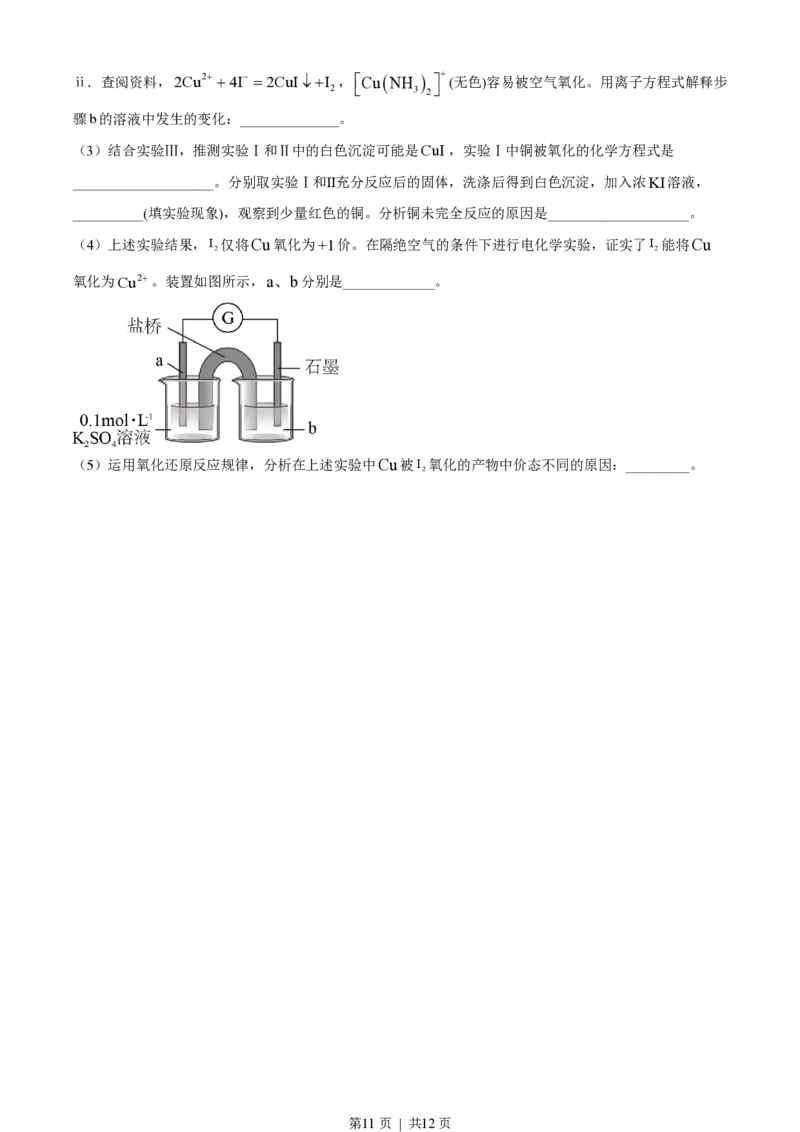
(4)上述实验结果,I 仅将Cu氧化为+1价。在隔绝空气的条件下进行电化学实验,证实了I 能将Cu
2 2
氧化为Cu2+。装置如图所示,a、b分别是_____________。
(5)运用氧化还原反应规律,分析在上述实验中Cu被I 氧化的产物中价态不同的原因:_________。
2
第11页 | 共12页第12页 | 共12页