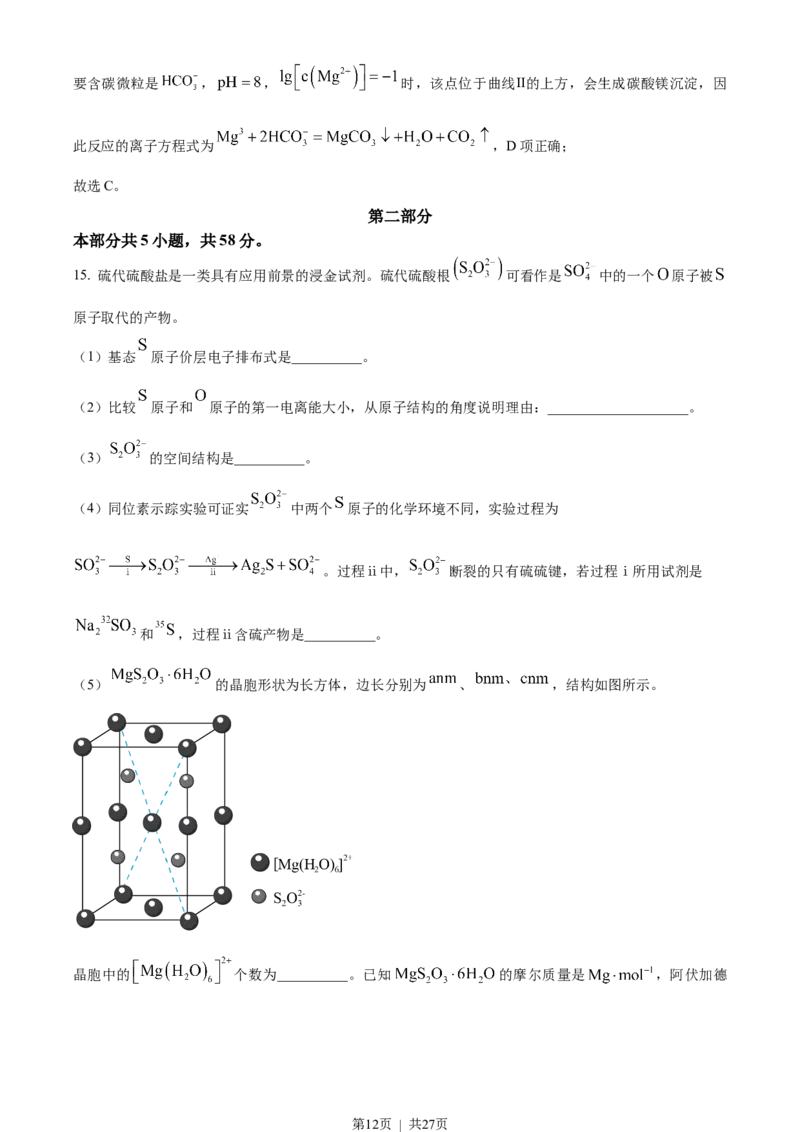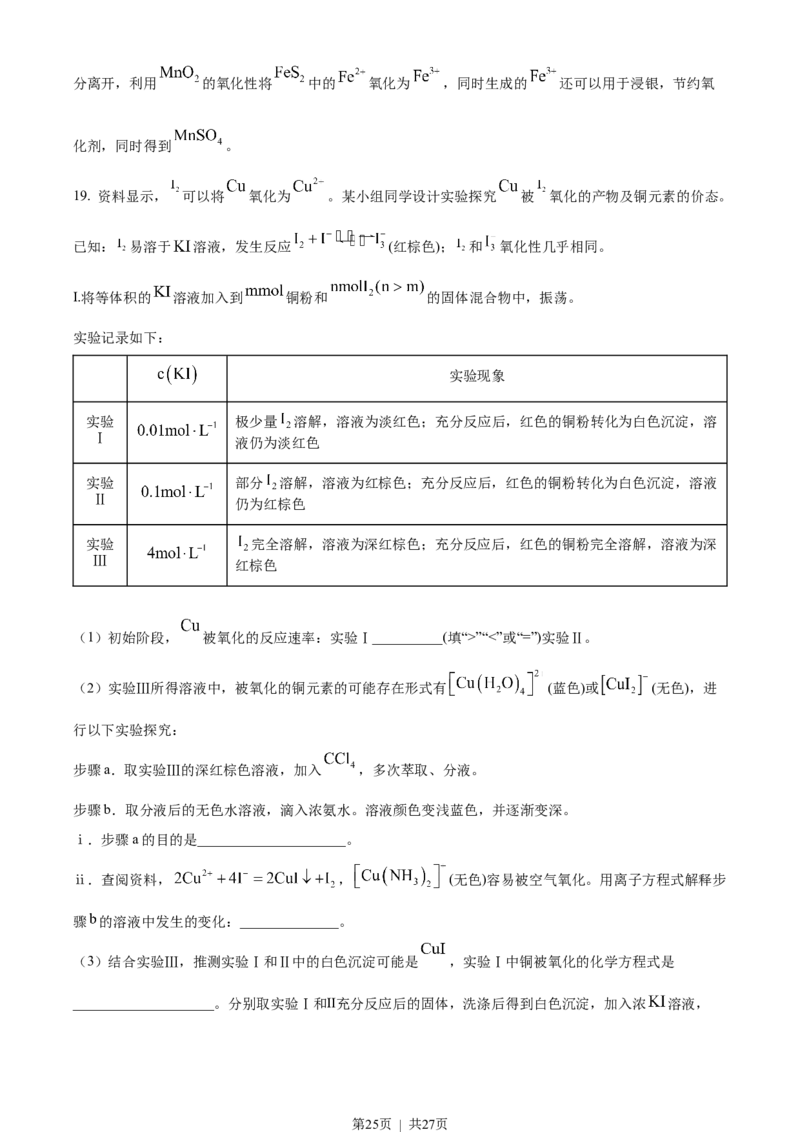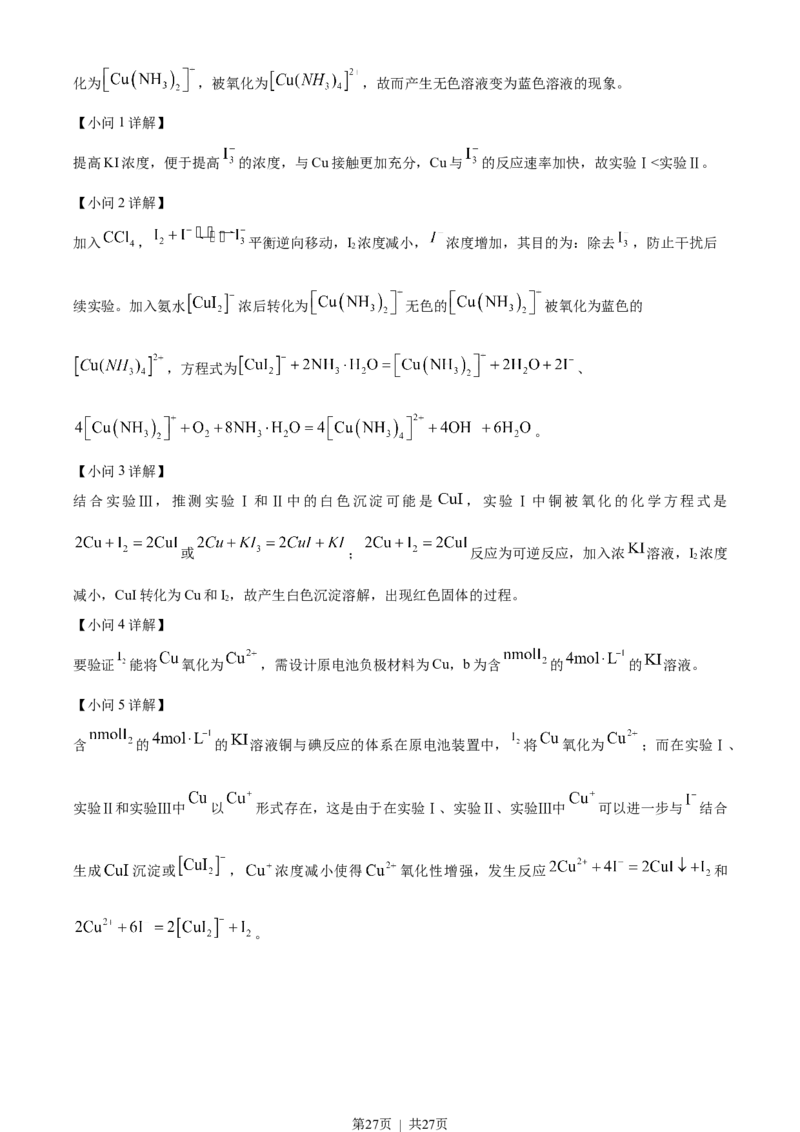文档内容
2023 年普通高中学业水平等级性考试
(北京卷)
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Mg-24 S-32
第一部分
本部分共14小题,每题3分,共42分。在每题列出的四个选项中,选出最符合题目要求的
一项。
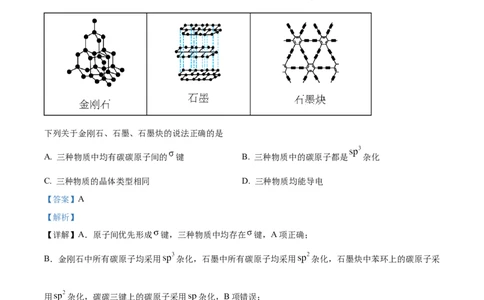
1. 中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是
A. 三种物质中均有碳碳原子间的 键 B. 三种物质中的碳原子都是 杂化
C. 三种物质的晶体类型相同 D. 三种物质均能导电
【答案】A
【解析】
【详解】A.原子间优先形成 键,三种物质中均存在 键,A项正确;
B.金刚石中所有碳原子均采用 杂化,石墨中所有碳原子均采用 杂化,石墨炔中苯环上的碳原子采
用 杂化,碳碳三键上的碳原子采用 杂化,B项错误;
C.金刚石为共价晶体,石墨炔为分子晶体,石墨为混合晶体,C项错误;
D.金刚石中没有自由移动电子,不能导电,D项错误;
故选A。
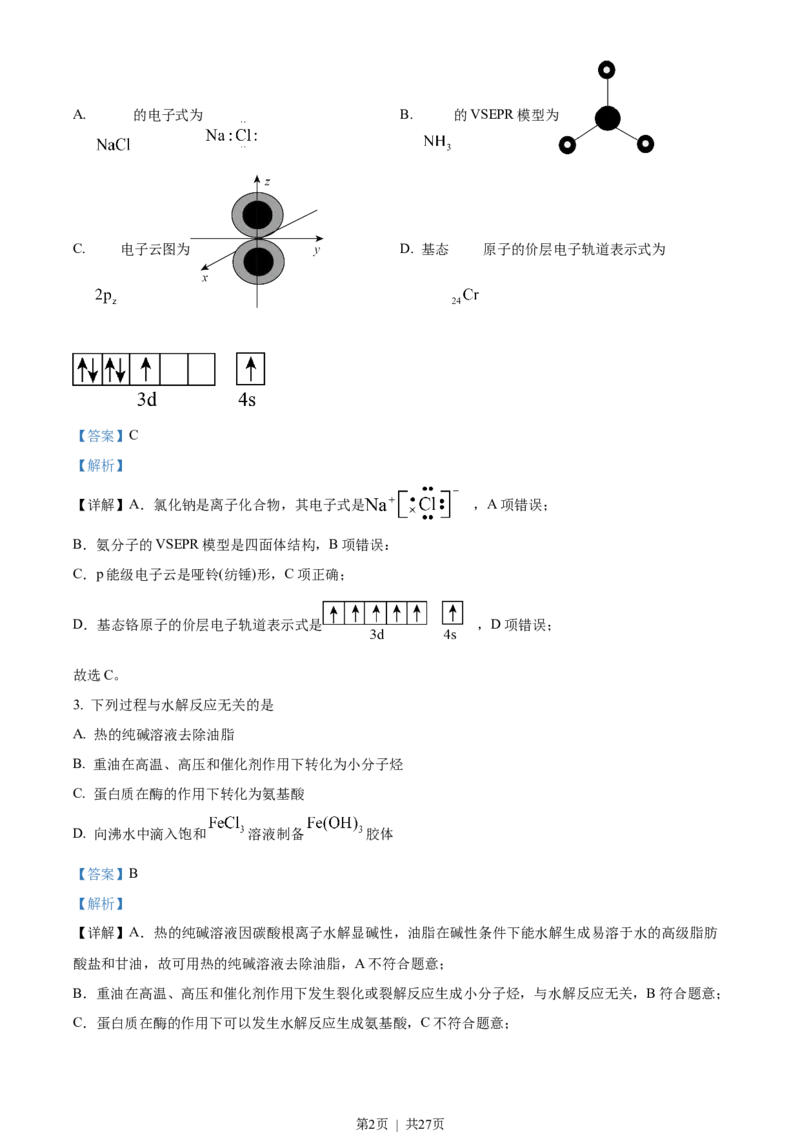
2. 下列化学用语或图示表达正确的是
第1页 | 共27页A. 的电子式为 B. 的VSEPR模型为
C. 电子云图为 D. 基态 原子的价层电子轨道表示式为
【答案】C
【解析】
【详解】A.氯化钠是离子化合物,其电子式是 ,A项错误;
B.氨分子的VSEPR模型是四面体结构,B项错误:
C.p能级电子云是哑铃(纺锤)形,C项正确;
D.基态铬原子的价层电子轨道表示式是 ,D项错误;
故选C。
3. 下列过程与水解反应无关的是
A. 热的纯碱溶液去除油脂
B. 重油在高温、高压和催化剂作用下转化为小分子烃
C. 蛋白质在酶的作用下转化为氨基酸
D. 向沸水中滴入饱和 溶液制备 胶体
【答案】B
【解析】
【详解】A.热的纯碱溶液因碳酸根离子水解显碱性,油脂在碱性条件下能水解生成易溶于水的高级脂肪
酸盐和甘油,故可用热的纯碱溶液去除油脂,A不符合题意;
B.重油在高温、高压和催化剂作用下发生裂化或裂解反应生成小分子烃,与水解反应无关,B符合题意;
C.蛋白质在酶的作用下可以发生水解反应生成氨基酸,C不符合题意;
第2页 | 共27页D. Fe3+能发生水解反应生成 Fe(OH) ,加热能增大Fe3+ 的水解程度,D不符合题意;
3
故选B。
4. 下列事实能用平衡移动原理解释的是
A. 溶液中加入少量 固体,促进 分解
的
B. 密闭烧瓶内 和 的混合气体,受热后颜色加深
C. 铁钉放入浓 中,待不再变化后,加热能产生大量红棕色气体
D. 锌片与稀 反应过程中,加入少量 固体,促进 的产生
【答案】B
【解析】
【详解】A.MnO 会催化 HO 分解,与平衡移动无关,A项错误;
2 2 2
B.NO 转化为NO 的反应是放热反应,升温平衡逆向移动, NO 浓度增大,混合气体颜色加深,B项正
2 2 4 2
确;
C.铁在浓硝酸中钝化,加热会使表面的氧化膜溶解,铁与浓硝酸反应生成大量红棕色气体,与平衡移动
无关,C项错误;
D.加入硫酸铜以后,锌置换出铜,构成原电池,从而使反应速率加快,与平衡移动无关,D项错误;
故选B。
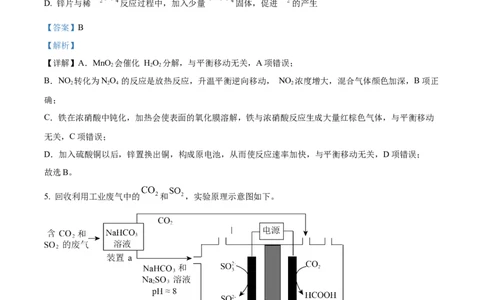
5. 回收利用工业废气中的 和 ,实验原理示意图如下。
下列说法不正确的是
A. 废气中 排放到大气中会形成酸雨
B. 装置a中溶液显碱性的原因是 的水解程度大于 的电离程度
第3页 | 共27页C. 装置a中溶液的作用是吸收废气中的 和
D. 装置 中的总反应为
【答案】C
【解析】
【详解】A. 是酸性氧化物,废气中 排放到空气中会形成硫酸型酸雨,故A正确;
B.装置a中溶液的溶质为 ,溶液显碱性,说明 的水解程度大于电离程度,故B正确;
C.装置a中 溶液的作用是吸收 气体, 与 溶液不反应,不能吸收 ,故C
错误;
D.由电解池阴极和阳极反应式可知,装置b中总反应为 ,故D
正确;
选C。
6. 下列离子方程式与所给事实不相符的是
A. 制备84消毒液(主要成分是 ):
B. 食醋去除水垢中的 :
C. 利用覆铜板制作印刷电路板:
D. 去除废水中的 :
【答案】B
【解析】
【详解】A.Cl 和NaOH溶液反应产生NaCl、NaClO、HO,除了Cl 和HO不能拆写其余均可拆写为离
2 2 2 2
子,A项正确;
B.食醋为弱酸不能拆写为离子,反应为2CHCOOH+CaCO =Ca2++2CH COO-+CO +H O,B项错误;
3 3 3 2 2
C.FeCl 将Cu氧化为CuCl 而自身被还原为FeCl ,反应为2Fe3++Cu=2Fe2++Cu2+,C项正确;
3 2 2
D.NaS将Hg2+转化为沉淀除去,反应为Hg2++S2−=HgS↓,D项正确;
2
故选B。
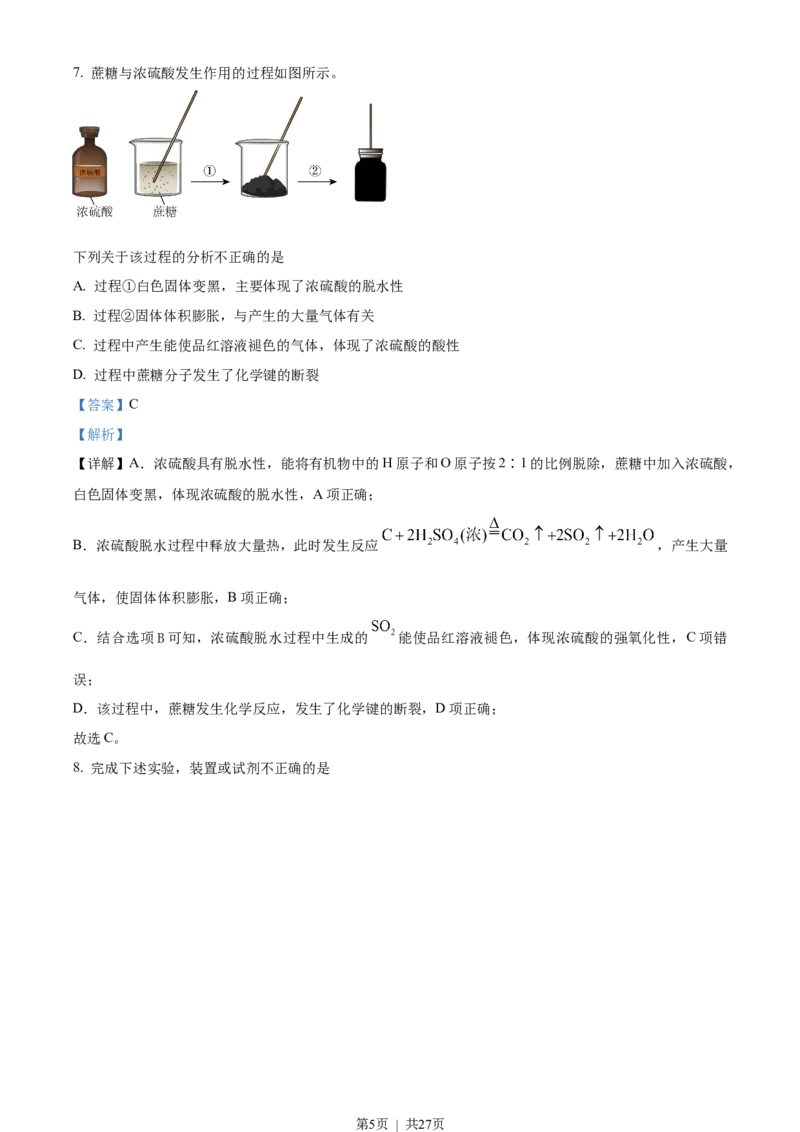
第4页 | 共27页7. 蔗糖与浓硫酸发生作用的过程如图所示。
下列关于该过程的分析不正确的是
A. 过程①白色固体变黑,主要体现了浓硫酸的脱水性
B. 过程②固体体积膨胀,与产生的大量气体有关
C. 过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D. 过程中蔗糖分子发生了化学键的断裂
【答案】C
【解析】
【详解】A.浓硫酸具有脱水性,能将有机物中的H原子和O原子按2∶1的比例脱除,蔗糖中加入浓硫酸,
白色固体变黑,体现浓硫酸的脱水性,A项正确;
B.浓硫酸脱水过程中释放大量热,此时发生反应 ,产生大量
气体,使固体体积膨胀,B项正确;
C.结合选项B可知,浓硫酸脱水过程中生成的 能使品红溶液褪色,体现浓硫酸的强氧化性,C项错
误;
D.该过程中,蔗糖发生化学反应,发生了化学键的断裂,D项正确;
故选C。
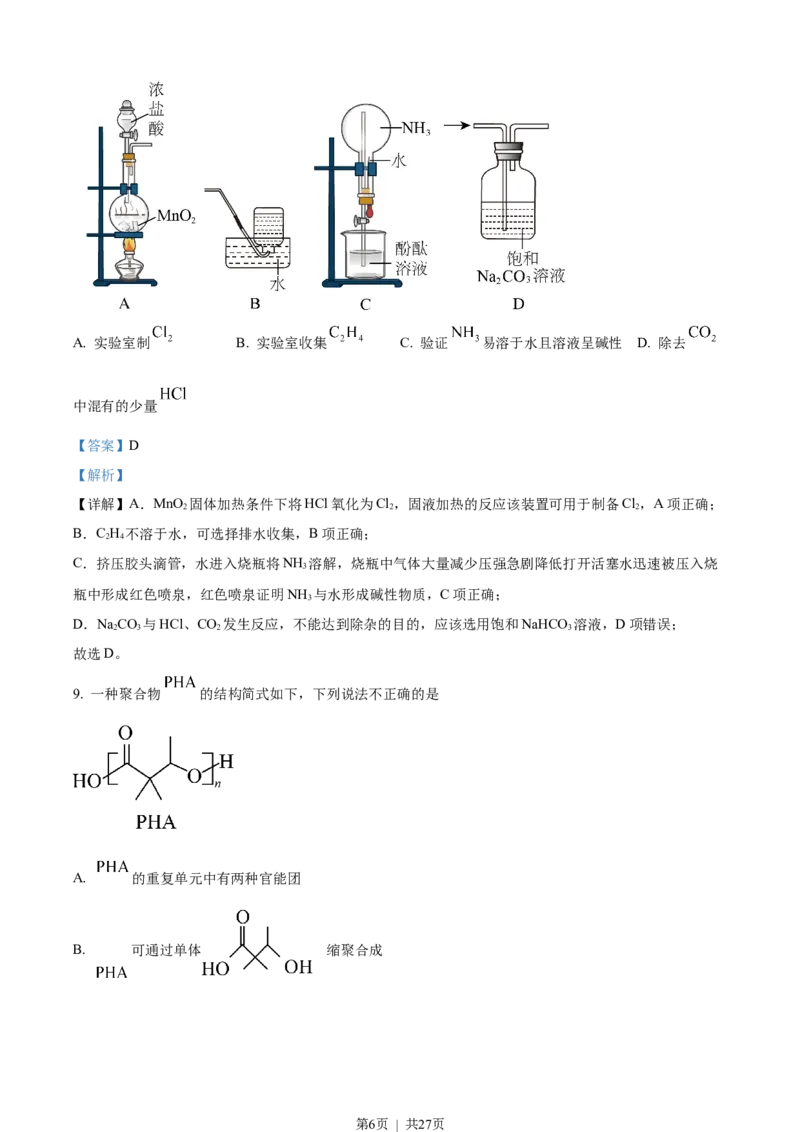
8. 完成下述实验,装置或试剂不正确的是
第5页 | 共27页A. 实验室制 B. 实验室收集 C. 验证 易溶于水且溶液呈碱性 D. 除去
中混有的少量
【答案】D
【解析】
【详解】A.MnO 固体加热条件下将HCl氧化为Cl,固液加热的反应该装置可用于制备Cl,A项正确;
2 2 2
B.C H 不溶于水,可选择排水收集,B项正确;
2 4
C.挤压胶头滴管,水进入烧瓶将NH 溶解,烧瓶中气体大量减少压强急剧降低打开活塞水迅速被压入烧
3
瓶中形成红色喷泉,红色喷泉证明NH 与水形成碱性物质,C项正确;
3
D.NaCO 与HCl、CO 发生反应,不能达到除杂的目的,应该选用饱和NaHCO 溶液,D项错误;
2 3 2 3
故选D。
9. 一种聚合物 的结构简式如下,下列说法不正确的是
A. 的重复单元中有两种官能团
B. 可通过单体 缩聚合成
第6页 | 共27页C. 在碱性条件下可发生降解
D. 中存在手性碳原子
【答案】A
【解析】
【详解】A. 的重复单元中只含有酯基一种官能团,A项错误;
B.由 的结构可知其为聚酯,由单体 缩聚合成,B项正确;
C. 为聚酯,碱性条件下可发生降解,C项正确;
的
D. 重复单元中只连有1个甲基的碳原子为手性碳原子,D项正确;
故选A。
10. 下列事实不能通过比较氟元素和氯元素的电负性进行解释的是
A. 键的键能小于 键的键能
B. 三氟乙酸的 大于三氯乙酸的
C. 氟化氢分子的极性强于氯化氢分子的极性
D. 气态氟化氢中存在 ,而气态氯化氢中是 分子
【答案】A
【解析】
【详解】A.F原子半径小,电子云密度大,两个原子间的斥力较强, 键不稳定,因此 键的键
能小于 键的键能,与电负性无关,A符合题意;
B.氟的电负性大于氯的电负性。 键的极性大于 键的极性,使 —的极性大于 —的极
性,导致三氟乙酸的羧基中的羟基极性更大,更容易电离出氢离子,酸性更强,B不符合题意;
C.氟的电负性大于氯的电负性, 键的极性大于 键的极性,导致 分子极性强于 ,C
不符合题意;
第7页 | 共27页D.氟的电负性大于氯的电负性,与氟原子相连的氢原子可以与另外的氟原子形成分子间氢键,因此气态
氟化氢中存在 ,D不符合题意;
故选A。
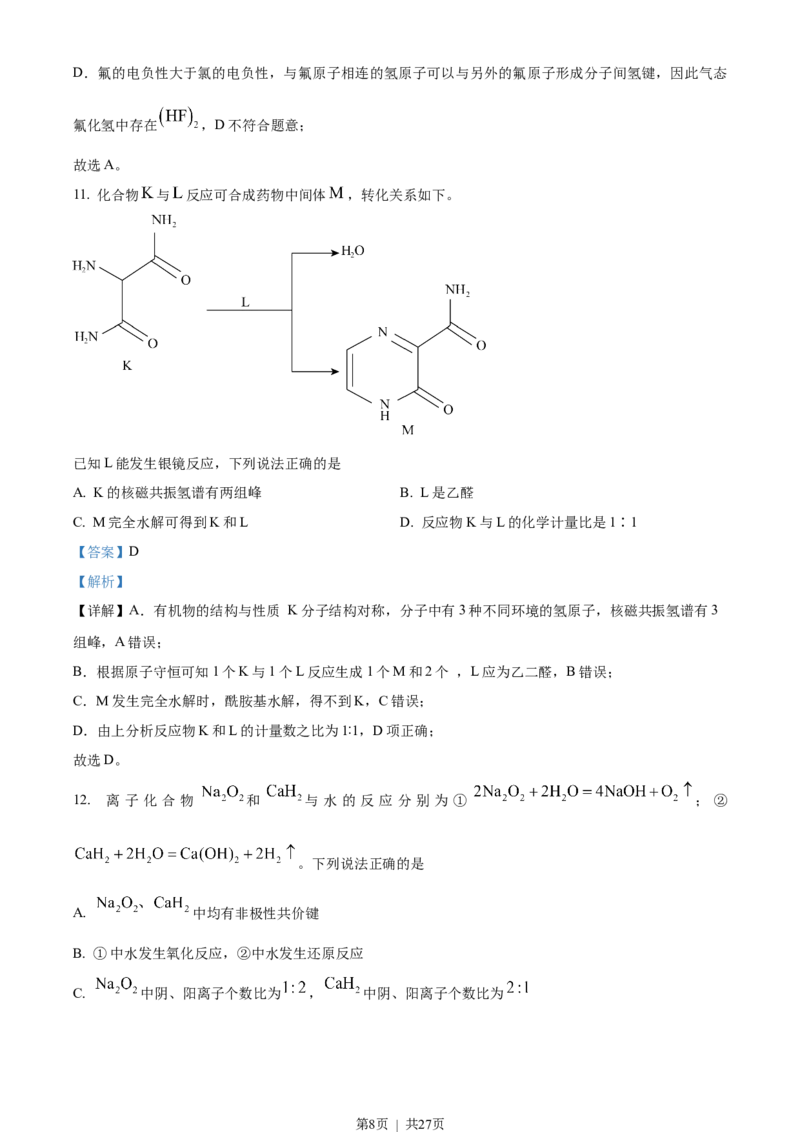
11. 化合物 与 反应可合成药物中间体 ,转化关系如下。
已知L能发生银镜反应,下列说法正确的是
A. K的核磁共振氢谱有两组峰 B. L是乙醛
C. M完全水解可得到K和L D. 反应物K与L的化学计量比是1∶1
【答案】D
【解析】
【详解】A.有机物的结构与性质 K分子结构对称,分子中有3种不同环境的氢原子,核磁共振氢谱有3
组峰,A错误;
B.根据原子守恒可知1个K与1个L反应生成1个M和2个 ,L应为乙二醛,B错误;
C.M发生完全水解时,酰胺基水解,得不到K,C错误;
D.由上分析反应物K和L的计量数之比为1∶1,D项正确;
故选D。
12. 离 子 化 合 物 和 与 水 的 反 应 分 别 为 ① ; ②
。下列说法正确的是
A. 中均有非极性共价键
B. ①中水发生氧化反应,②中水发生还原反应
C. 中阴、阳离子个数比为 , 中阴、阳离子个数比为
第8页 | 共27页D. 当反应①和②中转移的电子数相同时,产生的 和 的物质的量相同
【答案】C
【解析】
【详解】A.NaO 中有离子键和非极性键,CaH 中只有离子键面不含非极性键,A错误;
2 2 2
B.①中水的化合价不发生变化,不涉及氧化还原反应,②中水发生还原反应,B错误;
C.NaO 由Na+和 组成.阴、阳离子个数之比为1∶2,CaH 由Ca2+和H-组成,阴、阳离子个数之比为
2 2 2
2∶1,C正确;
D.①中每生成1个氧气分子转移2个电子,②中每生成1个氢气分子转移1个电子,转移电子数相同时,
生成氧气和氢气的物质的量之比为1∶2,D错误;
故选C。
13. 一种分解氯化铵实现产物分离的物质转化关系如下,其中 代表 或 中的一种。
下列说法正确的是
A. a、c分别是
B. 既可以是 ,也可以是
C. 已知 为副产物,则通入水蒸气可减少 的产生
D. 等压条件下,反应①、②的反应热之和,小于氯化铵直接分解的反应热
【答案】C
【解析】
【分析】 分解的产物是 和 ,分解得到的 与 反应生成 ,
又可以分解得到 和 ,则a为 ,b为 ,c为 ,d为 。
第9页 | 共27页【详解】A.由分析可知,a为 ,
c为 ,A项错误;
B.d为 ,B错误;
C.可以水解生成 ,通入水蒸气可以减少 的生成,C正确;
D.反应①和反应②相加即为氯化铵直接分解的反应,由盖斯定律可知,等压条件下,反应①、反应②的
反应热之和等于氯化铵直接分解的反应热,D错误;
故选C。
14. 利用平衡移动原理,分析一定温度下 在不同 的 体系中的可能产物。
已知:i.图1中曲线表示 体系中各含碳粒子的物质的量分数与 的关系。
ii.2中曲线Ⅰ的离子浓度关系符合 ;曲线Ⅱ的离子浓度关系符合
[注:起始 ,不同 下 由图 1
得到]。
第10页 | 共27页下列说法不正确的是
A. 由图1,
.
B 由图2,初始状态 ,无沉淀生成
C. 由图2,初始状态 ,平衡后溶液中存在
D. 由图1和图2,初始状态 、 ,发生反应:
【答案】C
【解析】
的
【详解】A.水溶液中 离子平衡 从图1可以看出 时,碳酸氢根离子与碳酸根离子浓度相同,
A项正确;
B.从图2可以看出 、 时,该点位于曲线Ⅰ和曲线Ⅱ的下方,不会产生碳酸镁沉
淀或氢氧化镁沉淀,B项正确;
C.从图2可以看出 、 时,该点位于曲线Ⅱ的上方,会生成碳酸镁沉淀,根据物
料守恒,溶液中 ,C项错误;D. 时,溶液中主
第11页 | 共27页要含碳微粒是 , , 时,该点位于曲线Ⅱ的上方,会生成碳酸镁沉淀,因
此反应的离子方程式为 ,D项正确;
故选C。
第二部分
本部分共5小题,共58分。
15. 硫代硫酸盐是一类具有应用前景的浸金试剂。硫代硫酸根 可看作是 中的一个 原子被
原子取代的产物。
(1)基态 原子价层电子排布式是__________。
(2)比较 原子和 原子的第一电离能大小,从原子结构的角度说明理由:____________________。
(3) 的空间结构是__________。
(4)同位素示踪实验可证实 中两个 原子的化学环境不同,实验过程为
。过程ⅱ中, 断裂的只有硫硫键,若过程ⅰ所用试剂是
和 ,过程ⅱ含硫产物是__________。
(5) 的晶胞形状为长方体,边长分别为 、 ,结构如图所示。
晶胞中的 个数为__________。已知 的摩尔质量是 ,阿伏加德
第12页 | 共27页罗常数为 ,该晶体的密度为__________ 。
(6)浸金时, 作为配体可提供孤电子对与 形成 。分别判断 中的中心
原子和端基 原子能否做配位原子并说明理由:____________________。
【答案】(1)
(2) ,氧原子半径小,原子核对最外层电子的吸引力大,不易失去一个电子
(3)四面体形 (4) 和
.
(5) ① 4 ②.
(6) 中的中心原子S的价层电子对数为4,无孤电子对,不能做配位原子;端基S原子含有孤电子
对,能做配位原子
【解析】
【小问1详解】
S是第三周期ⅥA族元素,基态S原子价层电子排布式为 。答案为 ;
【小问2详解】
S和O为同主族元素,O原子核外有2个电子层,S原子核外有3个电子层,O原子半径小,原子核对最外
层电子的吸引力大,不易失去1个电子,即O的第一电离能大于S的第一电离能。答案为I(O)>I (S),氧
1 1
原子半径小,原子核对最外层电子的吸引力大,不易失去一个电子;
【小问3详解】
的中心原子S的价层电子对数为4,无孤电子对,空间构型为四面体形, 可看作是 中1
个O原子被S原子取代,则 的空间构型为四面体形。答案为四面体形;
【小问4详解】
过程Ⅱ中 断裂的只有硫硫键,根据反应机理可知,整个过程中 最终转化为 ,S最终转化
第13页 | 共27页为 。若过程ⅰ所用的试剂为 和 ,过程Ⅱ的含硫产物是 和 。答案为
和 ;
【小问5详解】
由晶胞结构可知,1个晶胞中含有 个 ,含有4个 ;该晶
体的密度 。答案为4; ;
【小问6详解】
具有孤电子对的原子就可以给个中心原子提供电子配位。 中的中心原子S的价层电子对数为4,无
孤电子对,不能做配位原子;端基S原子含有孤电子对,能做配位原子。
16. 尿素 合成的发展体现了化学科学与技术的不断进步。
(1)十九世纪初,用氰酸银 与 在一定条件下反应制得 ,实现了由无机物
到有机物的合成。该反应的化学方程式是____________________。
(2)二十世纪初,工业上以 和 为原料在一定温度和压强下合成尿素。反应分两步:
ⅰ. 和 生成 ;
ⅱ. 分解生成尿素。
结合反应过程中能量变化示意图,下列说法正确的是__________(填序号)。
a.活化能:反应ⅰ<反应ⅱ
第14页 | 共27页b.ⅰ为放热反应,ⅱ为吸热反应
c.
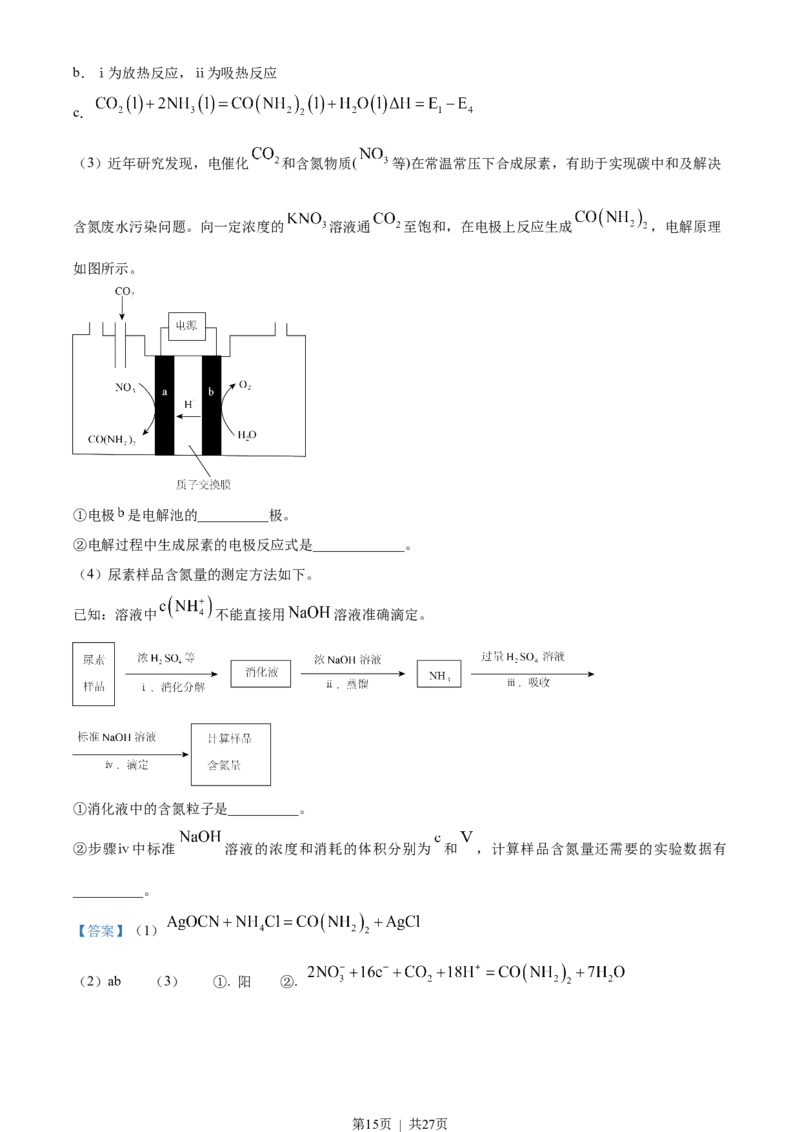
(3)近年研究发现,电催化 和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决
含氮废水污染问题。向一定浓度的 溶液通 至饱和,在电极上反应生成 ,电解原理
如图所示。
①电极 是电解池的__________极。
②电解过程中生成尿素的电极反应式是_____________。
(4)尿素样品含氮量的测定方法如下。
已知:溶液中 不能直接用 溶液准确滴定。
①消化液中的含氮粒子是__________。
②步骤ⅳ中标准 溶液的浓度和消耗的体积分别为 和 ,计算样品含氮量还需要的实验数据有
__________。
【答案】(1)
(2)ab (3) ①. 阳 ②.
第15页 | 共27页(4) ①. ②. 样品的质量、步骤Ⅲ所加入 溶液的体积和浓度
【解析】
【小问1详解】
根据原子守恒分析,二者反应生成尿素和氯化银,化学方程式是 。
答案为 ;
【小问2详解】
a.反应ⅰ的活化能是 ,反应ⅱ活化能是 , ,a项正确;
b.从图中反应物和生成物能量的相对大小可看出反应ⅰ放热,反应ⅱ吸热,b项正确;
c.总反应的: ,c项错误;
故选ab。
【小问3详解】
①电极b上发生 失电子生成 的氧化反应,是电解池的阳极。②a极硝酸根离子得电子转化为尿素,
再结合酸性环境可分析出电极反应式为 。答案为阳极;
;
【小问4详解】
①尿素消化分解生成 和 ,由于反应中存在浓 ,则消化液中含氮粒子为 。②除了已
知数据外,还需要的是样品的质量、步骤ⅲ所加入 溶液的体积和浓度。答案为 ;样品的质量、
步骤Ⅲ所加入HSO 溶液的体积和浓度。
2 4
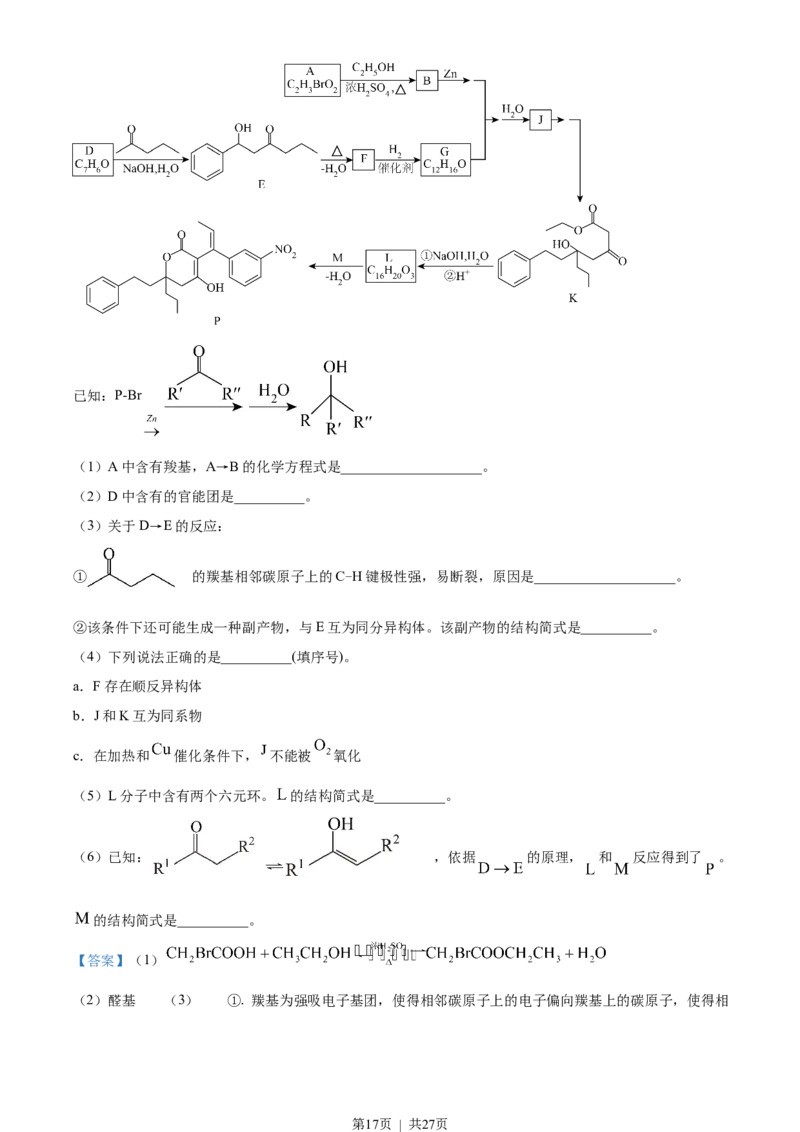
17. 化合物 是合成抗病毒药物普拉那韦的原料,其合成路线如下。
第16页 | 共27页已知:P-Br
(1)A中含有羧基,A→B的化学方程式是____________________。
(2)D中含有的官能团是__________。
(3)关于D→E的反应:
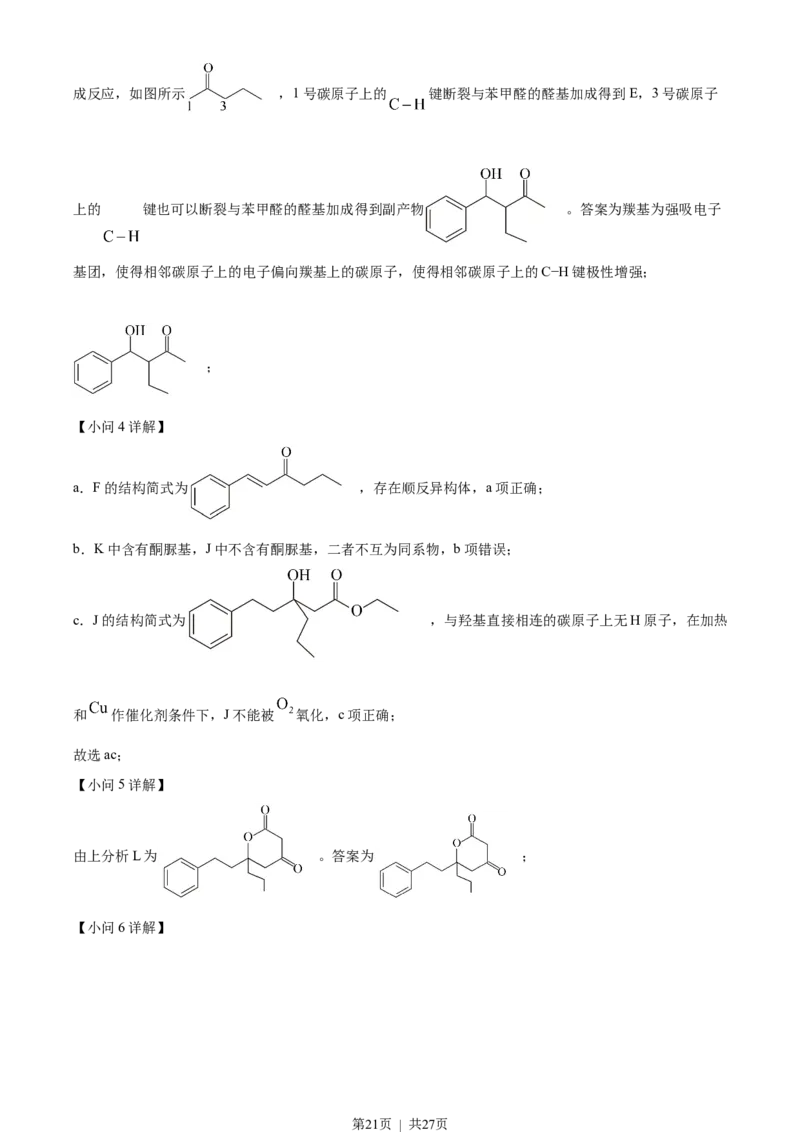
① 的羰基相邻碳原子上的C-H键极性强,易断裂,原因是____________________。
②该条件下还可能生成一种副产物,与E互为同分异构体。该副产物的结构简式是__________。
(4)下列说法正确的是__________(填序号)。
a.F存在顺反异构体
b.J和K互为同系物
c.在加热和 催化条件下, 不能被 氧化
(5)L分子中含有两个六元环。 的结构简式是__________。
(6)已知: ,依据 的原理, 和 反应得到了 。
的结构简式是__________。
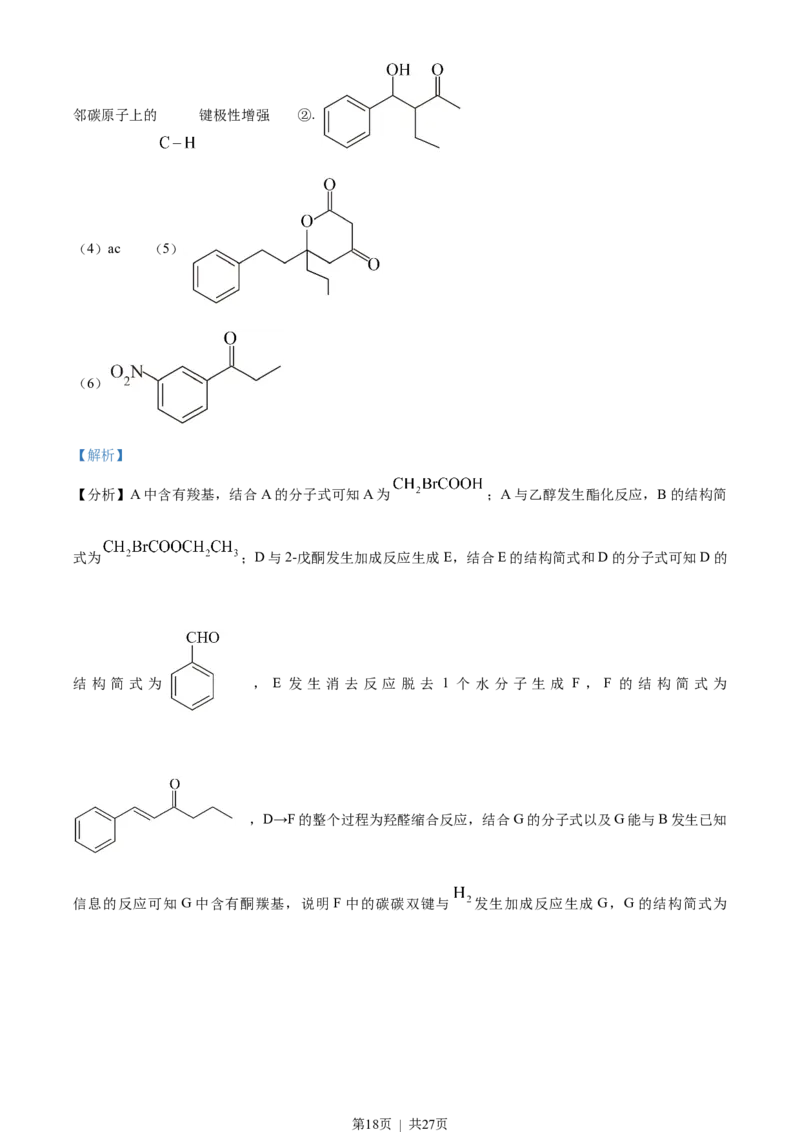
【答案】(1)
(2)醛基 (3) ①. 羰基为强吸电子基团,使得相邻碳原子上的电子偏向羰基上的碳原子,使得相
第17页 | 共27页邻碳原子上的 键极性增强 ②.
(4)ac (5)
(6)
【解析】
【分析】A中含有羧基,结合A的分子式可知A为 ;A与乙醇发生酯化反应,B的结构简
式为 ;D与2-戊酮发生加成反应生成E,结合E的结构简式和D的分子式可知D的
结 构 简 式 为 , E 发 生 消 去 反 应 脱 去 1 个 水 分 子 生 成 F , F 的 结 构 简 式 为
,D→F的整个过程为羟醛缩合反应,结合G的分子式以及G能与B发生已知
信息的反应可知G中含有酮羰基,说明 F中的碳碳双键与 发生加成反应生成 G,G的结构简式为
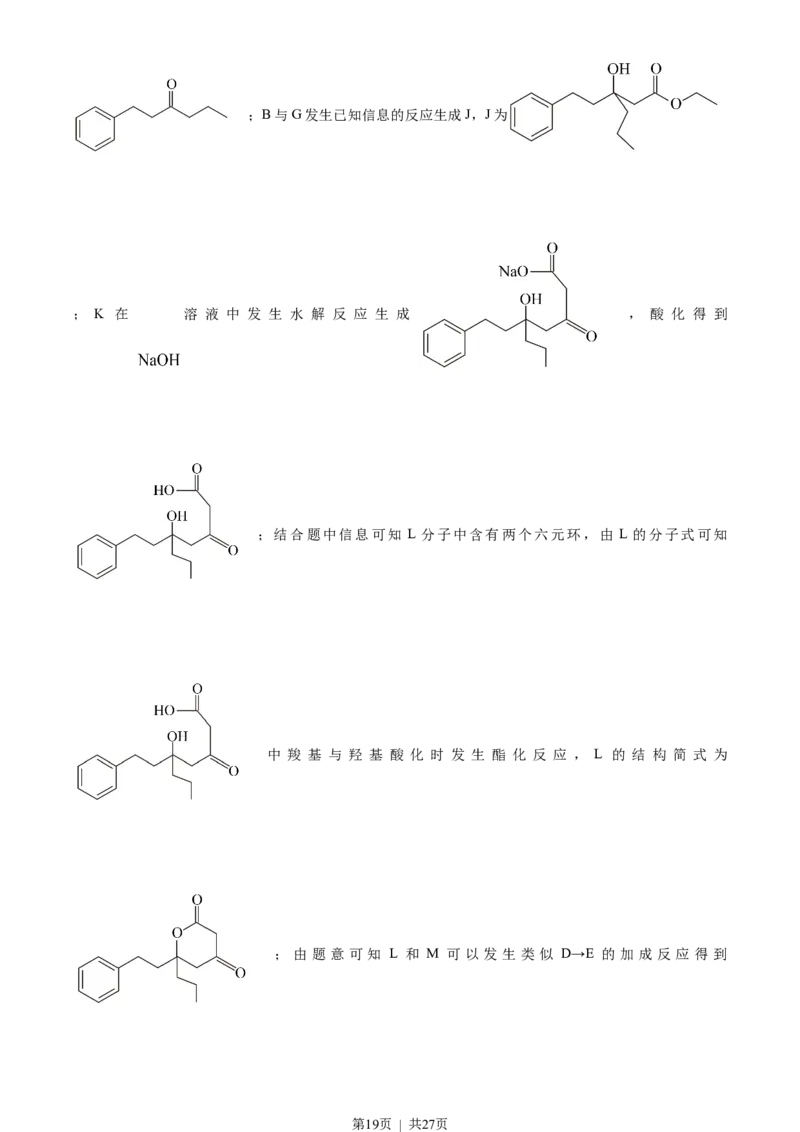
第18页 | 共27页;B与G发生已知信息的反应生成J,J为
; K 在 溶 液 中 发 生 水 解 反 应 生 成 , 酸 化 得 到
;结合题中信息可知 L 分子中含有两个六元环,由 L 的分子式可知
中 羧 基 与 羟 基 酸 化 时 发 生 酯 化 反 应 , L 的 结 构 简 式 为
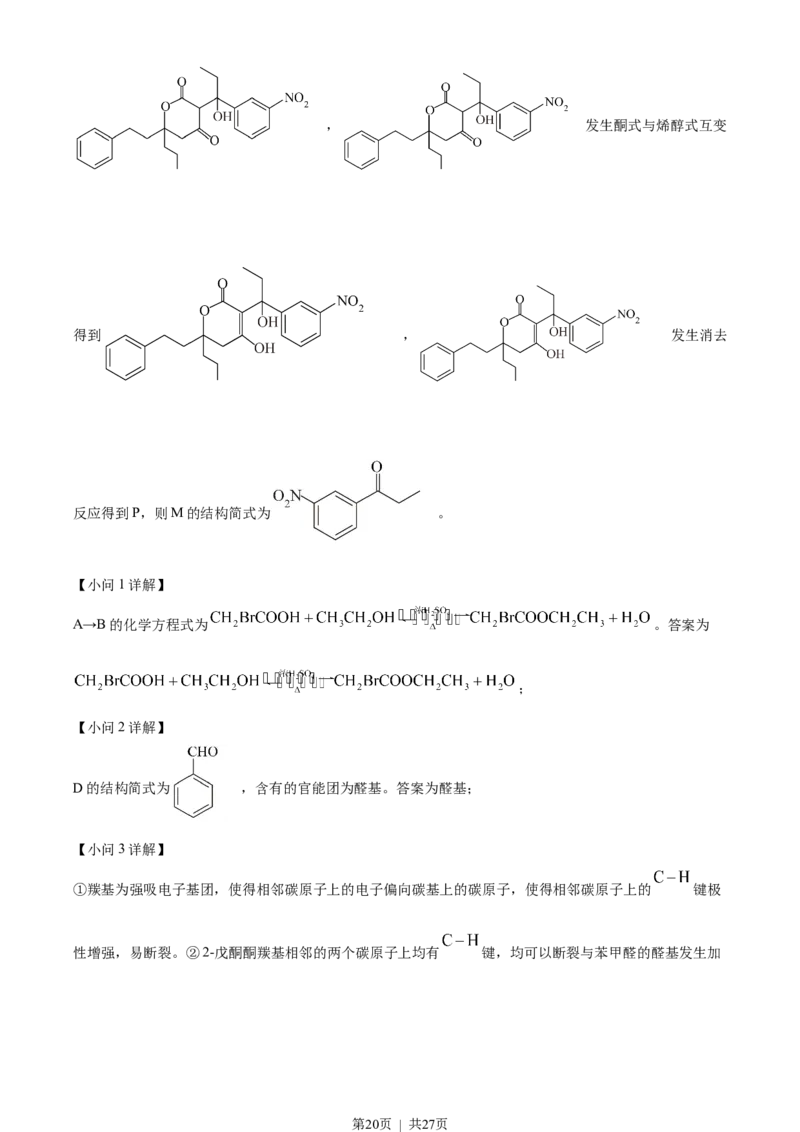
; 由 题 意 可 知 L 和 M 可 以 发 生 类 似 D→E 的 加 成 反 应 得 到
第19页 | 共27页, 发生酮式与烯醇式互变
得到 , 发生消去
反应得到P,则M的结构简式为 。
【小问1详解】
A→B的化学方程式为 。答案为
;
【小问2详解】
D的结构简式为 ,含有的官能团为醛基。答案为醛基;
【小问3详解】
①羰基为强吸电子基团,使得相邻碳原子上的电子偏向碳基上的碳原子,使得相邻碳原子上的 键极
性增强,易断裂。②2-戊酮酮羰基相邻的两个碳原子上均有 键,均可以断裂与苯甲醛的醛基发生加
第20页 | 共27页成反应,如图所示 ,1号碳原子上的 键断裂与苯甲醛的醛基加成得到E,3号碳原子
上的 键也可以断裂与苯甲醛的醛基加成得到副产物 。答案为羰基为强吸电子
基团,使得相邻碳原子上的电子偏向羰基上的碳原子,使得相邻碳原子上的C−H键极性增强;
;
【小问4详解】
a.F的结构简式为 ,存在顺反异构体,a项正确;
b.K中含有酮脲基,J中不含有酮脲基,二者不互为同系物,b项错误;
c.J的结构简式为 ,与羟基直接相连的碳原子上无H原子,在加热
和 作催化剂条件下,J不能被 氧化,c项正确;
故选ac;
【小问5详解】
由上分析L为 。答案为 ;
【小问6详解】
第21页 | 共27页由上分析M为 。答案为 。
18. 以银锰精矿(主要含 、 、 )和氧化锰矿(主要含 )为原料联合提取银和锰的一种流
程示意图如下。
已知:酸性条件下, 的氧化性强于 。
(1) “浸锰”过程是在 溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出:矿
石中的银以 的形式残留于浸锰渣中。
①“浸锰”过程中,发生反应 ,则可推断: __________(填“>”或
“<”) 。
②在 溶液中,银锰精矿中的 和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离子
有__________。
(2) “浸银”时,使用过量 和 的混合液作为浸出剂,将 中的银以 形式
浸出。
①将“浸银”反应的离子方程式补充完整:__________。
②结合平衡移动原理,解释浸出剂中 的作用:____________________。
(3) “沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有______________________________。
第22页 | 共27页②一定温度下, 的沉淀率随反应时间的变化如图所示。解释 分钟后 的沉淀率逐渐减小的原因:
______________。
(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势:________。
【答案】(1) ①. > ②. 、
(2) ①. ②. 是为了与 电离出的
结合生成 ,使平衡正向移动,提高 的浸出率; 是为了抑制 水解,防止生成
沉淀
(3) ①. 、 ②. 被氧气氧化为
, 把 氧化为
(4)可将两种矿石中的锰元素同时提取到浸锰液中,得到 ,同时将银元素和锰元素分离开;生成
的 还可以用于浸银,节约氧化剂
【解析】
【分析】银锰精矿(主要含 、 、 )和氧化锰矿(主要含 )混合加 溶液,使矿石
中的锰元素浸出,同时去除 ,矿石中的银以 的形式残留于浸锰渣中,浸锰液中主要的金属阳离
第23页 | 共27页子有 、 ;浸锰渣中 与过量 和 的混合液反应,将 中的银以
形式浸出,用铁粉把 还原为金属银。
【小问1详解】
①“浸锰”过程中,矿石中的银以 的形式残留于浸锰渣中, 发生反应
,硫化锰溶于强酸而硫化银不溶于强酸,则可推断: >
;
②根据信息,在 溶液中二氧化锰可将 氧化为 ,自身被还原为 ,则浸锰液中主要的
金属阳离子有 、 。
【小问2详解】
① 中S元素化合价升高,Fe元素化合价降低,根据得失电子守恒、元素守恒,该离子方程式为
;
② 是为了与 电离出的 结合生成 ,使平衡正向移动,提高 的浸出率; 是为
了抑制 水解,防止生成 沉淀。
【小问3详解】
①铁粉可将 还原为单质银,过量的铁粉还可以与铁离子发生反应,因此离子方程式为
、 ;
②溶液中生成的 会被空气中的氧气缓慢氧化为 , 把部分 氧化为 ,因此 后银
的沉淀率逐渐降低。
【小问4详解】
联合提取银和锰的优势在于“浸锰”过程可将两种矿石中的锰元素同时提取到浸锰液中,将银元素和锰元素
第24页 | 共27页分离开,利用 的氧化性将 中的 氧化为 ,同时生成的 还可以用于浸银,节约氧
化剂,同时得到 。
19. 资料显示, 可以将 氧化为 。某小组同学设计实验探究 被 氧化的产物及铜元素的价态。
已知: 易溶于 溶液,发生反应 (红棕色); 和 氧化性几乎相同。
I.将等体积的 溶液加入到 铜粉和 的固体混合物中,振荡。
实验记录如下:
实验现象
实验 极少量 溶解,溶液为淡红色;充分反应后,红色的铜粉转化为白色沉淀,溶
Ⅰ
液仍为淡红色
实验 部分 溶解,溶液为红棕色;充分反应后,红色的铜粉转化为白色沉淀,溶液
Ⅱ
仍为红棕色
实验 完全溶解,溶液为深红棕色;充分反应后,红色的铜粉完全溶解,溶液为深
Ⅲ
红棕色
(1)初始阶段, 被氧化的反应速率:实验Ⅰ__________(填“>”“<”或“=”)实验Ⅱ。
(2)实验Ⅲ所得溶液中,被氧化的铜元素的可能存在形式有 (蓝色)或 (无色),进
行以下实验探究:
步骤a.取实验Ⅲ的深红棕色溶液,加入 ,多次萃取、分液。
步骤b.取分液后的无色水溶液,滴入浓氨水。溶液颜色变浅蓝色,并逐渐变深。
ⅰ.步骤a的目的是_____________________。
ⅱ.查阅资料, , (无色)容易被空气氧化。用离子方程式解释步
骤 的溶液中发生的变化:______________。
(3)结合实验Ⅲ,推测实验Ⅰ和Ⅱ中的白色沉淀可能是 ,实验Ⅰ中铜被氧化的化学方程式是
____________________。分别取实验Ⅰ和Ⅱ充分反应后的固体,洗涤后得到白色沉淀,加入浓 溶液,
第25页 | 共27页__________(填实验现象),观察到少量红色的铜。分析铜未完全反应的原因是____________________。
(4)上述实验结果, 仅将 氧化为 价。在隔绝空气的条件下进行电化学实验,证实了 能将
氧化为 。装置如图所示, 分别是_____________。
(5)运用氧化还原反应规律,分析在上述实验中 被 氧化的产物中价态不同的原因:_________。
【 答 案 】 ( 1 ) < ( 2 ) ① . 除 去 , 防 止 干 扰 后 续 实 验 ② .
、
(3) ①. 或 ②. 白色沉淀逐渐溶解 ③. 溶液变为无
色铜与碘的反应为可逆反应(或 浓度小未能氧化全部的 )
(4)铜、含 的 的 溶液
(5)在实验Ⅰ、实验Ⅱ、实验Ⅲ中 可以进一步与 结合生成 沉淀或 , 浓度减小使
得 氧化性增强,发生反应 和 。
【解析】
【分析】因I 溶解度较小,Cu与I 接触不充分,将转化为 可以提高Cu与 的接触面积,提高反应速率。
2 2
加入 , 平衡逆向移动,I 浓度减小, 浓度增加, 浓度增加,加入氨水后转
2
第26页 | 共27页化为 ,被氧化为 ,故而产生无色溶液变为蓝色溶液的现象。
【小问1详解】
提高KI浓度,便于提高 的浓度,与Cu接触更加充分,Cu与 的反应速率加快,故实验Ⅰ<实验Ⅱ。
【小问2详解】
加入 , 平衡逆向移动,I 浓度减小, 浓度增加,其目的为:除去 ,防止干扰后
2
续实验。加入氨水 浓后转化为 无色的 被氧化为蓝色的
,方程式为 、
。
【小问3详解】
结合实验Ⅲ,推测实验Ⅰ和Ⅱ中的白色沉淀可能是 ,实验Ⅰ中铜被氧化的化学方程式是
或 ; 反应为可逆反应,加入浓 溶液,I 浓度
2
减小,CuI转化为Cu和I,故产生白色沉淀溶解,出现红色固体的过程。
2
【小问4详解】
要验证 能将 氧化为 ,需设计原电池负极材料为Cu,b为含 的 的 溶液。
【小问5详解】
含 的 的 溶液铜与碘反应的体系在原电池装置中, 将 氧化为 ;而在实验Ⅰ、
实验Ⅱ和实验Ⅲ中 以 形式存在,这是由于在实验Ⅰ、实验Ⅱ、实验Ⅲ中 可以进一步与 结合
生成 沉淀或 , 浓度减小使得 氧化性增强,发生反应 和
。
第27页 | 共27页