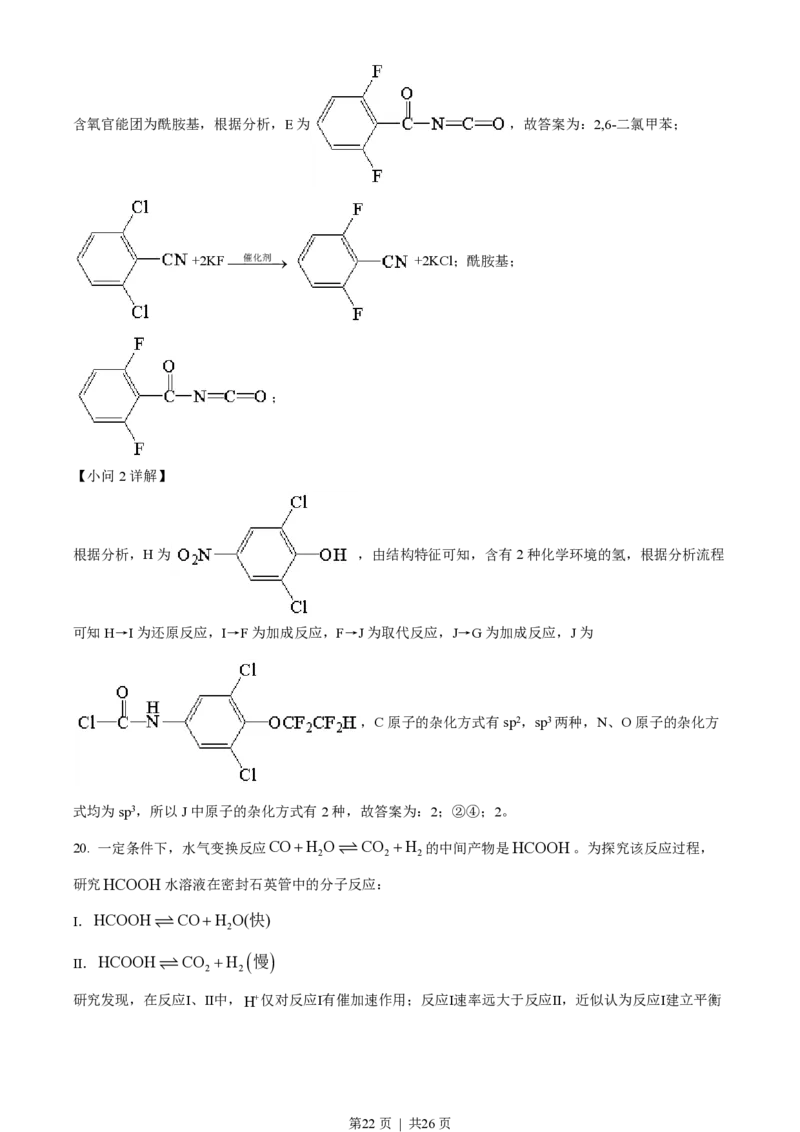
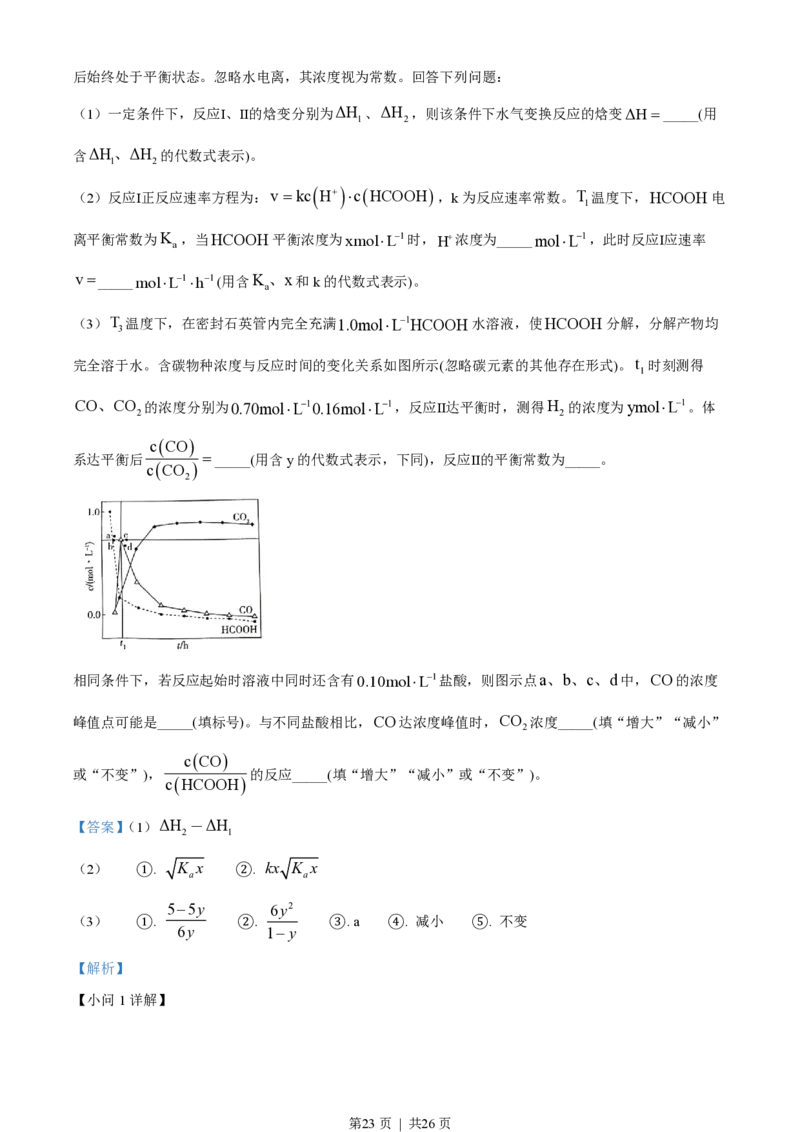
文档内容
山东省 2023 年普通高中学业水平等级考试
化学
可能用到的相对原子质量:H-1 C-12 N-14 O-16 F-19 Si-28 S-32 C1-35.5 K-39
Cu-64
一、选择题:本题共 10小题,每小题 2分,共 20分。每小题只有一个选项符合题目要求。
1. 下列之物具有典型的齐鲁文化特色,据其主要化学成分不能与其他三种归为一类的是
A. 泰山墨玉 B. 龙山黑陶 C. 齐国刀币 D. 淄博琉璃
【答案】C
【解析】
【详解】墨玉、黑陶、琉璃均为陶瓷制品,均属于硅酸盐制品,主要成分均为硅酸盐材料,而刀币的主要
成分为青铜,故答案为:C。
2. 实验室中使用盐酸、硫酸和硝酸时,对应关系错误的是
A. 稀盐酸:配制AlCl 溶液
3
B. 稀硫酸:蔗糖和淀粉的水解
C. 稀硝酸:清洗附有银镜的试管
D. 浓硫酸和浓硝酸的混合溶液:苯的磺化
【答案】D
【解析】
【详解】A.实验室配制AlCl 溶液时向其中加入少量的稀盐酸以抑制Al3+水解,A不合题意;
3
B.蔗糖和淀粉的水解时常采用稀硫酸作催化剂,B不合题意;
C.清洗附有银镜的试管用稀硝酸,反应原理为:3Ag+4HNO (稀)=3AgNO +NO↑+2H O,C不合题意;
3 3 2
D.苯的磺化是苯和浓硫酸共热,反应生成苯磺酸的反应,故不需要用到浓硫酸和浓硝酸的混合溶液,D
符合题意;
故答案为:D。
3. 下列分子属于极性分子的是
A. CS B. NF C. SO D. SiF
2 3 3 4
【答案】B
【解析】
1
【详解】A.CS 中C上的孤电子对数为 ×(4-2×2)=0,σ键电子对数为2,价层电子对数为2,CS 的空
2 2 2
第1页 | 共26页间构型为直线形,分子中正负电中心重合,CS 属于非极性分子,A项不符合题意;
2
1
B.NF 中N上的孤电子对数为 ×(5-3×1)=1,σ键电子对数为3,价层电子对数为4,NF 的空间构型为
3 2 3
三角锥形,分子中正负电中心不重合,NF 属于极性分子,B项符合题意;
3
1
C.SO 中S上的孤电子对数为 ×(6-3×2)=0,σ键电子对数为3,价层电子对数为3,SO 的空间构型为
3 2 3
平面正三角形,分子中正负电中心重合,SO 属于非极性分子,C项不符合题意;
3
1
D.SiF 中Si上的孤电子对数为 ×(4-4×1)=0,σ键电子对数为4,价层电子对数为4,SiF 的空间构型为
4 2 4
正四面体形,分子中正负电中心重合,SiF 属于非极性分子,D项不符合题意;
4
答案选B。
4. 实验室安全至关重要,下列实验室事故处理方法错误的是
A. 眼睛溅进酸液,先用大量水冲洗,再用饱和碳酸钠溶液冲洗
B. 皮肤溅上碱液,先用大量水冲洗,再用2%的硼酸溶液冲洗
C. 电器起火,先切断电源,再用二氧化碳灭火器灭火
D. 活泼金属燃烧起火,用灭火毯(石棉布)灭火
【答案】A
【解析】
【详解】A.眼睛溅进酸液,先用大量水冲洗,再用3%-5%的碳酸氢钠溶液冲洗,故A错误;
B.立即用大量水冲洗,边洗边眨眼,尽可能减少碱对眼睛的伤害,再用2%的硼酸中和残余的碱,故B
正确;
C.电器起火,先切断电源,再用二氧化碳灭火器灭火,故C正确;
D.活泼金属会与水反应,所以燃烧起火,用灭火毯(石棉布)灭火,故D正确;
答案为A。
5. 石墨与F 在450℃反应,石墨层间插入F得到层状结构化合物(CF) ,该物质仍具润滑性,其单层局部
2 x
结构如图所示。下列关于该化合物的说法正确的是
A. 与石墨相比,(CF) 导电性增强
x
第2页 | 共26页B. 与石墨相比,(CF) 抗氧化性增强
x
C. (CF) 中C-C的键长比C-F短
x
D. 1mol(CF) 中含有2xmol共价单键
x
【答案】B
【解析】
【详解】A.石墨晶体中每个碳原子上未参与杂化的1个2p轨道上电子在层内离域运动,故石墨晶体能导
电,而(CF) 中没有未参与杂化的2p轨道上的电子,故与石墨相比,(CF) 导电性减弱,A错误;
x x
B.(CF) 中C原子的所有价键均参与成键,未有未参与成键的孤电子或者不饱和键,故与石墨相比,
x
(CF) 抗氧化性增强,B正确;
x
C.已知C的原子半径比F的大,故可知(CF) 中C-C的键长比C-F长,C错误;
x
D.由题干结构示意图可知,在(CF) 中C与周围的3个碳原子形成共价键,每个C-C键被2个碳原子共
x
用,和1个F原子形成共价键,即1mol(CF) 中含有2.5xmol共价单键,D错误;
x
故答案为:B。
6. 鉴别浓度均为0.1mol×L-1的NaClO、Ba(OH) 、Al SO 三种溶液,仅用下列一种方法不可行的
2 2 4 3
是
A. 测定溶液pH B. 滴加酚酞试剂
C 滴加0.1mol×L-1KI溶液 D. 滴加饱和Na CO 溶液
. 2 3
【答案】C
【解析】
【详解】A.NaClO溶液显弱碱性,Ba(OH) 溶液显强碱性,Al SO 溶液显酸性,则测定溶液pH
2 2 4 3
是可以鉴别出来的,故A不符合题意;
B.NaClO溶液显弱碱性,滴入酚酞先变红后褪色,Ba(OH) 溶液显强碱性,滴入酚酞溶液,显红色,
2
Al SO 溶液显酸性,滴入酚酞不变色,则滴加酚酞试剂是可以鉴别出来的,故B不符合题意;
2 4 3
C.NaClO溶液滴入碘化钾溶液,发生氧化还原反应生成碘,液面会由无色变成黄色,振荡后会变成无
色,而Ba(OH) 溶液,Al SO 溶液滴入碘化钾溶液后,因不与两者反应而没有现象,则仅用滴加
2 2 4 3
0.1mol×L-1KI溶液无法鉴别,则C符合题意;
D.饱和Na CO 溶液和NaClO溶液不反应,和Ba(OH) 溶液反应生成碳酸钡沉淀,和Al SO 溶液
2 3 2 2 4 3
第3页 | 共26页发生双水解反应生成沉淀和气体,则滴入饱和Na CO 溶液是可以鉴别出来的,故D不符合题意;
2 3
答案C。
7. 抗生素克拉维酸的结构简式如图所示,下列关于克拉维酸的说法错误的是
A. 存在顺反异构
B. 含有5种官能团
C. 可形成分子内氢键和分子间氢键
D. 1mol该物质最多可与1molNaOH反应
【答案】D
【解析】
【详解】A.由题干有机物结构简式可知,该有机物存在碳碳双键,且双键两端的碳原子分别连有互不同
的原子或原子团,故该有机物存在顺反异构,A正确;
B.由题干有机物结构简式可知,该有机物含有羟基、羧基、碳碳双键、醚键和酰胺基等5种官能团,B
正确;
C.由题干有机物结构简式可知,该有机物中的羧基、羟基、酰胺基等官能团具有形成氢键的能力,故其
分子间可以形成氢键,其中距离较近的某些官能团之间还可以形成分子内氢键,C正确;
D.由题干有机物结构简式可知,1mol该有机物含有羧基和酰胺基各1mol,这两种官能团都能与强碱反
应,故1mol该物质最多可与2molNaOH反应,D错误;
故答案为:D。
8. 一定条件下,乙酸酐é ë CH 3 CO 2 Où û 醇解反应
éCH CO O+ROH¾¾®CH COOR+CH COOHù可进行完全,利用此反应定量测定有机醇
ë 3 2 3 3 û
ROH
中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入mgROH样品,充分反应后,加适量水使剩余乙酸酐
完全水解: CH CO O+H O¾¾®2CH COOH。
3 2 2 3
第4页 | 共26页③加指示剂并用cmol×L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol×L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液V mL。对于上述实验,下列做法正确的是
2
A. 进行容量瓶检漏时,倒置一次即可
B. 滴入半滴标准溶液,锥形瓶中溶液变色,即可判定达滴定终点
C. 滴定读数时,应单手持滴定管上端并保持其自然垂直
D. 滴定读数时,应双手一上一下持滴定管
【答案】C
【解析】
【详解】A.进行容量瓶检漏时,倒置一次,然后玻璃塞旋转180度后再倒置一次,故A错误;
B.滴入半滴标准溶液,锥形瓶中溶液变色,且半分钟内不变回原色,才是达到滴定终点,故B错误;
C.滴定读数时,应单手持滴定管上端无刻度处,并保持其自然垂直,故C正确;
D.滴定读数时,应单手持滴定管上端无刻度处,并保持其自然垂直,故D错误;
答案为C。
9. 一定条件下,乙酸酐é ë CH 3 CO 2 Où û 醇解反应
éCH CO O+ROH¾¾®CH COOR+CH COOHù可进行完全,利用此反应定量测定有机醇
ë 3 2 3 3 û
ROH
中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入mgROH样品,充分反应后,加适量水使剩余乙酸酐
完全水解: CH CO O+H O¾¾®2CH COOH。
3 2 2 3
③加指示剂并用cmol×L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液VmL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol×L-1NaOH-甲醇标准溶液滴定至终点,消耗标准溶液V mL。ROH样品中羟基含量(质量分数)计算
2
正确的是
cV -V ´17 cV-V ´17
A. 2 1 ´100% B. 1 2 ´100%
1000m 1000m
0.5cV -V ´17 c0.5V -V ´17
C. 2 1 ´100% D. 2 1 ´100%
1000m 1000m
第5页 | 共26页【答案】A
【解析】
【详解】根据滴定过程中,用cmol×L-1NaOH-甲醇标准溶液滴定乙酸酐完全水解生成的乙酸,消耗标准
溶液V mL,需要消耗cmol×L-1NaOH-甲醇的物质的量为V ´c´10-3mol,即乙酸酐的总物质的量=
2 2
V ´c´10-3 V ´c´10-3
2 mol;则ROH与乙酸酐反应后剩余的乙酸酐的物质的量= 1 mol;设醇解的乙酸酐
2 2
V ´c´10-3 V ´c´10-3
物质的量为x,水解的乙酸酐的物质的量为y,则x+y= 2 mol;x+2y= 1 mol;联立
2 2
计算得:x=n(ROH)=V ´c´10-3-V ´c´10-3mol,ROH样品中羟基质量分数=
2 1
V ´c´10-3-V ´c´10-3mol´17g/mol (V -V)´c´17
2 1 ´100%= 2 1 ´100%, A正确;故选A。
mg 103m
10. 一定条件下,乙酸酐é ë CH 3 CO 2 Où û 醇解反应
éCH CO O+ROH¾¾®CH COOR+CH COOHù可进行完全,利用此反应定量测定有机醇
ë 3 2 3 3 û
ROH
中的羟基含量,实验过程中酯的水解可忽略。实验步骤如下:
①配制一定浓度的乙酸酐-苯溶液。
②量取一定体积乙酸酐-苯溶液置于锥形瓶中,加入mg ROH样品,充分反应后,加适量水使剩余乙酸酐
完全水解: CH CO O+H O¾¾®2CH COOH。
3 2 2 3
③加指示剂并用cmol×L-1 NaOH-甲醇标准溶液滴定至终点,消耗标准溶液V mL。
1
④在相同条件下,量取相同体积的乙酸酐-苯溶液,只加适量水使乙酸酐完全水解;加指示剂并用
cmol×L-1 NaOH-甲醇标准溶液滴定至终点,消耗标准溶液V mL。根据上述实验原理,下列说法正确
2
的是
A. 可以用乙酸代替乙酸酐进行上述实验
B. 若因甲醇挥发造成标准溶液浓度发生变化,将导致测定结果偏小
C. 步骤③滴定时,不慎将锥形瓶内溶液溅出,将导致测定结果偏小
D. 步骤④中,若加水量不足,将导致测定结果偏大
【答案】B
【解析】
第6页 | 共26页【分析】用cmol×L-1 NaOH-甲醇标准溶液滴定乙酸酐完全水解生成的乙酸,消耗标准溶液V mL,则消
2
耗NaOH的物质的量为
V
´c´10-3
mol,即乙酸酐的总物质的量为
V
2
´c´10-3
mol,ROH与乙酸
2
2
V
´c´10-3
酐反应后剩余的乙酸酐的物质的量为 1 mol,所以与ROH反应消耗的乙酸酐的物质的量为
2
V ´c´10-3 -V ´c´10-3
2 1 mol。
2
【详解】A.乙酸与醇的酯化反应可逆,不能用乙酸代替乙酸酐进行上述实验,A项错误;
B.若甲醇挥发,NaOH-甲醇溶液的浓度将偏大,滴定时消耗NaOH-甲醇溶液的体积偏小,步骤④中所得
V ´c´10-3 -V ´c´10-3
V
2
偏小,而ROH的物质的量为 2 1 mol,故将导致测定结果偏小,B项正确;
2
C.步骤③滴定时,不慎将锥形瓶内溶液溅出,消耗NaOH-甲醇溶液的体积偏小即V 偏小,而ROH的物
1
V ´c´10-3 -V ´c´10-3
质的量为 2 1 mol,故将导致测定结果偏大,C项错误;
2
D.步骤④中,若加水量不足,乙酸酐未完全水解,生成乙酸的物质的量偏小,消耗NaOH-甲醇溶液的体
V ´c´10-3 -V ´c´10-3
积偏小即V
2
偏小,而ROH的物质的量为 2 1 mol,故将导致测定结果偏小,D
2
项错误;
答案选B。
二、选择题:本题共 5小题,每小题 4分,共 20 分。每小题有一个或两个选项符合题目要
求,全部选对得 4分,选对但不全的得 2分,有选错的得 0分。
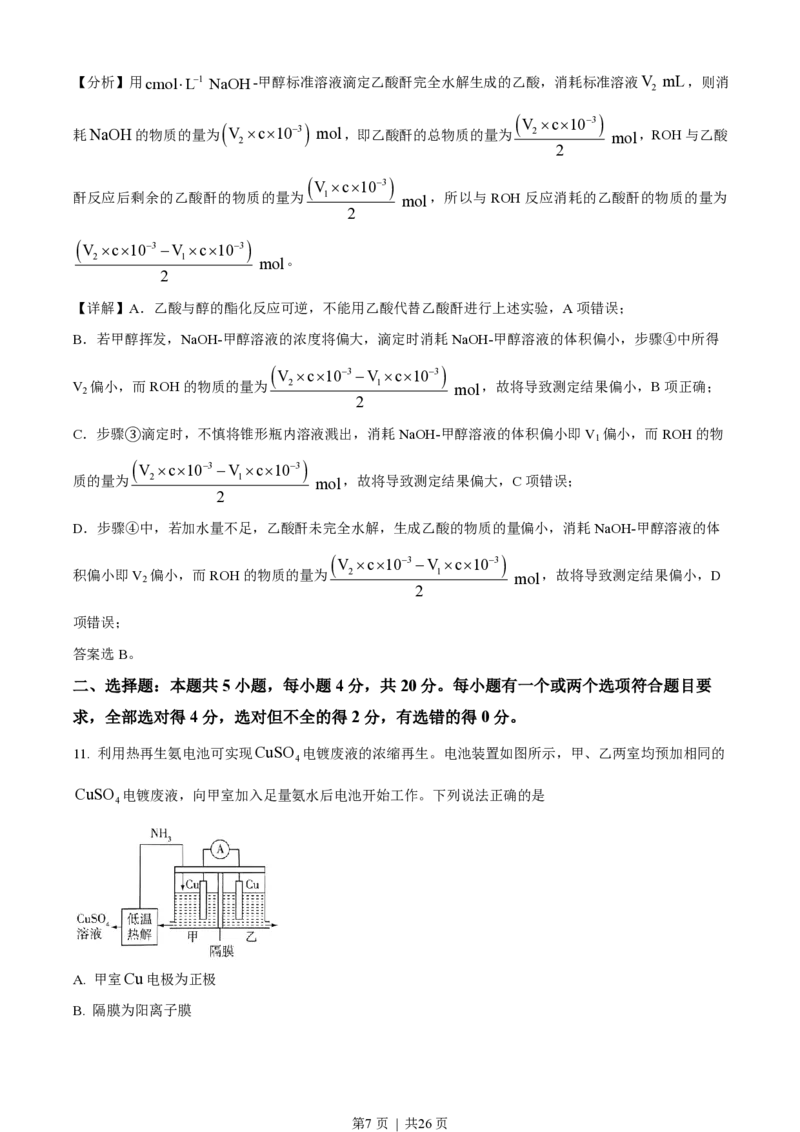
11. 利用热再生氨电池可实现CuSO 电镀废液的浓缩再生。电池装置如图所示,甲、乙两室均预加相同的
4
CuSO 电镀废液,向甲室加入足量氨水后电池开始工作。下列说法正确的是
4
A. 甲室Cu电极为正极
B. 隔膜为阳离子膜
第7页 | 共26页C. 电池总反应为:Cu2+ +4NH =éCuNH ù 2+
3 ë 3 4 û
D. NH 扩散到乙室将对电池电动势产生影响
3
【答案】CD
【解析】
【详解】A. 向甲室加入足量氨水后电池开始工作,则甲室Cu电极溶解,变为铜离子与氨气形成
éCuNH ù 2+ ,因此甲室Cu电极为负极,故A错误;
ë 3 4 û
B. 再原电池内电路中阳离子向正极移动,若隔膜为阳离子膜,电极溶解生成的铜离子要向右侧移动,通入
氨气要消耗铜离子,显然左侧阳离子不断减小,明显不利于电池反应正常进行,故B错误;
C. 左侧负极是Cu-2e- +4NH =éCuNH ù 2+ ,正极是Cu2+ +2e- =Cu,则电池总反应为:
3 ë 3 4 û
Cu2+ +4NH =éCuNH ù 2+ ,故C正确;
3 ë 3 4 û
D. NH 扩散到乙室会与铜离子反应生成éCuNH ù 2+ ,铜离子浓度降低,铜离子得电子能力减弱,因
3 ë 3 4 û
此将对电池电动势产生影响,故D正确。
综上所述,答案为CD。
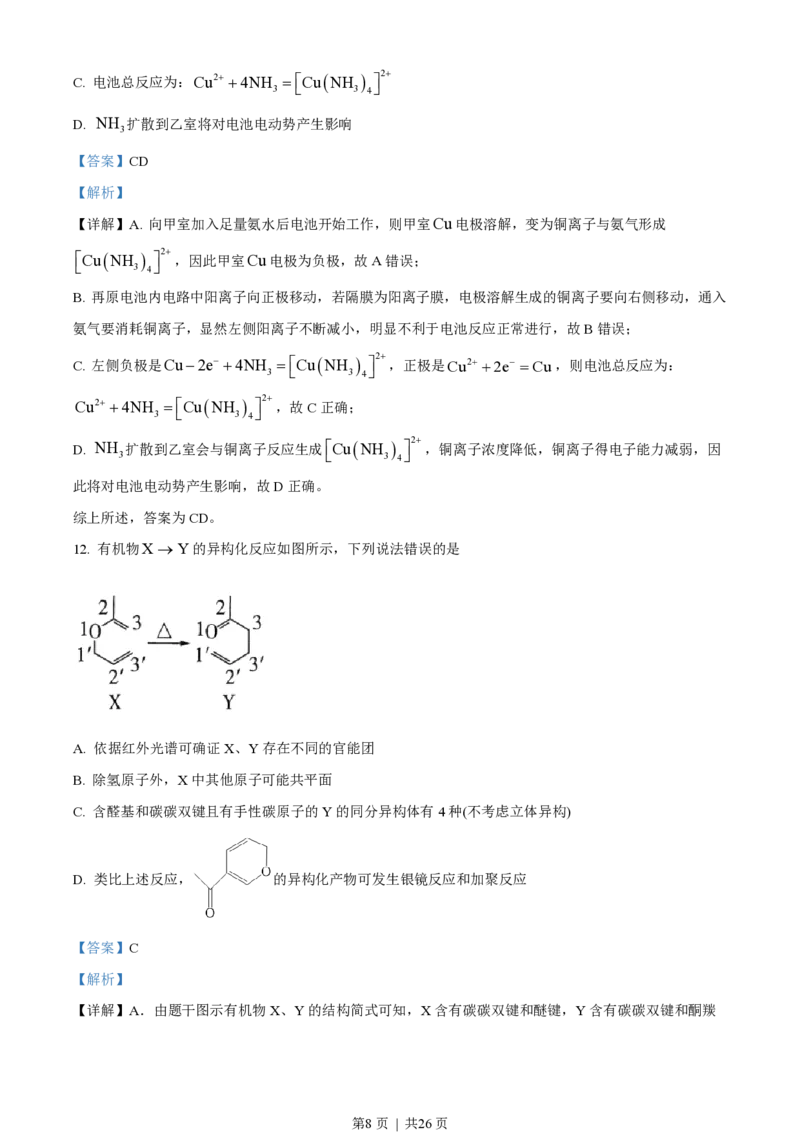
12. 有机物X® Y的异构化反应如图所示,下列说法错误的是
A. 依据红外光谱可确证X、Y存在不同的官能团
B. 除氢原子外,X中其他原子可能共平面
C. 含醛基和碳碳双键且有手性碳原子的Y的同分异构体有4种(不考虑立体异构)
D. 类比上述反应, 的异构化产物可发生银镜反应和加聚反应
【答案】C
【解析】
【详解】A.由题干图示有机物X、Y的结构简式可知,X含有碳碳双键和醚键,Y含有碳碳双键和酮羰
第8页 | 共26页基,红外光谱图中可以反映不同官能团或化学键的吸收峰,故依据红外光谱可确证X、Y存在不同的官能
团,A正确;
B.由题干图示有机物X的结构简式可知,X分子中存在两个碳碳双键所在的平面,单键可以任意旋转,
故除氢原子外,X中其他原子可能共平面,B正确;
C.由题干图示有机物Y的结构简式可知,Y的分子式为:C H O,则含醛基和碳碳双键且有手性碳原子
6 10
(即同时连有四个互不相同的原子或原子团的碳原子)的Y的同分异构体有:CH CH=CHCH(CH )CHO、
3 3
CH =C(CH )CH(CH )CHO、CH =CHCH(CH )CH CHO、CH =CHCH CH(CH )CHO和
2 3 3 2 3 2 2 2 3
CH =CHCH(CH CH )CHO共5种(不考虑立体异构),C错误;
2 2 3
D.由题干信息可知,类比上述反应, 的异构化产物为: 含有碳碳双键和醛基,
故可发生银镜反应和加聚反应,D正确;
故答案为:C。
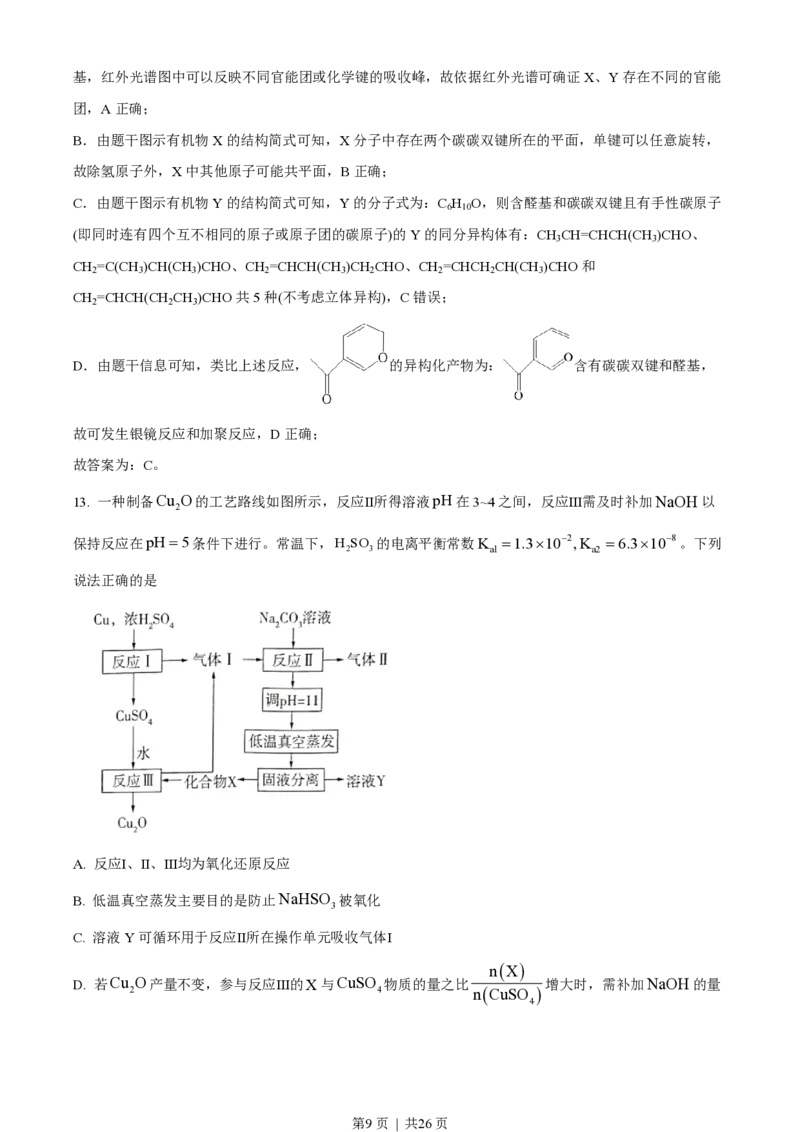
13. 一种制备Cu O的工艺路线如图所示,反应Ⅱ所得溶液pH在3~4之间,反应Ⅲ需及时补加NaOH以
2
保持反应在pH=5条件下进行。常温下,H SO 的电离平衡常数K =1.3´10-2,K =6.3´10-8。下列
2 3 al a2
说法正确的是
A. 反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B. 低温真空蒸发主要目的是防止NaHSO 被氧化
3
C. 溶液Y可循环用于反应Ⅱ所在操作单元吸收气体Ⅰ
nX
D. 若Cu O产量不变,参与反应Ⅲ的X与CuSO 物质的量之比 增大时,需补加NaOH的量
2 4 nCuSO
4
第9页 | 共26页减少
【答案】CD
【解析】
【分析】铜和浓硫酸反应(反应Ⅰ)生成二氧化硫气体(气体Ⅰ)和硫酸铜,生成的二氧化硫气体与碳酸钠反应(反
应 Ⅱ) , 所 得 溶 液 pH在 3~4 之 间 , 溶 液 显 酸 性 , 根 据 H SO 的 电 离 平 衡 常 数
2 3
K =1.3´10-2,K =6.3´10-8,可知NaHSO 溶液显酸性(电离大于水解),则反应Ⅱ所得溶液成分是
al a2 3
NaHSO ,调节溶液pH值至11,使NaHSO 转化为Na SO ,低温真空蒸发(防止Na SO 被氧化),故固
3 3 2 3 2 3
液分离得到Na SO 晶体和Na SO 溶液,Na SO 和CuSO 反应的离子方程式是SO2-+2Cu2++2H O=SO2-+
2 3 2 3 2 3 4 3 2 4
Cu O+4H+,反应过程中酸性越来越强,使 Na SO 转化成 SO 气体,总反应方程式是 2CuSO +3Na SO =
2 2 3 2 4 2 3
Cu O+2SO ↑+3Na SO ,需及时补加NaOH以保持反应在pH=5条件下进行,据此分析解答。
2 2 2 4
【详解】A.反应Ⅰ是铜和浓硫酸反应,生成二氧化硫,是氧化还原反应,反应Ⅱ是SO 和碳酸钠溶液反
2
应,生成NaHSO 、水和二氧化碳,是非氧化还原反应,反应Ⅲ是Na SO 和CuSO 反应生成Cu O,是
3 2 3 4 2
氧化还原反应,故A错误;
B.低温真空蒸发主要目的是防止Na SO 被氧化,而不是NaHSO ,故B错误;
2 3 3
C.经分析溶液Y的成分是Na SO 溶液,可循环用于反应Ⅱ的操作单元吸收SO 气体(气体Ⅰ),故C正确;
2 3 2
D.制取Cu O总反应方程式是2CuSO +3Na SO = Cu O+2SO ↑+3Na SO ,化合物X是指Na SO ,若
2 4 2 3 2 2 2 4 2 3
nX
Cu O产量不变,增大 比,多的Na SO 会消耗氢离子,用于控制pH值,可减少NaOH的
2 nCuSO 2 3
4
量,故D正确;
答案CD。
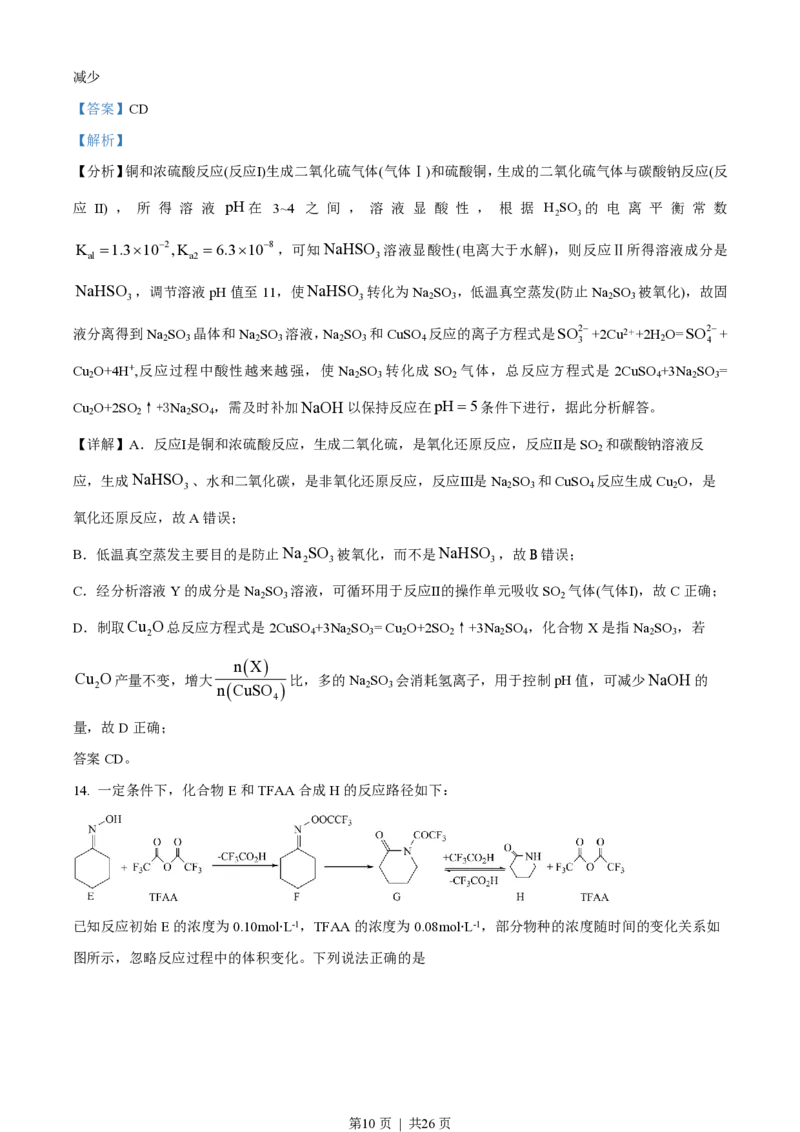
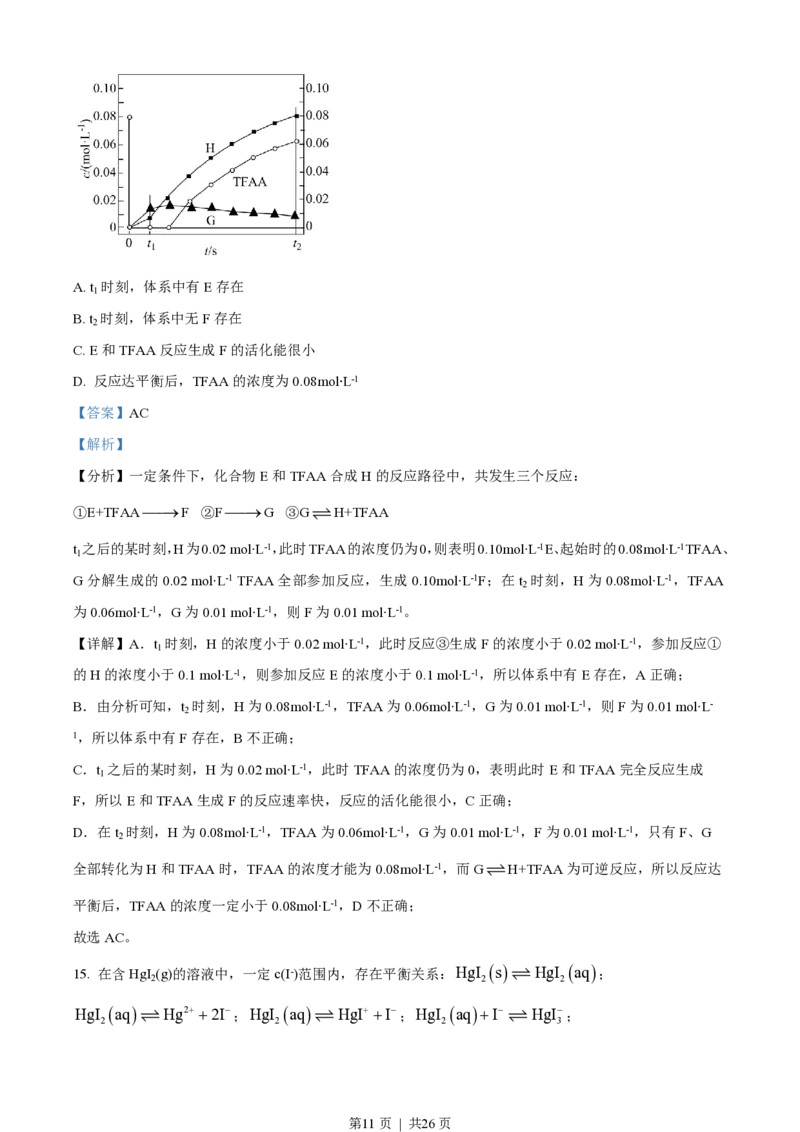
14. 一定条件下,化合物E和TFAA合成H的反应路径如下:
已知反应初始E的浓度为0.10mol∙L-1,TFAA的浓度为0.08mol∙L-1,部分物种的浓度随时间的变化关系如
图所示,忽略反应过程中的体积变化。下列说法正确的是
第10页 | 共26页A. t 时刻,体系中有E存在
1
B. t 时刻,体系中无F存在
2
C. E和TFAA反应生成F的活化能很小
D. 反应达平衡后,TFAA的浓度为0.08mol∙L-1
【答案】AC
【解析】
【分析】一定条件下,化合物E和TFAA合成H的反应路径中,共发生三个反应:
①E+TFAA¾¾®F ②F¾¾®G ③G H+TFAA
ƒ
t 之后的某时刻,H为0.02 mol∙L-1,此时TFAA的浓度仍为0,则表明0.10mol∙L-1E、起始时的0.08mol∙L-1TFAA、
1
G分解生成的0.02 mol∙L-1 TFAA全部参加反应,生成0.10mol∙L-1F;在t 时刻,H为0.08mol∙L-1,TFAA
2
为0.06mol∙L-1,G为0.01 mol∙L-1,则F为0.01 mol∙L-1。
【详解】A.t 时刻,H的浓度小于0.02 mol∙L-1,此时反应③生成F的浓度小于0.02 mol∙L-1,参加反应①
1
的H的浓度小于0.1 mol∙L-1,则参加反应E的浓度小于0.1 mol∙L-1,所以体系中有E存在,A正确;
B.由分析可知,t 时刻,H为0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,则F为0.01 mol∙L-
2
1,所以体系中有F存在,B不正确;
C.t 之后的某时刻,H为0.02 mol∙L-1,此时TFAA的浓度仍为0,表明此时E和TFAA完全反应生成
1
F,所以E和TFAA生成F的反应速率快,反应的活化能很小,C正确;
D.在t 时刻,H为0.08mol∙L-1,TFAA为0.06mol∙L-1,G为0.01 mol∙L-1,F为0.01 mol∙L-1,只有F、G
2
全部转化为H和TFAA时,TFAA的浓度才能为0.08mol∙L-1,而G H+TFAA为可逆反应,所以反应达
ƒ
平衡后,TFAA的浓度一定小于0.08mol∙L-1,D不正确;
故选AC。
15. 在含HgI 2 (g)的溶液中,一定c(I-)范围内,存在平衡关系:HgI 2 s ƒ HgI 2 aq ;
HgI
2
aq
ƒ
Hg2+ +2I-;HgI
2
aq
ƒ
HgI+ +I-;HgI
2
aq+I-
ƒ
HgI
3
-;
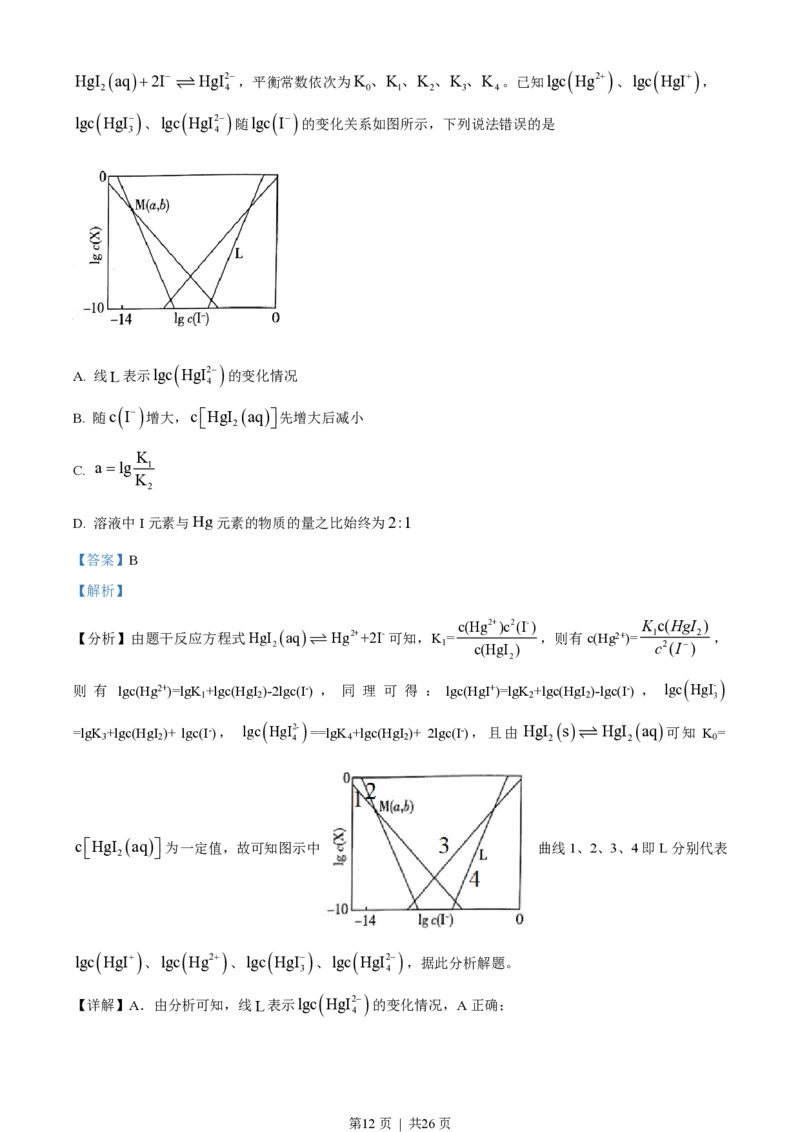
第11页 | 共26页HgI 2 aq+2I- ƒ HgI2 4 -,平衡常数依次为K 0 、K 1 、K 2 、K 3 、K 4 。已知lgc Hg2+ 、lgc HgI+ ,
lgc
HgI-
、lgc
HgI2-
随lgc
I-
的变化关系如图所示,下列说法错误的是
3 4
A. 线L表示lgc
HgI2-
的变化情况
4
B. 随c I- 增大,cé ë HgI 2 aqù û 先增大后减小
K
C. a =lg 1
K
2
D. 溶液中I元素与Hg元素的物质的量之比始终为2:1
【答案】B
【解析】
c(Hg2+)c2(I-) K c(HgI )
【分析】由题干反应方程式HgI aq Hg2++2I-可知,K = ,则有c(Hg2+)= 1 2 ,
2 ƒ 1 c(HgI ) c2(I-)
2
则 有 lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-) , 同 理 可 得 : lgc(HgI+)=lgK +lgc(HgI )-lgc(I-) , lgc
HgI-
1 2 2 2 3
=lgK 3 +lgc(HgI 2 )+ lgc(I-), lgc HgI2 4 - ==lgK 4 +lgc(HgI 2 )+ 2lgc(I-),且由 HgI 2 s ƒ HgI 2 aq 可知 K 0 =
cé
ë
HgI
2
aqù
û
为一定值,故可知图示中 曲线1、2、3、4即L分别代表
lgc
HgI+
、lgc
Hg2+
、lgc
HgI-
、lgc
HgI2-
,据此分析解题。
3 4
【详解】A.由分析可知,线L表示lgc
HgI2-
的变化情况,A正确;
4
第12页 | 共26页B.已知HgI 2 s ƒ HgI 2 aq 的化学平衡常数K 0 =cé ë HgI 2 aqù û ,温度不变平衡常数不变,故随c I-
增大,cé
ë
HgI
2
aqù
û
始终保持不变,B错误;
C.由分析可知,曲线1方程为:lgc(Hg2+)=lgK +lgc(HgI )-2lgc(I-),曲线2方程为:
1 2
lgc(HgI+)=lgK +lgc(HgI )-lgc(I-)即有①b= lgK +lgc(HgI )-2a,②b= lgK +lgc(HgI )-a,联合①②可知得:
2 2 1 2 2 2
K
a=lgK -lgK =lg 1 ,C正确;
1 2 K
2
D.溶液中的初始溶质为HgI ,根据原子守恒可知,该溶液中I元素与Hg元素的物质的量之比始终为
2
2:1,D正确;
故答案为:B。
三、非选择题:本题共 5小题,共 60分。
16. 卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1)-40℃时,F 与冰反应生成HOF 利HF。常温常压下,HOF 为无色气体,固态HOF 的晶体类型
2
为_____,HOF 水解反应的产物为_____(填化学式)。
(2)ClO 中心原子为Cl,Cl O中心原子为O,二者均为V 形结构,但ClO 中存在大π键
Π5
。
2 2 2 3
ClO 中Cl原子的轨道杂化方式_____;为O-Cl-O键角_____Cl-O-Cl键角(填“>”“ <”或
2
“=”)。比较ClO 与Cl O中Cl-O键的键长并说明原因_____。
2 2
(3)一定条件下,CuCl 、K和F 反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图所
2 2
示(晶胞参数a =b¹c,α =β= γ =90°),其中Cu化合价为+2。上述反应的化学方程式为_____。若阿伏
加德罗常数的值为N ,化合物X的密度ρ= _____g×cm-3(用含N 的代数式表示)。
A A
【答案】(1) ①. 分子晶体 ②. HF 、H O 和O
2 2 2
(2) ①. sp2 ②. > ③. ClO 分子中Cl-O键的键长小于Cl O中Cl-O键的键长,其原因
2 2
第13页 | 共26页是:ClO 分子中既存在σ键,又存在大π键,原子轨道重叠的程度较大,因此其中Cl-O键的键长较小,
2
而Cl O只存在普通的σ键。
2
436´1030
(3) ①. CuCl +4K+2F =K CuF +2KCl ②.
2 2 2 4 a2cN
A
【解析】
【小问1详解】
常温常压下,HOF为无色气体,则HOF的沸点较低,因此,固态HOF的晶体类型为分子晶体。HOF
分子中F显-1价,其水解时结合H O电离的H+生成HF,则OH+结合H O电离的OH- ,两者反应生成
2 2
H O ,H O 不稳定,其分解生成O ,因此,HOF水解反应的产物为HF 、H O 和O 。
2 2 2 2 2 2 2 2
【小问2详解】
ClO 中心原子为Cl,Cl O中心原子为O,二者均为V形结构,但ClO 中存在大π键(P5)。由ClO 中
2 2 2 3 2
存在P5可以推断,其中Cl原子只能提供1对电子,有一个O原子提供1个电子,另一个O原子提供1对
3
电子,这5个电子处于互相平行的p轨道中形成大π键,Cl提供孤电子对与其中一个O形成配位键,与
另一个O形成的是普通的共价键(σ键,这个O只提供了一个电子参与形成大π键), Cl的价层电子对
数为3,则Cl原子的轨道杂化方式为sp2;Cl O中心原子为O,根据价层电子对的计算公式可知
2
6+1´2
n = =4,因此,O的杂化方式为sp3;根据价层电子对互斥理论可知,n =4时,价电子对的几
2
何构型为正四面体,n =3时,价电子对的几何构型平面正三角形,sp2杂化的键角一定大于sp3的,因
此,虽然ClO 和Cl O均为V 形结构,但O-Cl-O键角大于Cl-O-Cl键角,孤电子对对成键电子对
2 2
的排斥作用也改变不了这个结论。ClO 分子中Cl-O键的键长小于Cl O中Cl-O键的键长,其原因
2 2
是:ClO 分子中既存在σ键,又存在大π键,原子轨道重叠的程度较大,因此其中Cl-O键的键长较
2
小,而Cl O只存在普通的σ键。
2
【小问3详解】
一定条件下,CuCl 、K和F 反应生成KCl和化合物X。已知X属于四方晶系,其中Cu化合价为+2。由
2 2
1 1 1
晶胞结构图可知,该晶胞中含有黑球的个数为8´ +2=4、白球的个数为16´ +4´ +2=8、灰色球
4 4 2
第14页 | 共26页1
的个数为8´ +1=2,则X中含有3种元素,其个数比为1:2:4,由于其中Cu化合价为+2、F的化合价为-
8
1、K 的化合价为+1,根据化合价代数和为 0,可以推断 X 为K CuF ,上述反应的化学方程式为
2 4
2´218
CuCl +4K+2F =K CuF +2KCl。若阿伏加德罗富数的值为N ,晶胞的质量为 g,晶胞的体
2 2 2 4 A N
A
2´218
g
积为a2cpm3 =a2c´10-30cm3,化合物X的密度 N 436´1030 g×cm-3。
r= A =
a2c´10-30cm3 a2cN
A
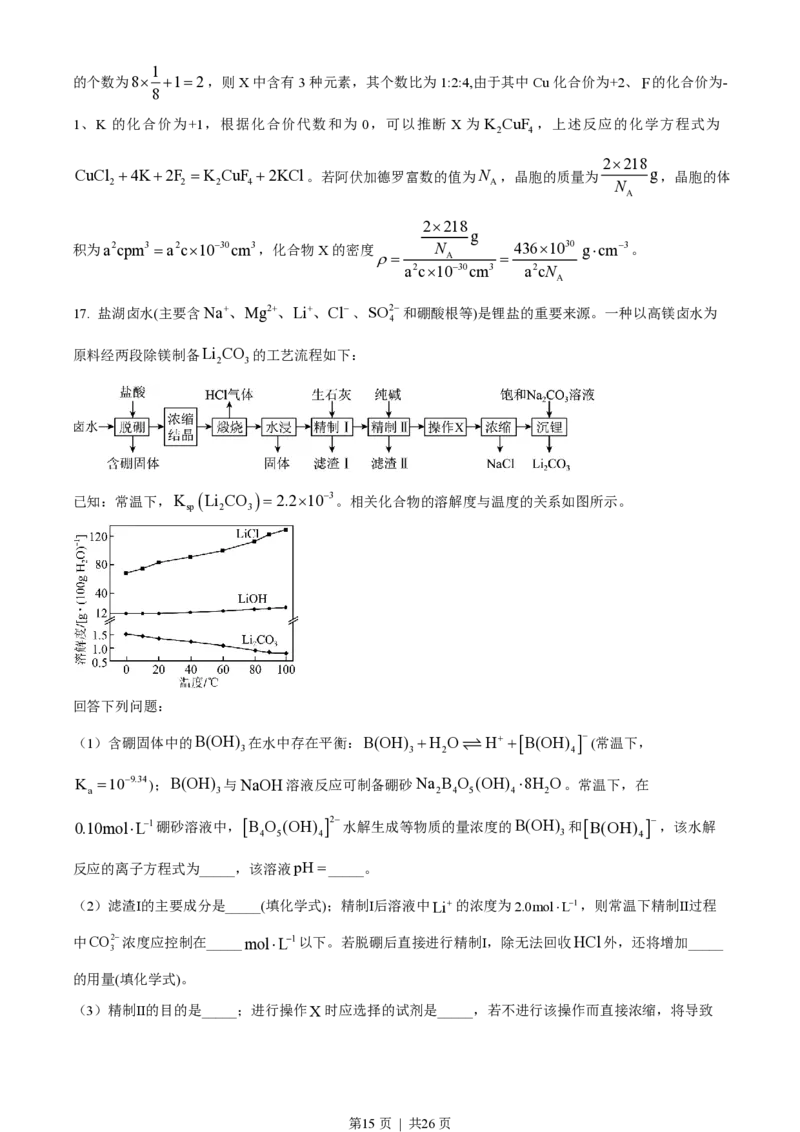
17. 盐湖卤水(主要含Na+、Mg2+、Li+、Cl-、SO2-和硼酸根等)是锂盐的重要来源。一种以高镁卤水为
4
原料经两段除镁制备Li CO 的工艺流程如下:
2 3
已知:常温下,K Li CO =2.2´10-3。相关化合物的溶解度与温度的关系如图所示。
sp 2 3
回答下列问题:
(1)含硼固体中的B(OH) 在水中存在平衡:B(OH) +H O H+ +B(OH) - (常温下,
3 3 2 ƒ 4
K =10-9.34);B(OH) 与NaOH溶液反应可制备硼砂Na B O (OH) ×8H O。常温下,在
a 3 2 4 5 4 2
0.10mol×L-1硼砂溶液中,B O (OH) 2- 水解生成等物质的量浓度的B(OH) 和B(OH) - ,该水解
4 5 4 3 4
反应的离子方程式为_____,该溶液pH=_____。
(2)滤渣Ⅰ的主要成分是_____(填化学式);精制Ⅰ后溶液中Li+的浓度为2.0mol×L-1,则常温下精制Ⅱ过程
中CO2-浓度应控制在_____mol×L-1以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,还将增加_____
3
的用量(填化学式)。
(3)精制Ⅱ的目的是_____;进行操作X时应选择的试剂是_____,若不进行该操作而直接浓缩,将导致
第15页 | 共26页_____。
【答案】(1) ①. [B O OH ]2- +5H O=2BOH +2[BOH ]- ②. 9.34
4 5 4 2 3 4
(2) ①. CaSO 、Mg(OH) ②. 5.5´10-4 ③. 纯碱
4 2
(3) ①. 加入纯碱将精制Ⅰ所得滤液中的Ca2+转化为CaCO (或除去精制Ⅰ所得滤液中的Ca2+),提
3
高Li CO 纯度 ②. 盐酸 ③. 浓缩液中因CO2-浓度过大使得Li+过早沉淀,即浓缩结晶得到的
2 3 3
NaCl中会混有Li CO ,最终所得Li CO 的产率减小
2 3 2 3
【解析】
【分析】由流程可知,卤水中加入盐酸脱硼后过滤,所得滤液经浓缩结晶后得到晶体,该晶体中含有Na+、
Li+、Cl-、SO2-等,焙烧后生成HCl气体;烧渣水浸后过滤,滤液中加生石灰后产生沉淀,在此条件下溶
4
解度最小的是CaSO ,则滤渣Ⅰ的主要成分为CaSO ;由于CaSO 微溶于水,精制Ⅰ所得滤液中再加纯碱
4 4 4
又生成沉淀,则滤渣Ⅱ为CaCO ;精制Ⅱ所得滤液经操作X后,所得溶液经浓缩结晶、过滤得到氯化钠,
3
浓缩后的滤液中加入饱和碳酸钠溶液沉锂,得到Li CO 。
2 3
【小问1详解】
含硼固体中的BOH 在水中存在平衡:BOH +H Oˆˆ†[BOH ]- +H+ (常温下,K =10-9.34);
3 3 2 ‡ˆˆ 4
BOH 与NaOH溶液反应可制备硼砂Na B O OH ×8H O。常温下.在0.10mol×L-1硼砂溶液中,
3 2 4 5 4 2
[B O OH ]2-水解生成等物质的量浓度的BOH 和[BOH ]-,该水解反应的离子方程式为
4 5 4 3 4
[B O OH ]2- +5H O=2BOH +2[BOH ]-,由B元素守恒可知,BOH 和[BOH ]-的浓度
4 5 4 2 3 4 3 4
c ×c(H+)
均为0.20mol×L-1,K =
[BOH
4
]-
=c(H+)=10-9.34,则该溶液pH=9.34。
c
BOH
3
【小问2详解】
由分析可知,滤渣I的主要成分是CaSO 、Mg(OH) ;精制I后溶液中Li+的浓度为2.0mol×L-1,由
4 2
2.2´10-3
K Li CO =2.2´10-3可知,则常温下精制Ⅱ过程中CO2-浓度应控制在 mol×L-1 =5.5´10-4
sp 2 3 3 2.02
mol×L-1以下。若脱硼后直接进行精制Ⅰ,除无法回收HCl外,后续在浓缩结晶时将生成更多的氯化钠晶
体,因此,还将增加纯碱(Na CO )的用量。
2 3
第16页 | 共26页【小问3详解】
精制Ⅰ中,烧渣水浸后的滤液中加生石灰后产生的滤渣Ⅰ的主要成分为CaSO ;由于CaSO 微溶于水,精
4 4
制Ⅰ所得滤液中还含有一定浓度的Ca2+,还需要除去Ca2+,因此,精制Ⅱ的目的是:加入纯碱将精制Ⅰ所得
滤液中的Ca2+转化为CaCO (或除去精制Ⅰ所得滤液中的Ca2+),提高Li CO 纯度。操作X是为了除去
3 2 3
剩余的碳酸根离子,为了防止引入杂质离子,应选择的试剂是盐酸;加入盐酸的目的是除去剩余的碳酸根
离子,若不进行该操作而直接浓缩,将导致浓缩液中因CO2-浓度过大使得Li+过早沉淀,即浓缩结晶得到
3
的NaCl中会混有Li CO ,最终所得Li CO 的产率减小。
2 3 2 3
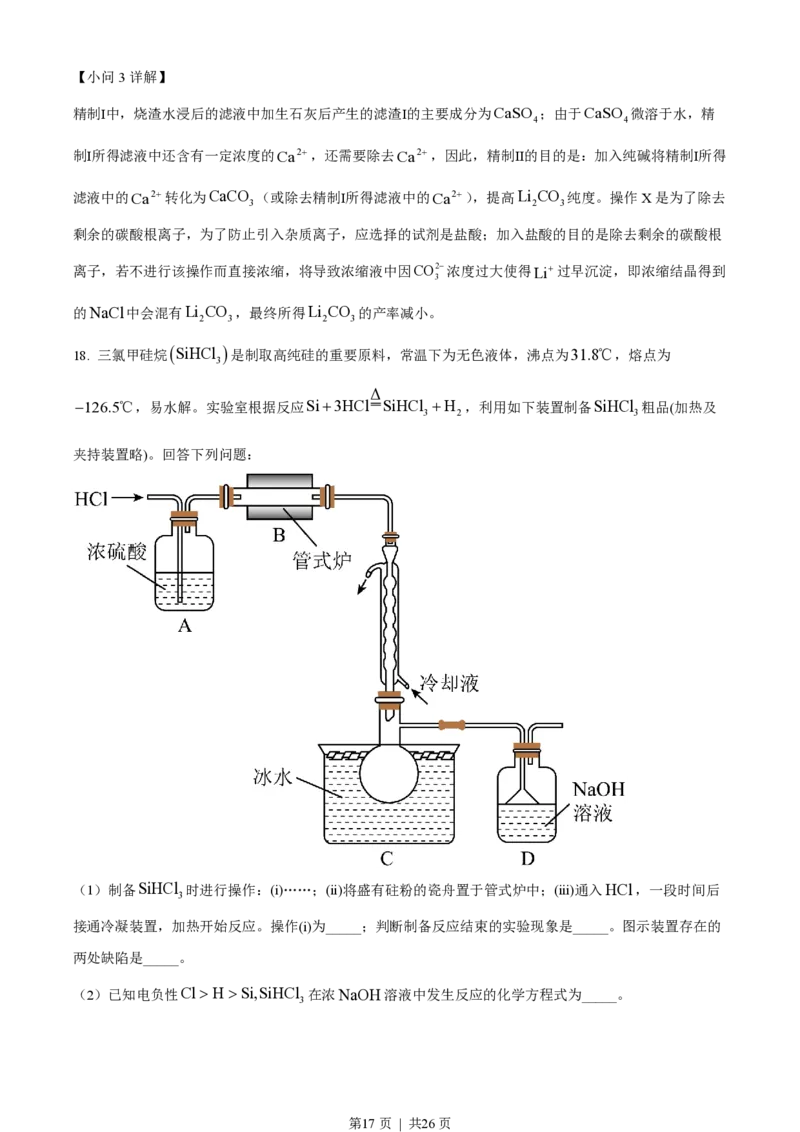
18. 三氯甲硅烷 SiHCl 是制取高纯硅的重要原料,常温下为无色液体,沸点为31.8℃,熔点为
3
Δ
-126.5℃,易水解。实验室根据反应Si+3HCl SiHCl +H ,利用如下装置制备SiHCl 粗品(加热及
3 2 3
夹持装置略)。回答下列问题:
(1)制备SiHCl 时进行操作:(ⅰ)……;(ⅱ)将盛有砫粉的瓷舟置于管式炉中;(ⅲ)通入HCl,一段时间后
3
接通冷凝装置,加热开始反应。操作(ⅰ)为_____;判断制备反应结束的实验现象是_____。图示装置存在的
两处缺陷是_____。
(2)已知电负性Cl> H >Si,SiHCl 在浓NaOH溶液中发生反应的化学方程式为_____。
3
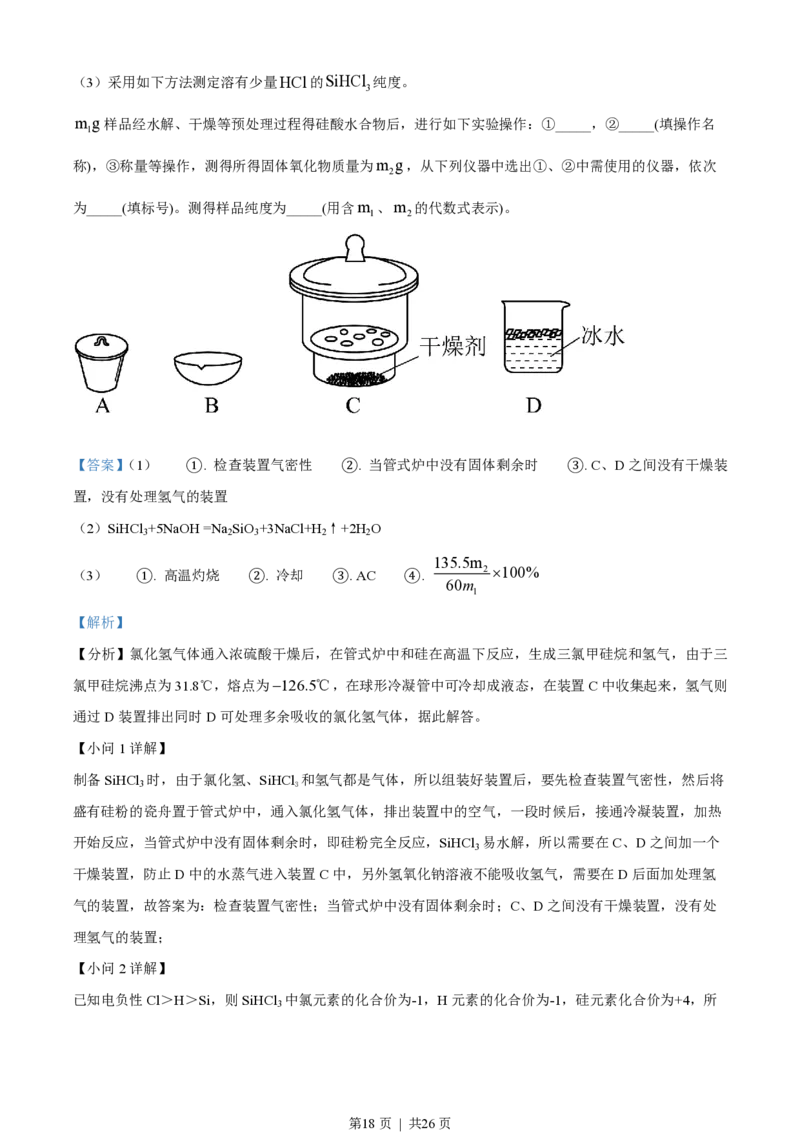
第17页 | 共26页(3)采用如下方法测定溶有少量HCl的SiHCl 纯度。
3
m g样品经水解、干燥等预处理过程得硅酸水合物后,进行如下实验操作:①_____,②_____(填操作名
1
称),③称量等操作,测得所得固体氧化物质量为m g,从下列仪器中选出①、②中需使用的仪器,依次
2
为_____(填标号)。测得样品纯度为_____(用含m 、m 的代数式表示)。
1 2
【答案】(1) ①. 检查装置气密性 ②. 当管式炉中没有固体剩余时 ③. C、D之间没有干燥装
置,没有处理氢气的装置
(2)SiHCl +5NaOH =Na SiO +3NaCl+H ↑+2H O
3 2 3 2 2
135.5m
(3) ①. 高温灼烧 ②. 冷却 ③. AC ④. 2 ´100%
60m
1
【解析】
【分析】氯化氢气体通入浓硫酸干燥后,在管式炉中和硅在高温下反应,生成三氯甲硅烷和氢气,由于三
氯甲硅烷沸点为31.8℃,熔点为-126.5℃,在球形冷凝管中可冷却成液态,在装置C中收集起来,氢气则
通过D装置排出同时D可处理多余吸收的氯化氢气体,据此解答。
【小问1详解】
制备SiHCl 时,由于氯化氢、SiHCl 和氢气都是气体,所以组装好装置后,要先检查装置气密性,然后将
3 3
盛有硅粉的瓷舟置于管式炉中,通入氯化氢气体,排出装置中的空气,一段时候后,接通冷凝装置,加热
开始反应,当管式炉中没有固体剩余时,即硅粉完全反应,SiHCl 易水解,所以需要在C、D之间加一个
3
干燥装置,防止D中的水蒸气进入装置C中,另外氢氧化钠溶液不能吸收氢气,需要在D后面加处理氢
气的装置,故答案为:检查装置气密性;当管式炉中没有固体剩余时;C、D之间没有干燥装置,没有处
理氢气的装置;
【小问2详解】
已知电负性Cl>H>Si,则SiHCl 中氯元素的化合价为-1,H元素的化合价为-1,硅元素化合价为+4,所
3
第18页 | 共26页以氢氧化钠溶液和SiHCl 反应时,要发生氧化还原反应,得到氯化钠、硅酸钠和氢气,化学方程式为:
3
SiHCl +5NaOH =Na SiO +3NaCl+H ↑+2H O,故答案为:SiHCl +5NaOH =Na SiO +3NaCl+H ↑+2H O;
3 2 3 2 2 3 2 3 2 2
【小问3详解】
m g样品经水解,干燥等预处理过程得到硅酸水合物后,高温灼烧,在干燥器中冷却后,称量,所用仪器
1
包括坩埚和干燥器,所得固体氧化物为二氧化硅,质量为m g,则二氧化硅的物质的量为n(SiO )=
2 2
m
m 2 ´(28+1+35.5´3) 135.5m
2 mol,样品纯度为 60 = 2 ´100%,故答案为:高温灼烧;冷却;
60 ´100% 60m
m 1
1
135.5m
AC; 2 ´100%。
60m
1
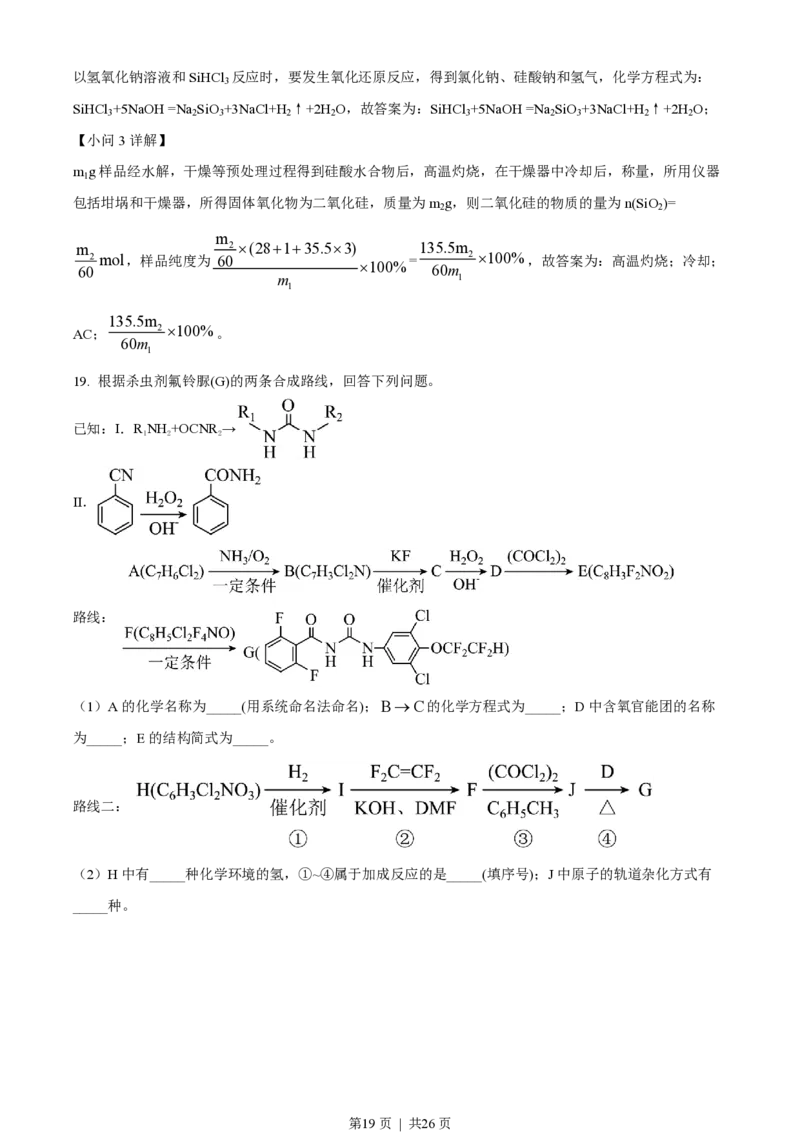
19. 根据杀虫剂氟铃脲(G)的两条合成路线,回答下列问题。
已知:Ⅰ.RNH+OCNR→
1 2 2
Ⅱ.
路线:
(1)A的化学名称为_____(用系统命名法命名);B®C的化学方程式为_____;D中含氧官能团的名称
为_____;E的结构简式为_____。
路线二:
(2)H中有_____种化学环境的氢,①~④属于加成反应的是_____(填序号);J中原子的轨道杂化方式有
_____种。
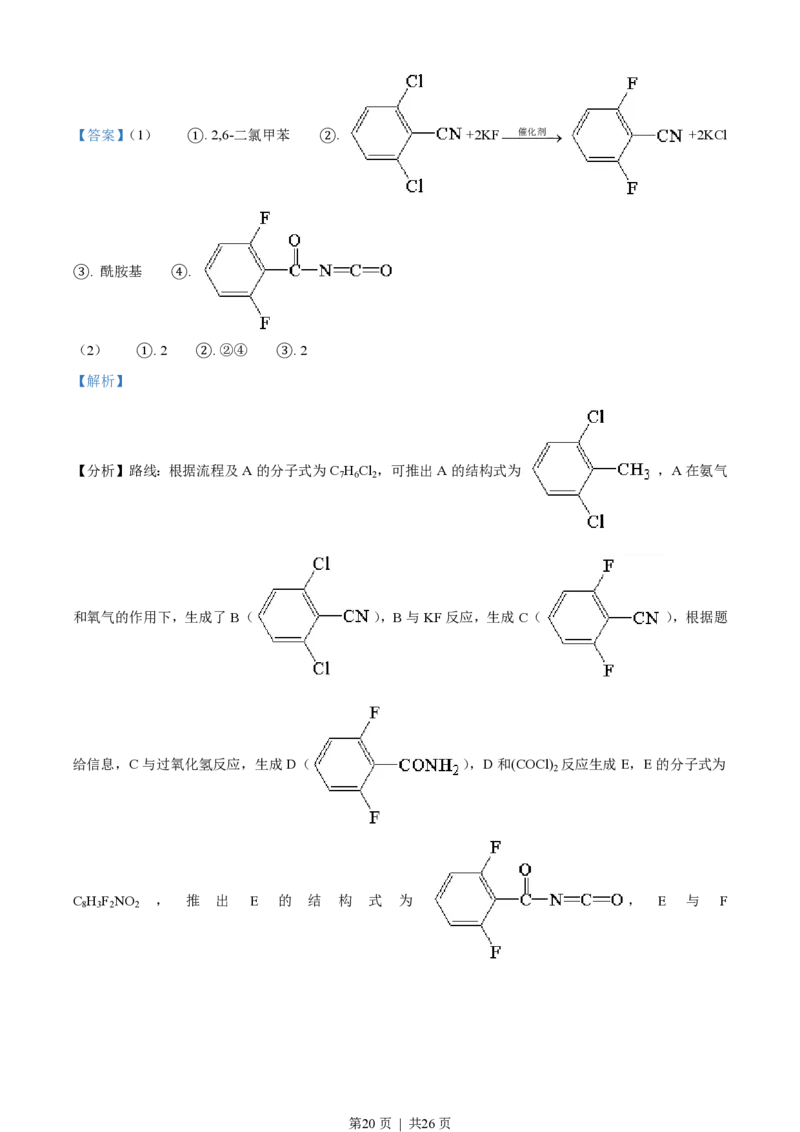
第19页 | 共26页【答案】(1) ①. 2,6-二氯甲苯 ②. +2KF¾催¾化¾剂® +2KCl
③. 酰胺基 ④.
(2) ①. 2 ②. ②④ ③. 2
【解析】
【分析】路线:根据流程及A的分子式为C H Cl ,可推出A的结构式为 ,A在氨气
7 6 2
和氧气的作用下,生成了B( ),B与KF反应,生成C( ),根据题
给信息,C与过氧化氢反应,生成D( ),D和(COCl) 反应生成E,E的分子式为
2
C H F NO , 推 出 E 的 结 构 式 为 , E 与 F
8 3 2 2
第20页 | 共26页( )反应生成了氟铃脲(G)。
路线二:
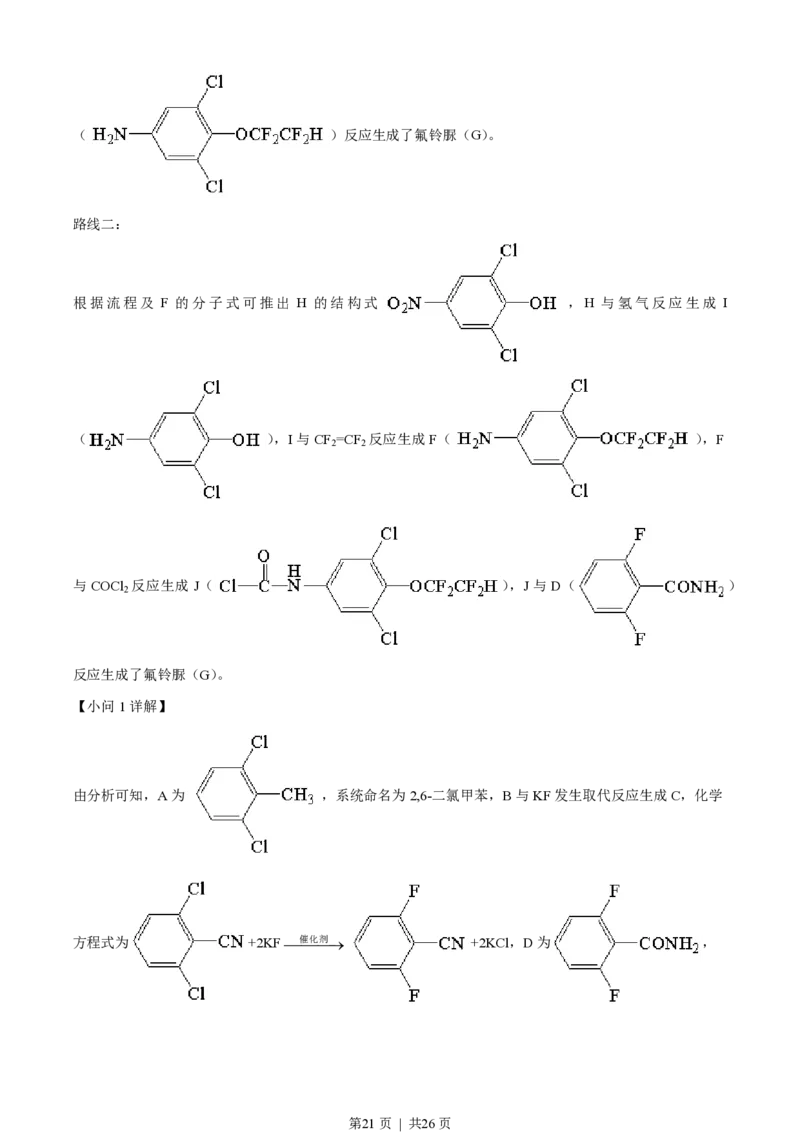
根据流程及 F 的分子式可推出 H 的结构式 ,H 与氢气反应生成 I
( ),I与CF =CF 反应生成F( ),F
2 2
与 COCl 反应生成J( ),J 与 D( )
2
反应生成了氟铃脲(G)。
【小问1详解】
由分析可知,A为 ,系统命名为2,6-二氯甲苯,B与KF发生取代反应生成C,化学
方程式为 +2KF¾催¾化¾剂® +2KCl,D为 ,
第21页 | 共26页含氧官能团为酰胺基,根据分析,E为 ,故答案为:2,6-二氯甲苯;
+2KF¾催¾化¾剂® +2KCl;酰胺基;
;
【小问2详解】
根据分析,H为 ,由结构特征可知,含有2种化学环境的氢,根据分析流程
可知H→I为还原反应,I→F为加成反应,F→J为取代反应,J→G为加成反应,J为
,C原子的杂化方式有sp2,sp3两种,N、O原子的杂化方
式均为sp3,所以J中原子的杂化方式有2种,故答案为:2;②④;2。
20. 一定条件下,水气变换反应CO+H 2 O ƒ CO 2 +H 2 的中间产物是HCOOH。为探究该反应过程,
研究HCOOH水溶液在密封石英管中的分子反应:
Ⅰ.HCOOH
ƒ
CO+H
2
O(快)
Ⅱ.HCOOH
ƒ
CO
2
+H
2
慢
研究发现,在反应Ⅰ、Ⅱ中,H+仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡
第22页 | 共26页后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为ΔH 、ΔH ,则该条件下水气变换反应的焓变ΔH=_____(用
1 2
含ΔH、ΔH 的代数式表示)。
1 2
(2)反应Ⅰ正反应速率方程为:v = kc H+ ×cHCOOH ,k为反应速率常数。T 温度下,HCOOH电
1
离平衡常数为K ,当HCOOH平衡浓度为xmol×L-1时,H+浓度为_____mol×L-1,此时反应Ⅰ应速率
a
v=_____mol×L-1×h-1(用含K 、x和k的代数式表示)。
a
(3)T 温度下,在密封石英管内完全充满1.0mol×L-1HCOOH水溶液,使HCOOH分解,分解产物均
3
完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。t 时刻测得
1
CO、CO 的浓度分别为0.70mol×L-10.16mol×L-1,反应Ⅱ达平衡时,测得H 的浓度为ymol×L-1。体
2 2
cCO
系达平衡后 =_____(用含y的代数式表示,下同),反应Ⅱ的平衡常数为_____。
cCO
2
相同条件下,若反应起始时溶液中同时还含有0.10mol×L-1盐酸,则图示点a、b、c、d中,CO的浓度
峰值点可能是_____(填标号)。与不同盐酸相比,CO达浓度峰值时,CO 浓度_____(填“增大”“减小”
2
cCO
或“不变”), 的反应_____(填“增大”“减小”或“不变”)。
cHCOOH
【答案】(1)ΔH -ΔH
2 1
(2) ①. K x ②. kx K x
a a
5-5y 6y2
(3) ①. ②. ③. a ④. 减小 ⑤. 不变
6y 1- y
【解析】
【小问1详解】
第23页 | 共26页根据盖斯定律,反应II-反应I=水气变换反应,故水气变换反应的焓变DH=ΔH -ΔH ;
2 1
【小问2详解】
T 温度时,HCOOH建立电离平衡:
1
HCOOH HCOO- + H+
ƒ
平衡浓度(mol·L-1) x c(HCOO-) c(H+)
c(HCOO-)c(H+)
K = ,c(HCOO-)=c(H+),故c(H+)= K x。
a c(HCOOH) a
v = kc H+ ×cHCOOH =kx K x 。
a
【小问3详解】
t 时刻时,c(CO)达到最大值,说明此时反应I达平衡状态。此时
1
HCOOH CO + H O
ƒ 2
t时刻转化浓度(mol·L-1) 0.70 0.70
1
HCOOH CO + H
ƒ 2 2
t时刻转化浓度(mol·L-1) 0.16 0.16 0.16
1
c(CO) 0.70
故t 时刻c(HCOOH)=1.0-0.70-0.16=0.14 mol·L-1,K(I)= = =5。t 时刻→反应II
1 c(HCOOH) 0.14 1
达平衡过程,
HCOOH CO + H O
ƒ 2
t时刻到反应II平衡
1 a a
转化浓度(mol·L-1)
HCOOH CO + H
ƒ 2 2
t时刻到反应II平衡
1 b b b
转化浓度(mol·L-1)
则c(H )=b+0.16=y,b=(y-0.16)mol·L-1,c(HCOOH)=0.14-a-b=0.3-a-y,c(CO)=a+0.7,K(I)=
2
0.8-5y
c(CO) 0.3-a- y 0.8-5y cCO +0.7 5-5y
= =5,a= 。故 = 6 = ,K(II)=
c(HCOOH) a+0.7 6 cCO 6y
2 y
c(CO )c(H ) y y 6y2
2 2 = g =
c(HCOOH) 0.8-5y 1- y 。
+0.7
6
加入0.1 mol·L-1盐酸后,H+对反应I起催化作用,加快反应I的反应速率,缩短到达平衡所需时间,故
第24页 | 共26页CO浓度峰值提前,由于时间缩短,反应Ⅱ消耗的HCOOH减小,体系中HCOOH浓度增大,导致CO浓度
大于t 时刻的峰值,故c(CO)最有可能在a处达到峰值。此时c(CO )会小于不含盐酸的浓度,
1 2
cCO cCO
=K(I),温度不变,平衡常数不变,则 的值不变。
cHCOOH cHCOOH
第25页 | 共26页第26页 | 共26页