偏差报告写作AI提示词框架(GMP合规版):5个场景变体,附实测说明和注意事项
覆盖5类偏差场景的可直接复制提示词,符合21 CFR 211.192 / GMP第七章 / ICH Q10偏差管理要求,在主流AI模型上实测有效。
使用前:选对场景
根据偏差类型选对应提示词,不要混用。
▼ 表1:5个场景速查索引
场景判断有疑问时,优先选最接近的类型,再在【偏差描述】字段补充细节
使用步骤(共3步)
Step 1:复制对应场景的提示词
粘贴进 Claude / GPT-4o / Kimi 的对话框,不要修改结构。
Step 2:替换所有【大括号内的变量】
见下方变量说明表,每个变量都必须填写,不要留空或填”/”。
Step 3:将AI输出粘贴进偏差系统,人工审核每项内容后签名
AI输出为初稿,不可直接作为最终记录使用,须由有资质QA人员复核并留痕。
▼ 表2:提示词变量说明(所有场景通用)
变量填得越具体,AI生成的内容越接近可用状态;模糊变量是导致初稿质量差的首要原因
5个场景提示词(复制即用)
提示词 A:生产过程参数偏差
适用:混合时间、压片压力、灭菌温度等工艺参数超出规定范围
📋 提示词A(可直接复制)|
你是一名有10年经验的GMP质量专员,负责起草符合{GMP版本}要求的偏差报告初稿。
【偏差基本信息】
品种名称:{品种名称}
批号:{批号}
生产步骤:{生产步骤,如:湿法制粒-混合}
偏差发现时间:{YYYY-MM-DD HH:MM}
偏差描述:{客观描述发生了什么,不加原因判断}
【参数信息】
规格要求:{参数名称} {规格要求,含单位}
实测值:{实测值,含单位}
超限持续时间:{如已知,填写分钟数;如未知,填"待确认"}
涉及设备编号:{设备ID}
【请生成以下内容】
1. 偏差描述(100字以内,客观事实,不含原因推断)
2. 即时控制措施(已采取的,条列式,每项注明负责人职位)
3. 初步影响评估(对本批次质量的直接影响,高/中/低风险分级,附简要依据)
4. 建议的根本原因分析方向(列出3—5个待调查方向,不要下结论)
5. 建议的CAPA措施框架(纠正措施 + 预防措施各2—3条,注明负责部门)
6. {GMP版本}下本类偏差的法规符合性核查清单(列出需核对的具体条款编号)
【输出要求】
- 使用第三人称叙述,不用"我"
- 所有推测性内容加"建议调查"或"待确认"标注
- 不生成最终批次处置结论(放行/报废由QA决策,不由AI决定)
提示词 B:检验结果OOS初步偏差
适用:成品检验、中间品检验、稳定性样品出现超规格结果,仅用于开立偏差记录阶段,不替代USP 1058 Phase I调查流程
📋 提示词B(可直接复制)|
你是一名熟悉USP 1058和{GMP版本}的QC检验专员,帮助起草OOS初步偏差记录。
【检验信息】
品种名称:{品种名称}
批号:{批号}
检验项目:{如:含量、溶出度、微生物限度}
检验方法编号:{内部方法编号或药典方法,如CP2025-0XXX}
检验日期:{YYYY-MM-DD}
检验人员:{工号或代码,不要真实姓名}
【结果信息】
规格要求:{规格要求,如:90.0—110.0%}
实测结果:{实测值,含单位;如有复测,一并列出}
是否已完成Phase I实验室调查:{是/否/进行中}
Phase I初步结论(如已完成):{排除/未排除实验室误差}
【请生成以下内容】
1. OOS偏差描述(80字以内,只描述结果,不判断原因)
2. 即时控制措施(样品留存、通知相关部门等,条列式)
3. Phase I调查清单(依据USP 1058,列出应核查的10项实验室误差来源)
4. 如Phase I未排除实验室误差,建议进入Phase II的调查方向(3—5条)
5. 批次风险初步分级(仅基于检验数据偏离程度,不涉及最终处置)
6. 需同步通知的部门清单(含通知时限建议,依据{GMP版本}要求)
【特别说明给AI】
- 不生成"批次合格/不合格"结论,此项由QA负责人决定
- 不生成召回建议,此项需监管申报流程支撑
- Phase II调查方向仅为建议,不作为调查结论
提示词 C:设备故障引发偏差
适用:生产或检验过程中设备报警、停机、异常读数,且已影响正在生产的批次
📋 提示词C(可直接复制)|
你是熟悉{GMP版本}设备管理要求的质量专员,起草设备故障偏差报告初稿。
【设备信息】
设备名称及编号:{设备名称} {设备ID}
设备验证状态:{已验证/验证有效期至YYYY-MM-DD}
最近一次维护日期:{YYYY-MM-DD}
故障现象:{报警代码或异常现象描述,如"E04温度超限报警,实测102℃,设定上限100℃"}
【生产影响信息】
故障发生时间:{YYYY-MM-DD HH:MM}
影响批次:{批号,如无影响填"无"}
故障时该批次生产状态:{如:湿法制粒第3步,已完成约60%}
已采取的紧急措施:{如:暂停生产、样品隔离等}
【请生成以下内容】
1. 偏差描述(客观、简洁,100字以内)
2. 设备故障对批次质量的初步影响评估(按GMP设备验证章节要求框架)
3. 设备故障根本原因分析方向(从人/机/料/法/环五个维度各列1—2个方向)
4. 设备恢复使用前需完成的确认项清单(含再验证触发条件判断)
5. CAPA建议(设备维护程序更新、人员培训、预防性维护频率调整等)
6. 是否需要触发产品质量回顾或监管报告的初步判断依据(不作最终结论)
【格式要求】
每项内容前标注对应的GMP条款编号({GMP版本}版本),便于审核引用。
提示词 D:人员操作失误偏差
适用:操作员遗漏步骤、顺序错误、加错物料等人为失误;注意:提示词D生成内容不含对当事人的评价,根本原因聚焦系统因素
📋 提示词D(可直接复制)|
你是熟悉{GMP版本}人员管理和偏差管理要求的质量专员,起草操作失误偏差报告初稿。
【失误基本信息】
发生时间:{YYYY-MM-DD HH:MM}
品种名称:{品种名称}
批号:{批号}
生产步骤:{发生失误的工序}
失误描述:{客观描述发生了什么,不含对人员的评价性语言}
发现方式:{自我发现/复核人员发现/设备报警等}
发现时间距失误发生时间:{约X分钟/小时,如未知填"待确认"}
【SOP信息】
对应SOP编号:{SOP-XXXX,如适用}
该步骤是否有双人复核要求:{是/否}
操作人员资质状态:{已培训/培训记录编号XXXX}
【请生成以下内容】
1. 偏差描述(客观事实,不含责任判断,80字以内)
2. 失误对批次质量的直接影响评估
3. 根本原因分析(聚焦系统性原因:SOP清晰度/培训有效性/工作环境/流程设计,不针对个人)
4. CAPA建议(SOP修订/培训方案/防错机制/操作环境改善,每项注明负责部门和预期完成时间)
5. 是否属于重复性偏差的判断框架(需核查近12个月同类偏差记录)
6. 操作记录和培训记录的核查清单
【重要约束】
- 不生成针对操作人员的处罚建议
- 根本原因分析必须聚焦系统因素,不写"操作员粗心"等个人归因
- 所有结论前加"初步判断:"或"建议核查:"
提示词 E:原辅料质量偏差
适用:来料检验不合格、供应商证书异常、原料外观/理化指标偏差
📋 提示词E(可直接复制)|测试模型:Claude Sonnet 4.6 / GPT-4o
你是熟悉{GMP版本}物料管理要求的质量专员,起草原辅料质量偏差报告初稿。
【物料信息】
物料名称:{物料通用名}
供应商名称及批号:{供应商名称} / {供应商批号}
内部接收批号:{内部编号}
接收日期:{YYYY-MM-DD}
物料用途:{用于生产哪个产品,如有}
【偏差信息】
偏差发现环节:{来料目检/入库检验/生产投料前复核}
偏差描述:{客观描述,如:外观颜色偏黄,CoA显示含量98.2%,内部规格要求≥99.0%}
规格要求:{具体指标及来源,如:药典标准/内部质量标准编号}
实测结果:{实测值,含单位}
该物料当前状态:{待检/隔离/已入库-需核查}
【请生成以下内容】
1. 偏差描述(客观描述,80字以内)
2. 即时控制措施(物料隔离/暂停使用/通知供应商,条列式)
3. 已使用同批次物料的产品批次追溯清单框架(需核查的字段和来源系统)
4. 供应商调查要求清单(向供应商发出调查请求时应包含的必要信息)
5. 物料放行/拒绝的评估框架(不作最终决定,列出决策所需的信息清单)
6. 是否需要更新供应商资质评估的触发条件判断(依据{GMP版本}供应商管理要求)
7. 对注册档案的潜在影响初步核查清单(该原料是否列入注册档案,变更是否需申报)
【格式要求】
第3条物料追溯清单须以表格形式呈现,包含:批次号/生产日期/产品名称/当前状态/存放位置。
实测效果说明
测试条件:国内外主流模型Claude Sonnet 4.6 和 豆包等,针对实际偏差场景(已脱敏)。
▼ 表3:各场景实测效果评分
场景C评分偏低因为设备再验证判断涉及设备台账信息,AI无法获取企业内部数据
常见错误与修正
▼ 表4:使用中常见问题与修正方法
表中问题在实测中均出现过,修正方法已验证有效
适用范围与边界
▼ 表5:使用范围与不适用情况
生物制品偏差报告需额外覆盖批放行规程(Batch Release),建议在提示词中明确补充
本工具说明
测试时间:2026年4月。测试样本:覆盖上述5类场景的实际偏差(已脱敏处理)。提示词内容不作为法规合规的保证,具体使用须结合企业质量体系要求调整。
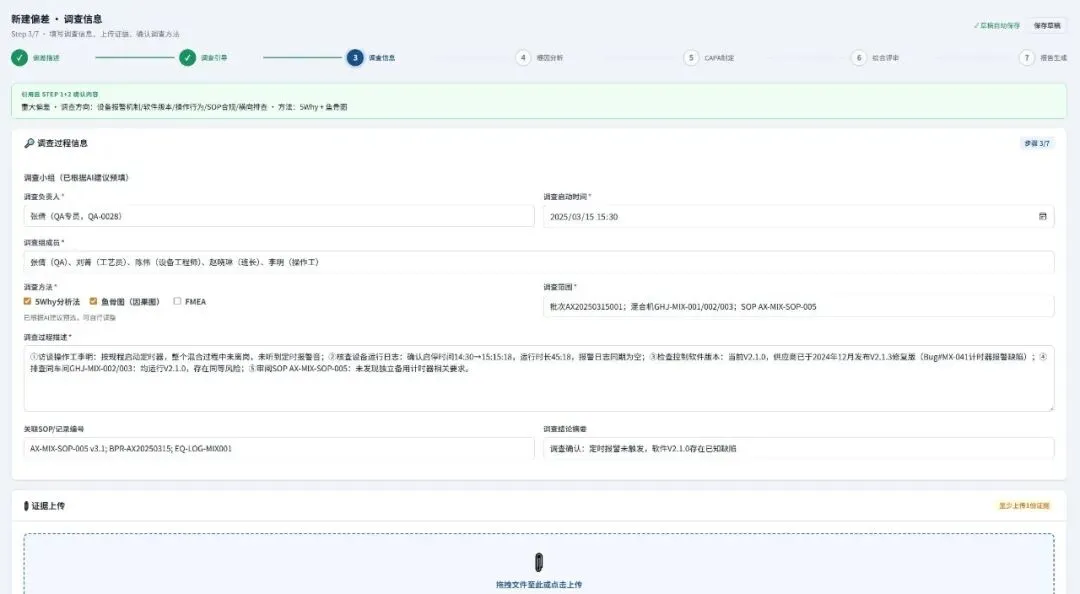
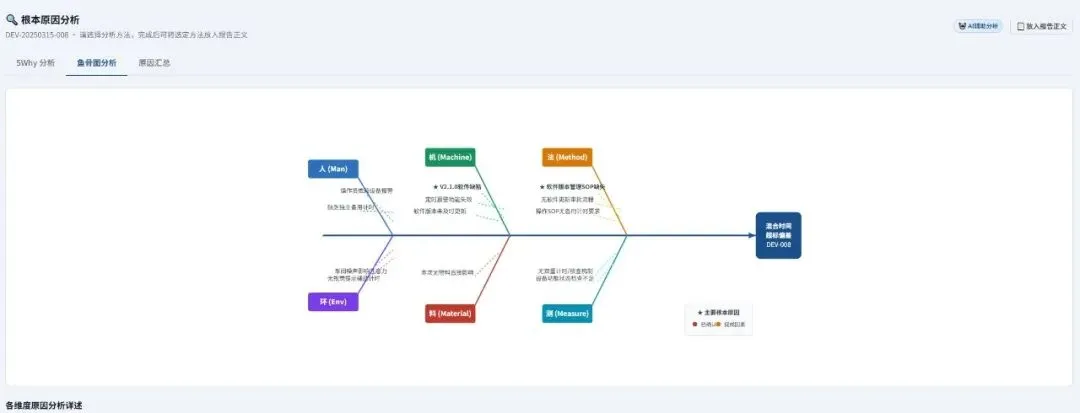
深耕AI+医药,我们开发的AI辅助偏差报告生成,已落地多家医药企业

 夜雨聆风
夜雨聆风




