文档内容
专练 13 金属材料 镁、铝及其化合物
一、选择题
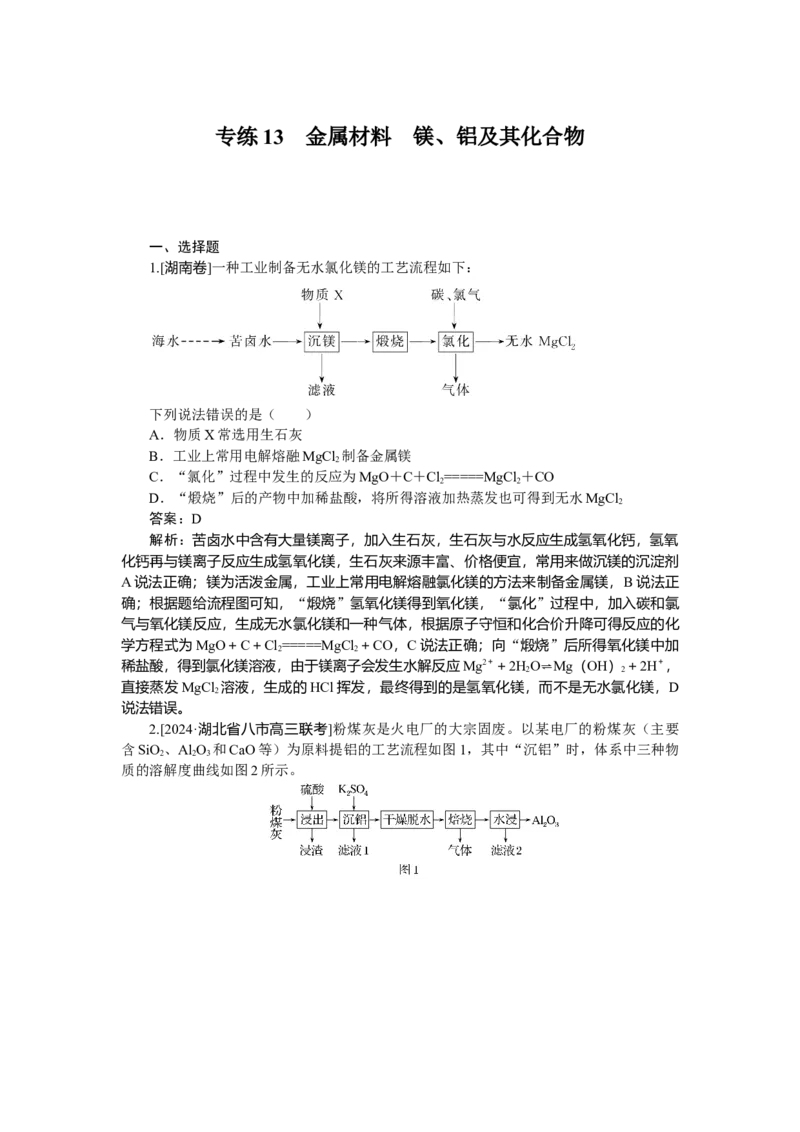
1.[湖南卷]一种工业制备无水氯化镁的工艺流程如下:
下列说法错误的是( )
A.物质X常选用生石灰
B.工业上常用电解熔融MgCl 制备金属镁
2
C.“氯化”过程中发生的反应为MgO+C+Cl=====MgCl +CO
2 2
D.“煅烧”后的产物中加稀盐酸,将所得溶液加热蒸发也可得到无水MgCl
2
答案:D
解析:苦卤水中含有大量镁离子,加入生石灰,生石灰与水反应生成氢氧化钙,氢氧
化钙再与镁离子反应生成氢氧化镁,生石灰来源丰富、价格便宜,常用来做沉镁的沉淀剂
A说法正确;镁为活泼金属,工业上常用电解熔融氯化镁的方法来制备金属镁,B说法正
确;根据题给流程图可知,“煅烧”氢氧化镁得到氧化镁,“氯化”过程中,加入碳和氯
气与氧化镁反应,生成无水氯化镁和一种气体,根据原子守恒和化合价升降可得反应的化
学方程式为MgO+C+Cl=====MgCl +CO,C说法正确;向“煅烧”后所得氧化镁中加
2 2
稀盐酸,得到氯化镁溶液,由于镁离子会发生水解反应Mg2++2H
2
O⇌Mg(OH)
2
+2H+,
直接蒸发MgCl 溶液,生成的HCl挥发,最终得到的是氢氧化镁,而不是无水氯化镁,D
2
说法错误。
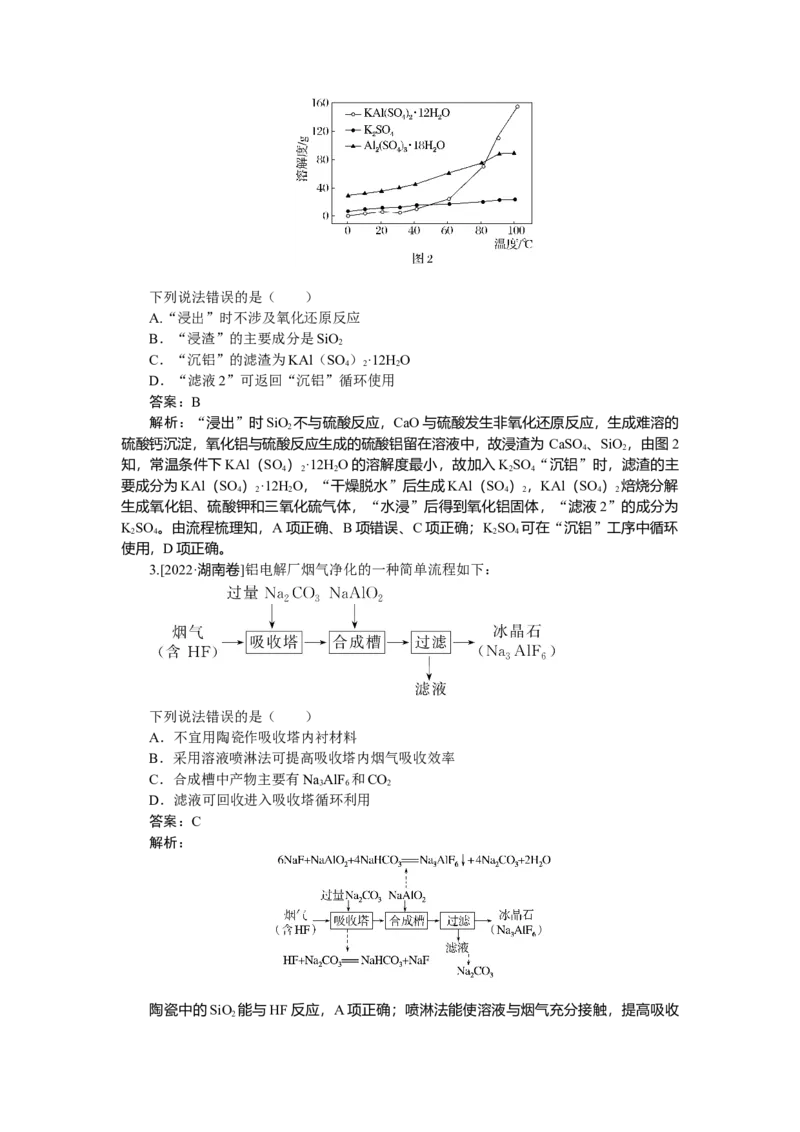
2.[2024·湖北省八市高三联考]粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰(主要
含SiO 、Al O 和CaO等)为原料提铝的工艺流程如图1,其中“沉铝”时,体系中三种物
2 2 3
质的溶解度曲线如图2所示。下列说法错误的是( )
A.“浸出”时不涉及氧化还原反应
B.“浸渣”的主要成分是SiO
2
C.“沉铝”的滤渣为KAl(SO )·12H O
4 2 2
D.“滤液2”可返回“沉铝”循环使用
答案:B
解析:“浸出”时SiO 不与硫酸反应,CaO与硫酸发生非氧化还原反应,生成难溶的
2
硫酸钙沉淀,氧化铝与硫酸反应生成的硫酸铝留在溶液中,故浸渣为 CaSO、SiO,由图2
4 2
知,常温条件下KAl(SO ) ·12H O的溶解度最小,故加入KSO “沉铝”时,滤渣的主
4 2 2 2 4
要成分为KAl(SO ) ·12H O,“干燥脱水”后生成KAl(SO ) ,KAl(SO ) 焙烧分解
4 2 2 4 2 4 2
生成氧化铝、硫酸钾和三氧化硫气体,“水浸”后得到氧化铝固体,“滤液2”的成分为
KSO 。由流程梳理知,A项正确、B项错误、C项正确;KSO 可在“沉铝”工序中循环
2 4 2 4
使用,D项正确。
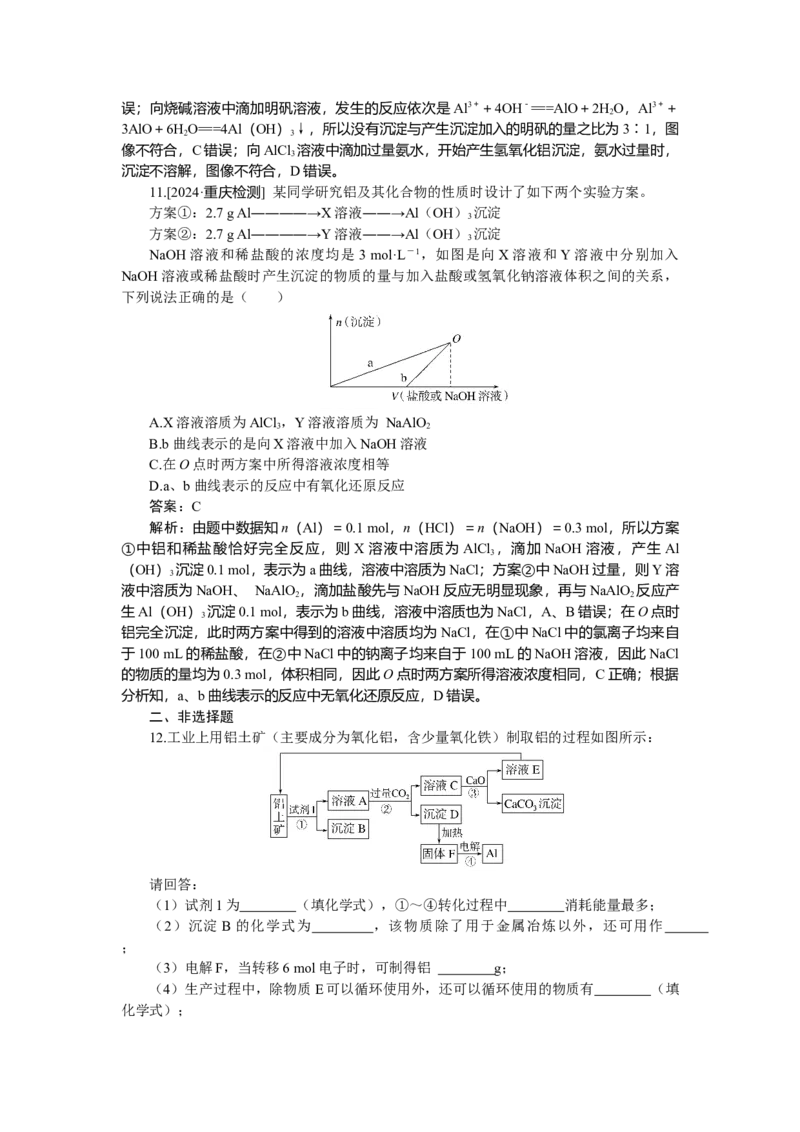
3.[2022·湖南卷]铝电解厂烟气净化的一种简单流程如下:
下列说法错误的是( )
A.不宜用陶瓷作吸收塔内衬材料
B.采用溶液喷淋法可提高吸收塔内烟气吸收效率
C.合成槽中产物主要有NaAlF 和CO
3 6 2
D.滤液可回收进入吸收塔循环利用
答案:C
解析:
陶瓷中的SiO 能与HF反应,A项正确;喷淋法能使溶液与烟气充分接触,提高吸收
2效率,B项正确;根据流程梳理知,C项错误;滤液中含有NaCO ,可用作吸收塔中的吸
2 3
收剂,D项正确。
4.下列关于铝及其化合物的说法不正确的是( )
A.Al既可用于食品包装,也可用作建筑材料
B.Al O 既可用来冶炼金属Al,也可用作耐火材料
2 3
C.明矾[KAl(SO )·12H O] 既可用作净水剂,也可用作消毒剂
4 2 2
D.Al(OH) 既可用作治疗胃酸过多的药物,也可用来制备一些铝盐
3
答案:C
解析:Al具有良好的延展性, 可用于食品包装,也可用作建筑材料, A正确; 电
解Al O 法冶炼Al,且氧化铝的熔点高,可用作耐火材料, B正确; 铝离子水解生成胶体
2 3
具有吸附性,可用作净水剂,不具有强氧化性,不能用作消毒剂, C错误; Al(OH)
3
的碱性较弱,可与胃酸中的盐酸反应, 可用作治疗胃酸过多的药物,也可用来制备一些铝
盐, D正确。
5.通过观察化学实验现象,分析归纳出正确的结论,是学习化学学科最基本的技能之
一。下列由实验现象得出正确结论的是( )
选项 实验现象 结论
把相同大小的一块铝和镁分别投入相同浓
A 度的NaOH溶液中:铝溶解有气泡放出, 由此得出:铝的金属性比镁强
而镁没有任何变化
取一块铝箔,用酒精灯点燃:铝箔只熔化
B 由此得出:铝不易燃烧
成液体而没有脱落
向氯化铵溶液中投入一铝片:铝片上产生
C 由此得出:该气体是氨气
大量气泡
向氯化铝溶液中逐滴滴加NaOH溶液至过
D 量:先产生白色沉淀,后沉淀逐渐溶解, 由此得出:氢氧化铝能溶于强碱溶液
最后沉淀完全消失
答案:D
解析:与NaOH是否反应,不能作为衡量金属性强弱的依据,A错误;铝箔用酒精灯
点燃,铝箔外面与氧气反应生成了一层熔点较高的致密的 Al O 薄膜,阻止了内部熔化的
2 3
铝的滴落,B错误;氯化铵溶液中存在水解平衡:NH+H
2
O⇌NH
3
·H
2
O+H+,铝在酸性条
件下发生反应:2Al+6H+===2Al3++3H↑,消耗H+,使得水解平衡右移,从而使铝能够
2
与H+反应放出氢气,因此铝片上产生的气体是氢气,C错误;向氯化铝溶液中逐滴滴加
NaOH溶液,发生的化学反应为 AlCl +3NaOH===Al(OH) ↓+3NaCl,Al(OH) +
3 3 3
NaOH===NaAlO+2HO,知氢氧化铝能溶于强碱溶液,D正确。
2 2
6.[2024·山西大学附中高三模块诊断试题]向m g镁和铝的混合物中加入适量的稀硫酸,
恰好完全反应生成标准状况下的气体b L。向反应后的溶液中加入c mol·L-1氢氧化钾溶液
V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g。再将得到的沉淀灼烧至质量不
再改变为止,得到固体p g。则下列关系不正确的是( )
A.n=m+17Vc B.p=m+
C.c= D.m