文档内容
专练 21 元素化合物的综合应用
授课提示:对应学生用书41页
1.[2022·广东卷]劳动开创未来。下列劳动项目与所述的化学知识没有关联的是( )
选项 劳动项目 化学知识
A 面包师用小苏打作发泡剂烘焙面包 NaCO 可与酸反应
2 3
B 环保工程师用熟石灰处理酸性废水 熟石灰具有碱性
铁与HO高
C 工人将模具干燥后再注入熔融钢水 2
温下会反应
D 技术人员开发高端耐腐蚀镀铝钢板 铝能形成致密氧化膜
答案:A
解析:小苏打是NaHCO ,与NaCO 无关,A项符合题意;用熟石灰处理酸性废水,
3 2 3
发生酸碱中和反应,B项不符合题意;钢的主要成分是铁,铁与水高温时发生氧化还原反
应生成Fe O 和H ,C项不符合题意;铝耐腐蚀主要是因为在铝的表面易形成致密氧化膜
3 4 2
D项不符合题意。
2.[2024·北师大附属学校开学考]固体化合物X由3种元素组成,X可以与浓盐酸反应
产生黄绿色气体,固体完全溶解,得到蓝色溶液。某学习小组进行了如下实验:
下列说法不正确的是( )
A.CuSO 由白色变蓝色是化学变化
4
B.由现象1得出化合物X含有氧元素
C.固体混合物Y的成分为Cu和Na
D.X与浓盐酸反应的化学方程式为 2NaCuO +8HCl(浓)===2NaCl+2CuCl +Cl↑+
2 2 2
4HO
2
答案:C
解析:由现象1可知混合气体含水蒸气,且含过量的氢气,固体混合物Y溶于水,得
到的紫红色固体单质应为Cu,得到的碱性溶液焰色试验呈黄色,说明含有 Na元素,可以
与盐酸发生中和反应,应为NaOH,则X含有Na、Cu、O元素,2.38 g X中含Cu的物质
的量n(Cu)==0.02 mol,含Na的物质的量n(Na)=0.02 mol,含O的物质的量n(O)==
0.04 mol,则X的化学式为NaCuO 。X与氢气反应生成的混合气体含水蒸气,硫酸铜与水
2
结合生成胆矾,发生的是化学变化,A项正确;由现象1可知混合气体含水蒸气,则X含
O元素,B项正确;由现象2和3可知,固体混合物Y的成分为Cu和NaOH,C项错误;
X的化学式为NaCuO ,X与浓盐酸反应产生黄绿色气体,说明盐酸被氧化生成氯气,反应
2
的化学方程式为2NaCuO +8HCl(浓)===2NaCl+2CuCl +Cl↑+4HO,D项正确。
2 2 2 2
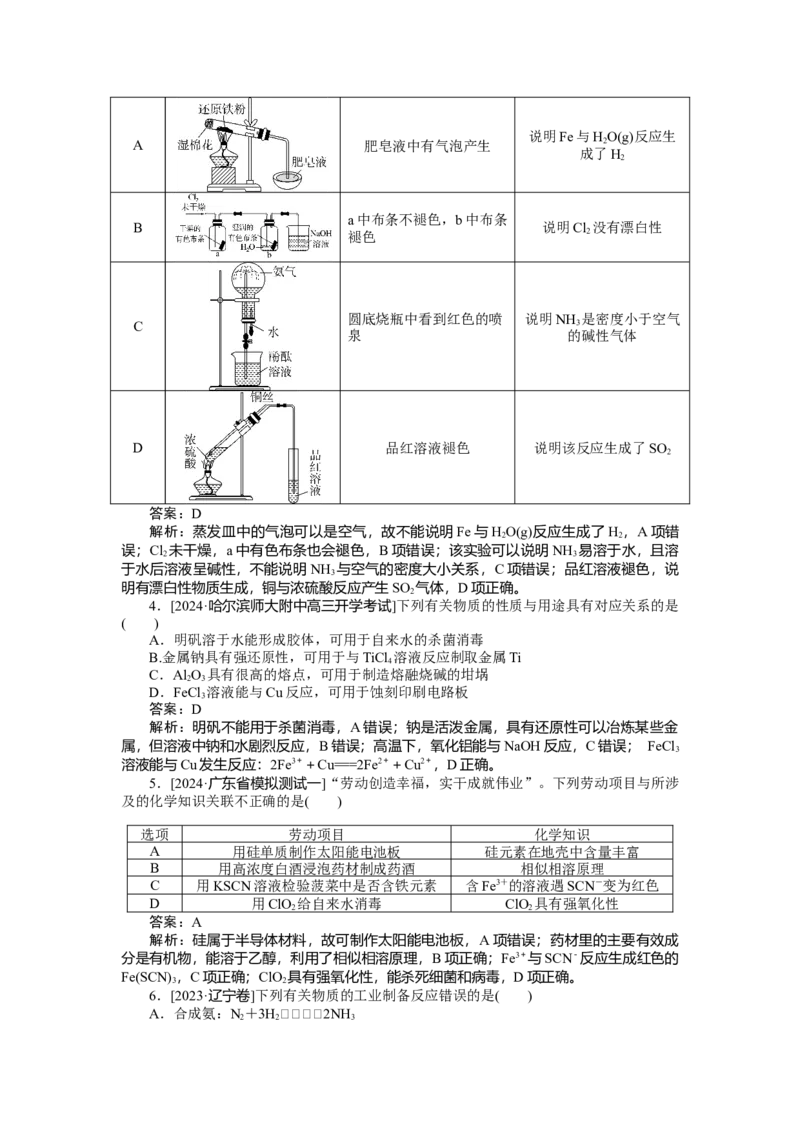
3.[2024·重庆南开中学模拟]下列实验装置、实验现象和实验结论均正确的是( )
选项 实验装置 实验现象 实验结论说明Fe与HO(g)反应生
A 肥皂液中有气泡产生 2
成了H
2
a中布条不褪色,b中布条
B 说明Cl 没有漂白性
褪色 2
圆底烧瓶中看到红色的喷 说明NH 是密度小于空气
C 3
泉 的碱性气体
D 品红溶液褪色 说明该反应生成了SO
2
答案:D
解析:蒸发皿中的气泡可以是空气,故不能说明Fe与HO(g)反应生成了H ,A项错
2 2
误;Cl 未干燥,a中有色布条也会褪色,B项错误;该实验可以说明NH 易溶于水,且溶
2 3
于水后溶液呈碱性,不能说明NH 与空气的密度大小关系,C项错误;品红溶液褪色,说
3
明有漂白性物质生成,铜与浓硫酸反应产生SO 气体,D项正确。
2
4.[2024·哈尔滨师大附中高三开学考试]下列有关物质的性质与用途具有对应关系的是
( )
A.明矾溶于水能形成胶体,可用于自来水的杀菌消毒
B.金属钠具有强还原性,可用于与TiCl 溶液反应制取金属Ti
4
C.Al O 具有很高的熔点,可用于制造熔融烧碱的坩埚
2 3
D.FeCl 溶液能与Cu反应,可用于蚀刻印刷电路板
3
答案:D
解析:明矾不能用于杀菌消毒,A错误;钠是活泼金属,具有还原性可以冶炼某些金
属,但溶液中钠和水剧烈反应,B错误;高温下,氧化铝能与NaOH反应,C错误; FeCl
3
溶液能与Cu发生反应:2Fe3++Cu===2Fe2++Cu2+,D正确。
5.[2024·广东省模拟测试一]“劳动创造幸福,实干成就伟业”。下列劳动项目与所涉
及的化学知识关联不正确的是( )
选项 劳动项目 化学知识
A 用硅单质制作太阳能电池板 硅元素在地壳中含量丰富
B 用高浓度白酒浸泡药材制成药酒 相似相溶原理
C 用KSCN溶液检验菠菜中是否含铁元素 含Fe3+的溶液遇SCN-变为红色
D 用ClO 给自来水消毒 ClO 具有强氧化性
2 2
答案:A
解析:硅属于半导体材料,故可制作太阳能电池板,A项错误;药材里的主要有效成
分是有机物,能溶于乙醇,利用了相似相溶原理,B项正确;Fe3+与SCN-反应生成红色的
Fe(SCN) ,C项正确;ClO 具有强氧化性,能杀死细菌和病毒,D项正确。
3 2
6.[2023·辽宁卷]下列有关物质的工业制备反应错误的是( )
A.合成氨:N+3H2NH
2 2 3B.制HCl:H+Cl=====2HCl
2 2
C.制粗硅:SiO+2C=====Si+2CO↑
2
D.冶炼镁:2MgO(熔融)=====2Mg+O↑
2
答案:D
解析:工业合成氨是利用氮气和氢气在催化剂的条件下反应生成的,反应方程式为N
2
+3H2NH ,A正确;工业制氯化氢是利用氢气和氯气反应生成的,反应方程式为
2 3
H +Cl=====2HCl,B正确;工业制粗硅是将SiO 与C在高温下反应生成粗硅,反应方程
2 2 2
式为SiO +2C=====Si+2CO↑,C正确;冶炼金属镁是电解熔融氯化镁,反应方程式为
2
MgCl (熔融)=====Mg+Cl↑,D错误;故答案选D。
2 2
7.下图为利用海水制备部分物质的过程。下列有关说法正确的是( )
A.制取NaHCO 的反应是利用其溶解度小于NaCl的溶解度
3
B.用澄清的石灰水可鉴别NaHCO 溶液和NaCO 溶液
3 2 3
C.在第③、④、⑤步骤中,溴元素均被氧化
D.加热MgCl 溶液制取无水氯化镁
2
答案:A
8.[2024·湖北十一校联考]生产生活中蕴藏着丰富的化学知识。下列项目与所述的化学
知识没有关联的是( )
选项 项目 化学知识
A 废旧铅酸蓄电池回收PbSO 时加入少量Fe2+ Fe2+可作该反应的催化剂
4
B 冰在室温下自动融化成水 冰融化成水时熵值增大
C 合成氨原料气进入合成塔前需经过亚铜氨溶液 亚铜氨溶液可除去CO
D BaSO 作“钡餐” BaSO 是强电解质
4 4
答案:D
解析:废旧铅酸蓄电池回收PbSO 时加入少量Fe2+,发生反应:2Fe2++PbO +4H++
4 2
SO===2Fe3++PbSO +2HO,2Fe3++Pb+SO===PbSO +2Fe2+,Fe2+作催化剂,A项项目
4 2 4
与所述的化学知识有关联;冰是固态,变为液态水时,混乱度增大,熵值增大,B项项目
与所述的化学知识有关联;合成氨工业中,原料气(N、H 及少量CO、NH 的混合气)在
2 2 3
进入合成塔前常用醋酸二氨合亚铜溶液来净化原料气,其反应为[Cu(NH ) ]OOCCH +
3 2 3
CO+NH 3⇌[Cu(NH
3
)
3
]CH
3
COO·CO,C项项目与所述的化学知识有关联;BaSO
4
作“钡
餐”,是因为BaSO 不溶于胃酸,且不被X射线透过,与其是否为强电解质无关,D项项
4
目与所述的化学知识没有关联。
9.甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转
化)。下列各组物质中,不满足下图所示转化关系的是( )
选项 甲 乙 丙 戊
A NH Cl N H
3 2 2 2
B C SiO CO CuO
2
C Al(OH) NaOH溶液 NaAlO 溶液 CO
3 2 2D 乙酸乙酯 NaOH溶液 乙醇 乙酸
答案:B
解析:B中甲是C,乙是SiO,二者发生以下反应SiO+2C=====Si+2CO↑,生成的
2 2
丙和丁是CO 和Si,CO和CuO 发生反应:CO+CuO=====Cu+CO ,不能实现丙到甲的
2
转化,故选B。
10.[2022·河北卷]LiBr溶液可作为替代氟利昂的绿色制冷剂。合成LiBr工艺流程如下:
下列说法错误的是( )
A.还原工序逸出的Br 用NaOH溶液吸收,吸收液直接返回还原工序
2
B.除杂工序中产生的滤渣可用煤油进行组分分离
C.中和工序中的化学反应为LiCO+2HBr===CO ↑+2LiBr+HO
2 3 2 2
D.参与反应的n(Br )∶n(BaS)∶n(HSO )为1∶1∶1
2 2 4
答案:A
解析:
逸出的Br 用NaOH溶液吸收后生成NaBr、NaBrO和水,若直接返回还原工序,会引
2
入杂质离子Na+,导致产品不纯,A项错误;滤渣中含S和BaSO ,单质S可溶于煤油,
4
而BaSO 不溶于煤油,故B项正确;中和工序中LiCO 与HBr反应生成LiBr、CO 和
4 2 3 2
HO,C项正确;根据Br +BaS===BaBr +S、BaBr +HSO ===BaSO ↓+2HBr知,参与
2 2 2 2 2 4 4
反应的n(Br )∶n(BaS)∶n(HSO )=1∶1∶1,D项正确。
2 2 4
11.下列实验操作与现象对应的结论不正确的是( )
选项 实验操作 实验现象 实验结论
向酸性KMnO 溶液中通入
A 4 紫红色褪去 SO 具有还原性
SO 2
2
B 向CuSO 溶液中通入HS 出现黑色沉淀 酸性:HS>HSO
4 2 2 2 4
碘在CCl 中的溶解度大于
C 向碘水中加入CCl ,振荡 上层褪色,下层变紫 4
4 它在水中的溶解度
向装有蔗糖的烧杯中加入浓
D 出现“黑面包”现象 浓HSO 具有脱水性
HSO 2 4
2 4
答案:B
解析:向酸性KMnO 溶液中通入SO ,紫红色褪去,体现SO 的还原性,A正确;向
4 2 2
CuSO 溶液中通入HS,生成CuS和硫酸,CuS不溶于硫酸,不能比较二者的酸性强弱,B
4 2
错误;根据CCl 萃取碘水中的碘单质的现象,可以说明碘在CCl 中的溶解度大于它在水中
4 4
的溶解度,C正确;向装有蔗糖的烧杯中加入浓 HSO ,出现“黑面包”现象,体现浓
2 4
HSO 的脱水性,D正确。
2 4
12.[2024·辽宁铁岭六校月考]已知A、B、C、D均为中学化学常见的物质,它们有如
图所示的反应关系,所需试剂与反应条件任选,下列说法正确的是( )A.若A是一种常见的气体,常用来制作氮肥,C、D是氧化物且会造成光化学污染,
标准状况下用试管收集D气体,倒扣在水槽中(不考虑溶质扩散),试管中所得溶液的浓
度为 mol·L-1
B.若A是应用最广泛的金属,C可用来腐蚀铜板,D是红褐色固体,则D胶体带正
电荷,因为胶粒对光线的反射而有丁达尔效应
C.若A为一元强碱且阴、阳离子所含的电子数相同,C可用于泡沫灭火器,D为日
常生活中常用的调味品,则⑤的反应原理可用于侯氏制碱法,其母液溶质中只有氯化铵
D.若A常温下是一种有臭鸡蛋气味气体,C是一种大气污染物,D是一种二元强酸,
则⑤的反应可以是铜丝和D的浓溶液反应,为了观察溶液中某产物颜色,应向反应后的溶
液中加入少量水
答案:A
解析:A是氨气,C为一氧化氮,D是二氧化氮,设试管容积为V L,根据反应3NO
2
+HO===2HNO +NO,消耗V L NO ,得到× mol HNO 和 L NO,HNO 溶液的体积为
2 3 2 3 3
L,所以HNO 的物质的量浓度为= mol·L-1,A正确;A是铁,B是氯化亚铁,C是氯化
3
铁,D是红褪色固体氢氧化铁沉淀,氢氧化铁胶体会产生丁达尔效应,是因为胶粒对光线
有散射作用,且氢氧化铁胶体不带电,其胶粒带正电荷,B错误;A是氢氧化钠,C是碳
酸氢钠,D是氯化钠,侯氏制碱法中,饱和氯化钠溶液、二氧化碳和氨气共同反应生成碳
酸氢钠和氯化铵,溶解度较低的碳酸氢钠析出,此时溶液中碳酸氢钠达到饱和,所以母液
溶质中有碳酸氢钠和氯化铵,C错误;A是硫化氢,C是二氧化硫,D是硫酸,因为反应
后溶液中有剩余的浓硫酸,若要观察溶液颜色,应在冷却后将试管里的物质慢慢倒入盛有
水的烧杯里,D错误。