文档内容
2009年广西桂林市中考化学试卷
一.慧眼识珠(单项选择题.每小题2分,共50分.用铅笔把答题卷上对应题目的答案标号涂黑,多选、错选均
不得分)
1.(2分)下列过程中,属于化学变化的是( )
A. 蜡烛燃烧 B. 冰雪融化
C. 菠萝榨汁 D. 砖头渗水
2.(2分)日常生活中加碘食盐中的“碘”是指( )
A.元素 B.分子 C.原子 D.单质
3.(2分)掌握化学用语是学好化学的关键.下列化学用语与含义相符的是( )
A.2H﹣﹣2个氢元素 B.Al O ﹣﹣氧化铝
2 3
C.O ﹣﹣2个氧原子 D. ﹣﹣一个钠离子
2
4.(2分)石英钟、电子表使用石英晶体代替传统钟表中的摆和游丝,提高了钟表计时的准确度.已知石英的
主要成分是二氧化硅(SiO ),其中硅元素的化合价为( )
2
A.+2 B.+3 C.+4 D.+6
5.(2分)能用于鉴别空气、二氧化碳和氧气的最简便方法是( )
A.用带火星的木条鉴别 B.加入澄清石灰水
C.用燃烧的木条鉴别 D.闻气味
6.(2分)节约用水是永恒的话题.下列生活习惯应该摒弃的是( )
A.用盆接水洗菜 B.用养鱼水浇花草
C.使用节水龙头 D.丢弃未喝完的矿泉水瓶
7.(2分)下列试验操作中,不正确的是( )
第 1 页 / 共 8 页A. 熄灭酒精灯 B. 取用固体粉末
C. 读液体体积 D. 滴加液体
8.(2分)以下是四种常用的危险品标志,在装运浓硫酸的包装箱上应贴的标志是( )
A. B.
C. D.
9.(2分)高锰酸钾与一定量水配成的溶液可用来消毒,该消毒液是( )
A.混合物 B.有机物 C.化合物 D.纯净物
10.(2分)下列化学方程式书写正确的是( )
A.铁丝在氧气中燃烧:4Fe+3O =2Fe O
2 2 3
B.红磷在氧气中燃烧:2P+5O =P O
2 2 5
C.铁和硫酸反应:2Fe+3H SO =Fe(SO )+3H ↑
2 4 2 4 3 2
D.氢气在氧气中燃烧:2H +O 2H O
2 2 2
11.(2分)下图信息能说明( )
第 2 页 / 共 8 页A.分子很小
B.分子间有间隔
C.分子总是在不断运动
D.分子是构成物质的唯一微粒
12.(2分)下列灭火方式中,不正确的是( )
A.油锅着火用水浇灭
B.实验桌上酒精着火用湿布盖灭
C.白磷着火用沙土盖灭
D.电器着火切断电源后用湿棉被盖灭
13.(2分)下列对“化学与生活”的认识,错误的是( )
A.A B.B C.C D.D
14.(2分)今天的午餐食谱是:主食﹣﹣面包;配菜和副食﹣﹣炸鸡腿、炸薯片、牛排、牛奶.则该午餐食谱缺
乏的营养素是( )
A.糖类 B.脂肪 C.蛋白质 D.维生素
15.(2分)下列各物质中加入稀硫酸后,有沉淀生成的是( )
A.碳酸钾溶液 B.石蕊溶液
C.硝酸钡溶液 D.氢氧化钠溶液
16.(2分)炼铁的主要反应原理是:Fe O +3CO 2Fe+3CO ,该反应属于( )
2 3 2
A.置换反应 B.化合反应
C.复分解反应 D.以上三种反应都不是
第 3 页 / 共 8 页17.(2分)下列各组内的两种物质不会发生化学反应的是( )
A.铁和硫酸铜溶液 B.铜和硫酸锌溶液
C.稀盐酸和纯碱 D.碳酸钠溶液和石灰水
18.(2分)取少量碳酸饮料“雪碧”滴入紫色石蕊试液,然后再加热,溶液颜色变化情况是( )
A.先变红后变紫 B.先变蓝后变紫
C.先变无色后变红 D.变红后颜色不再改变
19.(2分)下列实验方案不可行的是( )
A.用闻气味的方法区别食盐和白糖
B.用观察颜色的方法区别铁片和铜片
C.用燃烧的方法区别羊毛和合成纤维
D.用稀盐酸区别碳酸钠溶液和蒸馏水
20.(2分)下面是小明同学的实验报告记录,其中不正确的是( )
A.用量筒量取了7.5mL水
B.用pH试纸测得氯化钠溶液的pH为7
C.用托盘天平称取16.75g小苏打
D.测得某粗盐中氯化钠的质量分数为90.5%
21.(2分)除去下列括号内的杂质,对应的方法正确的是( )
A.硝酸钾(蔗糖)→溶解、过滤
B.食盐(细沙)→溶解、蒸发
C.O (H O)→通入浓硫酸
2 2
D.CO (CO)→通入氢氧化钠溶液
2
22.(2分)人类每年从自然界中提取大量的金属铁,下列关于铁的说法正确的是( )
A.钢是很纯的铁
B.生铁是含少量碳的铁合金
C.被腐蚀的铁制品属于不可回收垃圾
D.炼铁的过程是把金属铁变成氧化铁
23.(2分)将60℃饱和的硝酸钾溶液降温至20℃,没有发生变化的是( )
A.溶液的质量 B.溶液里溶质的质量
C.溶液里溶剂的质量 D.溶液里溶质的质量分数
24.(2分)合格奶粉每100g中含蛋白质约为18g,蛋白质中氮元素的平均质量分数为16%.现测定某奶粉每
100g中含有氮元素的质量为2g,计算该奶粉100g中蛋白质的质量并判断是否合格( )
第 4 页 / 共 8 页A.19g;合格 B.12.5g;不合格
C.14.5g;不合格 D.18.6g;合格
25.(2分)下列叙述完全符合质量守恒定律的是( )
A.水结成冰前后,质量保持不变
B.50mL水和50mL乙醇混合后总体积小于100mL
C.在100g过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
二.画龙点睛(填空题.共16分,请将答案填在答题卷上)
26.(5分)元素周期表是化学学习和研究的重要工具.如图是元素周期表的一部分.
1H 2He
1.008 4.003
3Li 4Be … 5B 6C 7N 8O 9F 10Ne
6.941 9.012 10.81 12.01 14.01 16.00 19.00 20.18
11Na 12Mg 13Al 14Si 15P 16S 17Cl 18Ar
22.99 24.31 26.98 28.09 30.97 32.06 35.45 39.95
(1)从表中查出硅(Si)元素的相对原子质量为 ;
(2)6~11号元素中属于金属元素的有 (填元素符号);
(3)目前为止,科学家已发现三千多万种物质,若有下列几种元素及化合价: 、 、 、 ,从中选择适当
的元素写出符合下列条件的一种物质的化学式:
非金属单质 ;
①氧化物 ;
②碱 .
27.③(6分)通过一年的化学学习,我们认识了“酸”和“碱”,请回答下列问题:
(1)常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在有相同的 离子(填符号),因此,它们有
很多相似的化学性质.
(2)碱有氢氧化钠、氢氧化钙等,氢氧化钠可作某些气体的干燥剂,如:干燥 气(举一例),氢氧化
钙可由生石灰与水反应制得,化学方程式为 .
(3)酸和碱能发生中和反应,它在日常生活和工农业生产中有广泛的应用,如硫酸厂的污水中含有硫酸等
杂质,可用熟石灰进行处理,反应的化学方程式为 .
28.(5分)考古研究与化学密不可分。 2007年12月22日南宋古沉船“南海一号”成功打捞出水。如图是古
船上的一些文物图片,根据图回答下列问题:
第 5 页 / 共 8 页(1)可以判断铁比铜活泼的信息是:
。
写出一个能说明铁比铜活泼的化学反应方程式:
。
(2)古沉船上铁锅生锈的主要原因是铁与 、 等物质发生了复杂的化学反应。
三.情景分析(简答题.共12分)
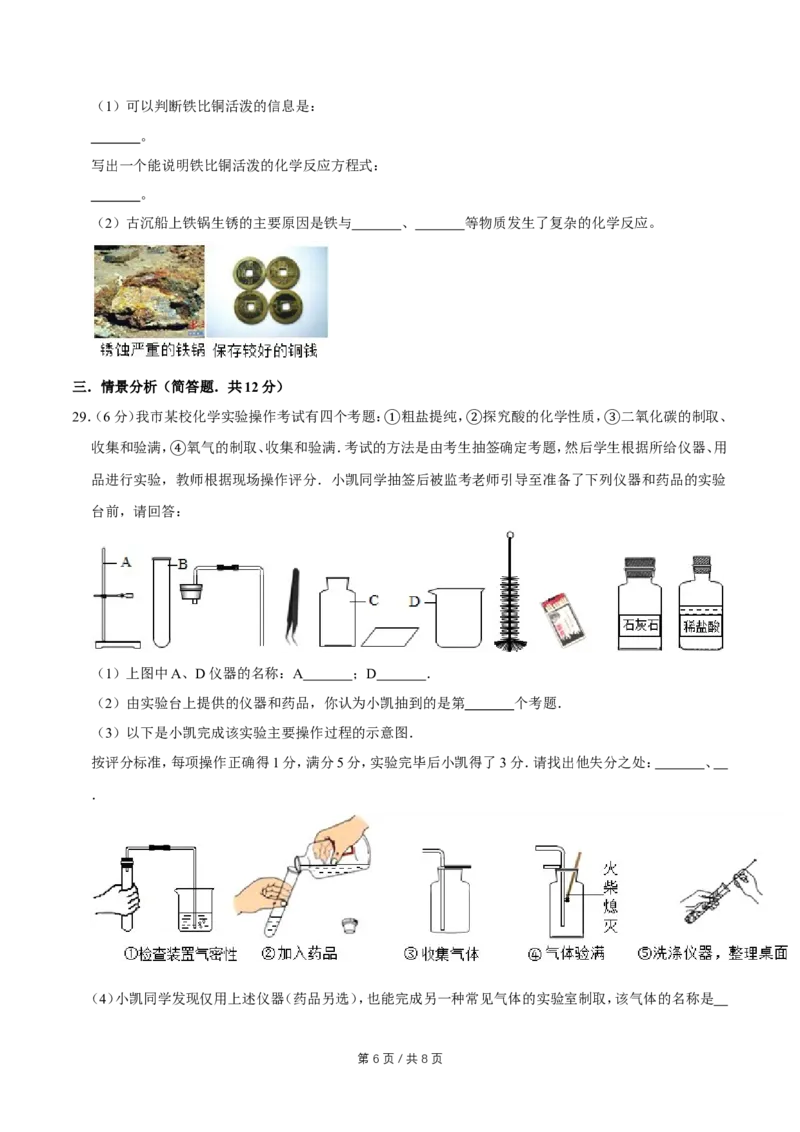
29.(6分)我市某校化学实验操作考试有四个考题: 粗盐提纯, 探究酸的化学性质, 二氧化碳的制取、
收集和验满, 氧气的制取、收集和验满.考试的①方法是由考生②抽签确定考题,然后学③生根据所给仪器、用
品进行实验,④教师根据现场操作评分.小凯同学抽签后被监考老师引导至准备了下列仪器和药品的实验
台前,请回答:
(1)上图中A、D仪器的名称:A ;D .
(2)由实验台上提供的仪器和药品,你认为小凯抽到的是第 个考题.
(3)以下是小凯完成该实验主要操作过程的示意图.
按评分标准,每项操作正确得1分,满分5分,实验完毕后小凯得了3分.请找出他失分之处: 、
.
(4)小凯同学发现仅用上述仪器(药品另选),也能完成另一种常见气体的实验室制取,该气体的名称是
第 6 页 / 共 8 页.
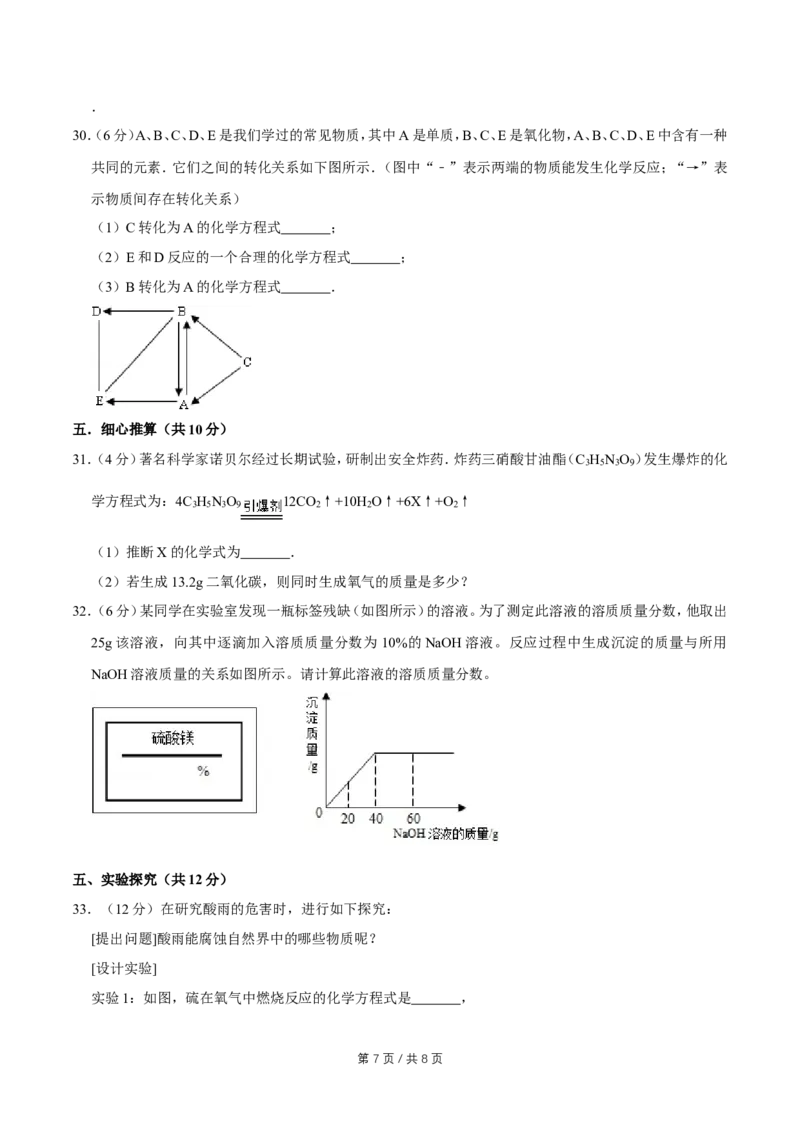
30.(6分)A、B、C、D、E是我们学过的常见物质,其中A是单质,B、C、E是氧化物,A、B、C、D、E中含有一种
共同的元素.它们之间的转化关系如下图所示.(图中“﹣”表示两端的物质能发生化学反应;“→”表
示物质间存在转化关系)
(1)C转化为A的化学方程式 ;
(2)E和D反应的一个合理的化学方程式 ;
(3)B转化为A的化学方程式 .
五.细心推算(共10分)
31.(4分)著名科学家诺贝尔经过长期试验,研制出安全炸药.炸药三硝酸甘油酯(C H N O )发生爆炸的化
3 5 3 9
学方程式为:4C H N O 12CO ↑+10H O↑+6X↑+O ↑
3 5 3 9 2 2 2
(1)推断X的化学式为 .
(2)若生成13.2g二氧化碳,则同时生成氧气的质量是多少?
32.(6分)某同学在实验室发现一瓶标签残缺(如图所示)的溶液。为了测定此溶液的溶质质量分数,他取出
25g该溶液,向其中逐滴加入溶质质量分数为10%的NaOH溶液。反应过程中生成沉淀的质量与所用
NaOH溶液质量的关系如图所示。请计算此溶液的溶质质量分数。
五、实验探究(共12分)
33.(12分)在研究酸雨的危害时,进行如下探究:
[提出问题]酸雨能腐蚀自然界中的哪些物质呢?
[设计实验]
实验1:如图,硫在氧气中燃烧反应的化学方程式是 ,
第 7 页 / 共 8 页实验中出现的错误是 .
若按正确操作,反应后向瓶中倒入蒸馏水,振荡,使SO 与水化合生成亚硫酸(H SO ),一段时间后,亚硫
2 2 3
酸与氧气反应生成硫酸,上述过程发生的化学反应方程式为: .
实验2:实验1即为硫酸型酸雨的形成原理.若将收集到的硫酸型酸雨溶液分成三等份,分别向其中加入
以下物质,观察到如下现象:
所得溶液 加入的物质 一段时间后,观察到的现象
第一份 植物树叶和果皮 树叶和果皮被腐蚀
第二份 镁条和铁丝 有气泡产生
第三份 石灰石和水泥残片 有气泡产生
[反思与交流]
(1)有同学提出,制取CO 时不能用大理石和稀硫酸反应,为什么硫酸型酸雨能腐蚀大理石雕像呢?你认
2
为原因是:生成的硫酸钙受雨水冲刷,脱离大理石表面,使反应持续进行;请再举一例酸雨对环境造成的
破坏 .
(2)土壤中有许多细小的石子,有人说酸雨还能加剧“效应”,这种说法的依据是 .
[拓展与应用]
怎样防治酸雨产生,请你提出两点建议: ; .
① ②
第 8 页 / 共 8 页