文档内容
2017 年海南省中考化学试卷
一、选择题(本大题共14小题,每小题只有1个选项符合题意.每小题3分,共42
分)
1.(3分)下列标志表示可回收利用的是( )
A. B. C. D.
2.(3分)下列物质属于纯净物的是( )
A.空气B.生铁 C.蒸馏水 D.浓盐酸
3.(3分)下列属于化学变化的是( )
A.瓷碗破碎B.钢铁生锈C.汽油挥发D.冰雪融化
4.(3分)葡萄糖(C H O )属于( )
6 l2 6
A.有机物 B.氧化物 C.酸 D.碱
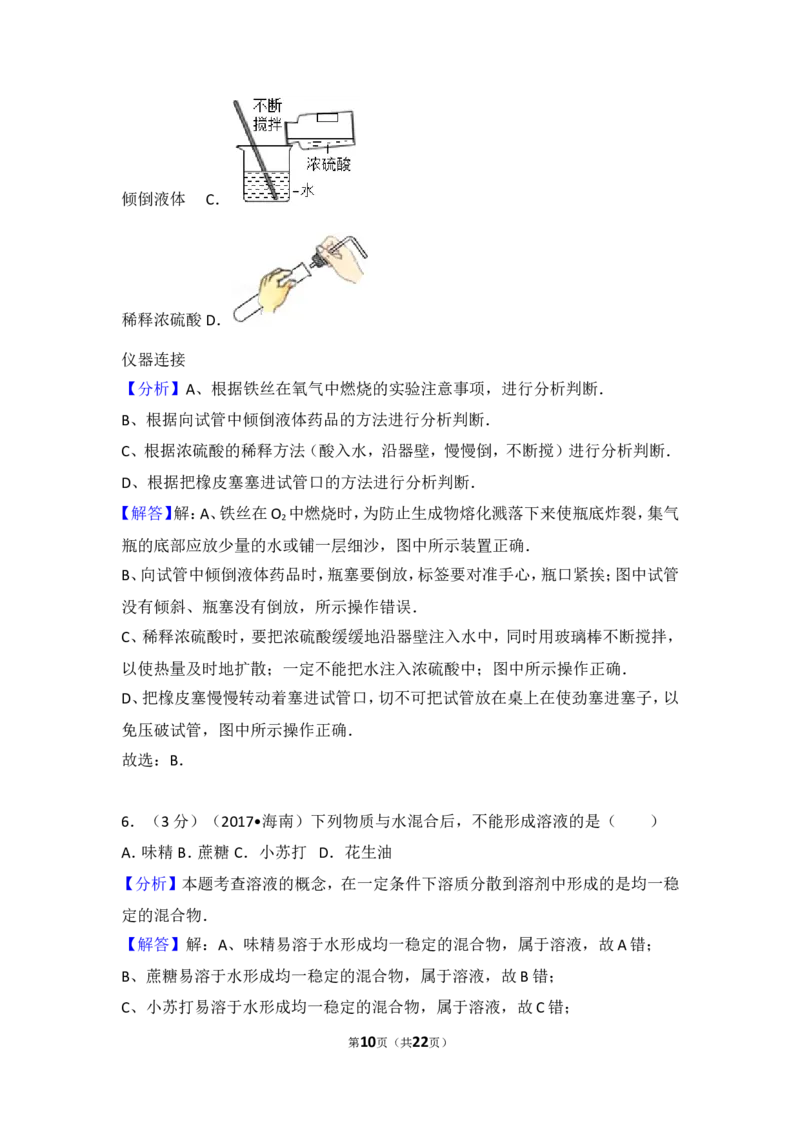
5.(3分)下列实验操作不正确的是( )
A.
铁丝燃烧 B.
倾倒液体 C.
第1页(共22页)稀释浓硫酸D.
仪器连接
6.(3分)下列物质与水混合后,不能形成溶液的是( )
A.味精B.蔗糖 C.小苏打 D.花生油
7.(3分)钙是人体含量最高的金属元素.人体缺钙时,可能导致( )
A.甲状腺肿B.骨质疏松症 C.贫血症 D.夜盲症
8.(3分)下列事实的微观解释不正确的是( )
A.干冰升华﹣﹣分子间隔变大
B.水烧开后把壶盖顶开﹣﹣分子数目变多
C.水在通电的条件下发生分解反应﹣﹣分子种类变化
D.湿衣服晾在太阳底下干得快﹣﹣分子运动速率变快
9.(3分)用硝酸钾固体配制溶质的质量分数为10%的硝酸钾溶液50g.下列做法
不正确的是( )
A.称量:用天平称量硝酸钾5g
B.量取:用量筒量取蒸馏水45mL
C.溶解:将硝酸钾倒入量筒中溶解
D.转移:将配好的溶液转移至试剂瓶
10.(3分)下列食物中富含糖类的是( )
A.白菜B.鸡蛋 C.牛肉D.米饭
11.(3分)下列关于燃烧和灭火的说法不正确的是( )
A.可燃物燃烧一定会生成二氧化碳
B.在加油站使用手机可能引发燃烧、爆炸
C.酒精灯不慎打翻起火,立即用湿抹布扑灭
D.炒菜时油锅中的油不慎着火,可用锅盖盖灭
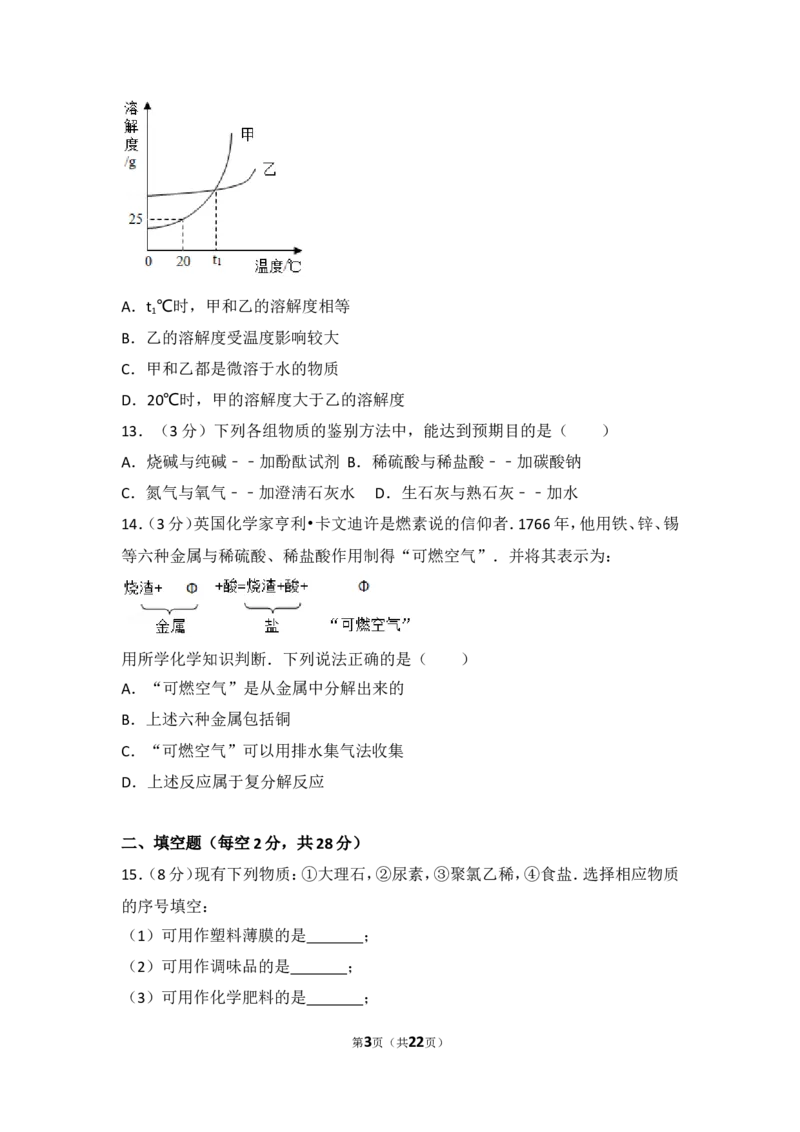
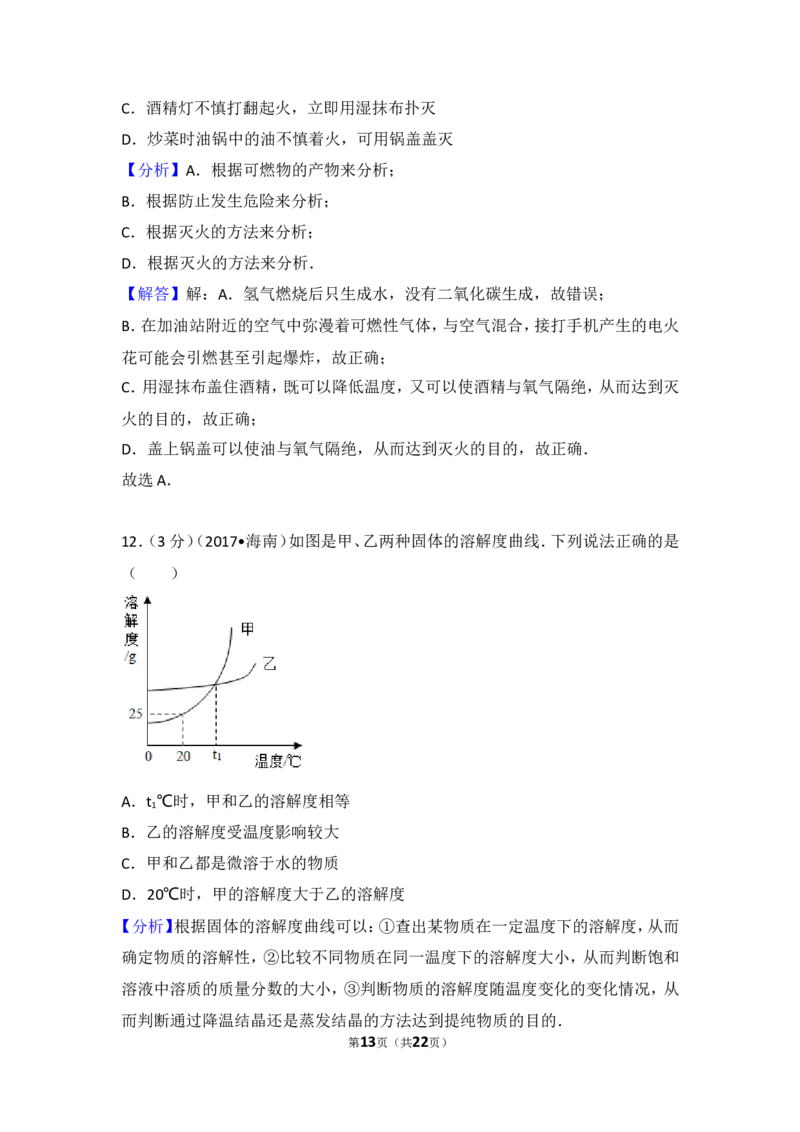
12.(3分)如图是甲、乙两种固体的溶解度曲线.下列说法正确的是( )
第2页(共22页)A.t ℃时,甲和乙的溶解度相等
1
B.乙的溶解度受温度影响较大
C.甲和乙都是微溶于水的物质
D.20℃时,甲的溶解度大于乙的溶解度
13.(3分)下列各组物质的鉴别方法中,能达到预期目的是( )
A.烧碱与纯碱﹣﹣加酚酞试剂 B.稀硫酸与稀盐酸﹣﹣加碳酸钠
C.氮气与氧气﹣﹣加澄淸石灰水 D.生石灰与熟石灰﹣﹣加水
14.(3分)英国化学家亨利•卡文迪许是燃素说的信仰者.1766年,他用铁、锌、锡
等六种金属与稀硫酸、稀盐酸作用制得“可燃空气”.并将其表示为:
用所学化学知识判断.下列说法正确的是( )
A.“可燃空气”是从金属中分解出来的
B.上述六种金属包括铜
C.“可燃空气”可以用排水集气法收集
D.上述反应属于复分解反应
二、填空题(每空2分,共28分)
15.(8分)现有下列物质:①大理石,②尿素,③聚氯乙稀,④食盐.选择相应物质
的序号填空:
(1)可用作塑料薄膜的是 ;
(2)可用作调味品的是 ;
(3)可用作化学肥料的是 ;
第3页(共22页)(4)可用于制备二氧化碳的是 .
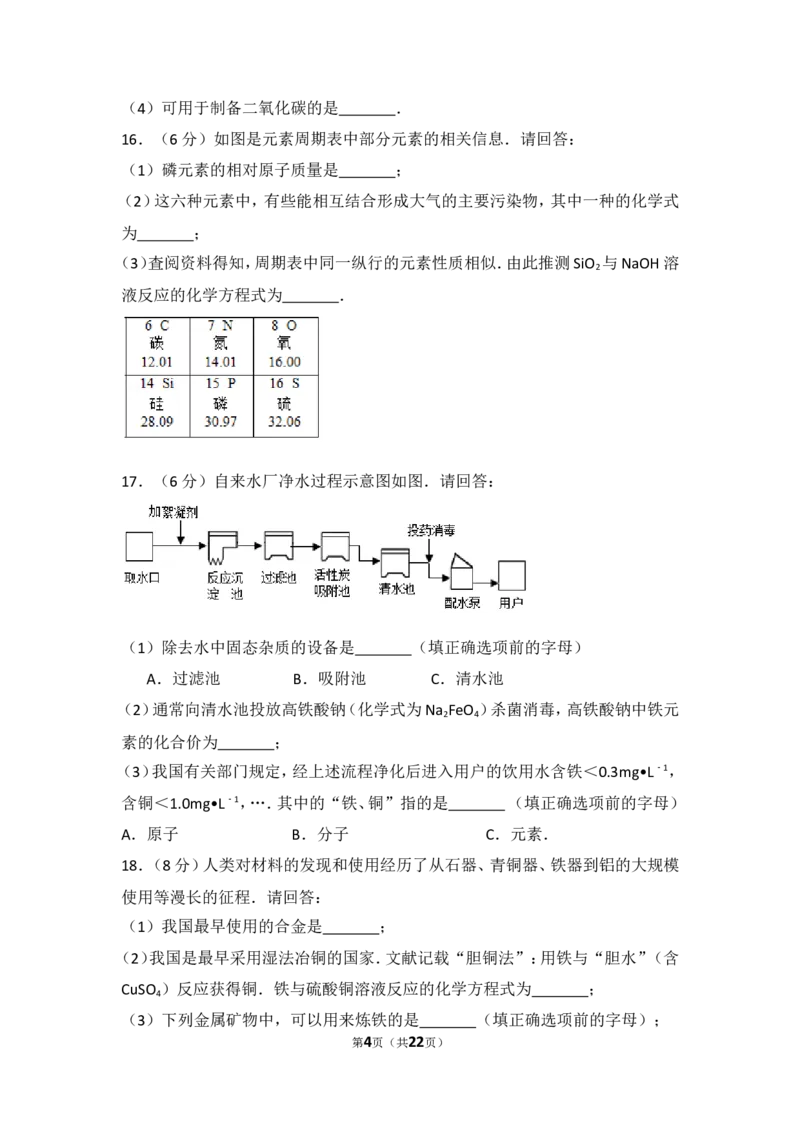
16.(6分)如图是元素周期表中部分元素的相关信息.请回答:
(1)磷元素的相对原子质量是 ;
(2)这六种元素中,有些能相互结合形成大气的主要污染物,其中一种的化学式
为 ;
(3)査阅资料得知,周期表中同一纵行的元素性质相似.由此推测SiO 与NaOH溶
2
液反应的化学方程式为 .
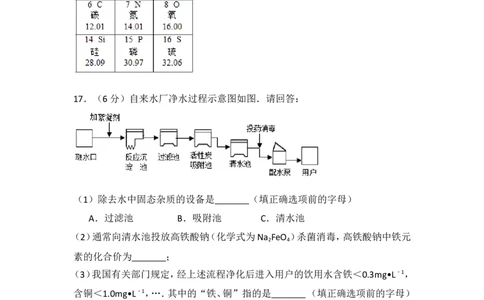
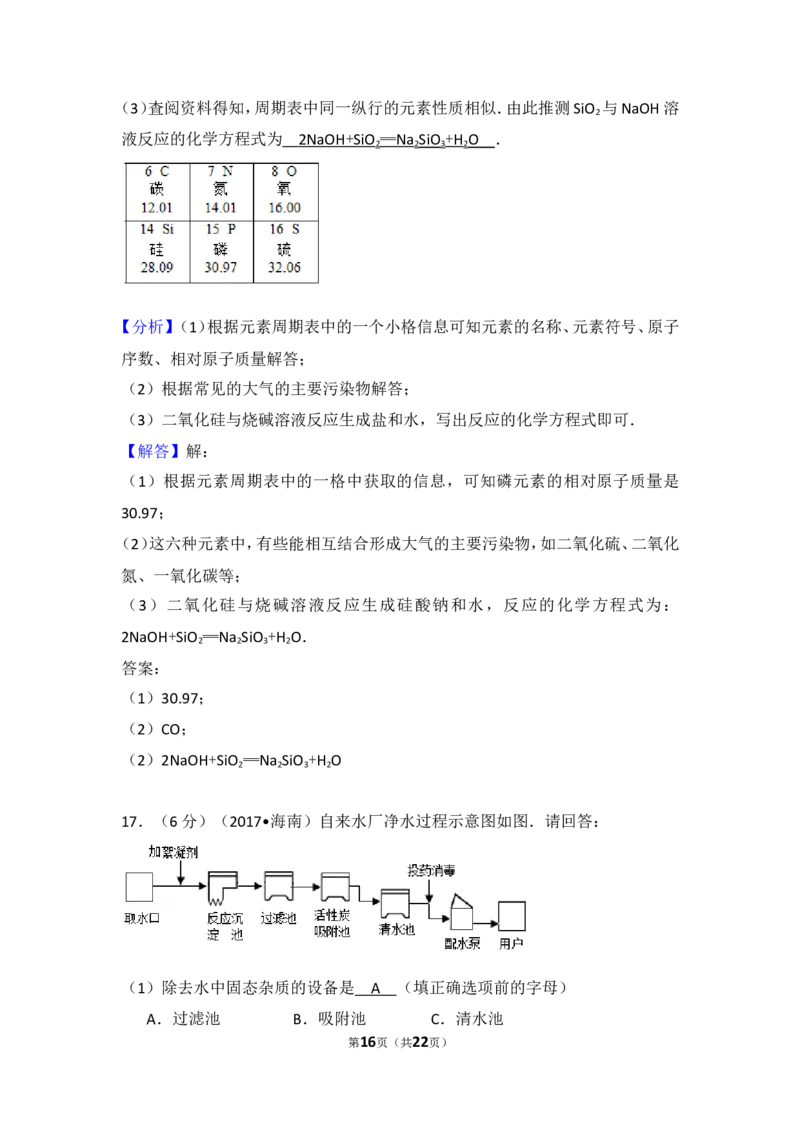
17.(6分)自来水厂净水过程示意图如图.请回答:
(1)除去水中固态杂质的设备是 (填正确选项前的字母)
A.过滤池 B.吸附池 C.清水池
(2)通常向清水池投放高铁酸钠(化学式为Na FeO )杀菌消毒,高铁酸钠中铁元
2 4
素的化合价为 ;
(3)我国有关部门规定,经上述流程净化后进入用户的饮用水含铁<0.3mg•L﹣1,
含铜<1.0mg•L﹣1,….其中的“铁、铜”指的是 (填正确选项前的字母)
A.原子 B.分子 C.元素.
18.(8分)人类对材料的发现和使用经历了从石器、青铜器、铁器到铝的大规模
使用等漫长的征程.请回答:
(1)我国最早使用的合金是 ;
(2)我国是最早采用湿法冶铜的国家.文献记载“胆铜法”:用铁与“胆水”(含
CuSO )反应获得铜.铁与硫酸铜溶液反应的化学方程式为 ;
4
(3)下列金属矿物中,可以用来炼铁的是 (填正确选项前的字母);
第4页(共22页)A.赤铜矿(Cu O) B.赤铁矿(Fe O ) C.软锰矿(MnO )
2 2 3 2
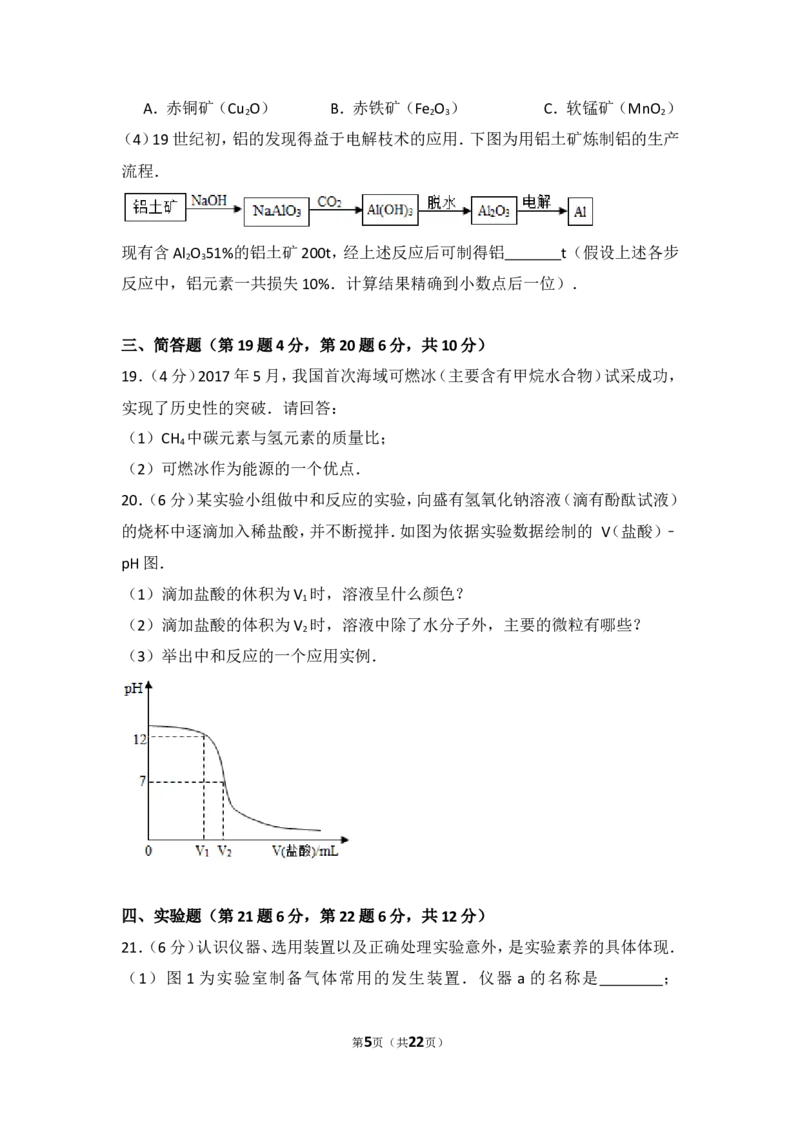
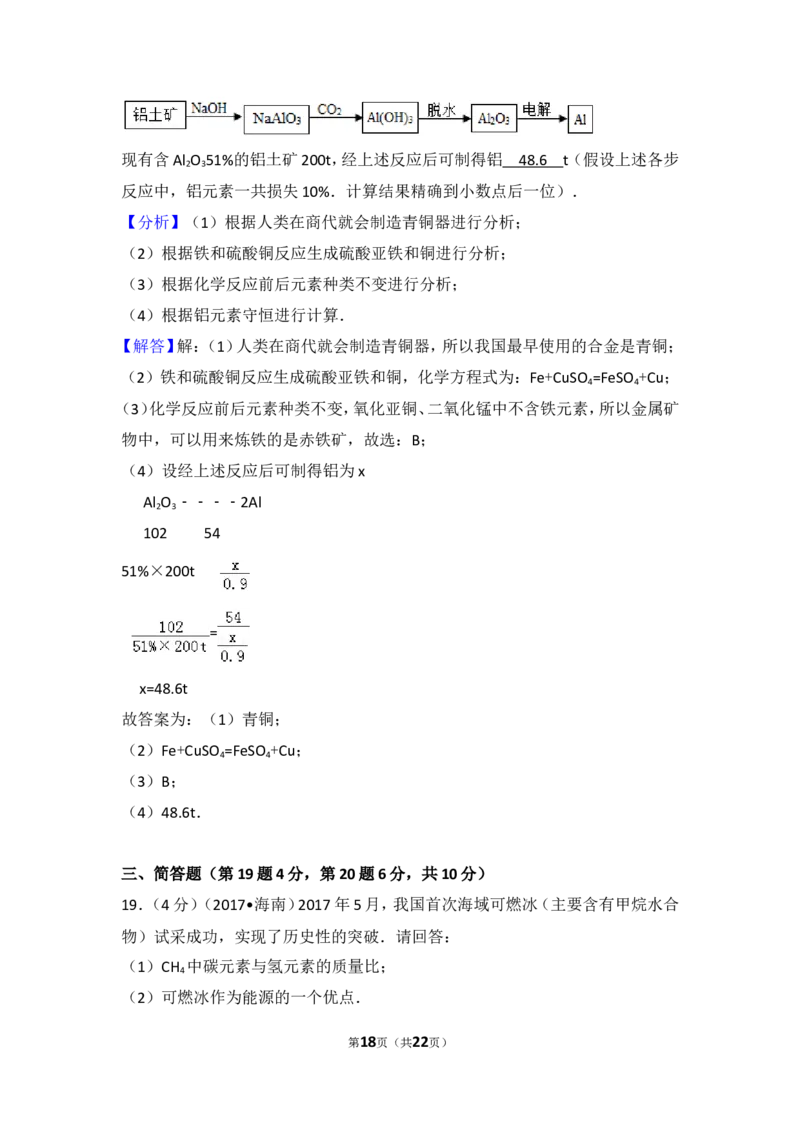
(4)19世纪初,铝的发现得益于电解枝术的应用.下图为用铝土矿炼制铝的生产
流程.
现有含Al O 51%的铝土矿200t,经上述反应后可制得铝 t( 假设上述各步
2 3
反应中,铝元素一共损失10%.计算结果精确到小数点后一位).
三、简答题(第19题4分,第20题6分,共10分)
19.(4分)2017年5月,我国首次海域可燃冰(主要含有甲烷水合物)试采成功,
实现了历史性的突破.请回答:
(1)CH 中碳元素与氢元素的质量比;
4
(2)可燃冰作为能源的一个优点.
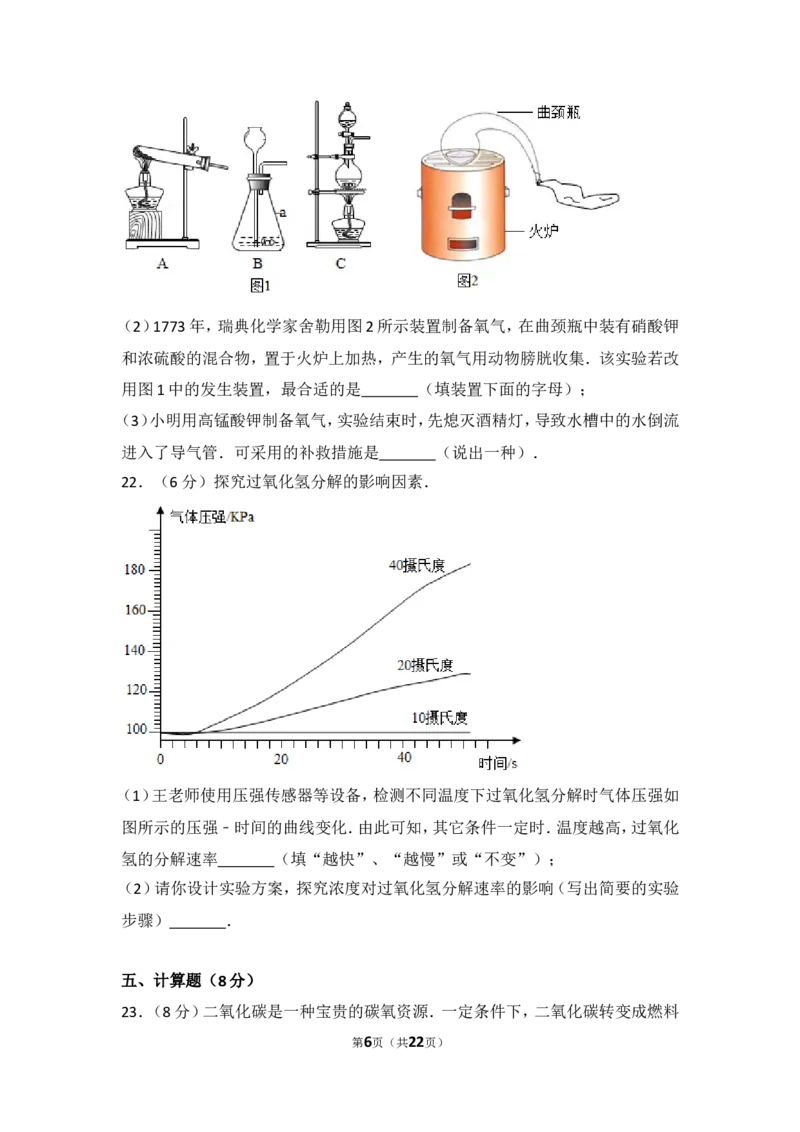
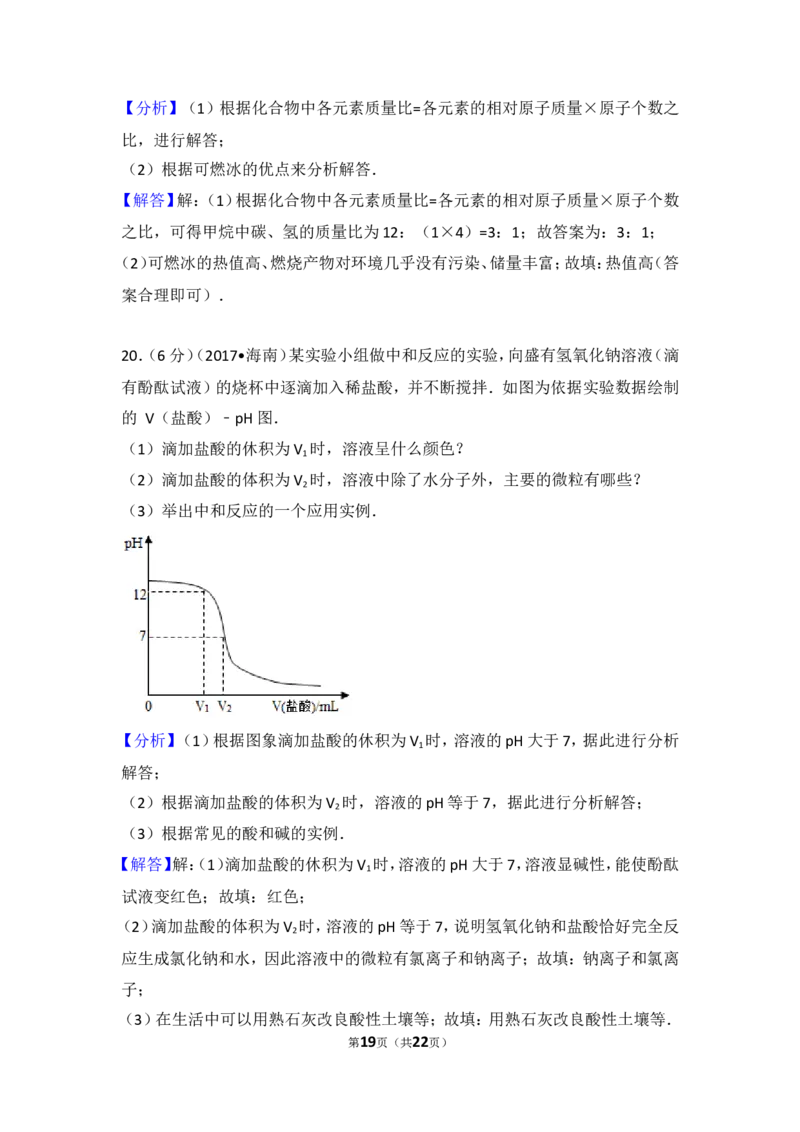
20.(6分)某实验小组做中和反应的实验,向盛有氢氧化钠溶液(滴有酚酞试液)
的烧杯中逐滴加入稀盐酸,并不断搅拌.如图为依据实验数据绘制的 V(盐酸)﹣
pH图.
(1)滴加盐酸的休积为V 时,溶液呈什么颜色?
1
(2)滴加盐酸的体积为V 时,溶液中除了水分子外,主要的微粒有哪些?
2
(3)举出中和反应的一个应用实例.
四、实验题(第21题6分,第22题6分,共12分)
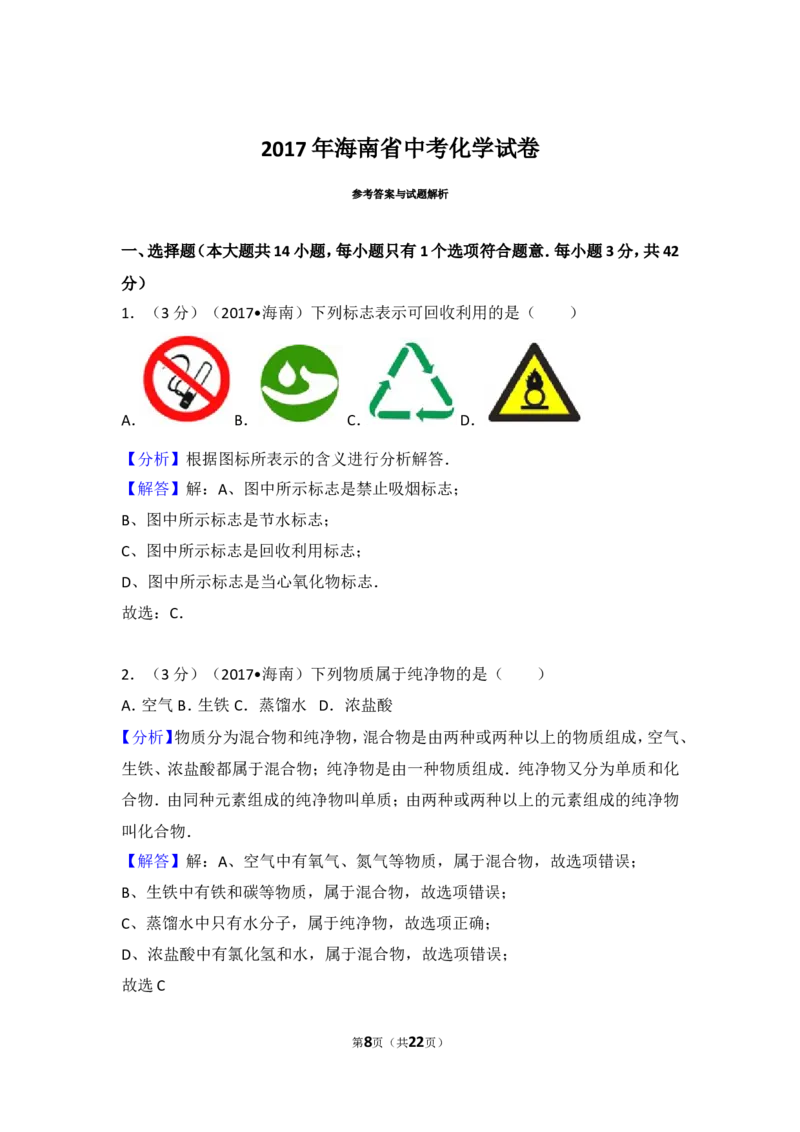
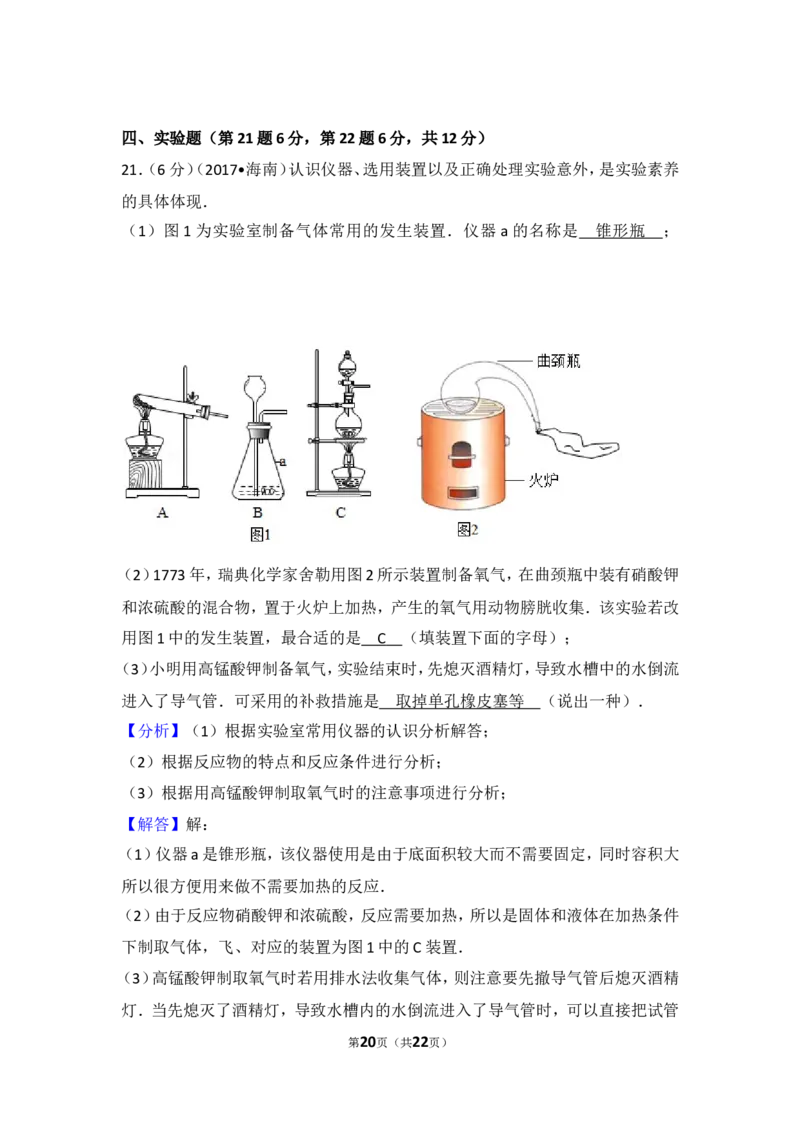
21.(6分)认识仪器、选用装置以及正确处理实验意外,是实验素养的具体体现.
(1)图 1 为实验室制备气体常用的发生装置.仪器 a 的名称是 ;
第5页(共22页)(2)1773年,瑞典化学家舍勒用图2所示装置制备氧气,在曲颈瓶中装有硝酸钾
和浓硫酸的混合物,置于火炉上加热,产生的氧气用动物膀胱收集.该实验若改
用图1中的发生装置,最合适的是 (填装置下面的字母);
(3)小明用高锰酸钾制备氧气,实验结束时,先熄灭酒精灯,导致水槽中的水倒流
进入了导气管.可采用的补救措施是 (说出一种).
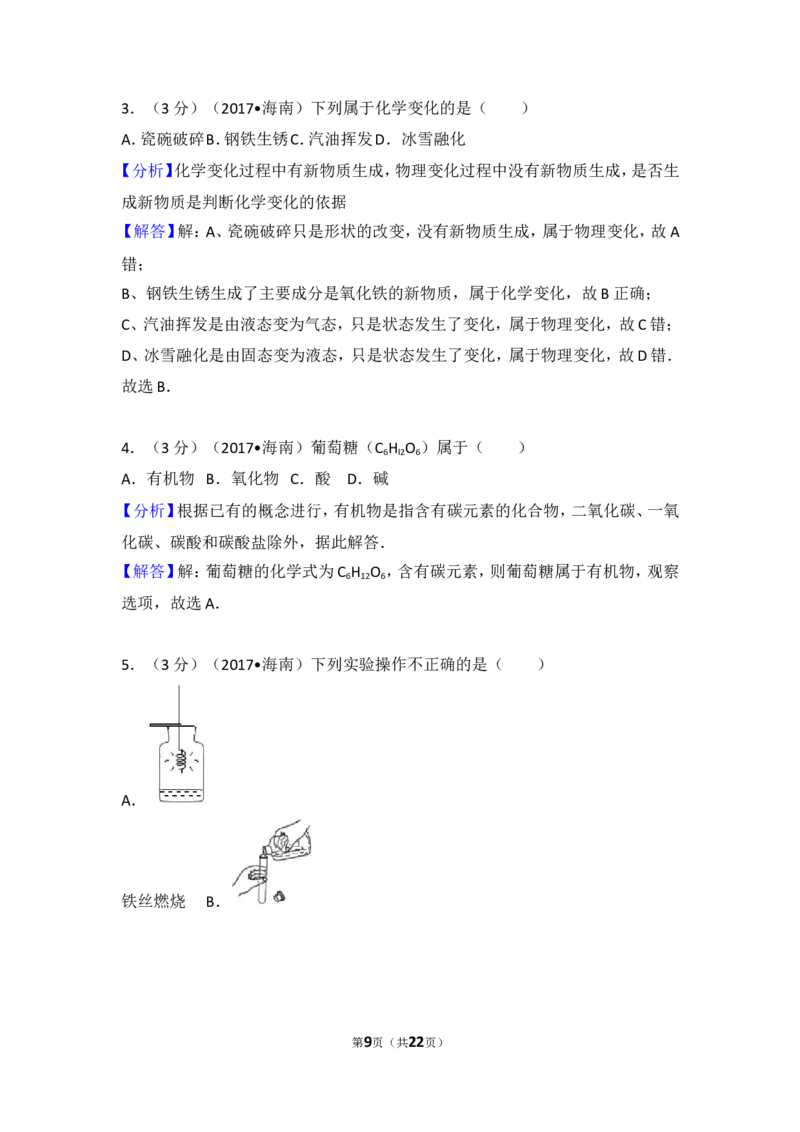
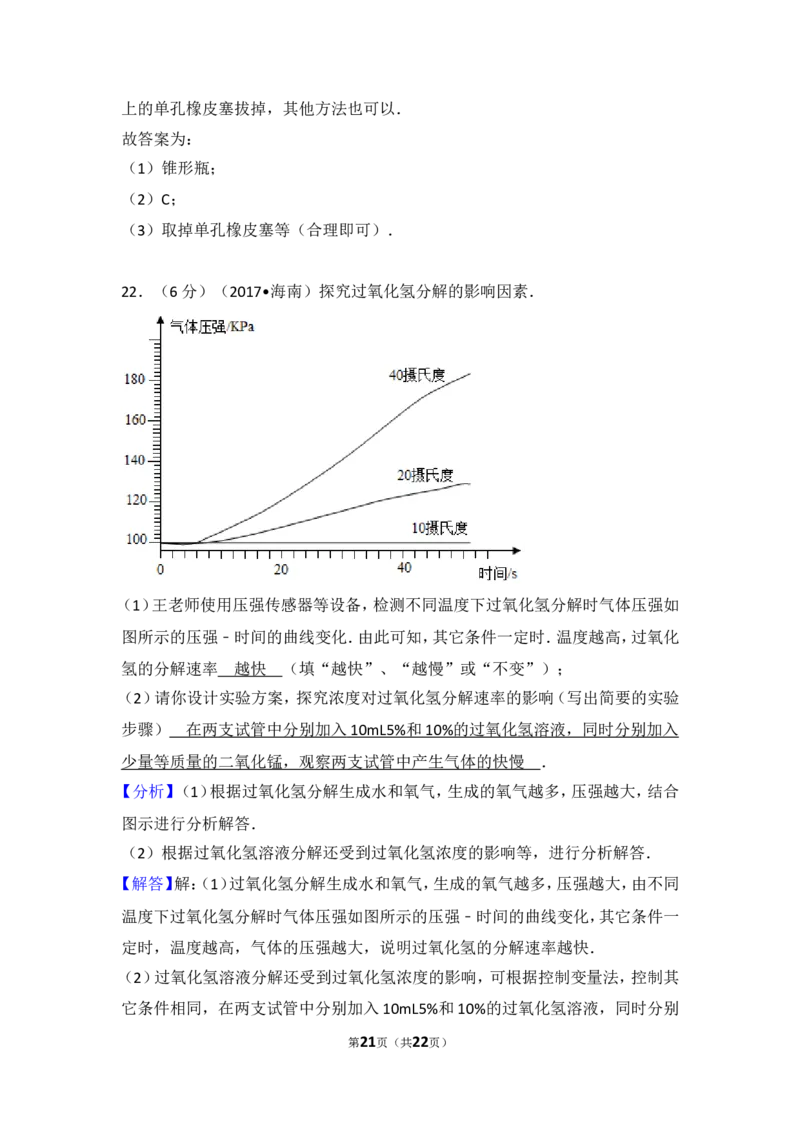
22.(6分)探究过氧化氢分解的影响因素.
(1)王老师使用压强传感器等设备,检测不同温度下过氧化氢分解时气体压强如
图所示的压强﹣时间的曲线变化.由此可知,其它条件一定时.温度越高,过氧化
氢的分解速率 (填“越快”、“越慢”或“不变”);
(2)请你设计实验方案,探究浓度对过氧化氢分解速率的影响(写出简要的实验
步骤) .
五、计算题(8分)
23.(8分)二氧化碳是一种宝贵的碳氧资源.一定条件下,二氧化碳转变成燃料
第6页(共22页)甲醇(CH OH)的化学方程式为CO +3H CH OH+H O.若生产64t甲醇,则
3 2 2 3 2
可回收二氧化碳多少吨?
第7页(共22页)2017 年海南省中考化学试卷
参考答案与试题解析
一、选择题(本大题共14小题,每小题只有1个选项符合题意.每小题3分,共42
分)
1.(3分)(2017•海南)下列标志表示可回收利用的是( )
A. B. C. D.
【分析】根据图标所表示的含义进行分析解答.
【解答】解:A、图中所示标志是禁止吸烟标志;
B、图中所示标志是节水标志;
C、图中所示标志是回收利用标志;
D、图中所示标志是当心氧化物标志.
故选:C.
2.(3分)(2017•海南)下列物质属于纯净物的是( )
A.空气B.生铁 C.蒸馏水 D.浓盐酸
【分析】物质分为混合物和纯净物,混合物是由两种或两种以上的物质组成,空气、
生铁、浓盐酸都属于混合物;纯净物是由一种物质组成.纯净物又分为单质和化
合物.由同种元素组成的纯净物叫单质;由两种或两种以上的元素组成的纯净物
叫化合物.
【解答】解:A、空气中有氧气、氮气等物质,属于混合物,故选项错误;
B、生铁中有铁和碳等物质,属于混合物,故选项错误;
C、蒸馏水中只有水分子,属于纯净物,故选项正确;
D、浓盐酸中有氯化氢和水,属于混合物,故选项错误;
故选C
第8页(共22页)3.(3分)(2017•海南)下列属于化学变化的是( )
A.瓷碗破碎B.钢铁生锈C.汽油挥发D.冰雪融化
【分析】化学变化过程中有新物质生成,物理变化过程中没有新物质生成,是否生
成新物质是判断化学变化的依据
【解答】解:A、瓷碗破碎只是形状的改变,没有新物质生成,属于物理变化,故A
错;
B、钢铁生锈生成了主要成分是氧化铁的新物质,属于化学变化,故B正确;
C、汽油挥发是由液态变为气态,只是状态发生了变化,属于物理变化,故C错;
D、冰雪融化是由固态变为液态,只是状态发生了变化,属于物理变化,故D错.
故选B.
4.(3分)(2017•海南)葡萄糖(C H O )属于( )
6 l2 6
A.有机物 B.氧化物 C.酸 D.碱
【分析】根据已有的概念进行,有机物是指含有碳元素的化合物,二氧化碳、一氧
化碳、碳酸和碳酸盐除外,据此解答.
【解答】解:葡萄糖的化学式为C H O ,含有碳元素,则葡萄糖属于有机物,观察
6 12 6
选项,故选A.
5.(3分)(2017•海南)下列实验操作不正确的是( )
A.
铁丝燃烧 B.
第9页(共22页)倾倒液体 C.
稀释浓硫酸D.
仪器连接
【分析】A、根据铁丝在氧气中燃烧的实验注意事项,进行分析判断.
B、根据向试管中倾倒液体药品的方法进行分析判断.
C、根据浓硫酸的稀释方法(酸入水,沿器壁,慢慢倒,不断搅)进行分析判断.
D、根据把橡皮塞塞进试管口的方法进行分析判断.
【解答】解:A、铁丝在O 中燃烧时,为防止生成物熔化溅落下来使瓶底炸裂,集气
2
瓶的底部应放少量的水或铺一层细沙,图中所示装置正确.
B、向试管中倾倒液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨;图中试管
没有倾斜、瓶塞没有倒放,所示操作错误.
C、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,
以使热量及时地扩散;一定不能把水注入浓硫酸中;图中所示操作正确.
D、把橡皮塞慢慢转动着塞进试管口,切不可把试管放在桌上在使劲塞进塞子,以
免压破试管,图中所示操作正确.
故选:B.
6.(3分)(2017•海南)下列物质与水混合后,不能形成溶液的是( )
A.味精B.蔗糖 C.小苏打 D.花生油
【分析】本题考查溶液的概念,在一定条件下溶质分散到溶剂中形成的是均一稳
定的混合物.
【解答】解:A、味精易溶于水形成均一稳定的混合物,属于溶液,故A错;
B、蔗糖易溶于水形成均一稳定的混合物,属于溶液,故B错;
C、小苏打易溶于水形成均一稳定的混合物,属于溶液,故C错;
第10页(共22页)D、花生油不溶于水,与水混合形成乳浊液,故D正确.
故选D.
7.(3分)(2017•海南)钙是人体含量最高的金属元素.人体缺钙时,可能导致(
)
A.甲状腺肿B.骨质疏松症 C.贫血症 D.夜盲症
【分析】根据钙的生理功能和缺乏症进行分析.
【解答】解:钙主要存在于骨胳和牙齿中,使骨和牙齿具有坚硬的结构支架,缺乏
幼儿和青少年会患佝偻病,老年人会患骨质疏松;
故答案为:B.
8.(3分)(2017•海南)下列事实的微观解释不正确的是( )
A.干冰升华﹣﹣分子间隔变大
B.水烧开后把壶盖顶开﹣﹣分子数目变多
C.水在通电的条件下发生分解反应﹣﹣分子种类变化
D.湿衣服晾在太阳底下干得快﹣﹣分子运动速率变快
【分析】根据分子的基本特征:分子质量和体积都很小;分子之间有间隔;分子是
在不断运动的;同种物质的分子性质相同,不同物质的分子性质不同,结合事实
进行分析判断即可.
【解答】解:A、干冰升华是因为二氧化碳分子间隔变大的缘故,故选项解释合理.
B、水烧开后,壶盖被顶开,发生的是物理变化,水分子本身没有发生改变,温度升
高,水分子间的间隔变大,引起水的体积膨胀,壶盖被顶开,分子数目不变,故解
释错误.
C、水在通电的条件下发生分解反应生成氢气和氧气,分子种类变化,故选项解释
合理.
D、湿衣服晾在太阳底下干得快,是因为温度升高,分子运动的速率加快,故选项
解释合理.
故选B.
9.(3分)(2017•海南)用硝酸钾固体配制溶质的质量分数为10%的硝酸钾溶液
第11页(共22页)50g.下列做法不正确的是( )
A.称量:用天平称量硝酸钾5g
B.量取:用量筒量取蒸馏水45mL
C.溶解:将硝酸钾倒入量筒中溶解
D.转移:将配好的溶液转移至试剂瓶
【分析】A、利用溶质质量=溶液质量×溶质的质量分数,进行分析判断.
B、根据溶剂质量=溶液质量﹣溶质质量,进行分析判断.
C、根据溶解操作的方法,进行分析判断.
D、根据根据配制溶质质量分数一定的溶液的实验步骤,进行分析判断.
【解答】解:A、溶质质量=溶液质量×溶质的质量分数,配制溶质的质量分数为
10%的硝酸钾溶液50g,需硝酸钾的质量=50g×10%=5g,故选项说法正确.
B、溶剂质量=溶液质量﹣溶质质量,则所需水的质量=50g﹣5g=45g(合45mL),故
选项说法正确.
C、溶解时,应将硝酸钾倒入烧杯中溶解,不能在量筒内进行,故选项说法错误.
D、溶液配制完成后,将配好的溶液转移至试剂瓶,故选项说法正确.
故选:C.
10.(3分)(2017•海南)下列食物中富含糖类的是( )
A.白菜B.鸡蛋 C.牛肉D.米饭
【分析】根据人体所需六大营养素的种类、食物来源,结合题中所给的食物判断所
含的营养素,进行分析判断.
【解答】解:A、白菜中主要含有维生素,所以错误.
B、鸡蛋中主要含有蛋白质,所以错误.
C、牛肉中主要含有蛋白质,所以错误.
D、米饭中主要含有淀粉,它属于糖类物质,所以正确.
故选D.
11.(3分)(2017•海南)下列关于燃烧和灭火的说法不正确的是( )
A.可燃物燃烧一定会生成二氧化碳
B.在加油站使用手机可能引发燃烧、爆炸
第12页(共22页)C.酒精灯不慎打翻起火,立即用湿抹布扑灭
D.炒菜时油锅中的油不慎着火,可用锅盖盖灭
【分析】A.根据可燃物的产物来分析;
B.根据防止发生危险来分析;
C.根据灭火的方法来分析;
D.根据灭火的方法来分析.
【解答】解:A.氢气燃烧后只生成水,没有二氧化碳生成,故错误;
B.在加油站附近的空气中弥漫着可燃性气体,与空气混合,接打手机产生的电火
花可能会引燃甚至引起爆炸,故正确;
C.用湿抹布盖住酒精,既可以降低温度,又可以使酒精与氧气隔绝,从而达到灭
火的目的,故正确;
D.盖上锅盖可以使油与氧气隔绝,从而达到灭火的目的,故正确.
故选A.
12.(3分)(2017•海南)如图是甲、乙两种固体的溶解度曲线.下列说法正确的是
( )
A.t ℃时,甲和乙的溶解度相等
1
B.乙的溶解度受温度影响较大
C.甲和乙都是微溶于水的物质
D.20℃时,甲的溶解度大于乙的溶解度
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而
确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和
溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从
而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
第13页(共22页)【解答】解:A、通过分析溶解度曲线可知,t ℃时,甲和乙的溶解度相等,故A正确;
1
B、甲物质的溶解度受温度变化影响较大,故B错误;
C、20℃时,甲、乙物质的溶解度都大于10g,所以甲和乙都是易溶于水的物质,故
C错误;
D、20℃时,甲的溶解度小于乙的溶解度,故D错误.
故选:A.
13.(3分)(2017•海南)下列各组物质的鉴别方法中,能达到预期目的是( )
A.烧碱与纯碱﹣﹣加酚酞试剂 B.稀硫酸与稀盐酸﹣﹣加碳酸钠
C.氮气与氧气﹣﹣加澄淸石灰水 D.生石灰与熟石灰﹣﹣加水
【分析】根据两种物质与同种试剂反应产生的不同现象来鉴别它们,若两种物质
与同种物质反应的现象相同,则无法鉴别它们.
【解答】解:A、烧碱与纯碱均显碱性,均能使酚酞试剂变红色,不能鉴别,故选项
错误.
B、稀硫酸与稀盐酸均能与碳酸钠反应生成二氧化碳气体,不能鉴别,故选项错误.
C、氮气与氧气均不能使澄清的石灰水变浑浊,不能鉴别,故选项错误.
D、生石灰与水反应生成氢氧化钙,反应放出大量的热,熟石灰微溶于水,溶于水
温度几乎无变化,可以鉴别,故选项正确.
故选:D.
14.(3分)(2017•海南)英国化学家亨利•卡文迪许是燃素说的信仰者.1766年,
他用铁、锌、锡等六种金属与稀硫酸、稀盐酸作用制得“可燃空气”.并将其表示
为:
用所学化学知识判断.下列说法正确的是( )
A.“可燃空气”是从金属中分解出来的
B.上述六种金属包括铜
C.“可燃空气”可以用排水集气法收集
D.上述反应属于复分解反应
第14页(共22页)【分析】根据排在氢前面的金属可以将酸中的氢置换出来,氢气的密度比空气小,
难溶于水进行分析.
【解答】解:A、“可燃空气”是从金属从酸中置换出来的,故A错误;
B、铜的金属活动性顺序排在氢之后,不会与酸反应生成氢气,故B错误;
C、“可燃空气”难溶于水,可以用排水集气法收集,故C正确;
D、金属和酸生成氢气的反应属于置换反应,故D错误.
故选:C.
二、填空题(每空2分,共28分)
15.(8分)(2017•海南)现有下列物质:①大理石,②尿素,③聚氯乙稀,④食盐.
选择相应物质的序号填空:
(1)可用作塑料薄膜的是 ③ ;
(2)可用作调味品的是 ④ ;
(3)可用作化学肥料的是 ② ;
(4)可用于制备二氧化碳的是 ① .
【分析】(1)根据聚乙烯可用作塑料薄膜判断.
(2)根据氯化钠无毒、有咸味的性质判断.
(3)根据尿素中含有氮元素,可用作化学肥料判断.
(4)根据实验室常用大理石和稀盐酸制取二氧化碳解答;
【解答】解:
(1)聚乙烯可用作塑料薄膜;
(2)氯化钠的化学式为NaCl,无毒、有咸味,是家庭厨房常用的调味品;
(3)尿素中含有氮元素,可用作化学肥料;
(4)实验室常用大理石和稀盐酸制取二氧化碳;
故答案为:(1)③;(2)④;(3)②;(4)①.
16.(6分)(2017•海南)如图是元素周期表中部分元素的相关信息.请回答:
(1)磷元素的相对原子质量是 30.97 ;
(2)这六种元素中,有些能相互结合形成大气的主要污染物,其中一种的化学式
为 CO ;
第15页(共22页)(3)査阅资料得知,周期表中同一纵行的元素性质相似.由此推测SiO 与NaOH溶
2
液反应的化学方程式为 2NaOH + SiO ═ N a SiO + H O .
2 2 3 2
【分析】(1)根据元素周期表中的一个小格信息可知元素的名称、元素符号、原子
序数、相对原子质量解答;
(2)根据常见的大气的主要污染物解答;
(3)二氧化硅与烧碱溶液反应生成盐和水,写出反应的化学方程式即可.
【解答】解:
(1)根据元素周期表中的一格中获取的信息,可知磷元素的相对原子质量是
30.97;
(2)这六种元素中,有些能相互结合形成大气的主要污染物,如二氧化硫、二氧化
氮、一氧化碳等;
(3)二氧化硅与烧碱溶液反应生成硅酸钠和水,反应的化学方程式为:
2NaOH+SiO ═Na SiO +H O.
2 2 3 2
答案:
(1)30.97;
(2)CO;
(2)2NaOH+SiO ═Na SiO +H O
2 2 3 2
17.(6分)(2017•海南)自来水厂净水过程示意图如图.请回答:
(1)除去水中固态杂质的设备是 A (填正确选项前的字母)
A.过滤池 B.吸附池 C.清水池
第16页(共22页)(2)通常向清水池投放高铁酸钠(化学式为Na FeO )杀菌消毒,高铁酸钠中铁元
2 4
素的化合价为 + 6 ;
(3)我国有关部门规定,经上述流程净化后进入用户的饮用水含铁<0.3mg•L﹣1,
含铜<1.0mg•L﹣1,….其中的“铁、铜”指的是 C (填正确选项前的字母).
A.原子 B.分子 C.元素.
【分析】(1)根据自来水厂生产流程中各装置的特点、作用分析回答;
(2)根据在化合物中正负化合价代数和为零,结合高铁酸钠(Na FeO )的化学式
2 4
进行解答本题;
(3)根据物是由元素组成的解答.
【解答】解:
(1)由自来水厂生产流程图可知,除去水中固态杂质的设备是:过滤池;
(2)钠元素显+1价,氧元素显﹣2价,
设铁元素的化合价是x,
根据在化合物中正负化合价代数和为零,
可得:(+1)×2+x+(﹣2)×4=0,
则x=+6价.
(3)经上述流程净化后进入用户的饮用水含铁<0.3mg•L﹣1,含铜<1.0mg•L﹣
1,….其中的“铁、铜”指的是元素.
答案:(1)A;(2)+6;(3)C.
18.(8分)(2017•海南)人类对材料的发现和使用经历了从石器、青铜器、铁器到
铝的大规模使用等漫长的征程.请回答:
(1)我国最早使用的合金是 青铜 ;
(2)我国是最早采用湿法冶铜的国家.文献记载“胆铜法”:用铁与“胆水”(含
CuSO )反应获得铜.铁与硫酸铜溶液反应的化学方程式为 F e + CuSO =FeSO + Cu
4 4 4
;
(3)下列金属矿物中,可以用来炼铁的是 B (填正确选项前的字母);
A.赤铜矿(Cu O) B.赤铁矿(Fe O ) C.软锰矿(MnO )
2 2 3 2
(4)19世纪初,铝的发现得益于电解枝术的应用.下图为用铝土矿炼制铝的生产
流程.
第17页(共22页)现有含Al O 51%的铝土矿200t,经上述反应后可制得铝 48.6 t( 假设上述各步
2 3
反应中,铝元素一共损失10%.计算结果精确到小数点后一位).
【分析】(1)根据人类在商代就会制造青铜器进行分析;
(2)根据铁和硫酸铜反应生成硫酸亚铁和铜进行分析;
(3)根据化学反应前后元素种类不变进行分析;
(4)根据铝元素守恒进行计算.
【解答】解:(1)人类在商代就会制造青铜器,所以我国最早使用的合金是青铜;
(2)铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为:Fe+CuSO =FeSO +Cu;
4 4
(3)化学反应前后元素种类不变,氧化亚铜、二氧化锰中不含铁元素,所以金属矿
物中,可以用来炼铁的是赤铁矿,故选:B;
(4)设经上述反应后可制得铝为x
Al O ﹣﹣﹣﹣2Al
2 3
102 54
51%×200t
=
x=48.6t
故答案为:(1)青铜;
(2)Fe+CuSO =FeSO +Cu;
4 4
(3)B;
(4)48.6t.
三、简答题(第19题4分,第20题6分,共10分)
19.(4分)(2017•海南)2017年5月,我国首次海域可燃冰(主要含有甲烷水合
物)试采成功,实现了历史性的突破.请回答:
(1)CH 中碳元素与氢元素的质量比;
4
(2)可燃冰作为能源的一个优点.
第18页(共22页)【分析】(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数之
比,进行解答;
(2)根据可燃冰的优点来分析解答.
【解答】解:(1)根据化合物中各元素质量比=各元素的相对原子质量×原子个数
之比,可得甲烷中碳、氢的质量比为12:(1×4)=3:1;故答案为:3:1;
(2)可燃冰的热值高、燃烧产物对环境几乎没有污染、储量丰富;故填:热值高(答
案合理即可).
20.(6分)(2017•海南)某实验小组做中和反应的实验,向盛有氢氧化钠溶液(滴
有酚酞试液)的烧杯中逐滴加入稀盐酸,并不断搅拌.如图为依据实验数据绘制
的 V(盐酸)﹣pH图.
(1)滴加盐酸的休积为V 时,溶液呈什么颜色?
1
(2)滴加盐酸的体积为V 时,溶液中除了水分子外,主要的微粒有哪些?
2
(3)举出中和反应的一个应用实例.
【分析】(1)根据图象滴加盐酸的休积为V 时,溶液的pH大于7,据此进行分析
1
解答;
(2)根据滴加盐酸的体积为V 时,溶液的pH等于7,据此进行分析解答;
2
(3)根据常见的酸和碱的实例.
【解答】解:(1)滴加盐酸的休积为V 时,溶液的pH大于7,溶液显碱性,能使酚酞
1
试液变红色;故填:红色;
(2)滴加盐酸的体积为V 时,溶液的pH等于7,说明氢氧化钠和盐酸恰好完全反
2
应生成氯化钠和水,因此溶液中的微粒有氯离子和钠离子;故填:钠离子和氯离
子;
(3)在生活中可以用熟石灰改良酸性土壤等;故填:用熟石灰改良酸性土壤等.
第19页(共22页)四、实验题(第21题6分,第22题6分,共12分)
21.(6分)(2017•海南)认识仪器、选用装置以及正确处理实验意外,是实验素养
的具体体现.
(1)图1为实验室制备气体常用的发生装置.仪器 a的名称是 锥形瓶 ;
(2)1773年,瑞典化学家舍勒用图2所示装置制备氧气,在曲颈瓶中装有硝酸钾
和浓硫酸的混合物,置于火炉上加热,产生的氧气用动物膀胱收集.该实验若改
用图1中的发生装置,最合适的是 C (填装置下面的字母);
(3)小明用高锰酸钾制备氧气,实验结束时,先熄灭酒精灯,导致水槽中的水倒流
进入了导气管.可采用的补救措施是 取掉单孔橡皮塞等 (说出一种).
【分析】(1)根据实验室常用仪器的认识分析解答;
(2)根据反应物的特点和反应条件进行分析;
(3)根据用高锰酸钾制取氧气时的注意事项进行分析;
【解答】解:
(1)仪器a是锥形瓶,该仪器使用是由于底面积较大而不需要固定,同时容积大
所以很方便用来做不需要加热的反应.
(2)由于反应物硝酸钾和浓硫酸,反应需要加热,所以是固体和液体在加热条件
下制取气体,飞、对应的装置为图1中的C装置.
(3)高锰酸钾制取氧气时若用排水法收集气体,则注意要先撤导气管后熄灭酒精
灯.当先熄灭了酒精灯,导致水槽内的水倒流进入了导气管时,可以直接把试管
第20页(共22页)上的单孔橡皮塞拔掉,其他方法也可以.
故答案为:
(1)锥形瓶;
(2)C;
(3)取掉单孔橡皮塞等(合理即可).
22.(6分)(2017•海南)探究过氧化氢分解的影响因素.
(1)王老师使用压强传感器等设备,检测不同温度下过氧化氢分解时气体压强如
图所示的压强﹣时间的曲线变化.由此可知,其它条件一定时.温度越高,过氧化
氢的分解速率 越快 (填“越快”、“越慢”或“不变”);
(2)请你设计实验方案,探究浓度对过氧化氢分解速率的影响(写出简要的实验
步骤) 在两支试管中分别加入 10mL5% 和 10% 的过氧化氢溶液,同时分别加入
少量等质量的二氧化锰,观察两支试管中产生气体的快慢 .
【分析】(1)根据过氧化氢分解生成水和氧气,生成的氧气越多,压强越大,结合
图示进行分析解答.
(2)根据过氧化氢溶液分解还受到过氧化氢浓度的影响等,进行分析解答.
【解答】解:(1)过氧化氢分解生成水和氧气,生成的氧气越多,压强越大,由不同
温度下过氧化氢分解时气体压强如图所示的压强﹣时间的曲线变化,其它条件一
定时,温度越高,气体的压强越大,说明过氧化氢的分解速率越快.
(2)过氧化氢溶液分解还受到过氧化氢浓度的影响,可根据控制变量法,控制其
它条件相同,在两支试管中分别加入10mL5%和10%的过氧化氢溶液,同时分别
第21页(共22页)加入少量等质量的二氧化锰,观察两支试管中产生气体的快慢(其它合理即可).
故答案为:(1)越快;(2)在两支试管中分别加入10mL5%和10%的过氧化氢溶液
同时分别加入少量等质量的二氧化锰,观察两支试管中产生气体的快慢.
五、计算题(8分)
23.(8分)(2017•海南)二氧化碳是一种宝贵的碳氧资源.一定条件下,二氧化碳
转变成燃料甲醇(CH OH)的化学方程式为CO +3H CH OH+H O.若生产
3 2 2 3 2
64t甲醇,则可回收二氧化碳多少吨?
【分析】根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
【解答】解:设可回收二氧化碳质量为x,
CO +3H CH OH+H O,
2 2 3 2
44 32
x 64t
= ,
x=88t,
答:若生产64t甲醇,则可回收二氧化碳88t.
第22页(共22页)