文档内容
马鞍山二中2025届高三年级高考适应性考试
化学试题
注意事项:
1.答卷前,务必将自己的姓名、考号和班级填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,务必
擦净后再选涂其他答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
可能用到的相对原子质量:Li 7 O 16 Na 23 Ti 48 Cu 64 Zn 65
一、选择题(本题共 14 小题,每小题 3 分,共 42 分。在每小题给出的四个选项中,只有一项是
符合题目要求的)
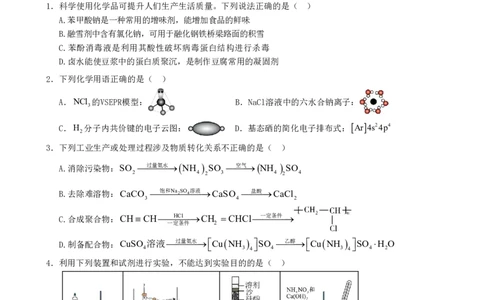
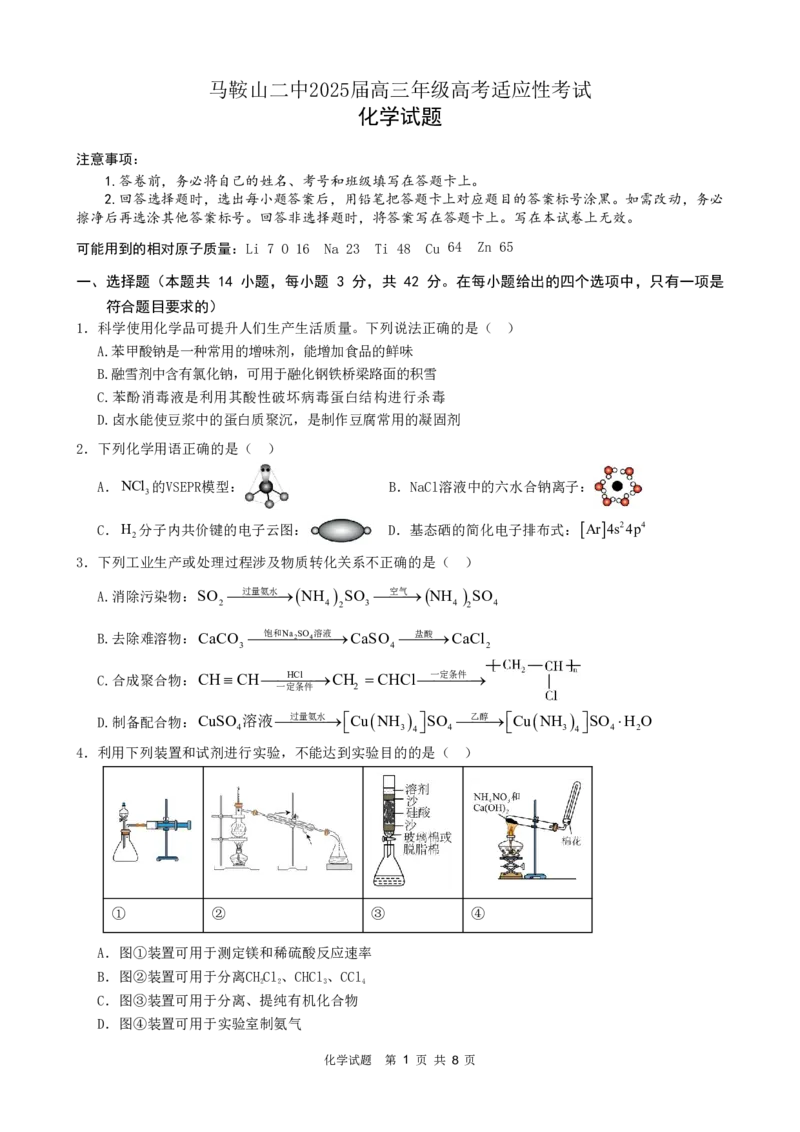
1.科学使用化学品可提升人们生产生活质量。下列说法正确的是( )
A.苯甲酸钠是一种常用的增味剂,能增加食品的鲜味
B.融雪剂中含有氯化钠,可用于融化钢铁桥梁路面的积雪
C.苯酚消毒液是利用其酸性破坏病毒蛋白结构进行杀毒
D.卤水能使豆浆中的蛋白质聚沉,是制作豆腐常用的凝固剂
2.下列化学用语正确的是( )
A.NCl 的VSEPR模型: B.NaCl溶液中的六水合钠离子:
3
C.H 分子内共价键的电子云图: D.基态硒的简化电子排布式: Ar 4s24p4
2
3.下列工业生产或处理过程涉及物质转化关系不正确的是( )
A.消除污染物:SO 过量氨水NH SO 空气NH SO
2 4 2 3 4 2 4
B.去除难溶物:CaCO 饱和Na 2 SO 4 溶液CaSO 盐酸CaCl
3 4 2
C.合成聚合物:CHCHHCl CH CHCl一定条件
一定条件 2
D.制备配合物:CuSO 溶液过量氨水CuNH SO 乙醇CuNH SO H O
4 3 4 4 3 4 4 2
4.利用下列装置和试剂进行实验,不能达到实验目的的是( )
① ② ③ ④
A.图①装置可用于测定镁和稀硫酸反应速率
B.图②装置可用于分离CHCl、CHCl、CCl
2 2 3 4
C.图③装置可用于分离、提纯有机化合物
D.图④装置可用于实验室制氨气
化学试题 第 1 页 共 8 页阅读下列材料,完成5∽6小题
硫元素及其化合物广泛应用于各个领域,例如:氯化亚砜(SOCl)极易与水反应,常用于脱去晶体中
2
的结晶水;过二硫酸根(S O 2-)因结构中含-O-O-,有强氧化性,常用作漂白剂、氧化剂。硫代硫酸钠
2 8
(NaSO)可看作SO2-中的1个氧原子被硫原子取代后的产物,因具有还原性用于去除自来水或纺织物中残
2 2 3 4
留的氯气。
已知25℃时,K(HSO)=10-1.89,K(HSO)=10-7.2 ,K(HS)=10-6.79,K(HS)=10-12.9
a1 2 3 a2 2 3 a1 2 a2 2
5.N是阿伏伽德罗常数的值,下列说法不正确的是( )
A
A.SO与O反应生成1molSO,转移的电子数为2N
2 2 3 A
B.1molSOCl含有的σ键数目为3N
2 A
C.1mol/L的NaS溶液中OH-的数目比1mol/L的NaSO多
2 2 3
D.25℃和101KPa下,1molHS气体体积约为24.5L
2
6.下列离子反应方程式或化学反应方程式书写错误的是( )
A.MgCl·6HO + 6SOCl △= MgCl + 6SO↑+ 12HCl↑
2 2 2 2 2
B.过量的SO通入NaS溶液中:2SO + 2HO + S2- = HS + 2HSO-
2 2 2 2 2 3
C.过二硫酸铵溶液中滴入KI溶液:SO2- + 2I- = 2SO2- + I
2 8 4 2
D.硫代硫酸钠去除自来水中残留的氯气:SO2- + 4Cl + 5HO = 2SO 2-+ 8Cl- +10H+
2 3 2 2 4
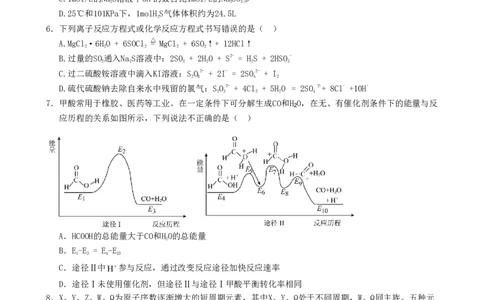
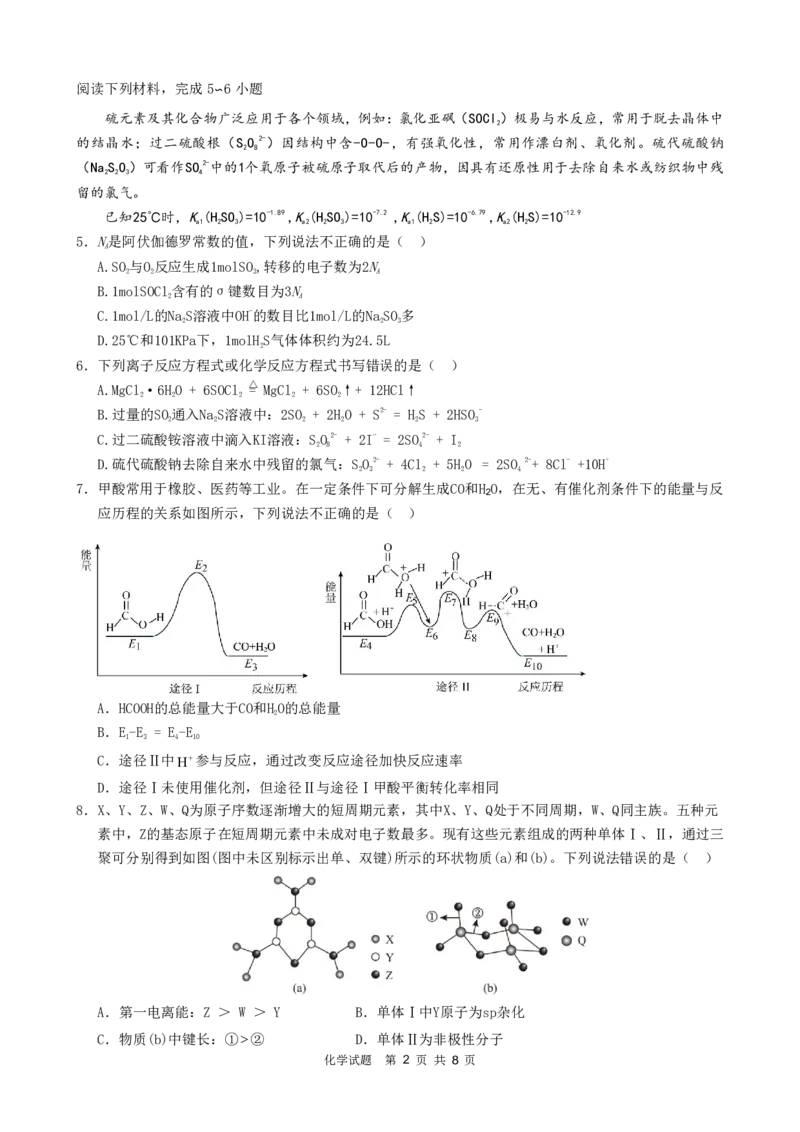
7.甲酸常用于橡胶、医药等工业。在一定条件下可分解生成CO和H O,在无、有催化剂条件下的能量与反
2
应历程的关系如图所示,下列说法不正确的是( )
A.HCOOH的总能量大于CO和HO的总能量
2
B.E-E = E-E
1 3 4 10
C.途径Ⅱ中H参与反应,通过改变反应途径加快反应速率
D.途径Ⅰ未使用催化剂,但途径Ⅱ与途径Ⅰ甲酸平衡转化率相同
8.X、Y、Z、W、Q为原子序数逐渐增大的短周期元素,其中X、Y、Q处于不同周期,W、Q同主族。五种元
素中,Z的基态原子在短周期元素中未成对电子数最多。现有这些元素组成的两种单体Ⅰ、Ⅱ,通过三
聚可分别得到如图(图中未区别标示出单、双键)所示的环状物质(a)和(b)。下列说法错误的是( )
A.第一电离能:Z > W > Y B.单体Ⅰ中Y原子为sp杂化
C.物质(b)中键长:①② D.单体Ⅱ为非极性分子
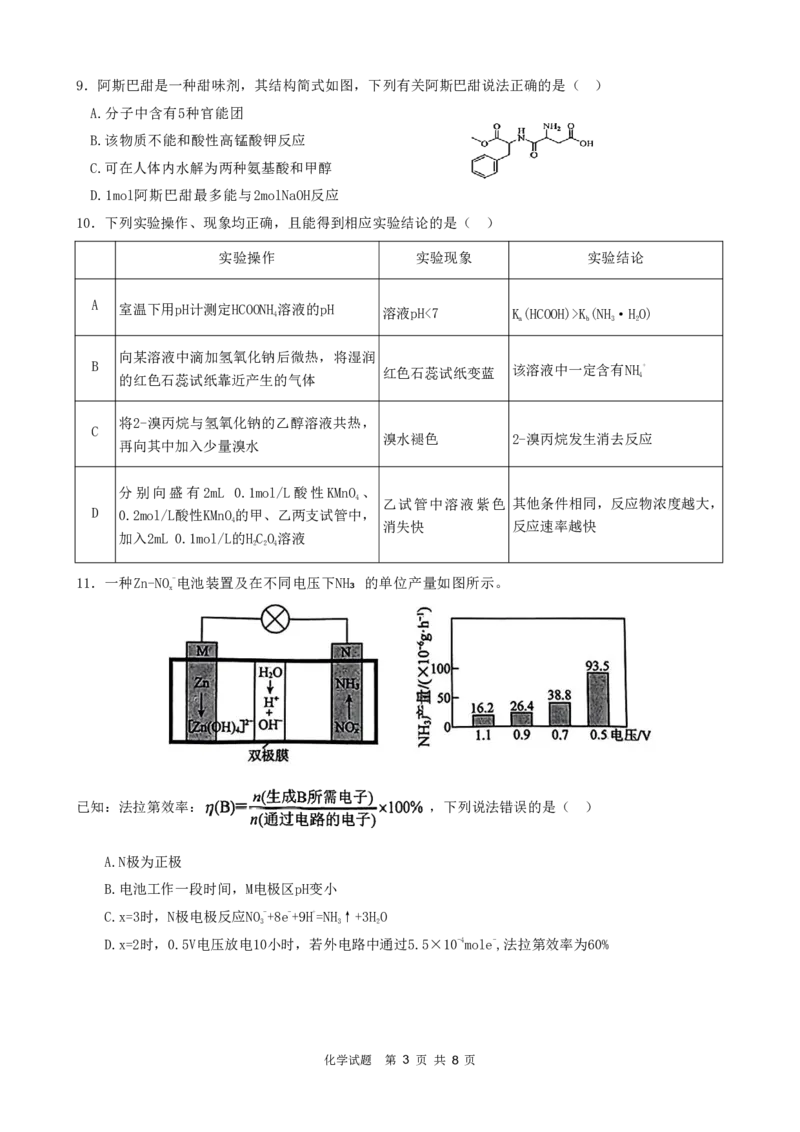
化学试题 第 2 页 共 8 页9.阿斯巴甜是一种甜味剂,其结构简式如图,下列有关阿斯巴甜说法正确的是( )
A.分子中含有5种官能团
B.该物质不能和酸性高锰酸钾反应
C.可在人体内水解为两种氨基酸和甲醇
D.1mol阿斯巴甜最多能与2molNaOH反应
10.下列实验操作、现象均正确,且能得到相应实验结论的是( )
实验操作 实验现象 实验结论
A
室温下用pH计测定HCOONH 4 溶液的pH 溶液pH<7 K(HCOOH)>K(NH·HO)
a b 3 2
向某溶液中滴加氢氧化钠后微热,将湿润
B
红色石蕊试纸变蓝
该溶液中一定含有NH+
的红色石蕊试纸靠近产生的气体 4
将2-溴丙烷与氢氧化钠的乙醇溶液共热,
C
溴水褪色 2-溴丙烷发生消去反应
再向其中加入少量溴水
分别向盛有2mL 0.1mol/L酸性KMnO 、
4 乙试管中溶液紫色 其他条件相同,反应物浓度越大,
D 0.2mol/L酸性KMnO的甲、乙两支试管中,
4 消失快 反应速率越快
加入2mL 0.1mol/L的HCO溶液
2 2 4
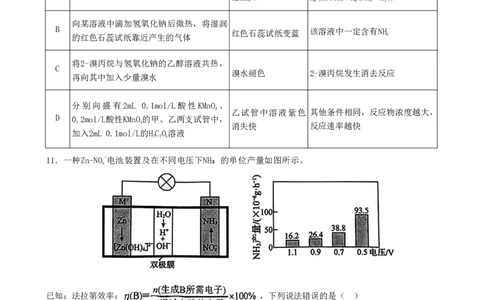
11.一种Zn-NO-电池装置及在不同电压下NH₃ 的单位产量如图所示。
x
已知:法拉第效率: ,下列说法错误的是( )
A.N极为正极
B.电池工作一段时间,M电极区pH变小
C.x=3时,N极电极反应NO-+8e-+9H+=NH↑+3HO
3 3 2
D.x=2时,0.5V电压放电10小时,若外电路中通过5.5×10-4mole-,法拉第效率为60%
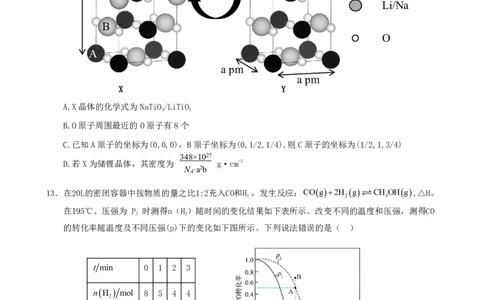
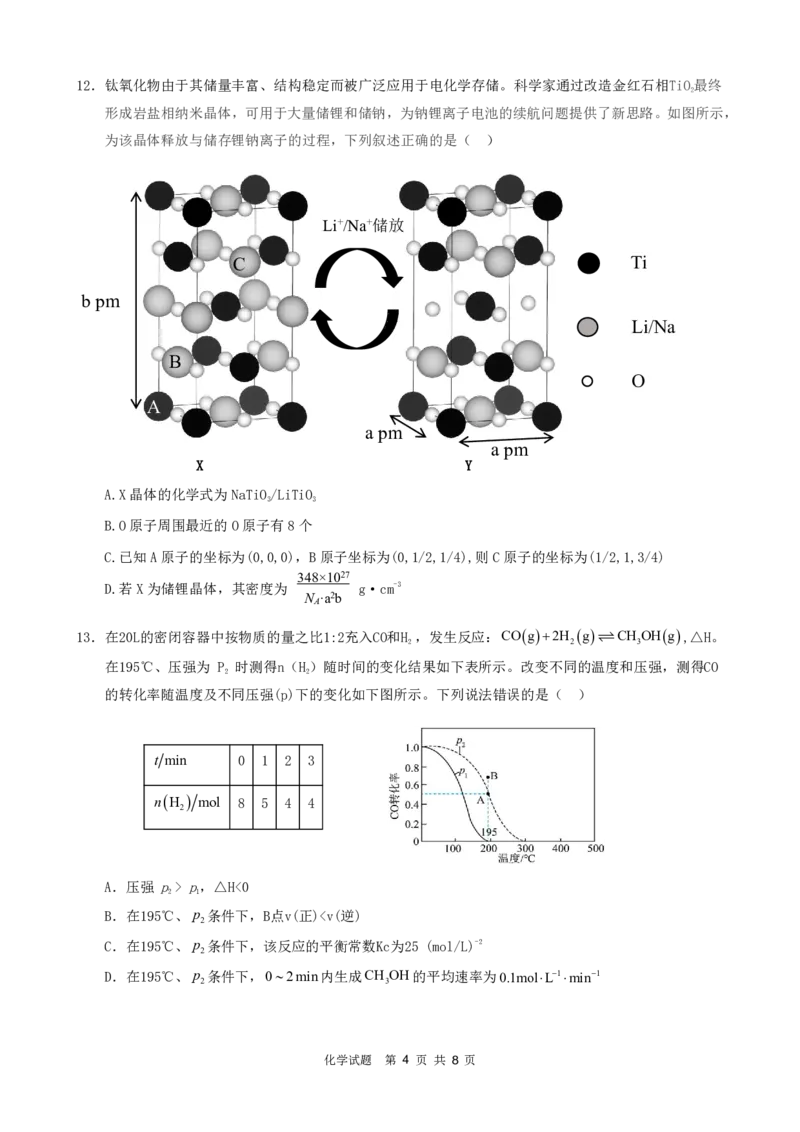
化学试题 第 3 页 共 8 页12.钛氧化物由于其储量丰富、结构稳定而被广泛应用于电化学存储。科学家通过改造金红石相TiO最终
2
形成岩盐相纳米晶体,可用于大量储锂和储钠,为钠锂离子电池的续航问题提供了新思路。如图所示,
为该晶体释放与储存锂钠离子的过程,下列叙述正确的是( )
Li+/Na+储放
C Ti
b pm
Li/Na
B
O
A
a pm
a pm
X Y
A.X晶体的化学式为NaTiO/LiTiO
3 3
B.O原子周围最近的O原子有8个
C.已知A原子的坐标为(0,0,0),B原子坐标为(0,1/2,1/4),则C原子的坐标为(1/2,1,3/4)
348×1027
D.若X为储锂晶体,其密度为 g·cm-3
N ·a2b
A
13.在20L的密闭容器中按物质的量之比1:2充入CO和H ,发生反应:COg2H g CH OHg,△H。
2 2 3
在195℃、压强为 P 时测得n(H)随时间的变化结果如下表所示。改变不同的温度和压强,测得CO
2 2
的转化率随温度及不同压强(p)下的变化如下图所示。下列说法错误的是( )
t min 0 1 2 3
nH mol 8 5 4 4
2
A.压强 p> p,△H<0
2 1
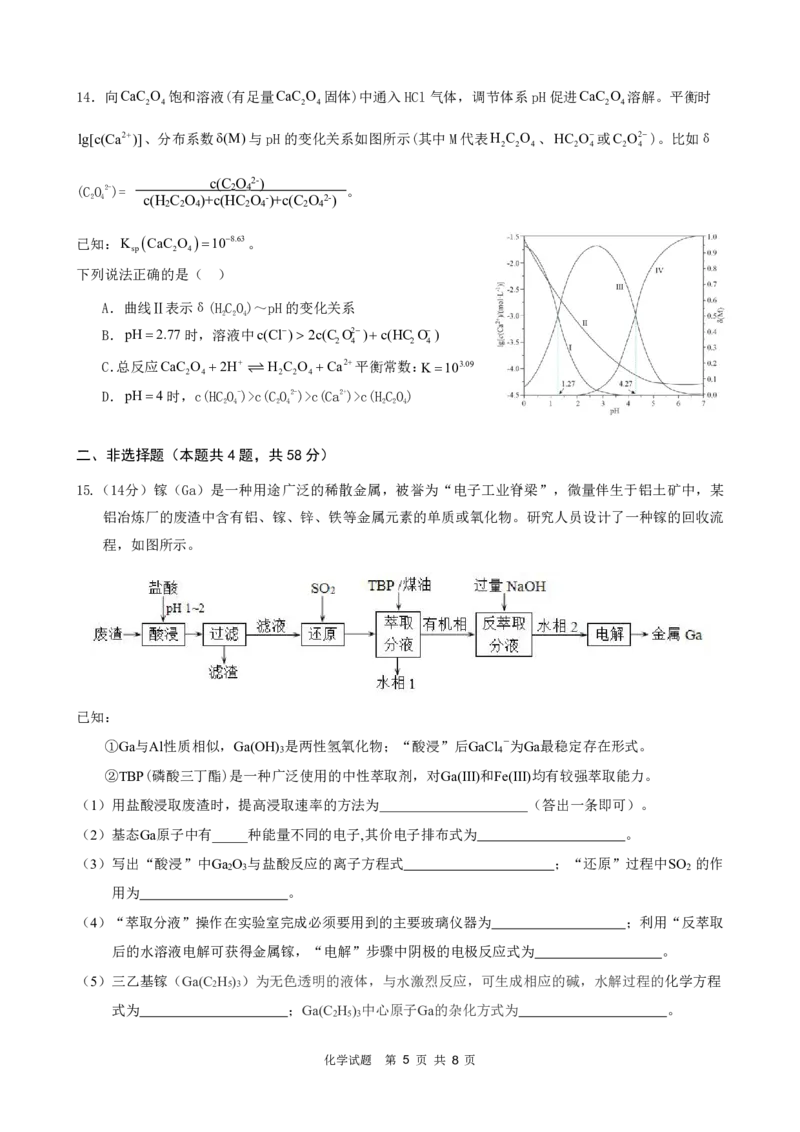
B.在195℃、 p 条件下,B点v(正)c(CO2-)>c(Ca2+)>c(HCO)
2 4 2 4 2 2 4
二、非选择题(本题共4题,共58分)
15.(14分)镓(Ga)是一种用途广泛的稀散金属,被誉为“电子工业脊梁”,微量伴生于铝土矿中,某
铝冶炼厂的废渣中含有铝、镓、锌、铁等金属元素的单质或氧化物。研究人员设计了一种镓的回收流
程,如图所示。
已知:
①Ga与Al性质相似,Ga(OH) 是两性氢氧化物;“酸浸”后GaCl -为Ga最稳定存在形式。
3 4
②TBP(磷酸三丁酯)是一种广泛使用的中性萃取剂,对Ga(Ⅲ)和Fe(Ⅲ)均有较强萃取能力。
(1)用盐酸浸取废渣时,提高浸取速率的方法为 (答出一条即可)。
(2)基态Ga原子中有_____种能量不同的电子,其价电子排布式为 。
(3)写出“酸浸”中Ga O 与盐酸反应的离子方程式 ;“还原”过程中SO 的作
2 3 2
用为 。
(4)“萃取分液”操作在实验室完成必须要用到的主要玻璃仪器为 ;利用“反萃取
后的水溶液电解可获得金属镓,“电解”步骤中阴极的电极反应式为 。
(5)三乙基镓(Ga(C H ) )为无色透明的液体,与水激烈反应,可生成相应的碱,水解过程的化学方程
2 5 3
式为 ;Ga(C H ) 中心原子Ga的杂化方式为 。
2 5 3
化学试题 第 5 页 共 8 页16.(15分)某小组欲探究钠与酸溶液反应速度的影响因素,查阅资料并设计实验进行分析和验证。
已知:
ⅰ.任何反应都会经历以下四个步骤:吸附、反应、解附、扩散。
ⅱ.钠与水反应动力学机理:
①钠在水分子作用下释放电子:(Na) (Na)x++ xe- ;
n ⟶ n
②释放的电子有如下两种过程:
与水形成溶剂化电子:HO + e- HOe-, HOe- OH-+ H, H + H H
2 ⟶ 2 2 ⟶ ⟶ 2
与水中水合氢离子结合:HO++ e- HO, HO HO + H, H + H H
3 ⟶ 3 3 ⟶ 2 ⟶ 2
ⅲ.30℃时含钠化合物的溶解度:
NaCl: 6.2 mol/L CHCOONa: 6.5 mol/L NaF: 1.0 mol/L
3
方案Ⅰ:取三块大小相同形状均匀的钠块,分别投入20mL0.1mol/L的盐酸、NaOH溶液和水中,测量反应时
间,如下:
溶液 HO 0.1mol/L的盐酸 0.1mol/LNaOH
2
反应时间/s 46 45 45
(1)实验室钠保存在 。下列图标与演示Na与水反应实验有关的是( )
A B C D
(2)从实验数据分析,写出钠在盐酸溶液中主要发生的化学反应方程式 ,
理由: 。
(3)为进一步验证上述结论,小组将质量相等,大小形状相同的Na分别与0.05mol/L和0.3mol/L的稀盐酸
(盐酸中滴加酚酞)反应后发现,前者实验过程中能够明显观察到钠球运动的轨迹上出现红色,而
后者没有观察到红色。
结合方程式解释Na与0.05mol/L的稀盐酸反应轨迹上出现红色可能的原因: 。
(4)小组研究又发现:盐酸浓度的改变也会影响其与钠的反应速度。
方案Ⅱ:取200mg形状几乎一样的7块钠,分别投入预先配制好的浓度不同的盐酸和水中,分别计时,实验
结果如下:
浓度/mol/L 6 3 1.5 1 0.1 0.05 0
反应时间/s 114 65 37 21 13 18 20
由该实验可知,当盐酸浓度大于1mol/L时,浓度越大,反应速度越慢,请分析可能的原因
。设计实验方案并根据预测现象证明你的猜想: 。
(可供选择的试剂:PH=1的氢氟酸,PH=1的醋酸溶液,PH=1的盐酸溶液)。
化学试题 第 6 页 共 8 页17.(15分)乙烯和丙烯是有机合成工业重要的原料,由相应烷烃制备的方法研究备受关注。回答下列问题:
【乙烷制乙烯】
(1)乙烷氧化脱氢制备乙烯是化工生产中的重要工艺。
主反应:2CH (g)+O (g) ══ 2CH (g)+2HO (g) ΔH= −209.8 kJ·mol−1 ;
2 6 2 2 4 2 1
副反应:CH (g) ══ CH (g)+H (g) ΔH > 0 。
2 4 2 2 2 2
①副反应在 (填“高温”或“低温”或“任意温度”)下易自发进行。
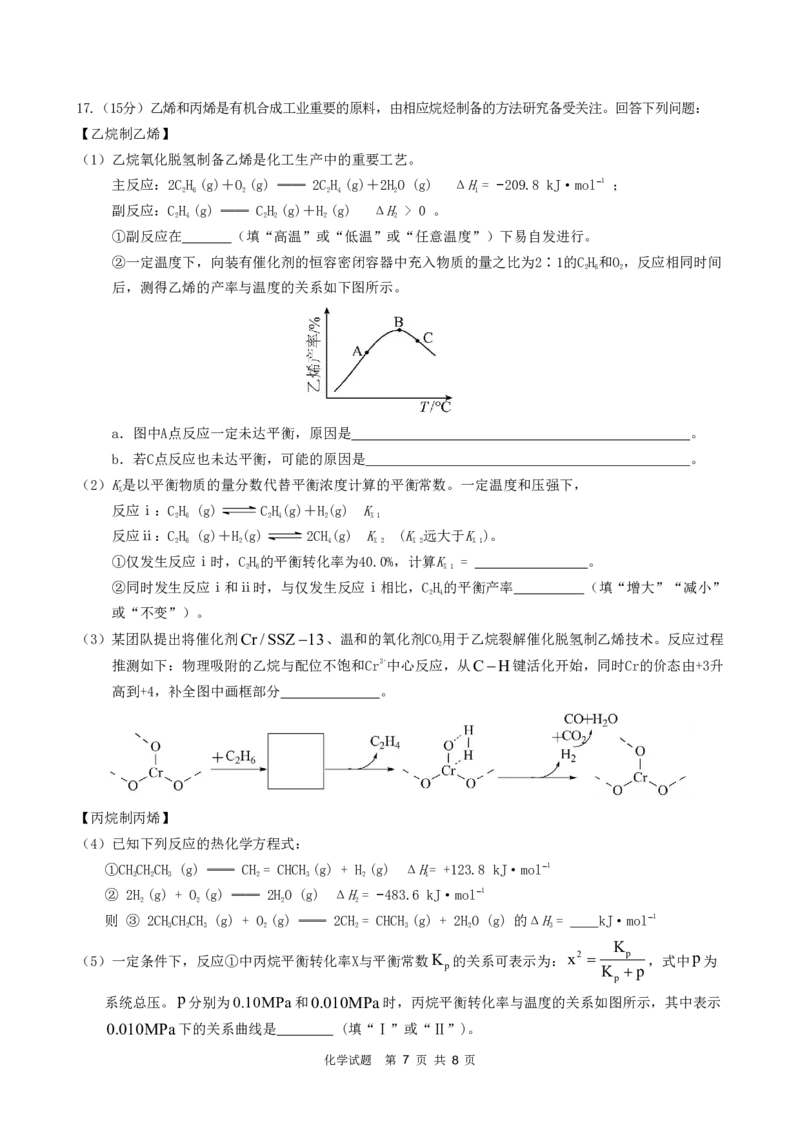
②一定温度下,向装有催化剂的恒容密闭容器中充入物质的量之比为2∶1的CH和O,反应相同时间
2 6 2
后,测得乙烯的产率与温度的关系如下图所示。
a.图中A点反应一定未达平衡,原因是 。
b.若C点反应也未达平衡,可能的原因是 。
(2)K是以平衡物质的量分数代替平衡浓度计算的平衡常数。一定温度和压强下,
X
反应ⅰ:CH (g) CH(g)+H(g) K
2 6 2 4 2 X1
反应ⅱ:CH (g)+H(g) 2CH(g) K (K 远大于K )。
2 6 2 4 X2 X2 X1
①仅发生反应ⅰ时,CH的平衡转化率为40.0%,计算K = 。
2 6 X1
②同时发生反应ⅰ和ⅱ时,与仅发生反应ⅰ相比,CH的平衡产率 (填“增大”“减小”
2 4
或“不变”)。
(3)某团队提出将催化剂Cr/SSZ13、温和的氧化剂CO用于乙烷裂解催化脱氢制乙烯技术。反应过程
2
推测如下:物理吸附的乙烷与配位不饱和Cr3+中心反应,从CH键活化开始,同时Cr的价态由+3升
高到+4,补全图中画框部分 。
【丙烷制丙烯】
(4)已知下列反应的热化学方程式:
①CHCHCH (g) ══ CH = CHCH (g) + H (g) ΔH= +123.8 kJ·mol−1
3 2 3 2 3 2 1
② 2H (g) + O (g) ══ 2HO (g) ΔH= −483.6 kJ·mol−1
2 2 2 2
则 ③ 2CHCHCH (g) + O (g) ══ 2CH = CHCH (g) + 2HO (g) 的ΔH= kJ·mol−1
3 2 3 2 2 3 2 3
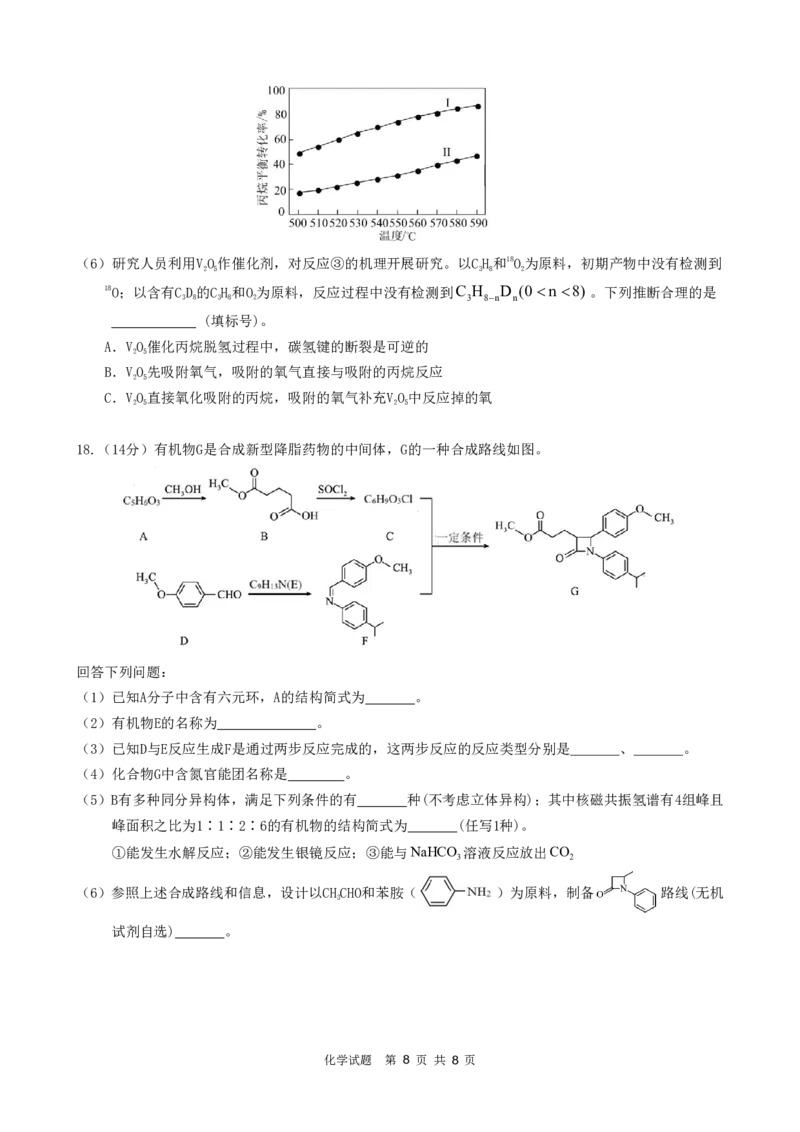
K
(5)一定条件下,反应①中丙烷平衡转化率X与平衡常数K 的关系可表示为:x2 p ,式中p为
p K p
p
系统总压。p分别为0.10MPa和0.010MPa时,丙烷平衡转化率与温度的关系如图所示,其中表示
0.010MPa下的关系曲线是 (填“Ⅰ”或“Ⅱ”)。
化学试题 第 7 页 共 8 页(6)研究人员利用VO作催化剂,对反应③的机理开展研究。以CH和18O为原料,初期产物中没有检测到
2 5 3 8 2
18O;以含有CD的CH和O为原料,反应过程中没有检测到C H D (0 n 8) 。下列推断合理的是
3 8 3 8 2 3 8n n
(填标号)。
A.VO催化丙烷脱氢过程中,碳氢键的断裂是可逆的
2 5
B.VO先吸附氧气,吸附的氧气直接与吸附的丙烷反应
2 5
C.VO直接氧化吸附的丙烷,吸附的氧气补充VO中反应掉的氧
2 5 2 5
18.(14分)有机物G是合成新型降脂药物的中间体,G的一种合成路线如图。
回答下列问题:
(1)已知A分子中含有六元环,A的结构简式为 。
(2)有机物E的名称为 。
(3)已知D与E反应生成F是通过两步反应完成的,这两步反应的反应类型分别是 、 。
(4)化合物G中含氮官能团名称是 。
(5)B有多种同分异构体,满足下列条件的有 种(不考虑立体异构);其中核磁共振氢谱有4组峰且
峰面积之比为1∶1∶2∶6的有机物的结构简式为 (任写1种)。
①能发生水解反应;②能发生银镜反应;③能与NaHCO 溶液反应放出CO
3 2
(6)参照上述合成路线和信息,设计以CHCHO和苯胺( )为原料,制备 路线(无机
3
试剂自选) 。
化学试题 第 8 页 共 8 页