文档内容
2026 届高三年级上学期中调研考试
化 学
本试卷满分100分,考试时间75 分钟。
可能用到的相对原子质量:H1 Li 7 C12 O 16 Al 27 Fe56 Co 59
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列物质性质与用途以及对应关系均正确的是
选项 性质 用途
A 碳酸钠能与酸反应 用于治疗胃酸过多
B 维生素 C 具有还原性 可作补铁剂中的抗氧化剂
C 明矾水解使溶液呈酸性 用作净水剂
D SiO₂是良好的半导体 用于制作光导纤维
2.下列各组实验方法中,可行的是
A.除去苯中少量苯酚:加入浓溴水,静置,过滤
B.除去 KNO₃ 中少量 NaCl:蒸发结晶、趁热过滤
C.分离铁粉和I₂的混合物:加热升华,收集碘蒸气
D.测定青蒿素的分子结构:X射线衍射技术
3.某利胆药物的结构如图所示。下列说法正确的是
A.分子式为 C H O N B.分子中含氧官能团有3种
13 10 3
C.能发生氧化、还原、水解反应 D.苯环上的一氯代物有8种
4.下列生产、生活实践中涉及的化学知识合理的是
选项 生产、生活实践 化学知识
A 电子工业中腐蚀印刷电路板 2FeCl₃+3Cu=2Fe+3CuCl₂
B 侯氏制碱法中制备NaHCO₃
NH₃+CO₂+H₂O=HCO₃⁻+NH₄⁺
C 纯碱溶液去除油污 CO₃²⁻+2H₂O=H₂CO₃+2OH⁻
D 利用“吹出法”进行海水提溴SO₂+Br₂+2H₂O=H₂SO₄+2HBr
5.某含氟化合物的结构如图所示(图中环上及与环直接相连的原子共面)。下列说法错误的是
A.环上C、N原子均为sp²杂化 B. BF₄ 中含配位键,为正四面体结构
C.该化合物室温时可能呈液态 D.涉及元素中,N的第一电离能最大
阅读下列材料,完成6~7小题。
氯是一种重要的“成盐元素”。氯气性质很活泼,能与大多数金属和大多数非金属单质化合。氯气
与水反应可生成次氯酸,在不同温度下与 NaOH溶液反应可生成 NaClO 或 NaClO 。Cl O和 ClO₂分子
3 2
均为Ⅴ形结构。Cl₂O的中心原子为O,可利用氯气和HgO或潮湿的碳酸钠反应生成;ClO₂的中心原子为
Cl,存在大π键,可用NaClO₃在强酸性溶液中与SO₂反应制得。
6.下列叙述正确的是
A.次氯酸的结构式为 H—O—Cl
B.常温下,潮湿的液氯可储存于钢瓶中
C.铜在氯气中燃烧可生成蓝色氯化铜固体
D.氯气能与HgO 反应生成 Cl₂O 和单质 Hg
7.下列有关物质结构或性质的比较中,正确的是
A.键角:( Cl O>SO B. Cl—O键的键长:( Cl O>ClO
2 2 2 2
C.25℃时同浓度水溶液的1pH :NaClO >NaClO D.酸性条件下氧化性: SO >Cl
3 2 2
8. NA 是阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,2.24 L三氧化硫中氧原子数为0.3N
A
B.常温常压下,11.2g 乙烯中含有的价电子总数为4.8N
A
C. Na₂O₂与CO₂反应中,生成1.6g O₂时转移电子数为0.2N
A
D.16.8g 铁与水蒸气完全反应,生成H₂分子的数目为0.3N
A
9.某化合物结构如图所示,其中元素X、Y、Z、R、W分布在三个短周期,原子序数依次增大,Y、Z
相邻。下列说法正确的是A.电负性:Y>Z>X
B.简单离子半径:ZCO₃²⁻
将3体积乙醇慢慢加入1 体积浓硫酸中,混
D 溴水褪色 有乙烯生成
匀后170 ℃共热,生成的气体通入溴水中
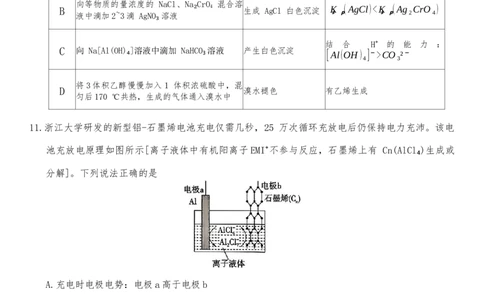
11.浙江大学研发的新型铝-石墨烯电池充电仅需几秒,25 万次循环充放电后仍保持电力充沛。该电
池充放电原理如图所示[离子液体中有机阳离子EMI⁺不参与反应,石墨烯上有 Cn(AlCl₄)生成或
分解]。下列说法正确的是
A.充电时电极电势:电极a高于电极b
B.比能量:新型铝-石墨烯电池小于锂电池
C.充电时电子流向:电极 a→离子液体→电极b
D.放电时离子液体中
n(AlCl-)/n(Al Cl-)的值变大
4 2 7
12.用天然气制备( CS 的反应为 CH (g)+2H S(g)=CS (g)+4H (g)。 为探究平衡体系组成与温度的关
2 4 2 2 2
系,某小组按 n(CS ):n(H )=1:4投料、维持压强不变进行实验,结果如图(图中x表示平衡体系中各
2 2
组分的物质的量分数)。下列说法正确的是A. b、d 分别表示 CH₄和CS₂
B.840 ℃时, x(CH ):x(H )=1:2
4 2
C.升高温度,CS₂制备反应的平衡常数减小
D.其他条件不变,增加 H₂的量,平衡体系中x(H₂S)增大
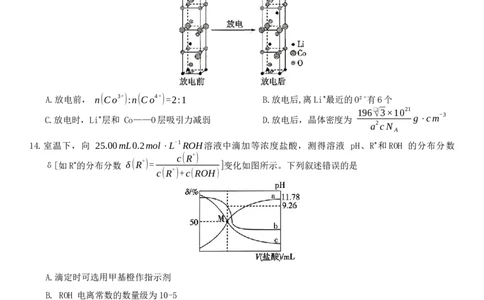
13.某钴酸锂电池电极材料 Li CoO 放电时发生如图变化(其中 Co为+3 价或+4价;晶胞为六方晶系,放电
1-x 2
后晶胞参数为a nm、a nm、c nm,夹角为90°、90°、60°)。下列说法错误的是
A.放电前, n(Co3+):n(Co4+)=2:1 B.放电后,离Li⁺最近的O²⁻有6个
196❑√3×1021
C.放电时,Li⁺层和 Co——O层吸引力减弱 D.放电后,晶体密度为
g⋅cm-3
a2cN
A
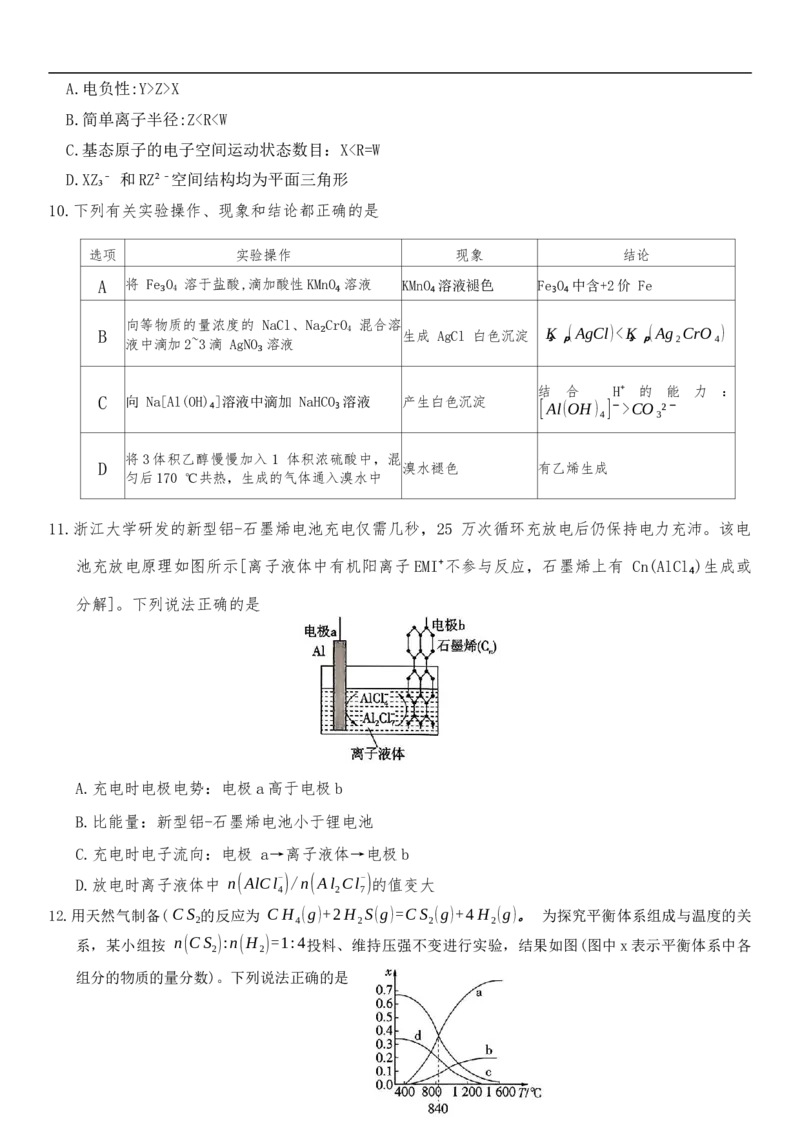
14.室温下,向 25.00mL0.2mol⋅L-1ROH溶液中滴加等浓度盐酸,测得溶液 pH、R⁺和ROH 的分布分数
c(R+)
δ[如R⁺的分布分数
δ(R+)=
]变化如图所示。下列叙述错误的是
c(R+)+c(ROH)
A.滴定时可选用甲基橙作指示剂
B. ROH 电离常数的数量级为10-5
C. V(盐酸)=12.50 mL时,c(ROH)>c(R⁺)
D. pH=7时, c(ROH)+c(Cl-)>0.1mol⋅L-1
二、非选择题:本题共4 小题,共58分。
15.(15分)苯甲酸的制备、分离提纯及含量测定实验如下:
反应原理:
实验装置示意图(夹持及加热装置已省略):实验步骤:
1.向三颈烧瓶中加入2.7 mL甲苯、100mL水和2~3片碎瓷片,连接好仪器。通入冷凝水,启动搅拌
器,加热至沸腾,分批加入8.5g高锰酸钾,煮沸至甲苯层消失,停止加热和搅拌。
2.反应混合物过滤(除去MnO₂)后,用少量热水洗涤滤渣,合并滤液和洗涤液,并放入冷水浴中冷却,
用浓盐酸酸化,至苯甲酸全部析出为止,过滤得苯甲酸粗品。
3.将苯甲酸粗品溶于沸水制成饱和溶液,趁热过滤,所得滤液置于冰水浴中结晶,抽滤、干燥后称
重。
4.称取1.200g所得产品,配成100 mL乙醇溶液,移取25.00 mL 溶液于锥形瓶中,滴加2~3滴酚酞溶
液,用0.1200 mol·L⁻¹木标准 KOH 溶液滴定,平行测定三次,终点时平均消耗20.00 mL KOH溶液。
回答下列问题:
(1)球形冷凝管的作用为 ,进水口为 (填“a”或“b”)。
(2)将高锰酸钾粉末分批加入的目的是 。制备反应中甲苯与高
锰酸钾的物质的量之比为 。
(3)步骤1反应完成后,若混合物呈紫色,须加入草酸还原(生成MnO₂和KHCO₃),反应的离子方程式
为 。
(4)苯甲酸提纯操作中,趁热过滤前加少量热水的目的是 ;抽滤的优点是
(答1点即可)。
(5)滴定终点的现象是 ;产品中苯甲酸的质量分数
为 。
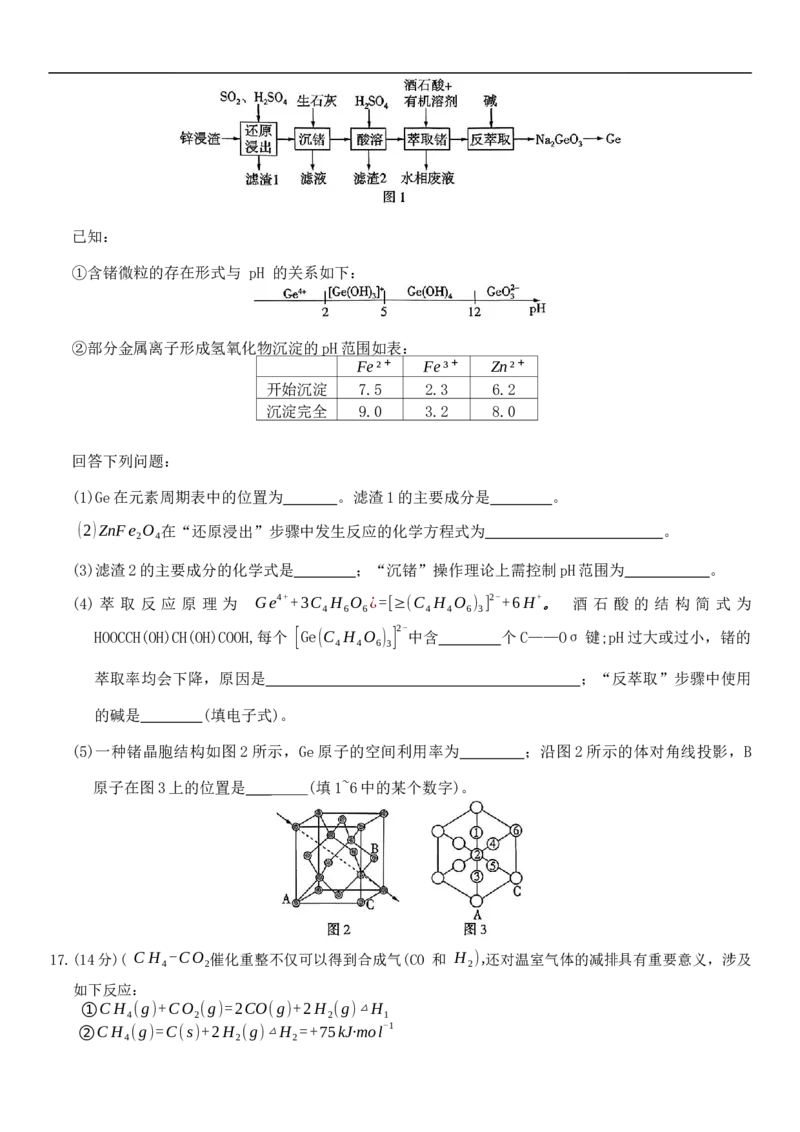
16.(14分)锗是一种具有重要战略价值的稀有金属,广泛应用于半导体、光电子和航天等领域。利用某
锌浸渣(主要含有 ZnFe O 、GeO SiO 等)提取 Ge的流程如图1 所示。
2 4 2 2已知:
①含锗微粒的存在形式与 pH 的关系如下:
②部分金属离子形成氢氧化物沉淀的pH范围如表:
Fe²⁺ Fe³⁺ Zn²⁺
开始沉淀 7.5 2.3 6.2
沉淀完全 9.0 3.2 8.0
回答下列问题:
(1)Ge在元素周期表中的位置为 。滤渣1的主要成分是 。
(2)ZnFe O 在“还原浸出”步骤中发生反应的化学方程式为 。
2 4
(3)滤渣2的主要成分的化学式是 ;“沉锗”操作理论上需控制pH范围为 。
(4) 萃 取 反 应 原 理 为 Ge4++3C H O ¿=[≥(C H O ) ] 2-+6H+ 。 酒 石 酸 的 结 构 简 式 为
4 6 6 4 4 6 3
2-
HOOCCH(OH)CH(OH)COOH,每个 [Ge(C H O ) ] 中含 个C——Oσ键;pH过大或过小,锗的
4 4 6 3
萃取率均会下降,原因是 ;“反萃取”步骤中使用
的碱是 (填电子式)。
(5)一种锗晶胞结构如图2所示,Ge原子的空间利用率为 ;沿图2所示的体对角线投影,B
原子在图3上的位置是 (填1~6中的某个数字)。
17.(14分)( CH -CO 催化重整不仅可以得到合成气(CO 和 H ),还对温室气体的减排具有重要意义,涉及
4 2 2
如下反应:
①CH (g)+CO (g)=2CO(g)+2H (g)△H
4 2 2 1
②CH (g)=C(s)+2H (g)△H =+75kJ·mol-1
4 2 2③2CO(g)=CO (g)+C(s)△H =-172kJ·mol-1
2 3
④CO (g)+H (g)=CO(g)+H O(g)△H =+41kJ·mol-1
2 2 2 4
回答下列问题:
(1)△H =_。
1
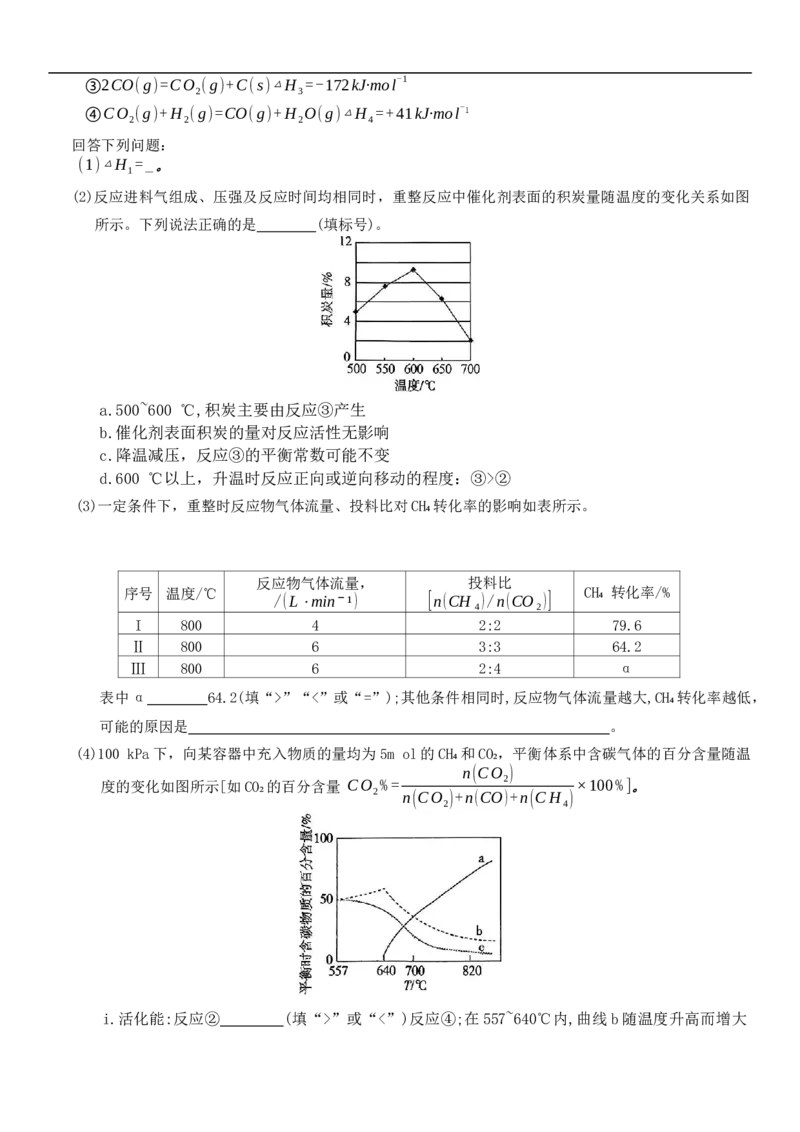
(2)反应进料气组成、压强及反应时间均相同时,重整反应中催化剂表面的积炭量随温度的变化关系如图
所示。下列说法正确的是 (填标号)。
a.500~600 ℃,积炭主要由反应③产生
b.催化剂表面积炭的量对反应活性无影响
c.降温减压,反应③的平衡常数可能不变
d.600 ℃以上,升温时反应正向或逆向移动的程度:③>②
(3)一定条件下,重整时反应物气体流量、投料比对CH₄转化率的影响如表所示。
反应物气体流量, 投料比
序号 温度/℃ CH₄ 转化率/%
/(L⋅min⁻¹) [n(CH₄)/n(CO₂)]
I 800 4 2:2 79.6
Ⅱ 800 6 3:3 64.2
Ⅲ 800 6 2:4 α
表中α 64.2(填“>”“<”或“=”);其他条件相同时,反应物气体流量越大,CH₄转化率越低,
可能的原因是 。
(4)100 kPa下,向某容器中充入物质的量均为5m ol的CH₄和CO₂,平衡体系中含碳气体的百分含量随温
n(CO )
度的变化如图所示[如CO₂的百分含量 CO %= 2 ×100%]。
2 n(CO )+n(CO)+n(CH )
2 4
i.活化能:反应② (填“>”或“<”)反应④;在557~640℃内,曲线b随温度升高而增大的原因是 。
n(H )
ii.840℃时,曲线a、b对应含碳物质的百分含量分别为70%、20%, 2 =6,则CH₄的转化率
n(H O)
2
为 ,反应④的 K =
p
n(CO)
iii.恒温恒容条件下,向平衡体系中通入少量 CH₄,重新达平衡后, 的值将 (填
n(CO )
2
“增大”“减小”或“不变”)。
18.(15 分)某药物中间体G的合成路线如下:
已知:
❑
②RBr+Mg→RMgBr(RMgBrr不能与酸、水、醇等共存)。
回答下列问题:
(1)F→G 的反应类型为 。
(3)下列说法错误的是 (填标号)。
a. A→B 涉及加成反应
b.1m ol C 最多可与6m ol H₂反应
c. C→D转化中,原子利用率为100%
d.CH =CHMgBr与醇、醛和羧酸均能反应
2
(4)D的结构简式为 。
(5)已知物质X的分子式为C₃H₃OCl,写出B→C 的化学反应方程式 。
(6)A的芳香族同分异构体中,同时满足下列条件的有 种;其中核磁共振氢谱中显示有6组
峰,可能的结构是 (任写1种)。
①能与 NaOH 溶液反应 ②能发生银镜反应 ③不含甲基(7)参照上述合成路线,设计以和 丙 酮 为 原 料 制 取 4◯ ◯ 0H 的 路 线
(其他试剂任选)。
化学答案
1-5 BDCDD 6-10 ABBCC 11-14 BBCC