文档内容
长沙市一中2026届高三月考试卷(四)
化 学
时量:75分钟 满分:100分
得分:
可能用到的相对原子质量:H—1 C—12 N—14 O—16 Cl—35.5
一、选择题(本题共14小题,每小题3分,共42分。每小题只有一项符合题目要求)
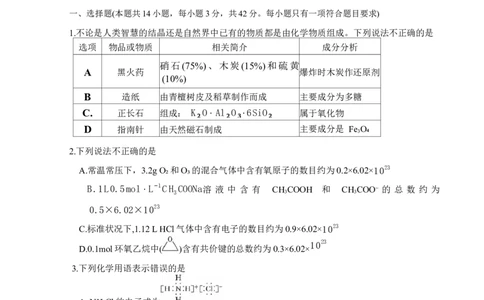
1.不论是人类智慧的结晶还是自然界中已有的物质都是由化学物质组成。下列说法不正确的是
选项 物品或物质 相关简介 成分分析
硝石(75%)、木炭(15%)和硫黄
A 黑火药 爆炸时木炭作还原剂
(10%)
B 造纸 由青檀树皮及稻草制作而成 主要成分为多糖
C. 正长石 组成: K₂O⋅Al₂O₃⋅6SiO₂ 属于氧化物
D 指南针 由天然磁石制成 主要成分是 Fe O₄
3
2.下列说法不正确的是
A.常温常压下,3.2g O₂和O₃的混合气体中含有氧原子的数目约为0.2×6.02×1023
B.1L0.5mol⋅L−1CH COONa溶 液 中 含 有 CH COOH 和 CH COO⁻ 的 总 数 约 为
3 3 3
0.5×6.02×1023
C.标准状况下,1.12 L HCl气体中含有电子的数目约为0.9×6.02×1023
1023
D.0.1mol环氧乙烷中( )含有共价键的总数约为0.3×6.02×
3.下列化学用语表示错误的是
A. NH Cl的电子式为
4
B.基态氧原子的核外电子轨道表示式:
C. NCl 的 VSEPR模型:
3
D.乙醚的结构简式为 CH OCH
3 34.如图利用海带提取单质碘的实验原理与装置不能达到实验目的的是
A.用装置甲灼烧海带 B.用装置乙过滤海带灰浸泡液
C.用装置丙得到 I 的 CCl 溶液 D.用装置丁提纯粗碘
2 4
5.一种农业常用肥料的结构如图所示,该物质的水溶液显酸性。其中 X、Y、Z、W为核电荷数依
次增大的前四周期元素,且位于不同周期,基态 W 原子内层有空轨道且最高能级有1个未成对
电子。下列说法正确的是
A.W⁺可通过强相互作用力与冠醚组成超分子
B. Z的简单气态氢化物的热稳定性比Y 的强
C. Y与其他三种元素均可形成两种或两种以上的二元化合物
(D.该物质的水溶液中: c(X ZY )>c(XZY2−)
3 4 4
6.下列实验能达到目的的是
选项 实验目的 实验方法或操作
酸碱中和滴定的同时,用温度传感器采集锥形瓶内
A 测定中和反应的反应热
溶液的温度
探究浓度对化学反应速率量取同体积不同浓度的 NaClO 溶液,分别加入等体
B
的影响 积等浓度的NaSO₃溶液,对比现象
2
判断反应后 Ba²⁺是否沉淀将NaSO₃溶液与BaCl₂ 溶液混含₂反应后静置,向
2
C
完全 上层清液中再加1滴NaSO₃溶液
2
D 检验淀粉是否发生了水解向淀粉水解液中加入碘水7.下列离子方程式或化学方程式书写正确且符合题意的是
A.向 Ba(NO ) 溶液中通入SO₂,产生白色沉淀,发生的离子反应为
3 2
Ba2++SO + H O=BaSO ↓+2H+
2 2 3
B.向K [Fe(CN)₆]溶液中加入少量铁粉,产生蓝色沉淀,发生的离子反应为
3
Fe+2 [Fe(CN) ] 3− =Fe2++2[Fe(CN) ] 4− , K++Fe2++[Fe(CN) ]3-= KFe[Fe(CN) ]↓
6 6 6 6
C.向硫酸酸化的 KMnO₄ 溶液中加入少量 NaS,再滴加 BaCl 溶液,产生白色沉淀,证明一定发生
2 2
了离子反应: 8MnO−+5S2− +24H+=8Mn2++5SO2− +12H O
4 4 2
D.铝和重氢氧化钠的HO溶液反应的化学方程式:
2
2Al+2NaOD+6H O= 2Na[Al(OH) ]+D ↑+2H ↑
2 4 2 2
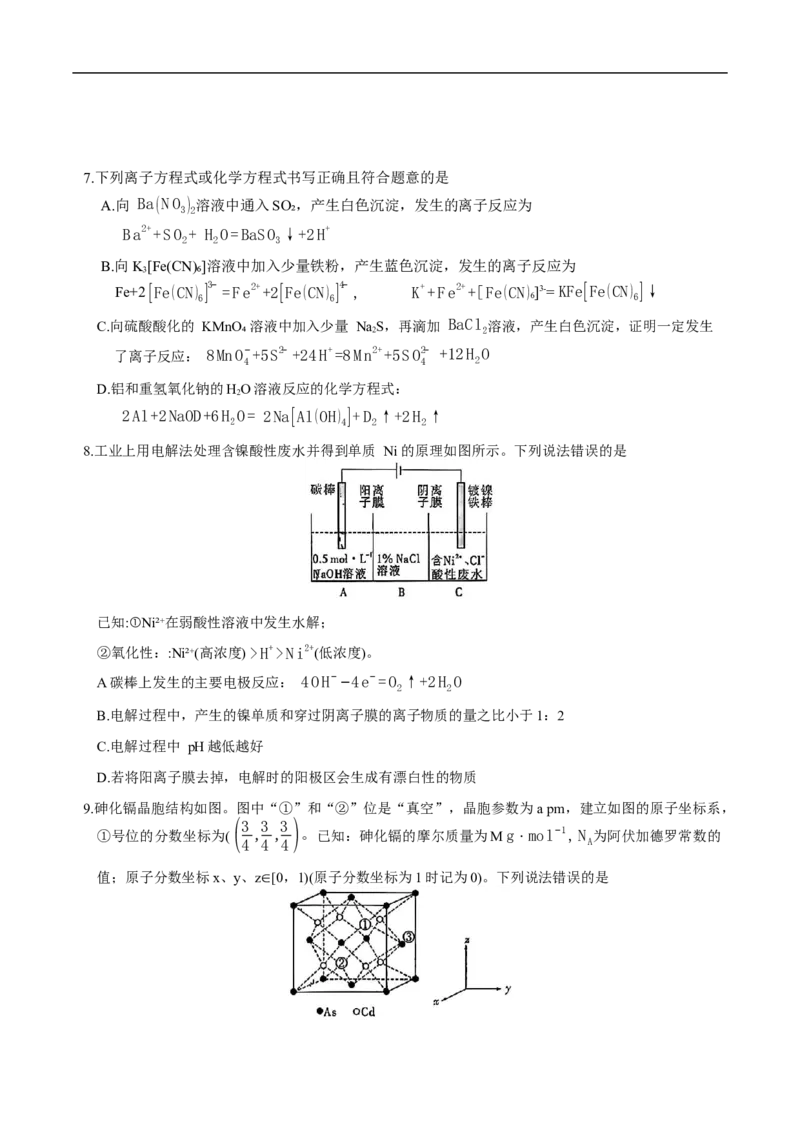
8.工业上用电解法处理含镍酸性废水并得到单质 Ni 的原理如图所示。下列说法错误的是
已知:①Ni²⁺在弱酸性溶液中发生水解;
②氧化性::Ni²⁺(高浓度) >H+>Ni2+(低浓度)。
A 碳棒上发生的主要电极反应: 4OH−−4e−=O ↑+2H O
2 2
B.电解过程中,产生的镍单质和穿过阴离子膜的离子物质的量之比小于1:2
C.电解过程中 pH越低越好
D.若将阳离子膜去掉,电解时的阳极区会生成有漂白性的物质
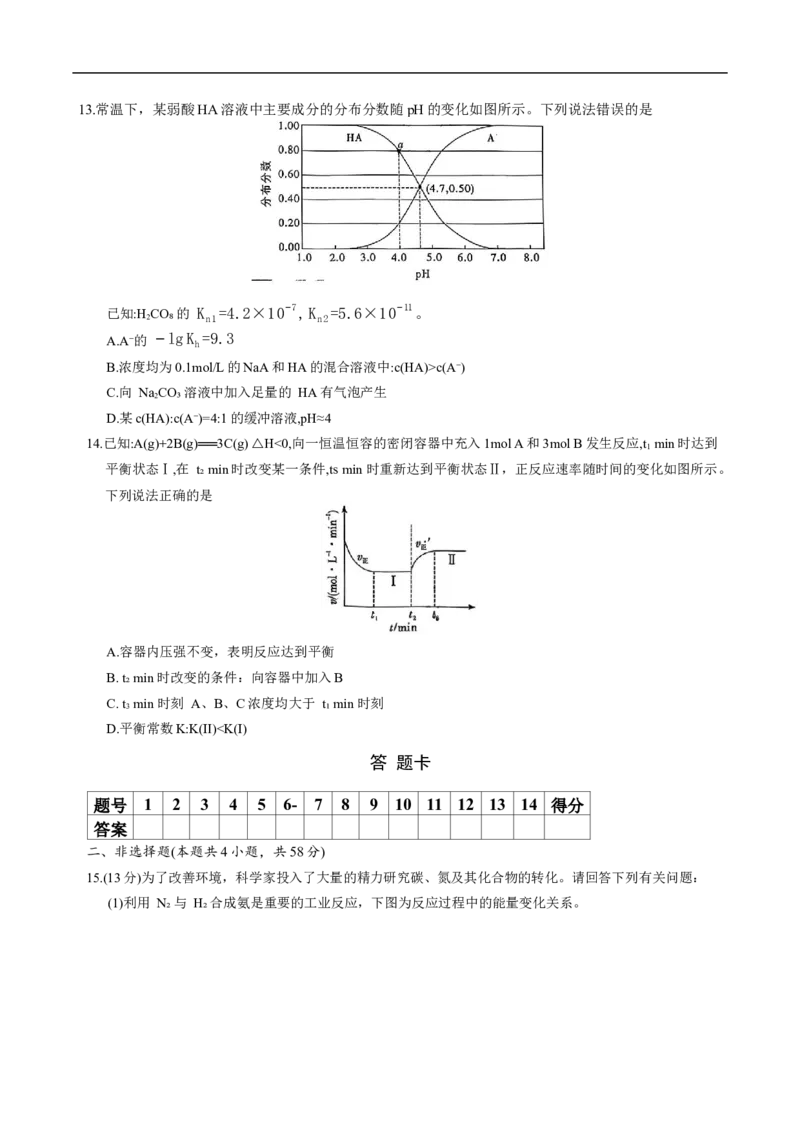
9.砷化镉晶胞结构如图。图中“①”和“②”位是“真空”,晶胞参数为a pm,建立如图的原子坐标系,
3 3 3
①号位的分数坐标为( ( , , )。已知:砷化镉的摩尔质量为M g⋅mol−1,N 为阿伏加德罗常数的
4 4 4 A
值;原子分数坐标x、y、z∈[0,1)(原子分数坐标为1时记为0)。下列说法错误的是A.砷化镉中 Cd与 As原子个数比为3:2
B.两个 Cd原子间最短距离为0.5a pm
1 1
C.③号位原子分数坐标为 ( ,0, )
2 2
M
D.该晶体的密度为
N (a×10−10) 3
g⋅cm−3
A
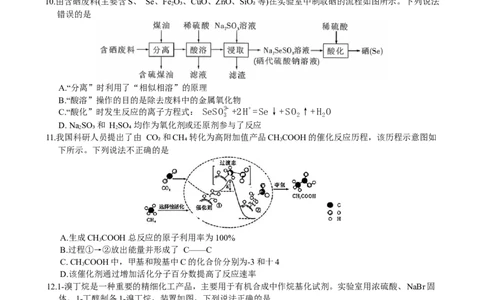
10.由含硒废料(主要含S、 Se、Fe O₃、CuO、ZnO、SiO₂等)在实验室中制取硒的流程如图所示。下列说法
2
错误的是
A.“分离”时利用了“相似相溶”的原理
B.“酸溶”操作的目的是除去废料中的金属氧化物
C.“酸化”时发生反应的离子方程式: SeSO2− +2H+=Se↓+SO ↑+H O
3 2 2
D. Na SO₃和 HSO₄ 均作为氧化剂或还原剂参与了反应
2 2
11.我国科研人员提出了由 CO₂和CH₄转化为高附加值产品CHCOOH的催化反应历程,该历程示意图如
3
下所示。下列说法不正确的是
A.生成CHCOOH 总反应的原子利用率为100%
3
B.过程①→②放出能量并形成了 C——C
C. CHCOOH中,甲基和羧基中C的化合价分别为-3和十4
3
D.该催化剂通过增加活化分子百分数提高了反应速率
12.1-溴丁烷是一种重要的精细化工产品,主要用于有机合成中作烷基化试剂。实验室用浓硫酸、NaBr固
体、1-丁醇制备1-溴丁烷,装置如图,下列说法正确的是
A.图中所示冷凝管的作用均为冷凝
B.浓硫酸的作用有制取 HBr、吸水提高1-丁醇转化率、作催化剂
C.气体吸收装置可用蒸馏水吸收 HBr、Br₂,防止污染空气
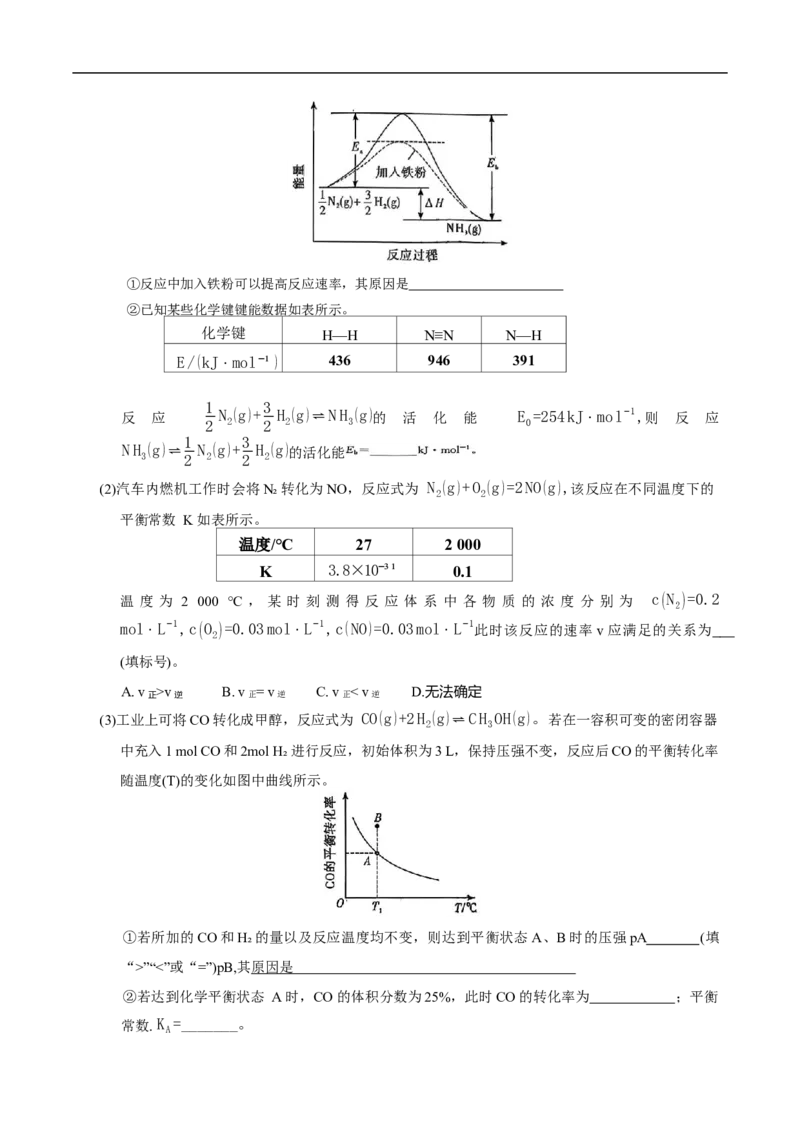
D.分液漏斗中要进行水洗分液、NaOH洗涤后分液、水洗分液以除去杂质13.常温下,某弱酸HA溶液中主要成分的分布分数随pH的变化如图所示。下列说法错误的是
已知:HCO₈的 K =4.2×10−7,K =5.6×10−11。
2 n1 n2
A.A⁻的 −lgK =9.3
h
B.浓度均为0.1mol/L的NaA和HA的混合溶液中:c(HA)>c(A⁻)
C.向 NaCO₃溶液中加入足量的 HA有气泡产生
2
D.某c(HA):c(A⁻)=4:1的缓冲溶液,pH≈4
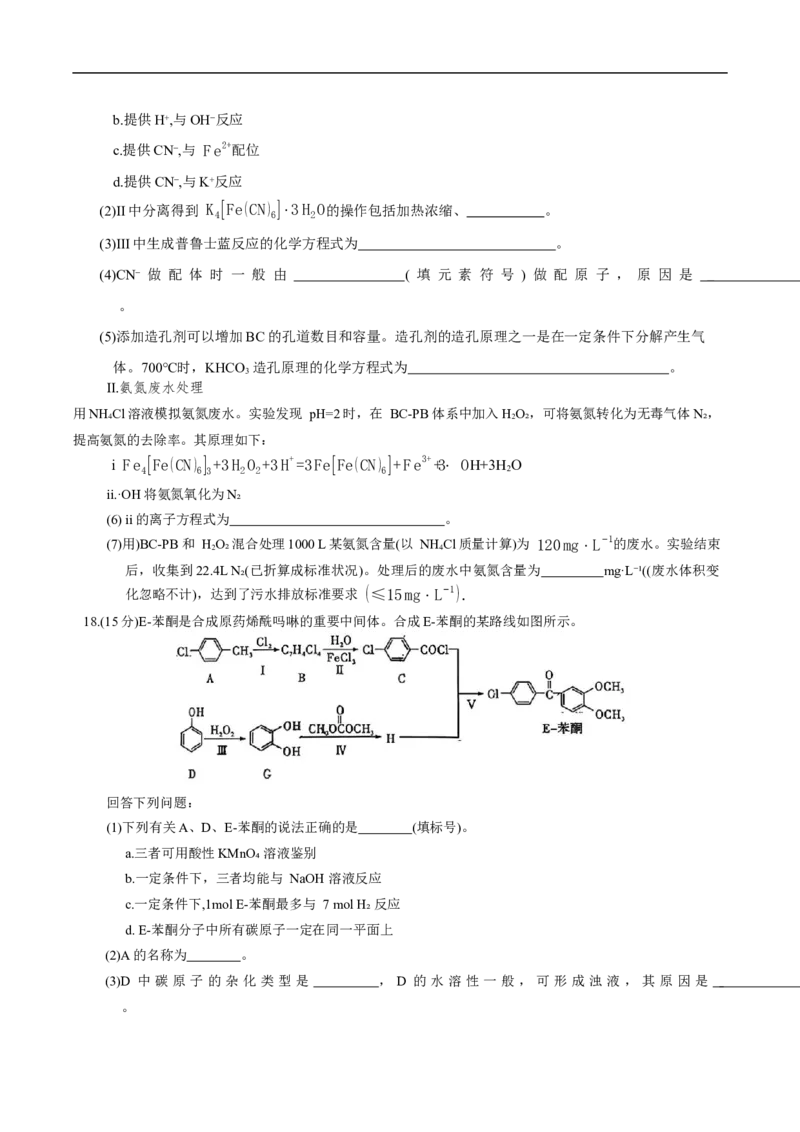
14.已知:A(g)+2B(g)══3C(g) △H<0,向一恒温恒容的密闭容器中充入1mol A 和3mol B发生反应,t min时达到
1
平衡状态Ⅰ,在 t₂ min时改变某一条件,ts min 时重新达到平衡状态Ⅱ,正反应速率随时间的变化如图所示。
下列说法正确的是
A.容器内压强不变,表明反应达到平衡
B. t₂ min时改变的条件:向容器中加入B
C. t min 时刻 A、B、C浓度均大于 t₁ min 时刻
3
D.平衡常数K:K(Ⅱ)v B. v = v C. v < v D.无法确定
正 逆 正 逆 正 逆
(3)工业上可将CO转化成甲醇,反应式为 CO(g)+2H (g)⇌ CH OH(g)。若在一容积可变的密闭容器
2 3
中充入1 mol CO和2mol H₂ 进行反应,初始体积为3 L,保持压强不变,反应后CO的平衡转化率
随温度(T)的变化如图中曲线所示。
①若所加的CO和H₂的量以及反应温度均不变,则达到平衡状态 A、B时的压强pA (填
“>”“<”或“=”)pB,其原因是
②若达到化学平衡状态 A 时,CO 的体积分数为25%,此时CO的转化率为 ;平衡
常数. K =_______。
A16.(15分)某炼锌废渣含有锌、铅、铁、钴、锰的+2价氧化物及锌和铜的单质,从该废渣中提取钴(Ⅱ`)的
一种工艺流程如下。
已知:Fe²⁺完全沉淀时pH≥9;Fe³⁺完全沉淀时pH≥3.2。回答下列问题:
(1)“酸浸”前,需将废渣磨碎,其目的是 。“浸渣”的主要成
分为 (填化学式)。
(2)“沉锰”步骤中加入 Na S O 的目的是 。
2 2 8
(3)“沉钴”步骤中,控制溶液pH=5.0~5.5,加入过量的 NaClO氧化( Co2+,其反应的离子方程式为
。
(4)“转化”步骤中有黄绿色气体产生,反应的离子方程式为
。 ;若用HO₂ 和稀硫酸代替浓盐酸,其优点是 。
2
(5)工业上利用电解含 Co(Ⅱ)的水溶液制备金属 Co和 H SO 的装置如图所示。
2 4
“电解”时石墨电极的电极反应为 ,膜Ⅱ为 (填“质子”“阴离
子”或“阳离子”)交换膜,目的是 。
17.(15分)研究人员合成了一种普鲁土蓝(PB)改性的生物炭(BC)复合材料(BC-PB),并将其应用于氨氮废
水(含 NH₃、NH⁺)的处理。
资料:①普鲁士蓝(PB)是亚铁氰化铁的俗称,化学式为Fe [Fe(CN)₆]₃,难溶于水;
4
BC-PB中,PB负载在 BC表面,没有产生新化学键,各自化学性质保持不变。
Ⅰ.复合材料BC-PB的合成
(1)下列关于 i 中 HCN参与反应的说法中,正确的是 (填标号)。
a.提供H⁺,与 Fe反应b.提供H⁺,与OH⁻反应
c.提供CN⁻,与 Fe2+配位
d.提供CN⁻,与K⁺反应
(2)Ⅱ中分离得到 K [Fe(CN) ]⋅3H O的操作包括加热浓缩、 。
4 6 2
(3)Ⅲ中生成普鲁士蓝反应的化学方程式为 。
(4)CN⁻ 做 配 体 时 一 般 由 ( 填 元 素 符 号 ) 做 配 原 子 , 原 因 是
。
(5)添加造孔剂可以增加BC的孔道数目和容量。造孔剂的造孔原理之一是在一定条件下分解产生气
体。700℃时,KHCO 造孔原理的化学方程式为 。
3
Ⅱ.氨氮废水处理
用NHCl溶液模拟氨氮废水。实验发现 pH=2时,在 BC-PB体系中加入HO₂,可将氨氮转化为无毒气体N₂,
4 2
提高氨氮的去除率。其原理如下:
i Fe
4
[Fe(CN)
6
]
3
+3H
2
O
2
+3H+=3Fe[Fe(CN)
6
]+Fe3++3⋅ OH+3H
2
O
ii.·OH将氨氮氧化为N₂
(6) ii的离子方程式为 。
(7)用)BC-PB 和 HO₂混合处理1000 L某氨氮含量(以 NHCl质量计算)为 120mg⋅L−1的废水。实验结束
2 4
后,收集到22.4L N₂(已折算成标准状况)。处理后的废水中氨氮含量为 mg·L⁻¹((废水体积变
化忽略不计),达到了污水排放标准要求 (≤15mg⋅L−1).
18.(15分)E-苯酮是合成原药烯酰吗啉的重要中间体。合成E-苯酮的某路线如图所示。
回答下列问题:
(1)下列有关A、D、E-苯酮的说法正确的是 (填标号)。
a.三者可用酸性KMnO₄ 溶液鉴别
b.一定条件下,三者均能与 NaOH 溶液反应
c.一定条件下,1mol E-苯酮最多与 7 mol H₂ 反应
d. E-苯酮分子中所有碳原子一定在同一平面上
(2)A的名称为 。
(3)D 中 碳 原 子 的 杂 化 类 型 是 , D 的 水 溶 性 一 般 , 可 形 成 浊 液 , 其 原 因 是
。(4)B的结构简式为 。
(5)步骤Ⅳ反应的化学方程式为 ,
与NaOH溶液反应的化学方程式为 。
(6)步骤Ⅴ的反应类型为 。
(7)J是C的同系物,其相对分子质量比C大14,同时符合下列条件的J的同分异构体有 种(不
考虑立体异构)。
①能发生银镜反应;②含有苯环;③苯环上至多有3个取代基。