文档内容
理科综合!化学参考答案
第!卷!选择题"#$分#"分$题%
%&’!(&)!*&+!!,&-!!!&)!!$&-!!.&+
%&$答案%’
$解析%)&海水淡化常用的方法有&蒸馏法’电渗析法’离子交换法等(活性炭的吸附性不能淡
化海水()错误)$选自,#人教版必修二第四章第二节/*,%
’&石膏的主要成分硫酸钙可以使豆浆中的蛋白质聚沉(是制作豆腐的凝固剂(’正确)$选自
!*人教版必修二第四章第二节/!!.%
+&米汤中含有淀粉(淀粉遇到碘单质变蓝(而加碘食盐中加入的是碘酸根或碘离子(+错误)
$选自,#人教版必修二第三章第四节/%*%
-&太阳能发电需要用硅的半导体性能(光导纤维仅是传输光讯号的媒体(-错误)$选自,#人
教版必修一第四章第一节/%0%
(&$答案%)
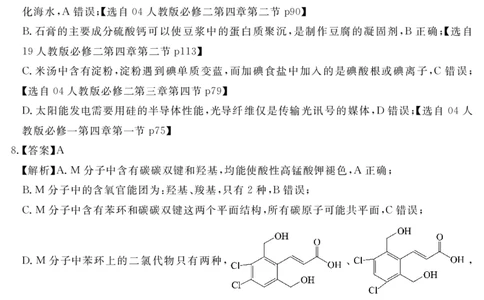
$解析%)&1分子中含有碳碳双键和羟基(均能使酸性高锰酸钾褪色()正确)
’&1分子中的含氧官能团为&羟基’羧基(只有$种(’错误)
+&1分子中含有苯环和碳碳双键这两个平面结构(所有碳原子可能共平面(+错误)
-&1分子中苯环上的二氯代物只有两种( ’ (
-错误*
$本题选自,#人教版必修二第三章第二节/""2%$知识点%
*&$答案%+
$解析%海水呈弱碱性(+3 发生歧化()正确*吸收塔中发生45 还原溴(’正确*乙醇与水
$ $
任意比互溶(不能作萃取剂(+错误*+3 在+氧化,+蒸馏,两过程消耗(-正确*
$
$本题选自!*人教版必修二第四章第一节/!,!思考与讨论%
!,&$答案%-
$解析%)&盐酸有挥发性(不能验证碳酸和硅酸的酸性强弱(需在锥形瓶和烧杯之间添加饱和
碳酸氢钠的洗气瓶()错误)
理科综合!化学试题答案 第!!!!!页"共"页#
{#{QQABZYAQggggABIAARhCQQXICgCQkBCCCIoGQAAMIAABABNABAA=}#}
书书书’&因为6175 浓度不同颜色不同(褪色时间自然不同(所以应改变草酸的浓度(用草酸滴高
#
锰酸钾溶液(’错误)$选自,#人教版选修四第二章第二节/$,实验$2$%
+&浓硫酸应先在烧杯中稀释(冷却至室温后(再转移定容(+错误)$选自,#人教版必修一第
一章第二节/!"实验!20’/!%思考与交流%
-&浓硫酸和铜在加热条件下反应生成二氧化硫(二氧化硫具有漂白性(通入到品红溶液中(
若品红褪色(则证明生成二氧化硫(二氧化硫气体是大气污染物(不能排放到空气中(试管口
用浸有氢氧化钠溶液棉花团吸收二氧化硫(图示正确(故-能达到实验目的*$选自,#人教
版必修二第三章第三节/%0实验.2#%
!!&$答案%)
$解析%根据题干信息(相对分子质量&8比9大!"(:比;大!"(9"8’;":可能为氧化的过程)
转化关系中(8和:与<反应均能得到强酸(则8可能为45 (:为=5 (<为 > 5(?为5 (则
. $ $ $
9为45 (;为=5(盐@溶液与盐酸反应得到A(与=A5>反应得到B(A与5 得到45 (则A
$ $ $
为>4(B与5 得到=5(则B为=> (因此@可以是=> >4或"=> #4(C’D’E’<分别
$ $ . # # $
为>’=’5’4*$人教版必修一第四章/**%
)&原子半径大小应为&4#=#5(即&<#D#E()错误)
’&=> 分子间形成氢键(熔沸点升高(’正确)
.
+&@可以是=> >4或"=> #4(+正确)
# # $
-&由题干知(非金属性4#=(则最高价含氧酸的酸性F#G(-正确*
!$&$答案%-
$解析%)&从图中信息可以判断(+H5$2穿过阴离子膜进入乙池(惰性电极9为阳极()正确)
#
’&惰性电极A为电解池的阴极(电极反应式为&> 5I$;2$$$$5>2I> %(与铅蓄电池的
$ $
负极相连(甲池中=A5>浓度逐渐增大(’正确)
+&正确*$选自,#人教版选修四第四章第二节/%"%
-&铅蓄电池负极&J92$;2I45$2$$$J945 (电路中转移,K$LM3电子(理论上负极增加的
# #
重量为,K!LM345$2的重量(为*K"F(-错误*$选自,#人教版选修四第四章第二节/%"%
#
!.&$答案%+
$解析%)&由图分析(A292;代表<74沉淀溶解曲线(A282B代表+N4沉淀溶解曲线(
)错误)
’&B点溶液有+N4’=A4(加入稀硫酸(无法回到A点(’错误)
$
! "<74# !K,Q!,2$0K#
+&!O P/ O O!K,Q!,!,(+正确)
! "+N4# !K,Q!,2.0K#
P/
,K,!RQ,K!LM3-R
-&B点存在&! "+N4#O""+N$I#""4$2#O!K,Q!,2.0K#(此时溶液中""4$2#O (
P/ ,K,.R
! "+N4#
""+N$I#O P/ O.K,Q!,2.#K#LM3-R(#O23F".K,Q!,2.#K##(#&.#K#(-错误*
""4$2#
理科综合!化学试题答案 第!!!!$页"共"页#
{#{QQABZYAQggggABIAARhCQQXICgCQkBCCCIoGQAAMIAABABNABAA=}#}第"卷!非选择题"0(分%
$"&"!#分#
"!#蒸馏烧瓶"!分#
"$#熔融的6=5 I=A=5 盐浴"!分#!!避免环戊酮蒸气燃烧并引发爆炸"$分#
. .
".#蒸馏烧瓶的支管口"!分#
"##除去馏出液中的己二酸"或将己二酸转化为离子化合物除去($分#!!干燥环戊酮"$分#
"0#%0K,S"$分#!!降低"!分#
""#$0,"$分#
&解析’!!"A为具支烧瓶或蒸馏烧瓶#
!$"反应需维持温度$(02$*,T$自来水水浴温度最高!,,T$酒精灯直接加热温度过高!约
.,,T"且受热不均匀$故选择熔融6=5 %=A=5 盐浴#
. .
!."蒸馏时温度计用来检出馏分温度#
!#"第一次用6+5 将乙二酸转化为盐除去$第二次无水6+5 起干燥作用#
$ . $ .
!0">5+
理科综合!化学试题答案 第!!!!.页"共"页#
$$
5
’’!+> "’’+5>
$ #
$$
5 +> ’’+>
$ $
’A!5>"或’A+5 )
’’’’ $ ’’’" . ) +$$5 I+5 %I>5%$由反
( ) $ $
+> ’’+>
$ $
应原理可知理论上!LM3己二酸#!LM3环戊酮$$*K$F己二酸为,K$LM3$则理论上应生成
!$K"F
环戊酮的质量为,K$LM3Q(#K,F&LM3O!"K(F$产率O Q!,,SO%0K,S’步骤!温度
!"K(F
高于.,,T$己二酸升华%分解导致产率降低#
!""由图知在$0,E时环戊酮产量最高#
$%&"!#分#
"!#I#"!分#
"$#4U5 "!分#!!!V$"!分#
$
反应温度为!0,T(>5 易分解"或产物中的W;.I可以催化>5 的分解#"$分#
$ $ $ $
".#+5"=> #I$>5*+=>II>+52I=> "写=>!>5且配平亦可($分#!!
$ $ $ # . . . $
!"$分#
煅烧
"##XU5"5>#I+A+3!$>5$$$+AXU5 I$>+3%I$>5%"$分#
$ $ $ . $
坩埚’坩埚钳"!分(漏坩埚扣!分(漏坩埚钳不扣分#
"0#+"$分#
&解析’!!"根据+A为I$价%5为2$价和+AXU5 中的化合价的代数和为,$计算得XU为
.
I##
!$"4U5 难溶于酸及氧化剂中#> 5 中 5由2!价还原成2$价生成 > 5$作氧化剂$
$ $ $ $
{#{QQABZYAQggggABIAARhCQQXICgCQkBCCCIoGQAAMIAABABNABAA=}#}W;XU5 作还原剂$配平得方程式$W;XU5 I> 5 I!,>I$$$$W;.II$XU5$II"> 5$氧化
. . $ $ $
剂V还原剂O!V$’反应温度在!0,T$>5 受热易分解!或产物中的W;.I可以催化>5 的
$ $ $ $
分解"#
!."由信息知+5!=>"
$
水解为可逆过程#XU5!5>" $!4"*+XU5$I!AY"I$5>2!AY"$XU5$I
水解的转化率达**S$则水解后溶液中"!XU5$I"O,K!Q!SO!Q!,2.LM3&R$"!5>2"O
!Q!,2$*
槡 O!Q!,2!.LM3&R$"!>I"O,K!LM3&R$/>O!#
!Q!,2.
!#"XU5!5>"与+A+3($>5煅烧生成+AXU5 是非氧化还原反应$通过配平得出其它产物$
$ $ $ .
煅烧
既得方程式为XU5!5>"I+A+3($> 5$$$+AXU5 I$>+3%I$> 5%’灼烧固体应选择
$ $ $ . $
坩埚$还需要坩埚%坩埚钳#
!0")不仅带入杂质离子 =AI影响产品纯度$还不能为产品提供 6I$液氨成本太高$另外
!LM365>中和!LM3>I$!LM36+5 反应$LM3>I$反应相同量的 >I$’成本比+高$
$ .
所以最好是6+5 #
$ .
$(&"!0分#
"!#$,%K$Z[!LM32!"$分#
"$#增大"!分#!!’-"$分#
".##LM3-"R!LU7#"$分#!!变大"!分#!!&"$分#!!.""$分#
电解"或通电#
"##$=5I#>5$$$$$$.> I$=52I$>I"$分#!!高温"!分#
$ $ .
&解析’!!"$
正
2$
逆
O$%$$
逆
O$,%K$Z[(LM32!#
!$"增大5 浓度$反应%"平衡正移$=5转化率增大’=5 和5 不是按照$V!消耗$)不能
. $ $
判断平衡#
!K,LM3&RQ#,S
!."由图可知$&%,K!LU7时$=5转化率为#,S$则’,O O#LM3&!R(LU7"’
$ ,K!LU7
(
催化剂降低反应活化能$加快化学反应速率$(
正
%(
逆
均变大’
(
正O!$$%&,$温度升高$!减
逆
’
小$由图可知)&&&$则! &! ’由反应=5!F"I5 !F"$$$=5 !F"I5 !F"知)=点 正
! $ 1 = . $ $ ’
逆
"!=5""!5 " ,K"Q,K" ,K(Q,K(
O!Q . O Q O."#
"!=5 ""!5 " ,K#Q,K# ,K$Q,K$
$ $
通电
!#"电池的总反应为$=5I#>5$$$.> I$=52I$>I$该反应的还原产物为 > $其还原
$ $ . $
性强于=5$该反应氧化产物=52!>I"$其氧化性强于 >5$由此可知$该总反应$%#,$
. $
故该反应在高温下自发#根据熵判据$$)#,$在高温下能自发进行#
.0&"!0分#
"!#R"!分#!! "!分#
理科综合!化学试题答案 第!!!!#页"共"页#
{#{QQABZYAQggggABIAARhCQQXICgCQkBCCCIoGQAAMIAABABNABAA=}#}"$#!V!"!分#!!)-"$分#
".#&%"$分#
’有机物’易形成分子内氢键(对羟基苯甲醛易形成分子间氢键(故’的沸点低"$分#
"##不能"!分#!!0"#."$分#
"0#"
!
(!(!#"或"
!
(,(,#!分#!!
#(!*
)
"+.
!
I+.
$
#Q!,2.,
Q!,,S"$分#
$ $ $$0
&解析’!!"基态碳原子核外电子排布在6%R层$所以最高能层为R#
!$"基态+H.I的外围电子排布式为.B.$所以外围电子排布图为 $
+5中含有!个)键和$个(键$+5和+H形成"个配位键$故+H!+5"中)键和(键的个数
"
比为!"I""V!$O!V!$与+5互为等电子体的是+$2%+=2#
$
!."&苯环和羰基碳原子均为P/$杂化$故为%’’有机物’中羟基与醛基位于苯环的邻位碳
原子上$故易形成分子内氢键$而对羟基苯甲醛处于对位$易形成分子间氢键#
!#"第一电离能是指基态的气态原子失去最外层的一个电子变为气态离子所需能量$图中表
示的是固态+N原子$故不能确定+N原子的第一电离能#晶格能是指气态基态离子形成
!LM3离子化合物所释放的能量$故 +N= 的晶格能为.$(0Z[(LM32!2($$Z[(LM32!I
.
.!(,Z[(LM32!O0"#.Z[(LM32!#
!0"晶体学中的分数!原子"坐标的取值通常要小于!$但因中学生未掌握*等同点+的概念$所
!
以! $!$!"亦给分,参见$,$!年海南高考化学第!*题!""-#利用均摊法$!个晶胞中含有#
$
#Q#(!+.I+." #Q%0
个=U$I和#个 5$2$故离子的体积为 ! $ /L.$!个晶胞的体积是 8L.O
. !*
)
#Q%0
Q!,.,/L.$则该晶胞中离子的体积占晶胞体积的百分率为
#(!*
)
!+.
!
I+.
$
"Q!,2.,
!*
)
$$0
Q!,,S#
."&"!0分#
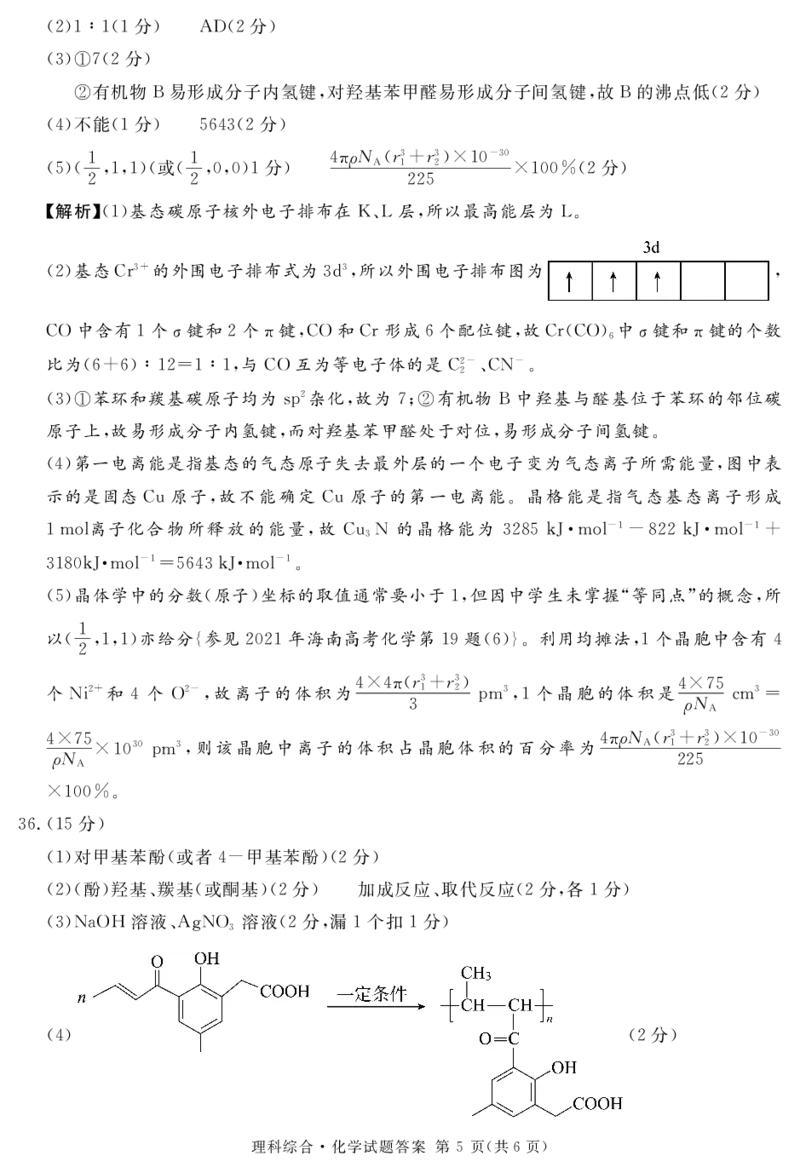
"!#对甲基苯酚"或者#2甲基苯酚#"$分#
"$#"酚#羟基’羰基"或酮基#"$分#!!加成反应’取代反应"$分(各!分#
".#=A5>溶液’)F=5 溶液"$分(漏!个扣!分#
.
"## "$分#
理科综合!化学试题答案 第!!!!0页"共"页#
{#{QQABZYAQggggABIAARhCQQXICgCQkBCCCIoGQAAMIAABABNABAA=}#}=>
$
))
+$$5
))
5
))
"0#))-)) "$分#
))
+
..
+
))
>
//
’’////’’5> >I5
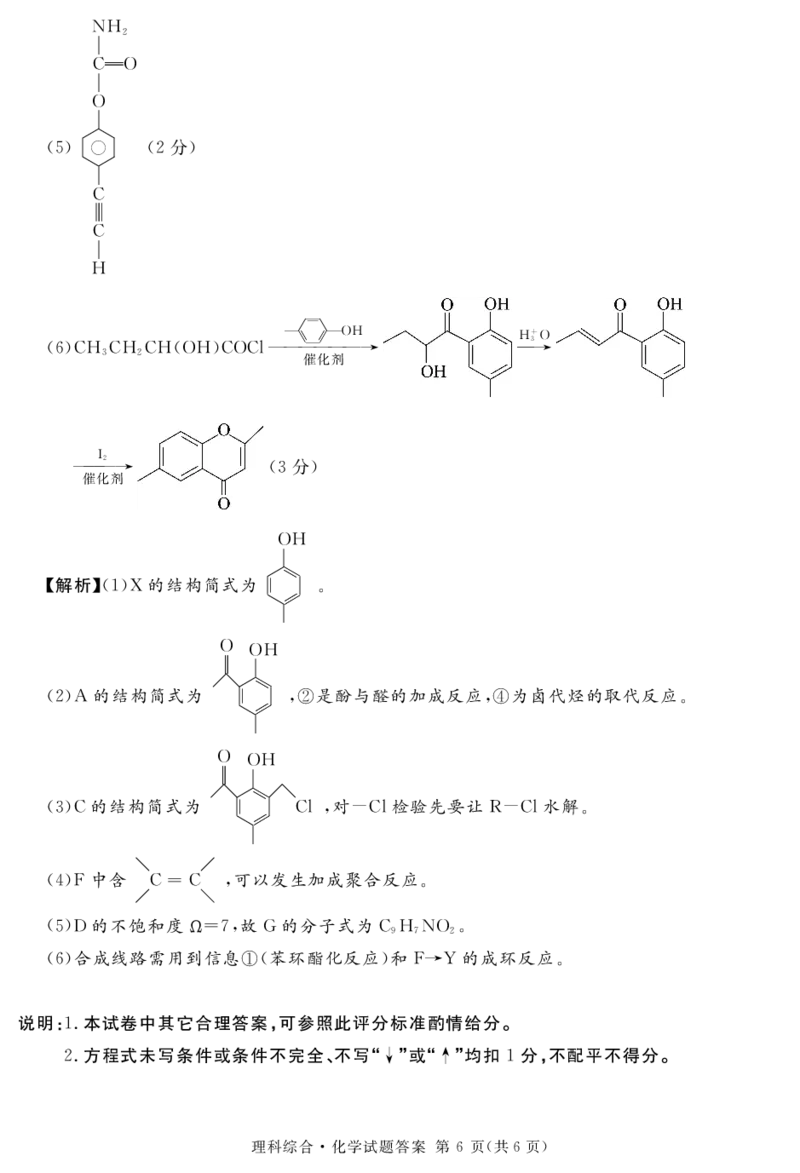
""#+>+>+>"5>#+5+3’’’’’’’’" ’’ . "
. $ 催化剂
\
! ’’’ $ " ".分#
催化剂
5>
))
//
&解析’!!"@的结构简式为00//)) #
))
5>
))
//
!$")的结构简式为 00//))
))
理科综合!化学试题答案 第!!!!"页"共"页#
$$
5
$’是酚与醛的加成反应$*为卤代烃的取代反应#
5>
))
//
!."+的结构简式为 00//))
))
$$
5
+3$对2+3检验先要让]2+3水解#
!#"W中含 +O+ $可以发生加成聚合反应#
!0"-的不饱和度+O%$故^的分子式为+> =5 #
* % $
!""合成线路需用到信息&!苯环酯化反应"和W"_的成环反应#
说明(!&本试卷中其它合理答案#可参照此评分标准酌情给分)
$&方程式未写条件或条件不完全*不写+1,或+%,均扣!分#不配平不得分)
{#{QQABZYAQggggABIAARhCQQXICgCQkBCCCIoGQAAMIAABABNABAA=}#}