文档内容
重难点 01 离子反应及其应用
1.(2024·高一上·山西省部分学校·期末)NaCl溶于水的过程如图所示。下列叙述正确的是
A.NaCl固体不导电的原因是不含导电的离子
B.NaCl溶于水发生了化学变化
C.水分子能减弱 和 之间的作用力
D. 、 分别与水分子形成大小相同的环
2.(2024·高一上·福建省龙岩市一级校联盟·期末)下列化学方程式或离子方程式中,正确的是
A.盐酸与铁屑的反应:
B. 与NaOH溶液的反应:
C. 溶液与铁粉的反应:
D.稀硝酸与铜片的反应:
3.(2024·高一上·河南省开封市联考·期末)下列各组离子能在溶液中大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
4.(2024·高一上·河南省开封市联考·期末)下列反应的离子方程式书写正确的是
A.氧化亚铁与稀盐酸反应:
B.氢氧化钡溶液与硫酸铜溶液反应:
C.过氧化钠与水反应:
D.碳酸氢钠溶液与 溶液反应:
5.(2024·高一上·广东省茂名市·期末)下列反应方程式或离子方程式正确的是
A.铁和氯气反应的化学方程式:
B.钠和水反应的化学方程式:
学科网(北京)股份有限公司C.用 溶液腐蚀覆铜板:
D.碳酸氢钠溶液和稀硫酸反应的离子方程式:
6.(2024·高一上·山西省部分学校·期末)下列指定反应的离子方程式书写正确的是
A. 溶液与过量NaOH溶液反应:
B. 溶液与 溶液反应:
C.酸性条件下 溶液与KI溶液发生反应生成 :
D.MgO与稀盐酸反应:
7.(2024·高一上·江西省新余市·期末)下列实验对应的离子方程式书写正确的是
A.家庭中用食醋溶解水垢中的 :
B.向 溶液中加入过量的氨水:
C.碘化钾溶液酸化后加入少量双氧水:
D.将 通入水中与水反应:
8.(2024·高一上·山东省青岛市·期末)能正确表示下列反应的离子方程式为
A.用稀硝酸清洗试管内壁的银:
B.铜箔制作印刷电路板:
C.向 溶液中加足量 溶液:
D. 溶液中通入足量氯气:
9.(2024·高一上·湖南省名校联考联合体·期末)下列反应的离子方程式书写正确的是
A.金属铝溶于盐酸中:
B.向硫酸知中加入过量的氨水:
C. 溶液与 溶液混合:
D.实验室用二氧化锰和浓盐酸制氯气:
10.(2024·高一上·江西省部分学校·期末)下列离子方程式中,正确的是
A. 和稀盐酸反应:
B. 溶液与过量氨水反应:
C. 与稀硫酸反应:
D. 溶液与 溶液反应:
11.(2024·高一上·山东省日照市·期末)下列反应的离子方程式书写正确的是
学科网(北京)股份有限公司A.向 溶液中投入少量 :
B.向酸性 溶液中滴加少量双氧水:
C.向漂白粉溶液中通入足量 :
D.向 溶液中滴加足量澄清石灰水:
12.(2024·高一上·湖北省荆门市·期末)下列指定反应的离子方程式书写正确的是
A. 溶液中加入足量 溶液:
B.氢氧化钠溶液中加入过量碳酸氢钙溶液:
C.氢氧化镁溶于稀醋酸中:
D.向酸性 溶液中滴入少量 稀溶液:
13.(2024·高一上·重庆·期末)下列各组离子在水溶液中能大量共存的是
A. 、 、 、 B. 、 、 、
C. 、 、 、 D. 、 、 、
14.(2024·高一上·天津市重点校·期末)下列指定反应的离子方程式正确的是
A.向 溶液中加入过量的 溶液:
B.将一粒钠投入硫酸铜溶液中:
C.向 的溶液中通入 :
D.向澄清石灰水中加入过量的 溶液:
15.(2024·高一上·江西省新余市·期末)下列各组离子在指定溶液中一定能大量共存的是
A.强酸性溶液中: 、 、 、
B.澄清透明溶液中: 、 、 、
C.含有 的溶液: 、 、 、
D.与Al反应能生成 的溶液: 、 、 、
16.(2024·高一上·吉林省长春市东北师范大学附属中学·期末)下列各组溶液中的离子能大量共存,且加
入(或通入)X试剂后发生反应的离子方程式书写正确的是
选项 离子组 X试剂 离子方程式
溶
A 、 、 、
液
B 、 、 、 过量氨水
学科网(北京)股份有限公司C 、 、 、 少量盐酸
D 、 、 、 足量
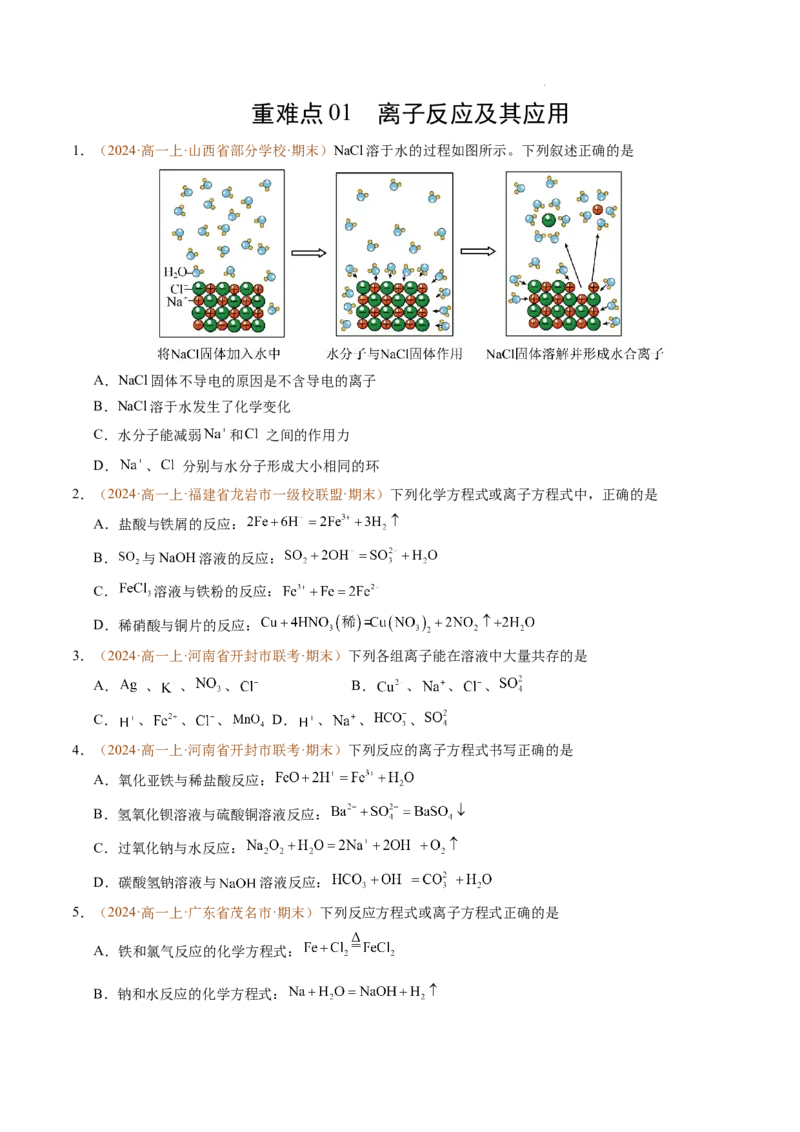
17.(2024·高一上·湖南省怀化市·期末)向Ba(OH) 溶液中滴入NaHSO 溶液,其导电能力随滴入溶液体
2 4
积的变化关系如图所示,下列分析不正确的是
A.NaHSO 是离子化合物
4
B.a至b对应反应的离子方程式为Ba2+ +H+ +OH-+SO = BaSO↓+H O
4 2
C.b点溶液呈中性
D.c点溶液中存在大量的Na+、H+、SO
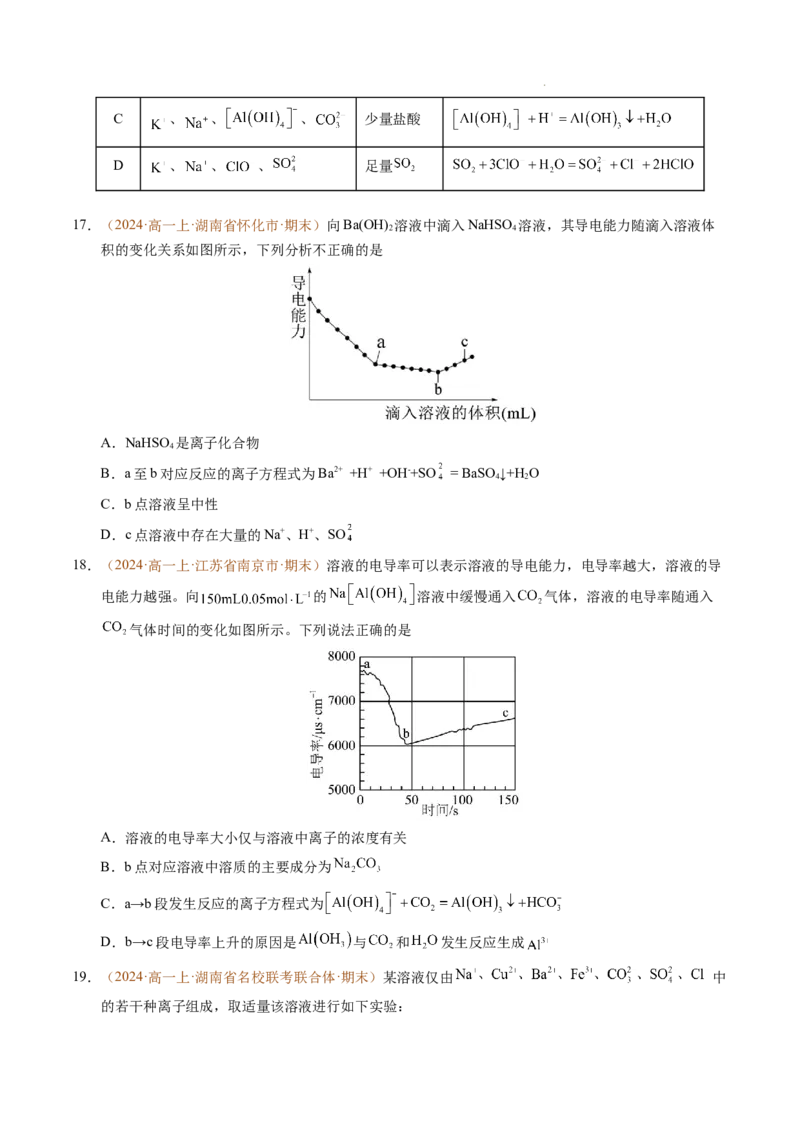
18.(2024·高一上·江苏省南京市·期末)溶液的电导率可以表示溶液的导电能力,电导率越大,溶液的导
电能力越强。向 的 溶液中缓慢通入 气体,溶液的电导率随通入
气体时间的变化如图所示。下列说法正确的是
A.溶液的电导率大小仅与溶液中离子的浓度有关
B.b点对应溶液中溶质的主要成分为
C.a→b段发生反应的离子方程式为
D.b→c段电导率上升的原因是 与 和 发生反应生成
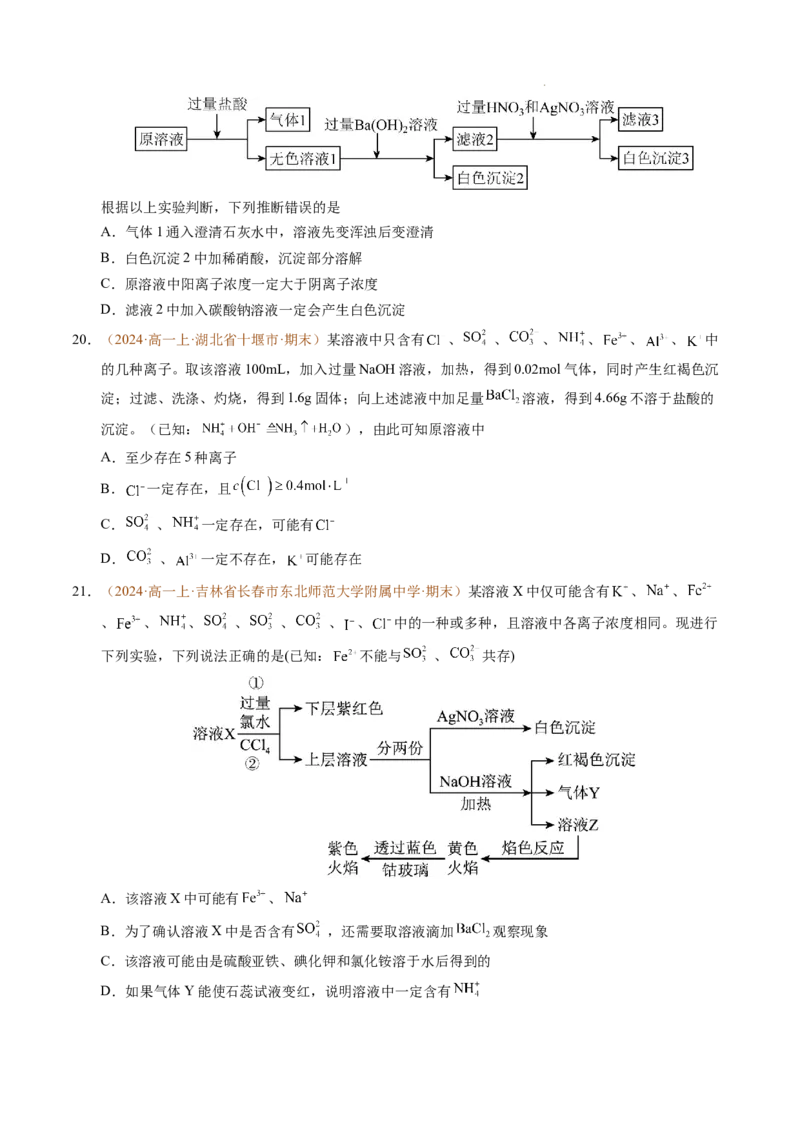
19.(2024·高一上·湖南省名校联考联合体·期末)某溶液仅由 中
的若干种离子组成,取适量该溶液进行如下实验:
学科网(北京)股份有限公司根据以上实验判断,下列推断错误的是
A.气体1通入澄清石灰水中,溶液先变浑浊后变澄清
B.白色沉淀2中加稀硝酸,沉淀部分溶解
C.原溶液中阳离子浓度一定大于阴离子浓度
D.滤液2中加入碳酸钠溶液一定会产生白色沉淀
20.(2024·高一上·湖北省十堰市·期末)某溶液中只含有 、 、 、 、 、 、 中
的几种离子。取该溶液100mL,加入过量NaOH溶液,加热,得到0.02mol气体,同时产生红褐色沉
淀;过滤、洗涤、灼烧,得到1.6g固体;向上述滤液中加足量 溶液,得到4.66g不溶于盐酸的
沉淀。(已知: ),由此可知原溶液中
A.至少存在5种离子
B. 一定存在,且
C. 、 一定存在,可能有
D. 、 一定不存在, 可能存在
21.(2024·高一上·吉林省长春市东北师范大学附属中学·期末)某溶液X中仅可能含有 、 、
、 、 、 、 、 、 、 中的一种或多种,且溶液中各离子浓度相同。现进行
下列实验,下列说法正确的是(已知: 不能与 、 共存)
A.该溶液X中可能有 、
B.为了确认溶液X中是否含有 ,还需要取溶液滴加 观察现象
C.该溶液可能由是硫酸亚铁、碘化钾和氯化铵溶于水后得到的
D.如果气体Y能使石蕊试液变红,说明溶液中一定含有
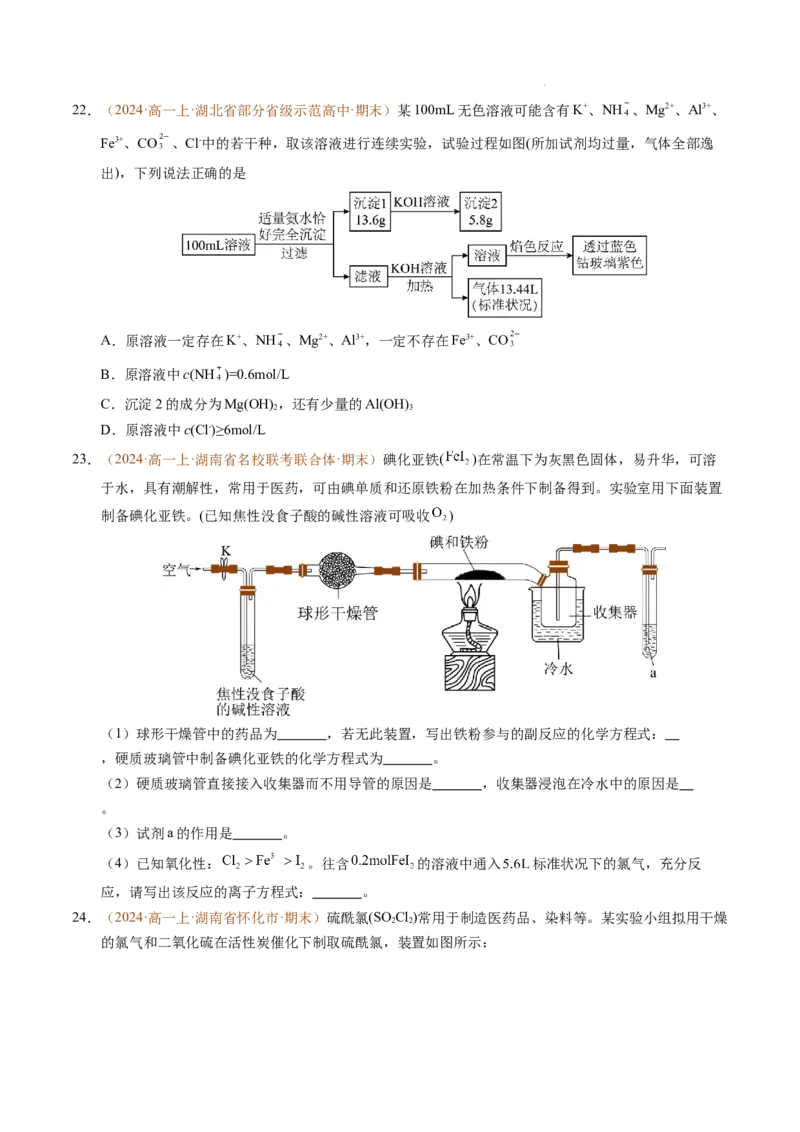
学科网(北京)股份有限公司22.(2024·高一上·湖北省部分省级示范高中·期末)某100mL无色溶液可能含有K+、NH 、Mg2+、Al3+、
Fe3+、CO 、Cl-中的若干种,取该溶液进行连续实验,试验过程如图(所加试剂均过量,气体全部逸
出),下列说法正确的是
A.原溶液一定存在K+、NH 、Mg2+、Al3+,一定不存在Fe3+、CO
B.原溶液中c(NH )=0.6mol/L
C.沉淀2的成分为Mg(OH) ,还有少量的Al(OH)
2 3
D.原溶液中c(Cl-)≥6mol/L
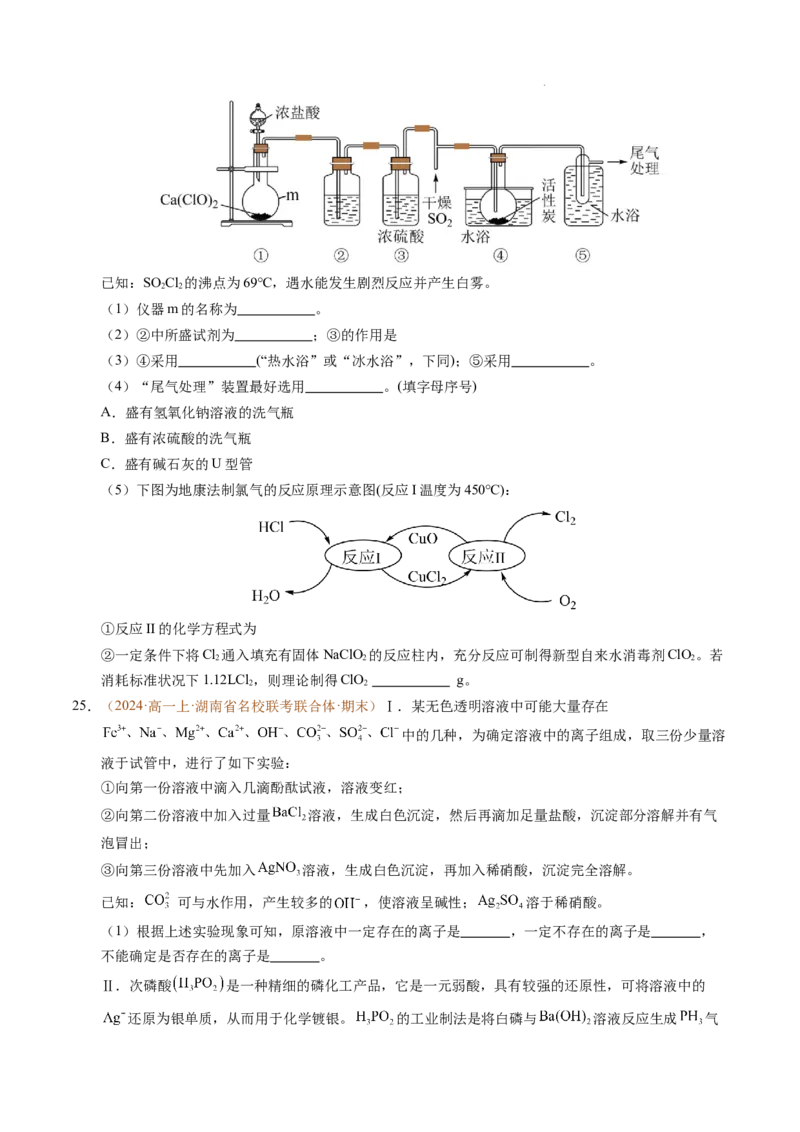
23.(2024·高一上·湖南省名校联考联合体·期末)碘化亚铁( )在常温下为灰黑色固体,易升华,可溶
于水,具有潮解性,常用于医药,可由碘单质和还原铁粉在加热条件下制备得到。实验室用下面装置
制备碘化亚铁。(已知焦性没食子酸的碱性溶液可吸收 )
(1)球形干燥管中的药品为 ,若无此装置,写出铁粉参与的副反应的化学方程式:
,硬质玻璃管中制备碘化亚铁的化学方程式为 。
(2)硬质玻璃管直接接入收集器而不用导管的原因是 ,收集器浸泡在冷水中的原因是
。
(3)试剂a的作用是 。
(4)已知氧化性: 。往含 的溶液中通入 标准状况下的氯气,充分反
应,请写出该反应的离子方程式: 。
24.(2024·高一上·湖南省怀化市·期末)硫酰氯(SO Cl)常用于制造医药品、染料等。某实验小组拟用干燥
2 2
的氯气和二氧化硫在活性炭催化下制取硫酰氯,装置如图所示:
学科网(北京)股份有限公司已知:SO Cl 的沸点为69℃,遇水能发生剧烈反应并产生白雾。
2 2
(1)仪器m的名称为 。
(2)②中所盛试剂为 ;③的作用是
(3)④采用 (“热水浴”或“冰水浴”,下同);⑤采用 。
(4)“尾气处理”装置最好选用 。(填字母序号)
A.盛有氢氧化钠溶液的洗气瓶
B.盛有浓硫酸的洗气瓶
C.盛有碱石灰的U型管
(5)下图为地康法制氯气的反应原理示意图(反应I温度为450℃):
①反应II的化学方程式为
②一定条件下将Cl 通入填充有固体NaClO 的反应柱内,充分反应可制得新型自来水消毒剂ClO 。若
2 2 2
消耗标准状况下1.12LCl ,则理论制得ClO g。
2 2
25.(2024·高一上·湖南省名校联考联合体·期末)Ⅰ.某无色透明溶液中可能大量存在
中的几种,为确定溶液中的离子组成,取三份少量溶
液于试管中,进行了如下实验:
①向第一份溶液中滴入几滴酚酞试液,溶液变红;
②向第二份溶液中加入过量 溶液,生成白色沉淀,然后再滴加足量盐酸,沉淀部分溶解并有气
泡冒出;
③向第三份溶液中先加入 溶液,生成白色沉淀,再加入稀硝酸,沉淀完全溶解。
已知: 可与水作用,产生较多的 ,使溶液呈碱性; 溶于稀硝酸。
(1)根据上述实验现象可知,原溶液中一定存在的离子是 ,一定不存在的离子是 ,
不能确定是否存在的离子是 。
Ⅱ.次磷酸 是一种精细的磷化工产品,它是一元弱酸,具有较强的还原性,可将溶液中的
还原为银单质,从而用于化学镀银。 的工业制法是将白磷与 溶液反应生成 气
学科网(北京)股份有限公司体和 ,后者再与 反应生成 。
(2)写出白磷 与 溶液反应的化学方程式: ,反应中每消耗 ,转移的电子
数为 。
(3)写出 与足量 溶液反应的离子方程式: 。
(4)工业上利用 进行化学镀银的反应中,当氧化剂与还原剂物质的量之比为4∶1时,则氧化产
物中 元素的化合价为 。
学科网(北京)股份有限公司