文档内容
2025 年重庆市普通高中学业水平选择性考试
高三第三次联合诊断检测 化学
化学测试卷共4页,满分100分。考试时间75分钟。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Co 59 Br 80 Sn 119 Cs 133
一、选择题:本题共14个小题,每小题3分,共42分。每小题只有一个选项符合题目要求。
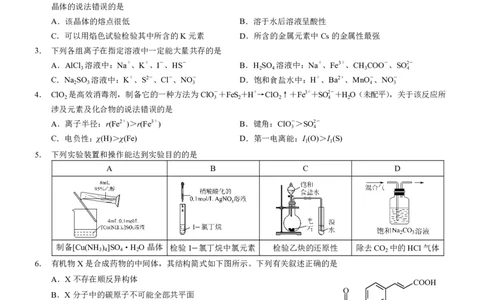
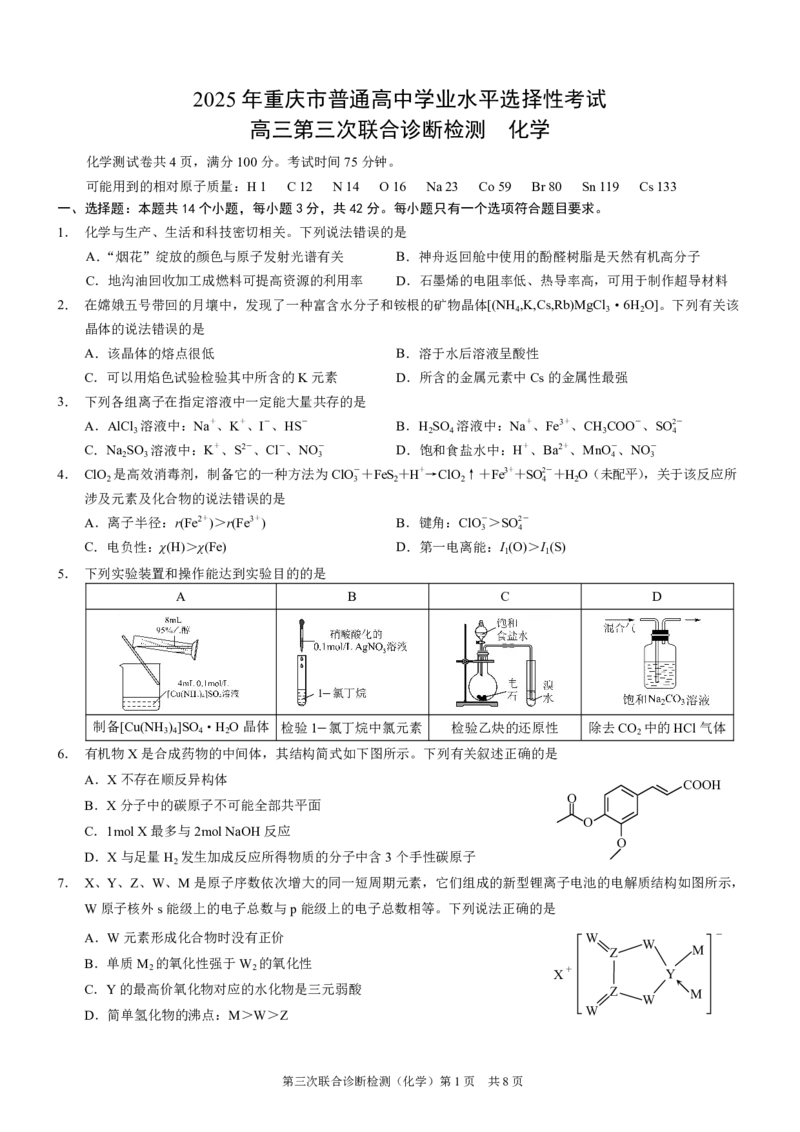
1. 化学与生产、生活和科技密切相关。下列说法错误的是
A.“烟花”绽放的颜色与原子发射光谱有关 B.神舟返回舱中使用的酚醛树脂是天然有机高分子
C.地沟油回收加工成燃料可提高资源的利用率 D.石墨烯的电阻率低、热导率高,可用于制作超导材料
2. 在嫦娥五号带回的月壤中,发现了一种富含水分子和铵根的矿物晶体[(NH ,K,Cs,Rb)MgCl ·6H O]。下列有关该
4 3 2
晶体的说法错误的是
A.该晶体的熔点很低 B.溶于水后溶液呈酸性
C.可以用焰色试验检验其中所含的K元素 D.所含的金属元素中Cs的金属性最强
3. 下列各组离子在指定溶液中一定能大量共存的是
A.AlCl 溶液中:Na+、K+、I-、HS- B.H SO 溶液中:Na+、Fe3+、CH COO-、SO2-
3 2 4 3 4
C.Na SO 溶液中:K+、S2-、Cl-、NO- D.饱和食盐水中:H+、Ba2+、MnO-、NO-
2 3 3 4 3
4. ClO 是高效消毒剂,制备它的一种方法为ClO-+FeS+H+→ClO ↑+Fe3++SO2-+HO(未配平),关于该反应所
2 3 2 2 4 2
涉及元素及化合物的说法错误的是
A.离子半径:r(Fe2+)>r(Fe3+) B.键角:ClO->SO2-
3 4
C.电负性:χ(H)>χ(Fe) D.第一电离能:I (O)>I (S)
1 1
5. 下列实验装置和操作能达到实验目的的是
A B C D
1 氯丁烷
制备[Cu(NH
3
)
4
]SO
4
·H
2
O晶体 检验1 氯丁烷中氯元素 检验乙炔的还原性 除去CO
2
中的HCl气体
6. 有机物X是合成药物的中间体,其结构简式如下图所示。下列有关叙述正确的是
A.X不存在顺反异构体
COOH
O
B.X分子中的碳原子不可能全部共平面
O
C.1mol X最多与2mol NaOH反应
O
D.X与足量H 发生加成反应所得物质的分子中含3个手性碳原子
2
7. X、Y、Z、W、M是原子序数依次增大的同一短周期元素,它们组成的新型锂离子电池的电解质结构如图所示,
W原子核外s能级上的电子总数与p能级上的电子总数相等。下列说法正确的是
A.W元素形成化合物时没有正价 W -
W
Z M
B.单质M 的氧化性强于W 的氧化性
2 2 X + Y
C.Y的最高价氧化物对应的水化物是三元弱酸 Z M
W
D.简单氢化物的沸点:M>W>Z W
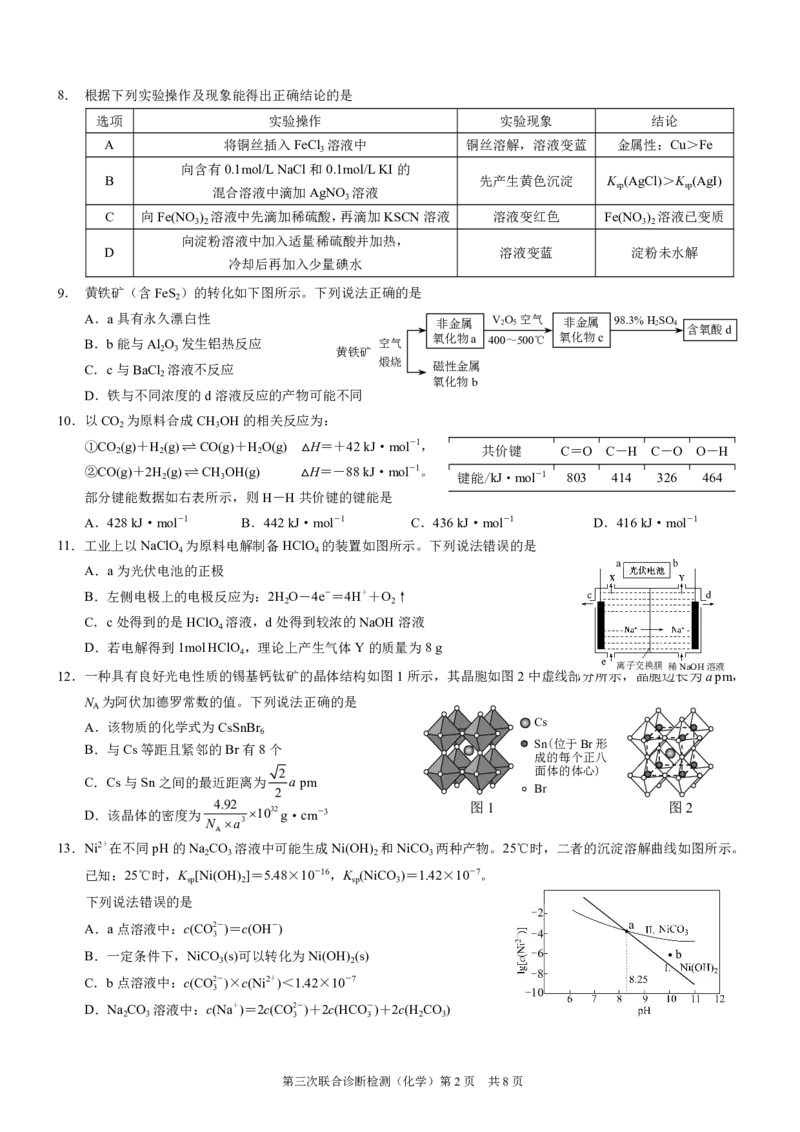
第三次联合诊断检测(化学)第1页 共8页8. 根据下列实验操作及现象能得出正确结论的是
选项 实验操作 实验现象 结论
A 将铜丝插入FeCl 溶液中 铜丝溶解,溶液变蓝 金属性:Cu>Fe
3
向含有0.1mol/L NaCl和0.1mol/L KI的
B 先产生黄色沉淀 K (AgCl)>K (AgI)
sp sp
混合溶液中滴加AgNO 溶液
3
C 向Fe(NO ) 溶液中先滴加稀硫酸,再滴加KSCN溶液 溶液变红色 Fe(NO ) 溶液已变质
3 2 3 2
向淀粉溶液中加入适量稀硫酸并加热,
D 溶液变蓝 淀粉未水解
冷却后再加入少量碘水
9. 黄铁矿(含FeS )的转化如下图所示。下列说法正确的是
2
A.a具有永久漂白性 非金属 V 2 O 5 空气 非金属 98.3% H 2 SO 4 含氧酸d
B.b能与Al O 发生铝热反应 空气 氧化物a 400~500℃ 氧化物c
2 3 黄铁矿
C.c与BaCl 溶液不反应
煅烧
磁性金属
2
氧化物b
D.铁与不同浓度的d溶液反应的产物可能不同
10.以CO 为原料合成CH OH的相关反应为:
2 3
①CO 2 (g)+H 2 (g)CO(g)+H 2 O(g) H=+42 kJ·mol-1, 共价键 C=O C-H C-O O-H
②CO(g)+2H 2 (g)CH 3 OH(g) △H=-88 kJ·mol-1。 键能/kJ·mol-1 803 414 326 464
部分键能数据如右表所示,则H-H共
△
价键的键能是
A.428 kJ·mol-1 B.442 kJ·mol-1 C.436 kJ·mol-1 D.416 kJ·mol-1
11.工业上以NaClO 为原料电解制备HClO 的装置如图所示。下列说法错误的是
4 4
a b
A.a为光伏电池的正极
B.左侧电极上的电极反应为:2H O-4e-=4H++O ↑ c d
2 2
C.c处得到的是HClO 溶液,d处得到较浓的NaOH溶液
4
D.若电解得到1mol HClO ,理论上产生气体Y的质量为8 g
4
e 离子交换膜 稀NaOH溶液
12.一种具有良好光电性质的锡基钙钛矿的晶体结构如图1所示,其晶胞如图2中虚线部分所示,晶胞边长为a pm,
N 为阿伏加德罗常数的值。下列说法正确的是
A
A.该物质的化学式为CsSnBr Cs
6
B.与Cs等距且紧邻的Br有8个
Sn(位于Br形
成的每个正八
2 面体的体心)
C.Cs与Sn之间的最近距离为 apm
2 Br
D.该晶体的密度为
4.92
1032 g·cm-3
图1 图2
N a3
A
13.Ni2+在不同pH的Na CO 溶液中可能生成Ni(OH) 和NiCO 两种产物。25℃时,二者的沉淀溶解曲线如图所示。
2 3 2 3
已知:25℃时,K [Ni(OH) ]=5.48×10-16,K (NiCO )=1.42×10-7。
sp 2 sp 3
下列说法错误的是
-2
A.a点溶液中:c(CO2
3
-)=c(OH-)
-4
a
B.一定条件下,NiCO (s)可以转化为Ni(OH) (s) -6 b
3 2
-8
C.b点溶液中:c(CO2-)×c(Ni2+)<1.42×10-7
3 -10
D.Na CO 溶液中:c(Na+)=2c(CO2-)+2c(HCO-)+2c(H CO )
2 3 3 3 2 3
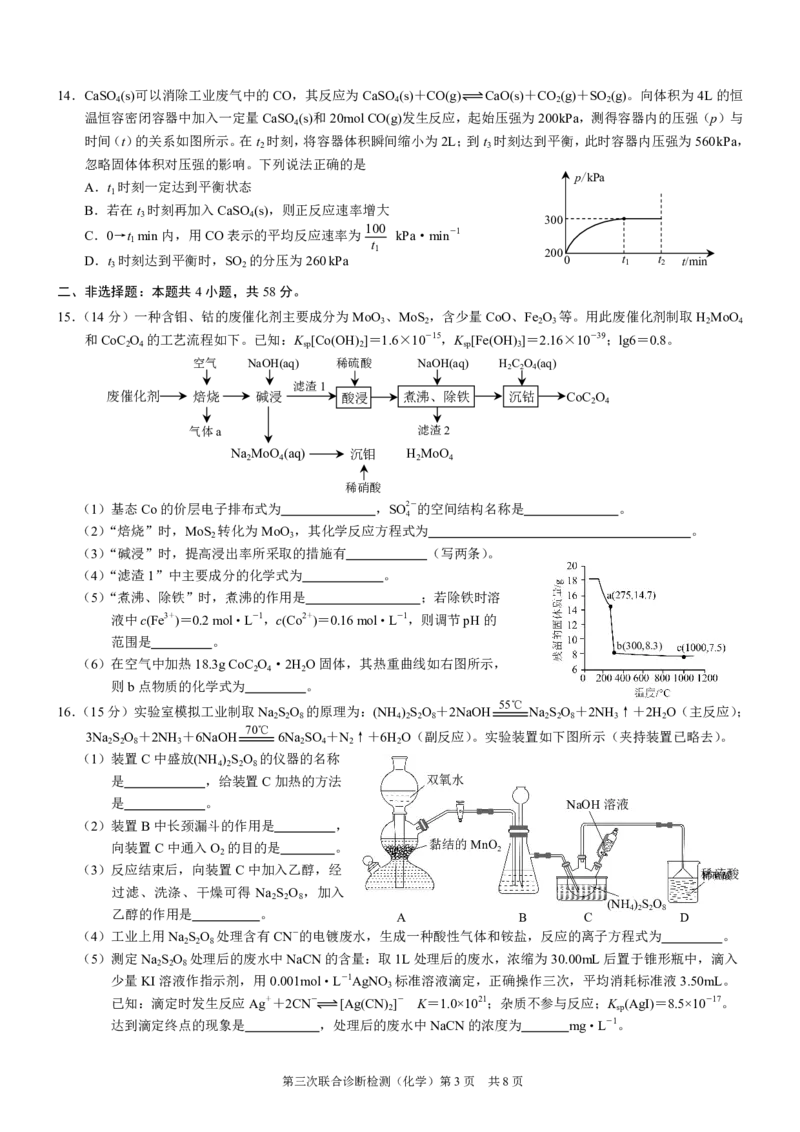
第三次联合诊断检测(化学)第2页 共8页14.CaSO (s)可以消除工业废气中的CO,其反应为CaSO (s)+CO(g) CaO(s)+CO (g)+SO (g)。向体积为4L的恒
4 4 2 2
温恒容密闭容器中加入一定量CaSO (s)和20mol CO(g)发生反应,起始压强为200kPa,测得容器内的压强(p)与
4
时间(t)的关系如图所示。在t
2
时刻,将容器体积瞬间缩小为2L;到t
3
时刻达到平衡,此时容器内压强为560 kPa,
忽略固体体积对压强的影响。下列说法正确的是
p/kPa
A.t 时刻一定达到平衡状态
1
B.若在t 时刻再加入CaSO (s),则正反应速率增大
3 4
300
C.0→t min内,用CO表示的平均反应速率为 1 0 0 kPa·min-1
1 t
1 200
D.t 3 时刻达到平衡时,SO 2 的分压为260 kPa 0 t 1 t 2 t/min
二、非选择题:本题共4小题,共58分。
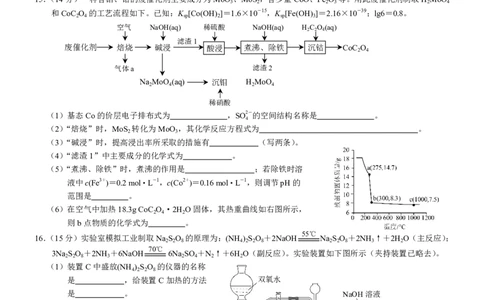
15.(14分)一种含钼、钴的废催化剂主要成分为MoO 、MoS ,含少量CoO、Fe O 等。用此废催化剂制取H MoO
3 2 2 3 2 4
和CoC O 的工艺流程如下。已知:K [Co(OH) ]=1.6×10-15,K [Fe(OH) ]=2.16×10-39;lg6=0.8。
2 4 sp 2 sp 3
空气 NaOH(aq) 稀硫酸 NaOH(aq) HC O(aq)
2 2 4
滤渣1
废催化剂 焙烧 碱浸 酸浸 煮沸、除铁 沉钴 CoC O
2 4
气体a 滤渣2
Na MoO (aq) 沉钼 H MoO
2 4 2 4
稀硝酸
(1)基态Co的价层电子排布式为 ,SO2-的空间结构名称是 。
4
(2)“焙烧”时,MoS 转化为MoO ,其化学反应方程式为 。
2 3
(3)“碱浸”时,提高浸出率所采取的措施有 (写两条)。
(4)“滤渣1”中主要成分的化学式为 。
(5)“煮沸、除铁”时,煮沸的作用是 ;若除铁时溶
液中c(Fe3+)=0.2 mol·L-1,c(Co2+)=0.16 mol·L-1,则调节pH的
范围是 。
b(300,8.3)
(6)在空气中加热18.3g CoC O ·2H O固体,其热重曲线如右图所示,
2 4 2
则b点物质的化学式为 。
55℃
16.(15分)实验室模拟工业制取Na S O 的原理为:(NH ) S O +2NaOH Na S O +2NH ↑+2H O(主反应);
2 2 8 4 2 2 8 2 2 8 3 2
70℃
3Na S O +2NH +6NaOH 6Na SO +N ↑+6H O(副反应)。实验装置如下图所示(夹持装置已略去)。
2 2 8 3 2 4 2 2
(1)装置C中盛放(NH ) S O 的仪器的名称
4 2 2 8
是 ,给装置C加热的方法 双氧水
是 。 NaOH溶液
(2)装置B中长颈漏斗的作用是 ,
向装置C中通入O
2
的目的是 。 黏结的MnO
2
(3)反应结束后,向装置C中加入乙醇,经
稀硫酸
过滤、洗涤、干燥可得 Na S O ,加入
2 2 8
(NH)S O
乙醇的作用是 。
A B C
4 2 2 8
D
(4)工业上用Na S O 处理含有CN-的电镀废水,生成一种酸性气体和铵盐,反应的离子方程式为 。
2 2 8
(5)测定Na S O 处理后的废水中NaCN的含量:取1L处理后的废水,浓缩为30.00mL后置于锥形瓶中,滴入
2 2 8
少量KI溶液作指示剂,用0.001mol·L-1AgNO 标准溶液滴定,正确操作三次,平均消耗标准液3.50mL。
3
已知:滴定时发生反应Ag++2CN- [Ag(CN) ]- K=1.0×1021;杂质不参与反应;K (AgI)=8.5×10-17。
2 sp
达到滴定终点的现象是 ,处理后的废水中NaCN的浓度为 mg·L-1。
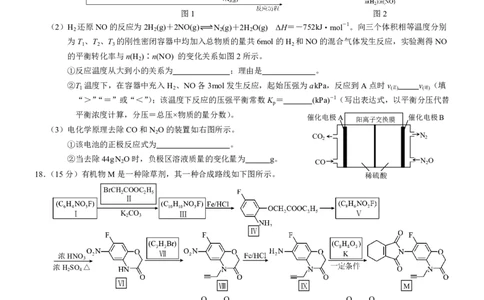
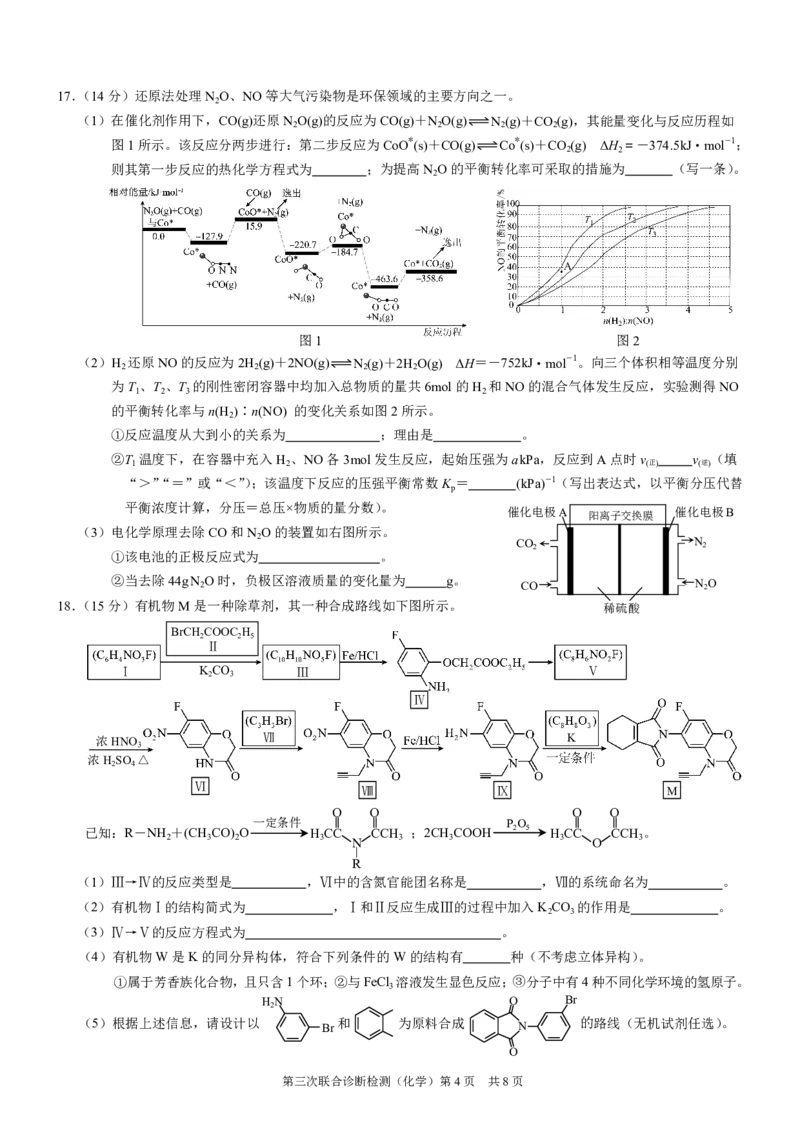
第三次联合诊断检测(化学)第3页 共8页17.(14分)还原法处理N O、NO等大气污染物是环保领域的主要方向之一。
2
(1)在催化剂作用下,CO(g)还原N
2
O(g)的反应为CO(g)+N
2
O(g) N
2
(g)+CO
2
(g),其能量变化与反应历程如
图1所示。该反应分两步进行:第二步反应为CoO * (s)+CO(g) Co * (s)+CO (g) ΔH =-374.5kJ·mol-1;
2 2
则其第一步反应的热化学方程式为 ;为提高N O的平衡转化率可采取的措施为 (写一条)。
2
A
图1 图2
(2)H 还原NO的反应为2H (g)+2NO(g) N (g)+2H O(g) ΔH=-752kJ·mol-1。向三个体积相等温度分别
2 2 2 2
为T 、T 、T 的刚性密闭容器中均加入总物质的量共6mol的H 和NO的混合气体发生反应,实验测得NO
1 2 3 2
的平衡转化率与n(H )∶n(NO) 的变化关系如图2所示。
2
①反应温度从大到小的关系为 ;理由是 。
②T 温度下,在容器中充入H 、NO各3mol发生反应,起始压强为akPa,反应到A点时v v (填
1 2 (正) (逆)
“>”“=”或“<”);该温度下反应的压强平衡常数K = (kPa)-1(写出表达式,以平衡分压代替
p
平衡浓度计算,分压=总压×物质的量分数)。
催化电极A
阳离子交换膜
催化电极B
(3)电化学原理去除CO和N O的装置如右图所示。
2
CO 2 N 2
①该电池的正极反应式为 。
②当去除44g N 2 O时,负极区溶液质量的变化量为 g。 CO N 2 O
18.(15分)有机物M是一种除草剂,其一种合成路线如下图所示。 稀硫酸
BrCH
2
COOC
2
H
5
Ⅱ
Ⅰ K
2
CO
3
Ⅲ Ⅴ
Ⅳ
浓HNO Ⅶ K
3
浓HSO △
2 4
Ⅵ
Ⅷ Ⅸ M
O O O O
一定条件 P O
已知:R-NH +(CH CO) O H C C C C H ;2CH COOH 2 5 H CC CCH 。
2 3 2 3 3 3 3 3
N O
R
(1)Ⅲ→Ⅳ的反应类型是 ,Ⅵ中的含氮官能团名称是 ,Ⅶ的系统命名为 。
(2)有机物Ⅰ的结构简式为 ,Ⅰ和Ⅱ反应生成Ⅲ的过程中加入K CO 的作用是 。
2 3
(3)Ⅳ→Ⅴ的反应方程式为 。
(4)有机物W是K的同分异构体,符合下列条件的W的结构有 种(不考虑立体异构)。
①属于芳香族化合物,且只含1个环;②与FeCl 溶液发生显色反应;③分子中有4种不同化学环境的氢原子。
3
HN O Br
2
(5)根据上述信息,请设计以
B r
和 为原料合成
N
的路线(无机试剂任选)。
O
第三次联合诊断检测(化学)第4页 共8页2025 年重庆市普通高中学业水平选择性考试
高三第三次联合诊断检测 化学参考答案
1~5 BACBA 6~10 DBBDC 11~14DDAC
1.B【解析】酚醛树脂是合成有机高分子,B不正确。
2.A【解析】[(NH ,K,Cs,Rb)MgCl ·6H O]是离子晶体,熔点较高,A不正确。
4 3 2
3.C【解析】A选项,Al3+与HS-会发生双水解,不能大量共存;B选项,H+与CH COO-不能大量共存;
3
D选项,酸性环境下,MnO-会氧化Cl-。
4
4.B【解析】ClO-的中心原子有1对孤电子对,ClO-为三角锥形,SO 2-的中心原子没有孤电子对,为正四面体
3 3 4
形,故ClO-的键角小于SO 2-的键角。
3 4
5.A【解析】A选项,在[Cu(NH ) ]SO 溶液中加入乙醇,可降低溶剂的极性,从而析出[Cu(NH ) ]SO ·H O晶
3 4 4 3 4 4 2
体,能达到实验目的;B选项,检验卤代烃中卤族元素,需先加入NaOH溶液加热,再加硝酸酸化,最后
加AgNO 溶液,B项不能达到实验目的;C选项,制得的气体中除乙炔外,还有H S等杂质,H S也能使
3 2 2
溴水褪色;D选项,CO 与Na CO 溶液反应,D项不能达到实验目的。
2 2 3
6.D【解析】A选项,X存在顺反异构体,A不正确;B选项,X分子中的碳原子有可能全部共平面,B不正确;
C选项,X发生反应水解后,苯环上有1个酚羟基,故1mol X最多可与3mol NaOH反应,C不正确;D
选项,X与足量H 发生加成反应所得的物质为 ,含有3个手性碳原子,D正确。
2
7.B【解析】由W原子核外s能级上的电子总数与p能级上的电子总数相等,观察物质结构可知W的电子排布
式为1s22s22p4,W是O元素,又由X、Y、Z、W、M是原子序数依次增大的同一短周期元素,则X、Y、
Z、M分别为Li、B、C、F元素。A 选项,O可与F形成OF ,其中O 为+2价,A不正确;B 选项,F
2 2
的氧化性强于O 的氧化性,B正确;C选项,H BO 是一元酸,C不正确;D选项,简单氢化物的沸点是
2 3 3
H O>HF>CH ,D不正确。
2 4
8.B【解析】A选项,发生的反应是Cu+2Fe3+=Cu2++2Fe2+,Cu不能置换Fe,金属性:Fe>Cu,A不正确;
B选项,Cl-和I-的浓度相同时,滴加AgNO 溶液先生成AgI沉淀,说明K (AgCl)>K (AgI),B正确;C
3 sp sp
选项,滴加稀硫酸后,HNO 可以氧化Fe2+,不能说明Fe(NO ) 溶液变质,C不正确;D选项,溶液变蓝,
3 3 2
有可能淀粉溶液部分水解,D不正确。
9.D【解析】a为SO ,没有永久漂白性,A不正确;b为Fe O ,不能与Al O 发生反应,B不正确;c为SO ,
2 3 4 2 3 3
与 BaCl 溶液反应生成 BaSO 沉淀,C 不正确;d 是 H SO ,浓硫酸和稀硫酸分别与铁反应的产物不同,D
2 4 2 4
正确。
第三次联合诊断检测(化学)第5页 共8页10.C【解析】由盖斯定律:反应①+②得CO (g)+3H (g)CH OH (g)+H O(g) H=-46 kJ·mol-1,
2 2 3 2
再由 H=反应物键能总和-生成物键能总和,得H-H共价键的键能为43 6 k△J·mol-1。
11.D【解析】根据Na+移动方向可知,a为光伏电池的正极,b为光伏电池的负极,左侧为阳极室,其电极反应
△
为:2H O-4e-=4H++O ↑,右侧为阴极室,其电极反应为2H O+2e-=H ↑+2OH-,由阳极反应可知,
2 2 2 2
生成1mol HClO ,电路中转移1mole-,由阴极反应可知,转移1mol e-,产生1g H ,D选项符合题意。
4 2
12.D【解析】A选项,根据图2中的晶胞可知,Cs位于晶胞体心,Sn位于晶胞顶角,Br位于晶胞12条棱上,
故1个晶胞中含1个Cs、1个Sn、3个Br,该物质的化学式为CsSnBr ,A不正确;B选项,与Cs等距
3
3
且紧邻的Br有12个,B不正确;C选项,Cs与Sn之间的最近距离应是晶胞体对角线的一半,即 apm,
2
C不正确;D选项,CsSnBr 的摩尔质量为492g·mol-1,1个晶胞中含1个CsSnBr ,该晶胞的质量为
3 3
4.92
(492/N )g,该晶胞的体积为(a3×10-30)cm3,该晶体的密度为 1032 g·cm-3。
A N a3
A
13.A【解析】A选项,a点溶液中:pH=8.25,c(OH-)=10-5.75mol/L,根据二者K 值计算得c(CO 2-)>c(OH-),
sp 3
A不正确;B选项,由图中曲线可知,NiCO (s)可以转化为Ni(OH) (s),B正确,曲线Ⅱ下方都属于NiCO
3 2 3
的不饱和溶液,b点溶液中:c(CO 2-)×c(Ni2+)<1.42×10-7,C正确,D选项,根据物料守恒,D正确。
3
14.C【解析】由题意,起始加入20mol CO(g)在4L容器中,压强为200kPa,反应到t 时刻压强为300kPa,
1
则t 时刻气体总物质的量为30mol,其转化如下:
1
CaSO (s)+CO(g) CaO(s)+CO (g)+SO (g) ①
4 2 2
起始(mol) 20
转化(mol) 10 10 10
平衡(mol) 10 10 10
此时CO、CO 、SO 的分压均为100kPa。
2 2
t 时刻将容器体积缩小为2L,则CO、CO 、SO 的分压均为200kPa,到t 时刻达平衡,总压为560kPa,
2 2 2 3
则此时气体总物质的量为28mol,存在如下转化:
CaO(s)+CO (g)+SO (g) CaSO (s)+CO(g) ②
2 2 4
起始(mol) 10 10 10
转化(mol) 2 2 2
平衡(mol) 8 8 12
此时CO、CO 、SO 的分压分别为240kPa、160kPa、160kPa。
2 2
160160 100100
根据t 时刻是平衡状态,可计算反应①的K = kPa,t 时刻反应①Q = kPa<K ,故t
3 p 1 p p 1
240 100
时刻反应未达到平衡状态,此时应是CaSO (s)不足量,A不正确;B选项,CaSO (s)是固体,加入CaSO (s)
4 4 4
反应速率不变,B不正确;C选项,由方程式可知,0→t min内CO的压强减少100kPa,用CO表示的平
1
100
均反应速率为 kPa·min-1,C正确;D选项,t 时刻SO 的分压为160kPa,D不正确。
3 2
t
1
第三次联合诊断检测(化学)第6页 共8页15.(14分,除标注外均2分)
(1)3d74s2(1分) 正四面体(1分)
(2)2MoS +7O 2MoO +4SO
2 2 3 2
(3)搅拌、适当升温、延长浸取时间等
(4)CoO、Fe O
2 3
(5)破坏Fe(OH) 胶体,让其转化为沉淀,便于过滤分离 2.8<pH<7
3
(6)Co O
2 3
【解析】
(5)Fe3+沉淀完全的pH:c(OH-)=3
2.161039
=6×10-12,pOH=11.2,pH=14-11.2=2.8,
1105
Co2+开始沉淀的pH:c(OH-)=
1.61015
=10-7,pH=7,则调节pH的范围是2.8<pH<7。
0.16
(6)18.3g CoC O ·2H O(摩尔质量为183g/mol)为0.1mol,0.1mol Co的质量为5.9g,b点处,O元素的质量
2 4 2
为8.3-5.9=2.4g,即0.15mol,n(Co)∶n(O)=0.1∶0.15=2∶3,故b点物质的化学式为Co O 。
2 3
16.(15分,除标注外均2分)
(1)三颈烧瓶(1分) 水浴加热
(2)平衡气压,防堵塞 将生成的NH 赶出C装置,防止副反应发生
3
(3)降低溶剂的极性,从而降低Na S O 的溶解度
2 2 8
(4)CN-+S O 2-+2H O=CO ↑+2SO 2-+NH+
2 8 2 2 4 4
(5)当滴入最后半滴AgNO 标准溶液,产生黄色浑浊,且半分钟内不消失
3
0.343
【解析】(5)m(NaCN)=3.5×10-3×0.001×2×49×103=0.343mg。
17.(14分,除标注外均2分)
(1)①Co* (s)+N O(g) CoO*(s)+N (g) ΔH=+15.9 kJ·mol -1
2 2
②适当降低温度或增大CO浓度(1分)
(2)①T >T >T 该反应的正反应是放热反应,n(H )∶n(NO)相同时,温度越高,NO的平衡转化率越低
3 2 1 2
40
②>(1分)
81a
(3)①N O+2e -+2H +=N +H O
2 2 2
②18
【解析】(2) ②2H (g)+2NO(g) N (g)+2H O(g)
2 2 2
起始(mol) 3 3
转化(mol) 1.2 1.2 0.6 1.2
平衡(mol) 1.8 1.8 0.6 1.2
第三次联合诊断检测(化学)第7页 共8页平衡时,总物质的量为1.8+1.8+0.6+1.2=5.4mol
设平衡时的压强为x kPa,则6∶a=5.4∶x,解得x=0.9a
1.2 0.6
( 0.9a)2( 0.9a)
K = 5.4 5.4 = 40 (kPa)-1
p 1.8 1.8 81a
( 0.9a)2( 0.9a)2
5.4 5.4
(3)②负极反应式为:CO-2e-+H O=CO +2H+,正极反应为:N O+2e-+2H+=N +H O,去除44gN O
2 2 2 2 2 2
时,转移2mole-,根据负极反应和H+转移到正极区,负极区减少1molH O的质量,即18g。
2
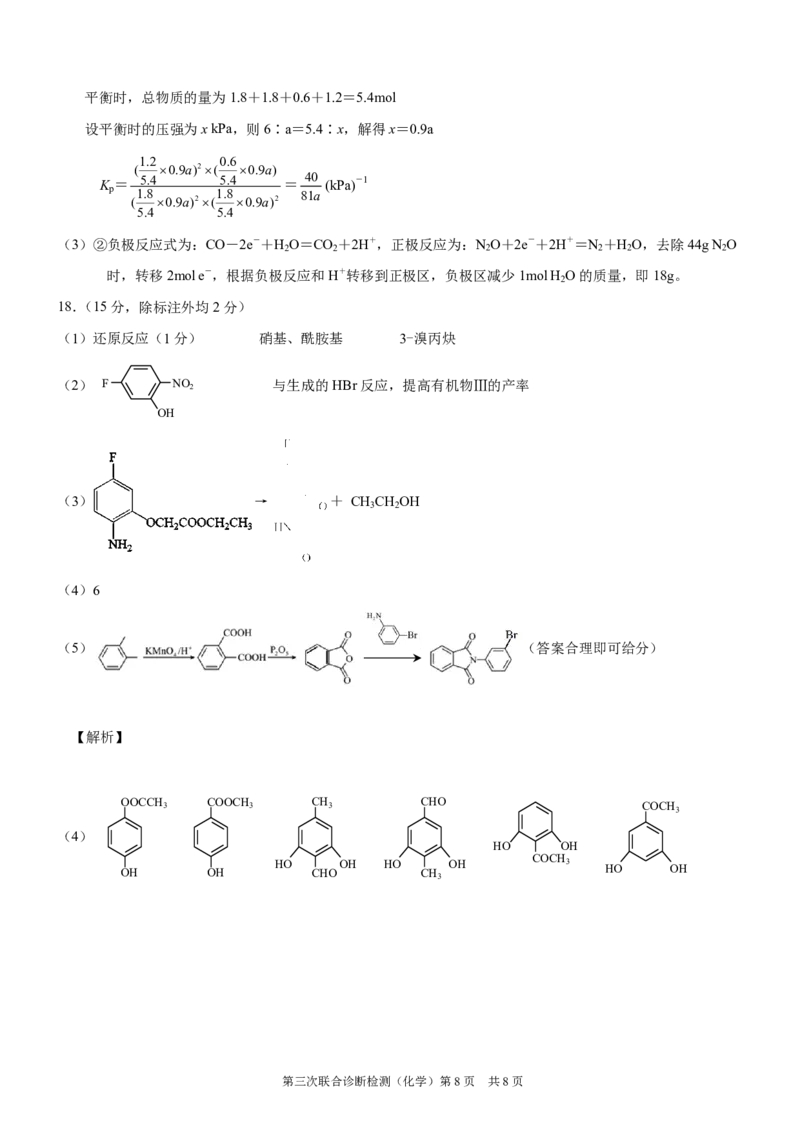
18.(15分,除标注外均2分)
(1)还原反应(1分) 硝基、酰胺基 3-溴丙炔
(2) F NO
2
与生成的HBr反应,提高有机物Ⅲ的产率
OH
(3) → + CH CH OH
3 2
(4)6
(5) (答案合理即可给分)
【解析】
OOCCH COOCH CH CHO
3 3 3 COCH
3
(4)
HO OH
COCH
HO OH HO OH 3
HO OH
OH OH CHO CH
3
第三次联合诊断检测(化学)第8页 共8页