文档内容
秘密 启用前
★
年高考考前适应性测试(押题卷
2025
化学参考答案详解及评分说明
评分说明:
考生如按其他方法或步骤解答,正确的,同样给分;有错的,根据错误的性质,参照评分参考中相应的规定评分。
一、选择题:本题共 小题,每小题 分,共 分。
14 3 42
1.D
【解析】液晶是介于晶体和非晶体的一种特殊物质状态,没有固定的熔沸点, 错误;燃煤中加入石灰石,可和
A SO2
反应减少酸雨的形成,同时释放 ,不能减少温室效应,错误;陶瓷的主要原料是黏土,错误;耐高温是共价
CO2 B C
晶体的性质,所以 属于共价晶体, 正确。
Si3N4 D
2.C
CH3
【解析】 的中心原子 没有孤电子对,其 模型为平面三角形,错误;聚丙烯的结构简式为 ,
—[ — —]
SO3 S VSEPR A CH2 CH n B
错误; 分子中共价键是由 个氯原子各提供 个容纳未成对电子的 轨道通过“头碰头”形成的 — 键,其
Cl2 2 1 3p p pσ
电子云轮廓图为 ,正确;基态 原子的价层电子排布式为 , 错误。
2 5
C Br 4s4p D
3.B
【解析】 溶液有强氧化性,应选择酸式滴定管, 错误; 和 溶液反应,使圆底烧瓶内压强减小,能完
KMnO4 A SO2 NaOH
成喷泉实验,正确;转移洗涤液时,应用玻璃棒引流,错误;制备乙酸乙酯时,要加入浓硫酸作为催化剂,且导
B C
管应通到饱和 溶液的液面上方, 错误。
Na2CO3 D
4.A
【解析】由于 的溶解度小于 ,所以会析出 晶体, 正确;根据“以少定多”,由于 的物
NaHCO3 Na2CO3 NaHCO3 A NaHSO4
质的量少,参加反应的n( )∶n( ) ∶,所以反应的离子方程式为 == ,
+ 2- + 2- - 2+
H SO4 =1 1 H +SO4 +OH +Ba BaSO4↓+H2O B
错误; 被 还原为 ,由于 过量,所以 == ,总反应离子方程式为 == ,
3+ 2- 2+ 2- 2- 2+ 2- 3+
Fe S Fe S S +Fe FeS↓ 3S +2Fe S↓+2FeS↓
错误;新制的 ( )又继续和过量的氨水反应,形成配位键,生成[ ( )], 错误。
2+
C Cu OH 2 Cu NH3 4 D
5.D
【解析】根据 和 的结构式可知,有机物 和苯甲醛反应除合成 外,还有 生成,不符合加成反应的特征,
X Y X Y H2O A
错误; 和 分子中都没有手性碳原子,错误; 分子中 原子有 、 两种杂化方式, 杂化空间结构为四面
2 3 3
X Y B X C sp sp sp
体形,所有 原子不可能共平面,错误; 分子中含有 == 键,能发生加成、氧化、加聚反应,— 能发生取
C C Y C C COOH
代反应, 正确。
D
6.B
【解析】、 对应含氧酸分别为 、 ,均为强电解质, 正确;工业上用 的催化氧化先合成 ,进一步
e e´ HNO3 HClO4 A NH3 NO
制备 ,并不通过合成 这一步骤, 错误;利用 还原 或 生成 可以消除氮氧化物的污染, 正
HNO3 N2 B NH3 NO NO2 N2 C
确; 见光分解生成 ,酸性会增强, 正确。
HClO HCl D
7.D
【解析】 的酸性大于 ,是因为电负性: ,原子比 原子的吸电子能力更强, 错误;
CF3COOH CCl3COOH F>Cl F Cl A SiO2
是共价晶体,而 为分子晶体,共价键的键能大于范德华力,所以熔点: , 错误;基态 原子的半径
CO2 SiO2>CO2 B Si
较大, 轨道的电子云难以“肩并肩”形成 键,所以 原子之间难形成 == 、 ,错误; 正确。
3p π Si Si Si Si Si C D
化学试题答案 第 页(共 页)
1 48.B
【解析】由图可知,物质被吸附在催化剂表面形成过渡态过程都是能量升高,是吸热过程,正确;形成过渡态 的活
A Ts1
化能为 ( ) ,错误;前三步历程中有 == 极性键和 — 非极性键的断裂,— 极性键
1.15eV- 1.0-0.9 eV=1.05eV B C O H H O H
的形成,正确;由反应历程图可看出能量变化最大的反应方程式是· 7 ()== (),
C HOCO+ H2 g ·CO+·OH+·H+3H2 g
2
正确。
D
9.B
【解析】加热后,溶液中蓝色的[ ( )]转化为黄色的[ ],则该转化反应为吸热反应, 正确; 不仅可
2+ 2+
Cu H2O 4 CuCl4 A Cl2
将 氧化为 ,溶液呈黄色,也可将 氧化为 ,碘溶液也呈黄色, 错误; 溶液中产生了黑色沉淀,而
2+ 3+ -
Fe Fe I I2 B CuSO4
溶液无明显变化,说明K( ) K( ),正确;淀粉遇 显蓝色,溶液未显蓝色,说明淀粉已水解完全,
ZnSO4 sp ZnS > sp CuS C I2
正确。
D
10.C
【解析】由基态 、 原子电子填充的最高能层均为 层,可推知 、 为第二周期元素,再结合分子结构中原子共
X Y L X Y
价键的数目,以及冠醚的结构特点,可知 为碳元素, 为氧元素; 形成一个共价键且原子序数比碳元素小,
X Y W
则 为氢元素;根据题意可推知,基态 原子的电子排布式为 ,为钠元素。该超分子中存在共价
2 2 6 1
W Z 1s2s2p3s Z
键、范德华力、金属键,但不存在氢键, 错误;该超分子能识别 ,反映了超分子“分子识别”的特性,错误;碳
A Na B
元素可形成金刚石、石墨、 等晶体,不一定为共价晶体, 错误。
C60 D
11.C
【解析】由题干信息和图像可知,点之前反应未达到平衡状态,随着温度升高,反应速率加快, 的体积分
b CH3OH
数逐渐增大,点时 的体积分数最大,达到平衡状态,点后随着温度升高, 的体积分数逐渐减
b CH3OH b CH3OH
小,说明平衡逆向进行,正反应 H ,由化学方程式可知 S ,根据 G H T S ,可知该反应低温自
Δ <0 Δ <0 Δ =Δ - Δ <0
发进行, 错误;平衡常数只和温度有关,该反应为放热反应,温度越高,平衡常数越小,所以K K K, 错
A a > b > c B
误;根据图像可知 、两点各组分的浓度分别相同,但 点的温度高于 点,所以 点的反应速率高于 点,
a c c a c a
v(逆) v(正) v(正),正确;点时反应达到平衡状态,向容器中再充入等物质的量的 和 ,根据等效平
c = c > a C c CO2 H2
衡原理,再次达到平衡时,相当于增大体系的压强,平衡正向移动, 的体积分数变小, 错误。
CO2 D
12.D
【解析】 中硼原子的价层电子数为 ,孤电子对数为 ,空间结构为正四面体形, 错误;根据晶胞中微粒的位
-
BH4 4 0 A
置,计算得到晶胞中含有 个 ,个[ ( )]n ,根据化合价规则,可推知 个[ ( )]n 共显 价,所以
- + +
8 BH4 4 Fe NH3 6 4 Fe NH3 6 +8
显 价,错误;和“ ”距离最近且相等的“ ”数目为 ,错误; 正确。
Fe +2 B 8 C D
13.D
【解析】根据电解装置图中物质的进出以及所要制备的物质,可知 室中的 要进入 室,所以离子交换膜
-
Ⅱ NO3 Ⅰ Ⅰ
为阴离子交换膜。 要进入 室,离子交换膜 为阳离子交换膜, 正确; 室中电极产生 ,电极反应式为
+ +
NH4 Ⅲ Ⅱ D Ⅰ H
== ,发生氧化反应,电极 为阳极,接外电源的正极, 错误;电极 为阴极,电极反应式
- +
2H2O-4e O2↑ +4H M A N
为 == 错误;每当产生标准状况下 ,根据电子守恒, 室溶液中就要生成
- -
2H2O + 2e 2OH + H2↑,B 22.4 L O2 Ⅲ
,质量减少 ,同时依据电荷守恒, 通过阳离子交换膜进入 室,溶液质量增加 ,所以
+
2molH2 4g 4molNH4 Ⅲ 72g Ⅲ
室溶液的质量理论上共增加 ,错误。
68g C
14.C
【解析】根据图像中含 微粒只有两条线,所以对应的微粒为 和 ,溶液中不存在 分子,酸 为强电
- 2-
A HA A H2A H2A
解质,
-
为弱电解质,电离方程式为 ==
+ -
-
+ 2-
,正确; 越大,碱性越强,
2-
的分
HA H2A H +HA HA H +A B pH A
布分数越大, 的分布分数越小,所以 线为 , 线为 , 正确;当 为 时,c( ) c( ),对应的
- 2- - - 2-
HA Ⅰ A Ⅱ HA A δ 0.5 HA = A
,c( ) ,根据K 的表达式,K ,数量级为 , 正确;点对应溶液的溶质为
+ -8.4 -8.4 -9
pH ≈ 8.4 H = 1 × 10 a a ≈ 1 × 10 10 D c 2 ×
化学试题答案 第 页(共 页)
2 4、 ,根据电荷守恒可得c( ) c( ) c( ) c( ) c( ) c( ),
-3 -3 + + 2- - - 2-
10 molNa2SO4 2×10 molNaHA H + Na =2 SO4 + OH + HA +2 A
根据物料守恒可得c( ) c( ) c( ),联立两式可得c( ) c( ) c( ) c( ) c( ),
2- - 2- + + 2- - 2-
A + HA = SO4 H + Na = 3 SO4 + OH + A C
错误。
二、非选择题:本题共 小题,共 分。
4 58
( 分,除标注外每空 分)
15. 14 2
3d 4s
() ( 分)
1 1
()增大接触面积,加快反应速率,提高浸取率
2
()光导纤维( 分)
3 1
()c( ) c( ) c( ) c( ) c( )
2- + 3+ + -
4 SO4 > NH4 > Al > H > OH
() ( ) ====
2+ + + 2-
5 4NH4V SO4 2+O2+2H2O 4VO +4H +4NH4 +8SO4
() == 萃取剂与 的结合能力远大于 ,将 转化为 ,避免 影响 的萃取
3+ 2+ 3+ 2+ 3+ 2+ 3+ 2+
6 Fe+2Fe 3Fe Fe VO Fe Fe Fe VO
()
7 3
3d 4s
【解析】()元素 位于第四周期第 族,价层电子轨道表示式为 。
1 V ⅢB
()由于碱性: ( ),所以 的水解程度大于 ,溶液呈酸性,离子浓度从大到小的顺序
3+ +
4 NH3·H2O > Al OH 3 Al NH4
为c( ) c( ) c( ) c( ) c( )。()根据题目中所给的信息, 由 价被 氧化为 价,离子
2- + 3+ + -
SO4 > NH4 > Al > H > OH 5 V +3 O2 +4
方程式为 ( ) ====
2+ + + 2-
。()由于萃取剂与阳离子的结合能力:
4NH4V SO4 2 + O2 + 2H2O 4VO + 4H + 4NH4 + 8SO4 6
;为了萃取 ,所以用 将 还原成 ,离子方程式为 == ,目的是避
3+ 2+ 3+ 2+ 2+ 3+ 2+ 3+ 2+
Fe >VO >Al >Fe VO Fe Fe Fe Fe+2Fe 3Fe
免 影响 的萃取。()根据K 的表达式,可得出c( ) ,c( ) , 。
3+ 2+ - -11 + -3
Fe VO 7 sp OH =1×10 H =1×10 pH=3
( 分,除标注外每空 分)
16. 15 2
()
1 +2 4
()恒压滴液漏斗( 分) 平衡气压,使醋酸钴溶液顺利滴下( 分)
2 1 1
()乙酸或醋酸( 分)
3 1
()作为溶剂,使水杨醛和乙二胺溶解充分接触反应(合理即可)
4
()排尽装置中的空气,防止配合物[ ]被 氧化而变质
5 CoSaLen O2
()
6 ③①②
()液封,防止外界空气进入三颈烧瓶中
7
【解析】()由于中心原子 原子和两个 原子形成极性共价键,而和两个 原子形成配位键,配位键不影响中
1 Co O N
心原子 的价态,所以 显 价;两个 原子,两个 原子直接和 原子配位成键,所以中心原子 原子的
Co Co +2 O N Co Co
配位数为 。()配体与醋酸钴发生了取代反应,另一产物是 。()乙醇是有机溶剂,水杨醛和乙二胺能
4 3 CH3COOH 4
够溶解充分接触反应。()配合物[ ]具有还原性,易被氧化,所以通入 ,排尽装置中的空气,防止配合
5 CoSaLen N2
物[ ]被 氧化而变质。()用水液封,防止外界空气进入三颈烧瓶中,避免配合物[ ]被 氧化。
CoSaLen O2 7 CoSaLen O2
( 分,除标注外每空 分)
17. 15 2
() () ()== () () H
1 2NO g +2CO g N2 g +2CO2 g Δ =-746.5kJ/mol
() 高温( 分)
2 ①CO N2 ② 1 ③80%
()( 分) ( 分) 温度小于 时,反应未达到平衡状态,升高温度,反应速率加快, 生成
3 < 1 0.15 1 580K NO N2
的转化率逐渐增大,高于 以后,反应达到平衡状态,升温,平衡逆向移动, 生成 的转化率逐渐减小
580 K NO N2
(合理即可)
()7.5
4 p
化学试题答案 第 页(共 页)
3 4【解析】()根据题干中的已知条件, ()== () () H ,
1 ①2NO g N2 g +O2 g Δ =-180.5kJ/mol
() ()== () H , 可计算出 催化还原 的热化学方程式为
②2CO g + O2 g 2CO2 g Δ = -566 kJ/mol ① + ② CO NO
() ()== () () H 。
2NO g +2CO g N2 g +2CO2 g Δ =-746.5kJ/mol
()温度越高,反应速率越快。结合图像可知,高温时 和 的浓度较低,脱除率高,所以应选择高温条件。
2 CO NO
随着反应的进行, 和 的浓度逐渐降低,又根据两个反应中都消耗 ,而只有第一个反应消耗 ,随着
CO NO CO NO
浓度逐渐降低, 的浓度减小的趋势变小,到后来浓度基本不变,而 浓度减小的趋势较大,所以 是
N2O NO CO Ⅰ
, 是 。两个反应中都产生 , 的浓度大于 , 是 , 是 。根据 原子守恒,c( )
CO Ⅱ NO CO2 CO2 N2 Ⅲ CO2 Ⅳ N2 N NO 初始 =
,转化为 的c( ) ,故 的脱除
1500ppm×2+350ppm+200ppm×2=3750ppm N2 NO =1500ppm×2=3000ppm NO
率 3000 。
= =80%
3750
()根据题目的已知条件,开始只充入反应物,温度小于 时,反应未达到平衡状态,升高温度,反应速率加
3 580K
快, 生成 的转化率逐渐增大。温度大于 以后,反应达到平衡状态,转化率逐渐减小,说明升高温度
NO N2 580K
平衡逆向移动,正反应放热,H 。根据图像,转化的n( ) ( ) ,v( ) v( )
Δ <0 NO = 52%-2% ×3mol=1.5mol NH3 = NO
1.5mol ( )。
= =0.15mol/ L·min
2L × 5min
()设消耗 为x ,生成 为y 。
4 O2 mol N2O4 mol
() () ()
①2NO g +O2 g 2NO2 g
转化 x x x
2 2
() ();
②2NO2 g N2O4 g
转化 y y
2
根据n( ) n( )=n( )可得出 x x y y,经计算x ,y 。平衡后气体总物质的
O2 = NO2 N2O4 1- =2 -2 = =0.6mol =0.4mol
p
量为 ( ),p( ) p( ) 0.4 ,K 7.5。
0.8+0.4+0.4+0.4+1=3 mol NO2 = N2O4 = p= p
3
( 分,除标注外每空 分)
18. 14 2
() ( 分)
1 +3 1
()苯甲醚(或甲苯醚)( 分)
2 1
()醚键、酮羰基、羧基
3
()还原反应( 分) 消去反应( 分)
4 1 1
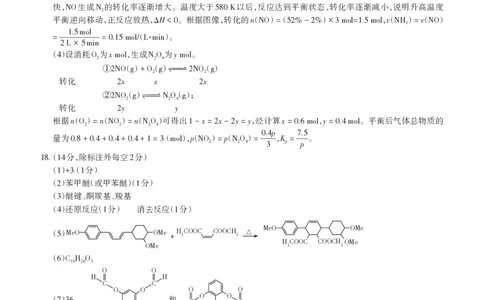
() MeO OMe
5 MeO OMe + H 3 COOC COOCH 3 △
OMe
H
3
COOC COOCH 3OMe
()
6 C19H26O3
O O
H H
C C
O O O O
() 和 O O
7 36 C CH C
H 2 H
CH
2 CH
3
CH
3
【解析】()由于电负性 大于 ,所以 显 价, 显 价。()根据物质 的结构简式,可推知苯酚中的—
1 H B H -1 B +3 2 D OH
和 发生取代反应生成苯甲醚。()用 做还原剂把 == 还原为— ,然后发生消去反应引入两个
CH3I 4 NaBH4 C O OH
== ,所以分别发生了还原反应和消去反应。()利用已知条件 ,发生双烯合成反应,生成 。()根据题目的
C C 5 ② H 7
条件限制,含有苯环以及三个支链,其中有两个酯基连在苯环上,共有 种组合,分别是 — 、 —、
4 ① CH2CH3 HCOO
—,有 种同分异构体; — 、 —、— ,有 种同分异构体; — 、 —、
HCOO 6 ② CH3 HCOO OOCCH3 10 ③ CH3 HCOO
— ,有 种同分异构体; — 、 —、— ,有 种同分异构体。所以一共有 种符合
CH2OOCH 10 ④ CH3 HCOO COOCH3 10 36
条件的同分异构体。
化学试题答案 第 页(共 页)
4 4