文档内容
让更多的孩子得到更好的教育
中考总复习:有关化学方程式的计算(提高)
撰稿:李伟 审稿:熊亚军
【巩固练习】
一、 选择题 (每小题只有一个选项符合题意)
1.电解水得到的氢气和氧气的质量比是( )
A.2:1 B.4:8 C.1:8 D.1:16
2.用铝和铁分别和足量的稀硫酸反应,都得到2克氢气,则消耗铝和铁的质量比为( )
A.1:1 B.27:28 C.9:28 D.3:2
3.镁在空气中燃烧不仅生成氧化镁,还有部分镁与氮气化合(生成物中N呈-3价),由此可以推知12g镁
在空气中燃烧后所得产物的质量为( )
A.等于20g B.小于20g C.大于20g D.以上情况都可能
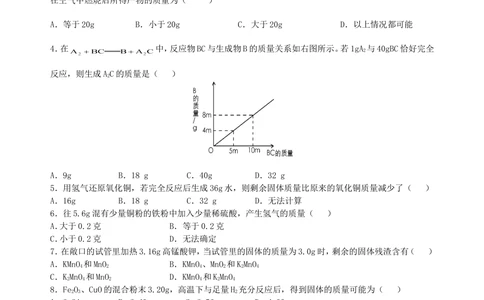
4.在 中,反应物BC与生成物B的质量关系如右图所示。若1gA 与40gBC恰好完全
2
反应,则生成AC的质量是( )
2
A.9g B.18 g C.40g D.32 g
5.用氢气还原氧化铜,若完全反应后生成36g水,则剩余固体质量比原来的氧化铜质量减少了( )
A.16g B.18 g C.32 g D.无法计算
6.往5.6g混有少量铜粉的铁粉中加入少量稀硫酸,产生氢气的质量( )
A.大于0.2克 B.等于0.2克
C.小于0.2克 D.无法确定
7.在敞口的试管里加热3.16g高锰酸钾,当试管里的固体的质量为3.0g时,剩余的固体残渣含有( )
A.KMnO 和MnO B.KMnO、MnO 和KMnO
4 2 4 2 2 4
C.KMnO 和MnO D.KMnO 和KMnO
2 4 2 4 2 4
8.FeO、CuO的混合粉末3.20g,高温下与足量H 充分反应后,得到固体的质量可能为( )
2 3 2
A.2.24g B.2.40g C.2.56g D.4.00g
9.在天平两端的烧杯中分别盛有等体积、等质量分数的稀硫酸,调节平衡后,向两只烧杯中分别
加入质量相等的镁和铝铜合金,恰好完全反应后,仍然保持平衡,则合金中铜与铝的质量比为(
)
A.3:1 B.1:3 C.2:1 D.1:1
10.将一定质量的碳酸钙和铜粉放置于同一敞口容器中,加热煅烧使其完全反应,反应前后容器中固体的
质量不变,则容器中铜和碳酸钙的质量比是( )
A.11:4 B.20:14 C.44:25 D.16:25
11.在实验室里用锌、氧化铜、稀硫酸为原料制取铜,有下列两种途径:
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共6页让更多的孩子得到更好的教育
(1)
(2)
若用这两种方法制得质量相同的铜,下列有关说法:①消耗相同质量的氧化铜 ②消耗相同质量的锌
③消耗相同质量的硫酸 ④生成硫酸锌的质量不同。符合实际情况的是( )
A.①② B.①④ C.①②③ D.①②③④
二、填空题
12.实验室里同学们要配制一定溶质质量分数的氯化钙溶液.药品柜中可供选择的药品只有氢氧化钙、氧
化钙、碳酸钙和硝酸钙四种固体及一定溶质质量分数的稀盐酸.同学们交流讨论后,选择了一种固体药品
并称取15g加入烧杯中,再向其中加入105.4g稀盐酸,充分反应后过滤,得到5g固体和111g氯化钙溶液
(实验中物质损耗忽略不计),并将上述配好的氯化钙溶液倒人贴有相应标签的试剂瓶中.请回答下列问
题:
(1)同学们选择的固体药品是_________
;
(2)请写出题中发生反应的化学方程式___________________________________
;
(3)请根据已知条件列出求解生成氯化钙质量(X)的比例式___________________________;
(4)试剂瓶标签上氯化钙溶液的溶质质量分数为_________。
13.现有CO和CO 的混合气体20g,其中氧元素的质量分数为64%.先使该混合气体通过足量灼热的氧化
2
铁,再通入足量的澄清石灰水中,生成沉淀的质量为________
g。(假设各步均完全反应)
三、计算题
14.已知氢气的密度是0.0899g/L(标准状况),那么,需用多少升(标准状况)氢气才能使8.8g氧化铜完全
被还原?
15.将CuO和Cu的固体混合物6.8g放入烧杯中,加入过量的稀硫酸,充分反应后,过滤、洗涤、干燥,得
2
到4.8g固体。计算原混合物中CuO与Cu的质量比(已知:CuO+HSO=CuSO+Cu+HO)。
2 2 2 4 4 2
16.(2012福建)根据如图所示的信息计算:
(1)加入的稀硫酸质量为 g。
(2)所用稀硫酸溶质的质量分数。 (化学方程式:2KOH + HSO = KSO + 2HO)
2 4 2 4 2
【答案与解析】
1.【答案】 C
【解析】2个水分子电解后得到2个氢气分子和1个氧气分子,质量比为4: 32=1:8。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共6页让更多的孩子得到更好的教育
2.【答案】 C
【解析】可以设制取2克氢气,消耗铝的质量为x,消耗铁质量为y,再列出化学方程式,计算可得。
3.【答案】 B
【解析】由反应方程式推知:12克镁与氧气充分燃烧可生成MgO 20g,若镁与氮气反应,12克镁能生成氮
化镁约16.7g。在空气中反应两种生成物都存在,所以所得产物质量小于20g,大于16.7g。
4.【答案】 A
【解析】由图可知, B与BC的反应的质量比为4:5,所以40gBC参加反应,会生成32g物质B,根据质量
守恒定律,B与AC的质量和为1g+40g=41g,所以生成AC的质量为:41g-32g=9g。
2 2
5.【答案】 C
【解析】氢气还原氧化铜的反应中,氢气夺取了氧化铜中的氧,生成水,同时氧化铜被还原成铜。因此可
分析出氧化铜减少的质量就是36g水中的氧元素的质量。
。
6.【答案】 C
【解析】假设5.6g金属粉末全部为铁粉,与稀硫酸完全反应放出氢气的质量为x。
Fe+HSO═FeSO+H↑
2 4 4 2
56 2
5.6g x
解得:x=0.2g
因此混有铜粉的5.6g金属粉末的混合物与少量稀硫酸产生氢气的质量小于0.2g。
7.【答案】 B
【解析】根据质量守恒定律,当试管里的固体质量为3.0g时,生成O 的质量为3.16g﹣3.0g=0.16g。
2
设生成0.16gO 所参加反应的KMnO 的质量为x。
2 4
△
2KMnO KMnO+MnO+O↑
4 2 4 2 2
316 32
x 0.16g
解得:x=1.58g
剩余高锰酸钾:3.16﹣1.58=1.58克。
8.【答案】 B
【解析】假设混合粉末全是FeO 用氢气还原可得铁的质量是x
2 3
FeO+3H 2Fe+3HO
2 3 2 2
160 112
3.2g x
解得:x=2.24g
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共6页让更多的孩子得到更好的教育
假设混合粉末全是CuO用氢气还原可得铜的质量是y。
△
CuO+H Cu+HO
2 2
80 64
3.2g y
解得:y=2.56g
所以与足量的H 反应后得到的固体质量只会介于2.24g和2.56g之间,选项B符合。
2
9.【答案】 B
【解析】铜与稀硫酸不反应,镁是二价金属,铝是三价金属,反应的关系式为Mg~H,2Al~3H。据题意:Mg
2 2
反应放出H 等于Al反应放出的H。为了便于答题,我们采用赋值假设法解这道无数据型的计算题就简单
2 2
了。
10.【答案】 C
【解析】敞口加热:碳酸钙受热分解放出二氧化碳气体;铜粉受热后与空气中氧气的结合变为氧化铜。
反应前后容器中固体质量保持不变的原因是:碳酸钙受热分解放出的二氧化碳气体的质量与铜粉受热结
合的空气中的氧气的质量相等。
方法一:常规解法
设容器中铜的质量为x,碳酸钙的质量为y
CaCO=CaO+ CO↑ 2Cu + O===2CuO
3 2 2
100 44 128 32
y 44y/100 x 32x/128
44y/100 =32x/128
解得:x/y =44/25。
方法二:赋值法
设氧气和二氧化碳的质量都为4g,则有
CaCO ~ CO 2Cu~O
3 2 2
100 44 128 32
(100g/11) 4g 16g 4g
所以铜与碳酸钙的质量比为16g:(100g/11)=44:25。
11.【答案】 B
【解析】因为整个制备过程中,所有Cu元素都能形成单质Cu,而都来自CuO,没有损失,所以①②氧化
铜质量相同。①Zn+HSO=ZnSO+H↑,H+CuO HO+Cu 生成1份Cu需要1份CuO和1份HSO 和1份Zn;
2 4 4 2 2 2 2 4
②CuO+HSO=CuSO+HO,CuSO+Zn=Cu+ZnSO 生成1份Cu需要1份CuO和1份HSO 和1份Zn,看上去都是
2 4 4 2 4 4 2 4
相同的。但氢气还原氧化铜,氢气必须过量,所以要使用更多锌更多硫酸。
12.【答案】(1)碳酸钙 (2)CaCO+2HCl=CaCl+HO+CO↑
3 2 2 2
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共6页让更多的孩子得到更好的教育
(3) (4)10%
【解析】
(1)因为碳酸钙与稀盐酸反应有气体生成,可以更好的收集数据;
(2)碳酸钙与稀盐酸反应的化学方程式为:CaCO+2HCl=CaCl+HO+CO↑;
3 2 2 2
(3)设生成氯化钙质量为x。
CaCO+2HCl=CaCl+HO+CO↑
3 2 2 2
111 44
x 15g+105.4g-111g-5g
解得:x=11g
(4)氯化钙溶质质量分数= ×100%=10%。
13.【答案】60
【解析】由CO和CO 的混合气体20g中氧元素的质量分数为64%,可推出碳元素的质量分数为:20g×
2
(1-64%)=7.2g,根据一氧化碳与氧化铁反应生成铁和二氧化碳,将原来的二氧化碳和新生成的二氧化碳
都通入石灰水中得到碳酸钙沉淀和水,所以碳酸钙中的碳元素都来自于一开始的一氧化碳和二氧化碳,
所以碳酸钙中碳元素的质量为7.2g,设碳酸钙的质量为X则:X× ×100%=7.2g解得X=60g。
14.【答案】设需用氢气的质量为x,则根据题意
解得:x=0.22g
答:需用2.4升氢气。
【解析】利用有关已知量来确定未知量,注意认真审题;在解题过程中格式规范、步骤完整、计算准确、
勿漏单位。
15.【答案】
解:设原混合物中含CuO的质量为x。
2
CuO+HSO=CuSO+Cu+HO 固体质量减少
2 2 4 4 2
144 64 144﹣64=80
x 6.8g﹣4.8g=2g
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共6页让更多的孩子得到更好的教育
144:x=80:2g
x=3.6g
原混合物中Cu的质量=6.8g﹣3.6g=3.2g
原混合物中CuO与Cu的质量比=3.6g:3.2g=9:8
2
答:原混合物中CuO与Cu的质量比9:8。
2
16.【答案】⑴ 24.5
⑵ 解:设所用稀硫酸溶质的质量为x。
HSO +2KOH = KSO + 2HO
2 4 2 4 2
98 112
x 56 g×10%
=
x = 4.9 g
所用稀硫酸溶质的质量分数 = ×100% = 20%。
答:所用稀硫酸溶质的质量分数为20%。
【解析】(1)据提供的化学方程式可知,反应后既没有沉淀也没有气体生成,混合后的溶液就是反应前
两种溶液的质量之和;得稀硫酸的质量为:80.5g-56g=24.5g。
(2)代入化学方程式的质量,必须纯物质的质量、参加化学反应的物质的质量,根据题意和提供的化学方
程式找到氯化钾的质量(56g×10%)和硫酸的质量比(化学方程式中各物质的质量比等于各相对分子质量
乘以前面的反应系数),列出对应的比例式,求解既得。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第6页 共6页