文档内容
关注湖北升学通获取最新消息
年湖北省八市高三 月 联考
2025 (3 )
化 学 试 卷
命题单位:潜江市教研室 审题单位:天门市教科院 黄石市教科院
2025.3
本试卷共 页, 题。 全卷满分 分。 考试用时 分钟。
8 19 100 75
祝考试顺利
★ ★
注意事项:
答题前,先将自己的姓名、准考证号填写在试卷和答题卡上,并将准考证号条形码
1.
粘贴在答题卡上的指定位置。
选择题的作答:每小题选出答案后,用 铅笔把答题卡上对应题目的答案标号涂
2. 2B
黑。 写在试卷、草稿纸和答题卡上的非答题区域均无效。
非选择题的作答:用黑色签字笔直接答在答题卡上对应的答题区域内。 写在试卷、
3.
草稿纸和答题卡上的非答题区域均无效。
考试结束后,请将本试卷和答题卡一并上交。
4.
可能用到的相对原子质量
:H 1 C 12 O 16 Mg 24 Fe 56 Cu 64
一、选择题:本题共有 小题,每小题 分,共 分。 在每小题给出的四个选项中,只有
15 3 45
一项是符合题目要求的。
化学与生活密切相关 下列叙述中没有涉及化学变化的是
1. 。
生物固氮 染发烫发 血液透析 油脂硬化
A. B. C. D.
下列有关物质应用的说法错误的是
2.
聚氯乙烯用于食品包装 苯甲酸及其钠盐用作食品防腐剂
A. B.
纤维素用于生产燃料乙醇 聚乙炔用于制备导电高分子材料
C. D.
下列化学用语表述正确的是
3.
的 模型 反式聚异戊二烯结构简式
A.SO2 VSEPR B.
四氯化碳的电子式 的结构示意图
2+
C. D.Fe
下列实验方法或试剂使用正确的是
4.
选项 实验目的 实验方法或试剂
测定乙酸晶体及分子结构 射线衍射法
A X
用 标准溶液滴定未知浓度的醋酸溶液 用甲基橙作指示剂
B NaOH
除去乙炔中混有的 通过酸性 溶液
C H2S KMnO4
测定 溶液的 使用 试纸
D NaClO pH pH
化学试卷 第 页 共 页
1 ( 8 )
关注湖北升学通获取最新消息关注湖北升学通获取最新消息
下列对有关物质结构或性质的描述错误的是
5.
图 为 冠 与 形成的超分子 其形成作用力主要存在于 与 之间
+ +
A. 1 18- -6 K , K O
图 为某合金原子层状结构 原子层之间的相对滑动变难导致合金的硬度变大
B. 2 ,
图 为烷基磺酸根离子在水中形成的胶束 表现出超分子自组装的特征
C. 3 ,
图 为由两个硅氧四面体形成的简单阴离子 其化学式为
4-
D. 4 , Si2O7
生活中两种常见的解热镇痛药物阿斯匹林 乙酰水杨酸 和扑热息痛 对乙酰氨基
6. ( ) (
酚 贝诺酯可由这二种物质在一定条件下反应制得 下列有关叙述错误的是
), 。
以上三种有机物中共有 种官能团
A. 4
可用 溶液鉴别乙酰水杨酸和对乙酰氨基酚
B. NaHCO3
贝诺酯作为缓释药可有效降低药物对肠胃的刺激性
C.
贝诺酯与足量 溶液反应消耗
D.1 mol NaOH 4 mol NaOH
化学反应中 量变可以引起质变 下列反应离子方程式书写错误的是
7. , 。
溶液中加入过量的盐酸
- + 3+
A.Na[Al(OH)4] :[Al(OH)4] +4H Al +4H2O
溴水中加入过量的 溶液
2- - - 2-
B. Na2SO3 :Br2+3SO3 +H2O2Br +2HSO3+SO4
溶液中通入过量的 气体
3+ +
C.FeCl3 H2S :2Fe +3H2S2FeS↓+S↓+6H
溶液中加入过量的氨水
2+ 2+
D.CuSO4 :Cu +4NH3·H2O[Cu(NH3)4] +4H2O
物质结构差异会引起物质性质差异 下列事实解释错误的是
8. 。
选项 事实 解释
前者形成分子间氢键
沸点 ,
A : > 后者形成分子内氢键
前者 原子 杂化
2
键角 O sp ,
B C—O—C : 后者 原子 杂化
3
O sp
前者烃基占比小
水溶性 ,
C :CH3CH2OH > CH3CH2CH2CH2CH2OH 后者烃基占比大
前者含有共价键
硬度 金刚石 ,
D : > C60 后者不含共价键
化学试卷 第 页 共 页
2 ( 8 )
关注湖北升学通获取最新消息关注湖北升学通获取最新消息
某荧光粉基材成分的化学式为 其中 三种元素位于短周期 是地壳中
9. XYZW3, Y、Z、W ,Y
含量最高的金属元素 的第一电离能高于它的同周期相邻元素 且其基态原子核外
,W ,
电子有 种空间运动状态 元素原子的最外层电子数是次外层的一半 的原子序数
5 ,Z ,X
是 和 原子序数之和 下列说法错误的是
Y W 。
的氧化物可以做半导体材料 的简单氢化物的分子构型为三角锥形
A.Z B.W
元素的氯化物可以做融雪剂 的氧化物中化学键既有离子性又有共价性
C.X D.Y
一种由离子交换树脂 碳纳米管构成的膜分离装置如图 侧可以连续去除空气中的
10. — ,M
并转化为 同时 侧实现了 的富集 下列说法正确的是
-
CO2 HCO3, N CO2 。
侧空气中发生变化的只有
A.M CO2
复合薄膜既能传导离子 又能传导电子
B. ,
侧收集到 时转移电子数为 N
C.N 2.24 L CO2 0.1 A
侧反应为
D.N H2 + 2e
-
+2HCO
-
3 2H2O + 2CO2
固态储氢材料具有不易泄露 不易爆炸等优点 下图是铁镁储氢材料的晶胞 晶胞参
11. , 。 ,
数为a 氢原子通过与铁镁形成化学键储存在晶体中 并位于以铁原子为中心的正
nm; ,
八面体顶点处 下列说法错误的是
。
该晶胞的化学式是
A. Mg2Fe
与铁原子最近的镁原子有 个
B. 8
储氢后晶体密度为416×10
21
-3
C. N
A×
a3 g·cm
晶胞中 与 的最短距离为 2a
D. Fe Fe nm
2
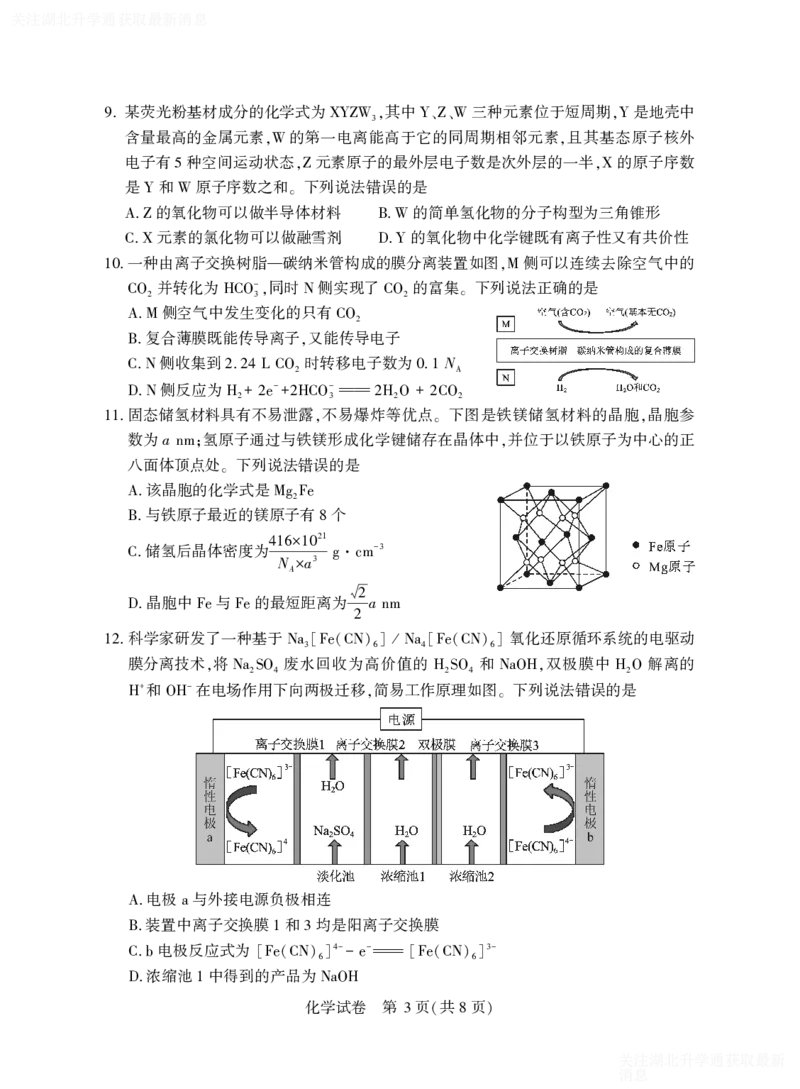
科学家研发了一种基于 氧化还原循环系统的电驱动
12. Na3[Fe(CN)6] / Na4[Fe(CN)6]
膜分离技术 将 废水回收为高价值的 和 双极膜中 解离的
, Na2SO4 H2SO4 NaOH, H2O
和 在电场作用下向两极迁移 简易工作原理如图 下列说法错误的是
+ -
H OH , 。
电极 与外接电源负极相连
A. a
装置中离子交换膜 和 均是阳离子交换膜
B. 1 3
电极反应式为
4- - 3-
C.b [Fe(CN)6] - e [Fe(CN)6]
浓缩池 中得到的产品为
D. 1 NaOH
化学试卷 第 页 共 页
3 ( 8 )
关注湖北升学通获取最新
消息关注湖北升学通获取最新消息
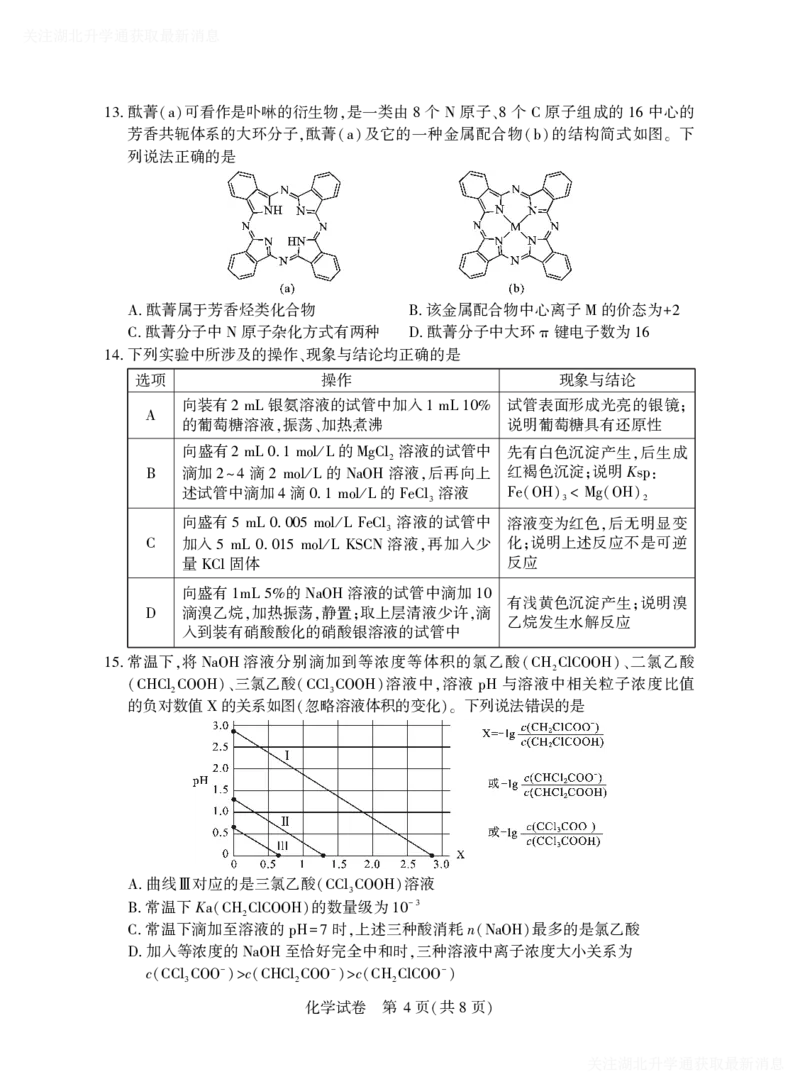
酞菁 可看作是卟啉的衍生物 是一类由 个 原子 个 原子组成的 中心的
13. (a) , 8 N 、8 C 16
芳香共轭体系的大环分子 酞菁 及它的一种金属配合物 的结构简式如图 下
, (a) (b) 。
列说法正确的是
酞菁属于芳香烃类化合物 该金属配合物中心离子 的价态为
A. B. M +2
酞菁分子中 原子杂化方式有两种 酞菁分子中大环 键电子数为
C. N D. π 16
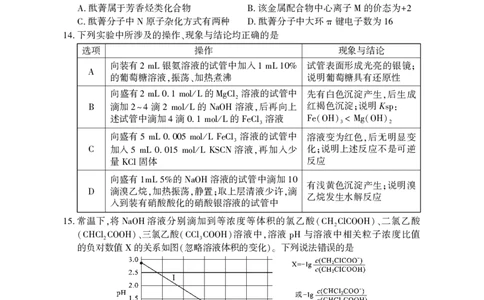
下列实验中所涉及的操作 现象与结论均正确的是
14. 、
选项 操作 现象与结论
向装有 银氨溶液的试管中加入 试管表面形成光亮的银镜
2 mL 1 mL 10% ;
A 的葡萄糖溶液 振荡 加热煮沸 说明葡萄糖具有还原性
, 、
向盛有 的 溶液的试管中 先有白色沉淀产生 后生成
2 mL0.1 mol/L MgCl2 ,
滴加 滴 的 溶液 后再向上 红褐色沉淀 说明K
B 2~4 2 mol/L NaOH , ; sp:
述试管中滴加 滴 的 溶液
4 0.1 mol/L FeCl3 Fe(OH)3 < Mg(OH)2
向盛有 溶液的试管中 溶液变为红色 后无明显变
5 mL 0.005 mol/L FeCl3 ,
加入 溶液 再加入少 化 说明上述反应不是可逆
C 5 mL 0.015 mol/L KSCN , ;
量 固体 反应
KCl
向盛有 的 溶液的试管中滴加
1mL 5% NaOH 10 有浅黄色沉淀产生 说明溴
滴溴乙烷 加热振荡 静置 取上层清液少许 滴 ;
D , , ; , 乙烷发生水解反应
入到装有硝酸酸化的硝酸银溶液的试管中
常温下 将 溶液分别滴加到等浓度等体积的氯乙酸 二氯乙酸
15. , NaOH (CH2ClCOOH)、
三氯乙酸 溶液中 溶液 与溶液中相关粒子浓度比值
(CHCl2COOH)、 (CCl3COOH) , pH
的负对数值 的关系如图 忽略溶液体积的变化 下列说法错误的是
X ( )。
曲线 对应的是三氯乙酸 溶液
A. Ⅲ (CCl3COOH)
常温下K 的数量级为
-3
B. a(CH2ClCOOH) 10
常温下滴加至溶液的 时 上述三种酸消耗n 最多的是氯乙酸
C. pH=7 , (NaOH)
加入等浓度的 至恰好完全中和时 三种溶液中离子浓度大小关系为
D. NaOH ,
c - c - c -
(CCl3COO )> (CHCl2COO )> (CH2ClCOO )
化学试卷 第 页 共 页
4 ( 8 )
关注湖北升学通获取最新消息关注湖北升学通获取最新消息
二、非选择题(本题共 个小题,共 分)
4 55
分
16.(14 )
醋酸铜可作色谱分析试剂和有机合成催化剂等 可以用碱式碳酸铜 x
, [ Cu(OH)2·
y 为原料制备
CuCO3] 。
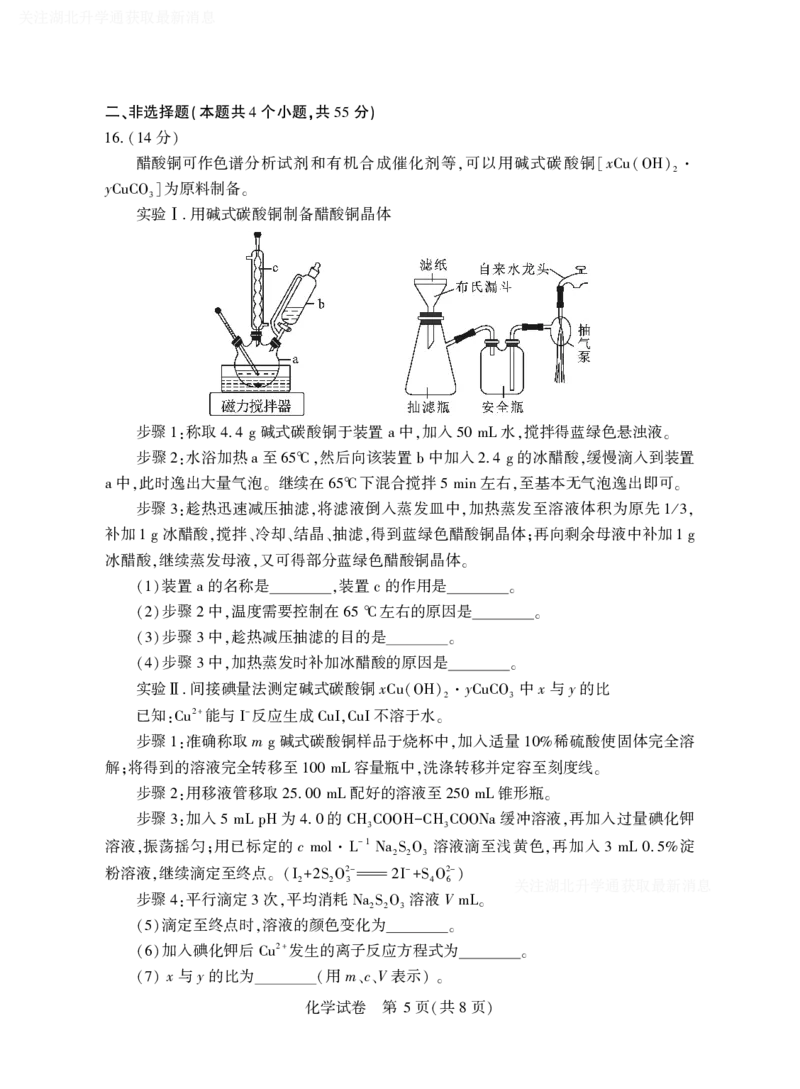
实验 用碱式碳酸铜制备醋酸铜晶体
Ⅰ.
步骤 称取 碱式碳酸铜于装置 中 加入 水 搅拌得蓝绿色悬浊液
1: 4.4 g a , 50 mL , 。
步骤 水浴加热 至 然后向该装置 中加入 的冰醋酸 缓慢滴入到装置
2: a 65℃, b 2.4 g ,
中 此时逸出大量气泡 继续在 下混合搅拌 左右 至基本无气泡逸出即可
a , 。 65℃ 5 min , 。
步骤 趁热迅速减压抽滤 将滤液倒入蒸发皿中 加热蒸发至溶液体积为原先
3: , , 1/3,
补加 冰醋酸 搅拌 冷却 结晶 抽滤 得到蓝绿色醋酸铜晶体 再向剩余母液中补加
1 g , 、 、 、 , ; 1 g
冰醋酸 继续蒸发母液 又可得部分蓝绿色醋酸铜晶体
, , 。
装置 的名称是 装置 的作用是
(1) a , c 。
步骤 中 温度需要控制在 左右的原因是
(2) 2 , 65 ℃ 。
步骤 中 趁热减压抽滤的目的是
(3) 3 , 。
步骤 中 加热蒸发时补加冰醋酸的原因是
(4) 3 , 。
实验 间接碘量法测定碱式碳酸铜x y 中x与y的比
Ⅱ. Cu(OH)2· CuCO3
已知 能与 反应生成 不溶于水
2+ -
:Cu I CuI,CuI 。
步骤 准确称取m 碱式碳酸铜样品于烧杯中 加入适量 稀硫酸使固体完全溶
1: g , 10%
解 将得到的溶液完全转移至 容量瓶中 洗涤转移并定容至刻度线
; 100 mL , 。
步骤 用移液管移取 配好的溶液至 锥形瓶
2: 25.00 mL 250 mL 。
步骤 加入 为 的 缓冲溶液 再加入过量碘化钾
3: 5 mL pH 4.0 CH3COOH-CH3COONa ,
溶液 振荡摇匀 用已标定的 c -1 溶液滴至浅黄色 再加入 淀
, ; mol·L Na2S2O3 , 3 mL 0.5%
粉溶液 继续滴定至终点
, 。 (I2+2S2O
2
3
-
2I
-
+S4O
2
6
-
) 关注湖北升学通获取最新消息
步骤 平行滴定 次 平均消耗 溶液V
4: 3 , Na2S2O3 mL。
滴定至终点时 溶液的颜色变化为
(5) , 。
加入碘化钾后 发生的离子反应方程式为
2+
(6) Cu 。
x与y的比为 用m c V表示
(7) ( 、 、 ) 。
化学试卷 第 页 共 页
5 ( 8 )关注湖北升学通获取最新消息
分
17.(14 )
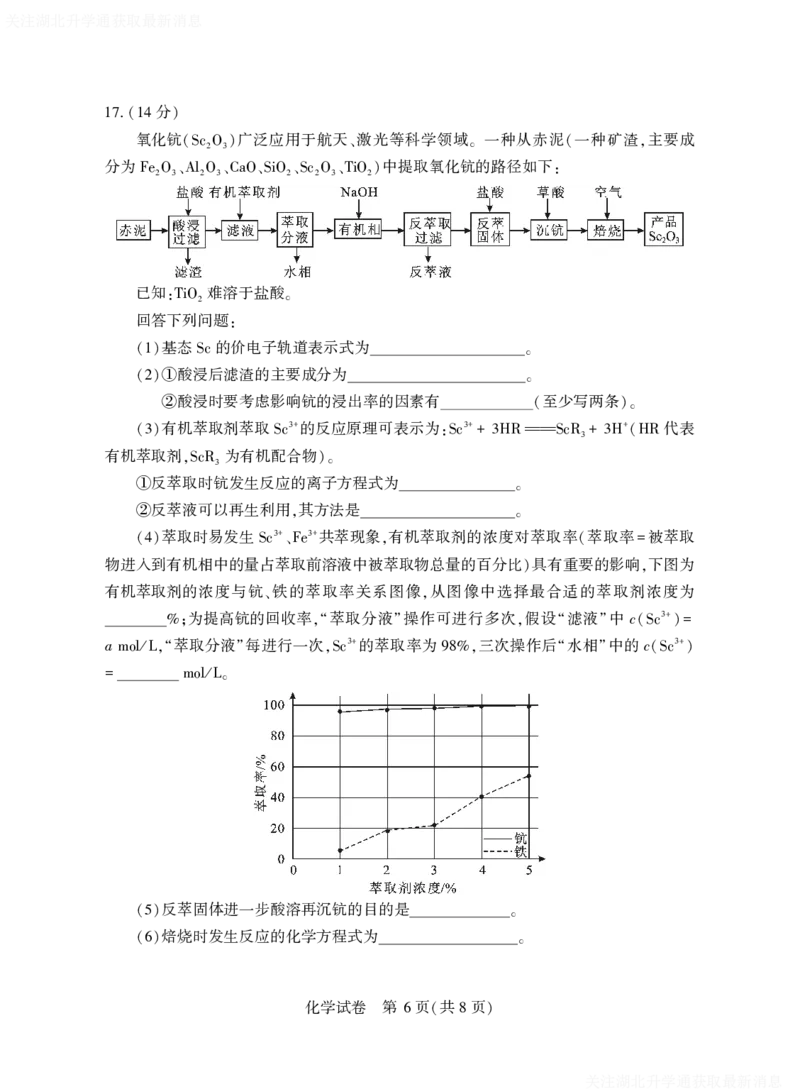
氧化钪 广泛应用于航天 激光等科学领域 一种从赤泥 一种矿渣 主要成
(Sc2O3) 、 。 ( ,
分为 中提取氧化钪的路径如下
Fe2O3、Al2O3、CaO、SiO2、Sc2O3、TiO2) :
已知 难溶于盐酸
:TiO2 。
回答下列问题
:
基态 的价电子轨道表示式为
(1) Sc 。
酸浸后滤渣的主要成分为
(2)① 。
酸浸时要考虑影响钪的浸出率的因素有 至少写两条
② ( )。
有机萃取剂萃取 的反应原理可表示为 代表
(3) Sc
3+
:Sc
3+
+ 3HRScR3 + 3H
+
(HR
有机萃取剂 为有机配合物
,ScR3 )。
反萃取时钪发生反应的离子方程式为
① 。
反萃液可以再生利用 其方法是
② , 。
萃取时易发生 共萃现象 有机萃取剂的浓度对萃取率 萃取率 被萃取
3+ 3+
(4) Sc 、Fe , ( =
物进入到有机相中的量占萃取前溶液中被萃取物总量的百分比 具有重要的影响 下图为
) ,
有机萃取剂的浓度与钪 铁的萃取率关系图像 从图像中选择最合适的萃取剂浓度为
、 ,
为提高钪的回收率 萃取分液 操作可进行多次 假设 滤液 中 c 3+
%; ,“ ” , “ ” (Sc )=
a 萃取分液 每进行一次 3+ 的萃取率为 三次操作后 水相 中的 c 3+
mol/L,“ ” ,Sc 98%, “ ” (Sc )
= mol/L。
反萃固体进一步酸溶再沉钪的目的是
(5) 。
焙烧时发生反应的化学方程式为
(6) 。
化学试卷 第 页 共 页
6 ( 8 )
关注湖北升学通获取最新消息关注湖北升学通获取最新消息
分
18.(13 )
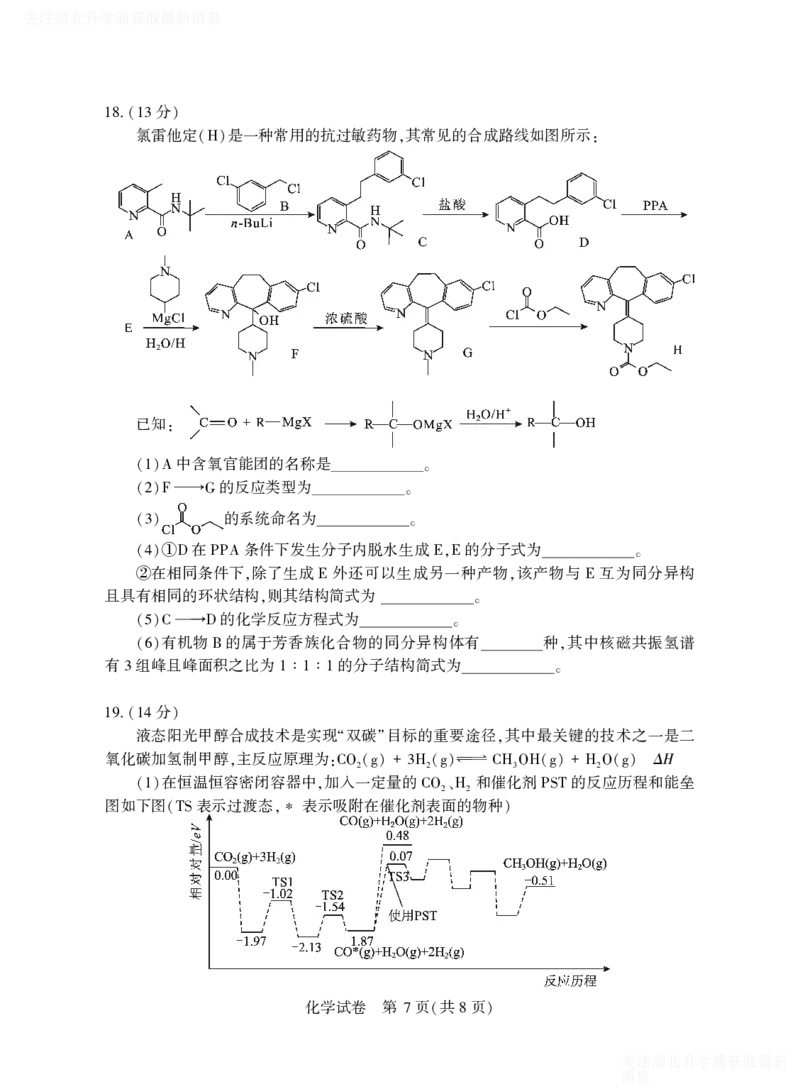
氯雷他定 是一种常用的抗过敏药物 其常见的合成路线如图所示
(H) , :
已知
:
中含氧官能团的名称是
(1)A 。
的反应类型为
(2)F →G 。
的系统命名为
(3) 。
在 条件下发生分子内脱水生成 的分子式为
(4)①D PPA E,E 。
在相同条件下 除了生成 外还可以生成另一种产物 该产物与 互为同分异构
② , E , E
且具有相同的环状结构 则其结构简式为
, 。
的化学反应方程式为
(5)C →D 。
有机物 的属于芳香族化合物的同分异构体有 种 其中核磁共振氢谱
(6) B ,
有 组峰且峰面积之比为 的分子结构简式为
3 1 ∶ 1 ∶ 1 。
分
19.(14 )
液态阳光甲醇合成技术是实现 双碳 目标的重要途径 其中最关键的技术之一是二
“ ” ,
氧化碳加氢制甲醇 主反应原理为 ΔH
, :CO2(g) + 3H2(g) CH3OH(g) + H2O(g)
在恒温恒容密闭容器中 加入一定量的 和催化剂 的反应历程和能垒
(1) , CO2、H2 PST
图如下图 表示过渡态 表示吸附在催化剂表面的物种
(TS ,∗ )
化学试卷 第 页 共 页
7 ( 8 )
关注湖北升学通获取最新
消息关注湖北升学通获取最新消息
① ΔH = kJ/mol( 保留两位小数 , 已知 1 eV ≈1.6×10 -19 J, N A≈6.02×10 23 /mol)
下列说法正确的是 填选项标号
② ( )
低温有利于主反应朝正方向自发进行
A.
是主要副产物 高选择性催化剂是提高制备效率的关键
B.CO ,
高温不利于甲醇生成 工业生产中应尽量保持低温
C. ,
反应中经历 的三个基元反应中起决速作用的是
D. TS1、TS2、TS3 TS3
某催化条件下的恒容体系 与 投料比和 的转化率 α 及
(2)2 MPa、280℃ ,H2 CO2 CO2
甲醇产率Φ的关系如下表 回答下列问题
。 :
n n
(H2)/ (CO2) 2 3 5 7
α
(CO2)/% 11.63 13.68 15.93 18.71
Φ
(CH3OH)/% 3.04 4.12 5.26 6.93
从表格中可以看出 该条件下随 与 投料比增大 的转化率和 产
① , H2 CO2 ,CO2 CH3OH
率均增大 所以有同学认为在实际生产中氢碳投料比越大越好 你是否认同这个观点并说
, ,
出你的理由
。
分析计算上述条件下 表格中甲醇产量最高的投料比为 填表格中数值
② , ( )。
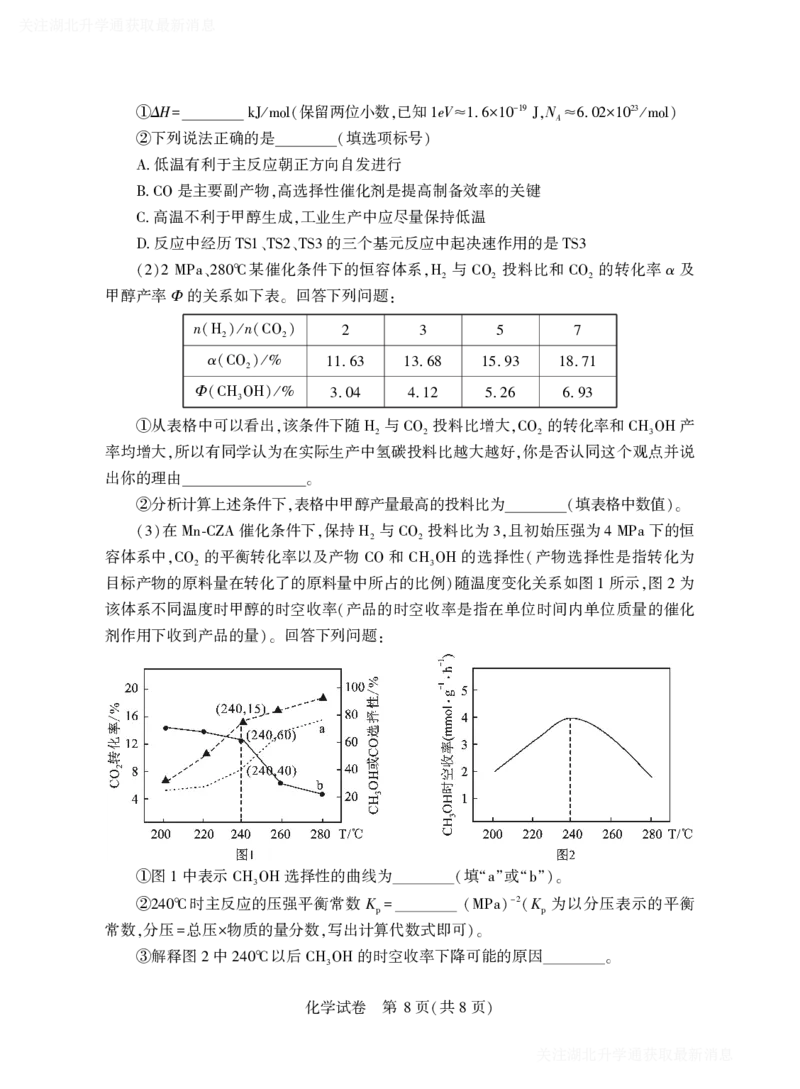
在 催化条件下 保持 与 投料比为 且初始压强为 下的恒
(3) Mn-CZA , H2 CO2 3, 4 MPa
容体系中 的平衡转化率以及产物 和 的选择性 产物选择性是指转化为
,CO2 CO CH3OH (
目标产物的原料量在转化了的原料量中所占的比例 随温度变化关系如图 所示 图 为
) 1 , 2
该体系不同温度时甲醇的时空收率 产品的时空收率是指在单位时间内单位质量的催化
(
剂作用下收到产品的量 回答下列问题
)。 :
图 中表示 选择性的曲线为 填 或
① 1 CH3OH ( “a” “b”)。
②240℃
时主反应的压强平衡常数 K
p = (MPa)
-2
(
K
p
为以分压表示的平衡
常数 分压 总压 物质的量分数 写出计算代数式即可
, = × , )。
解释图 中 以后 的时空收率下降可能的原因
③ 2 240℃ CH3OH 。
化学试卷 第 页 共 页
8 ( 8 )
关注湖北升学通获取最新消息