文档内容
2025 年湖北省八市高三(3 月)联考化学参考答案及评分细则
一、选择题:本题共有15小题,每小题3分,共45分。在每小题给出的四个选项中,只有
一项是符合题目要求的。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C A B A D D C D A B C D B B C
二、非选择题(本题共4个小题,共55分)
16.(14分)
(1)三颈烧瓶(1分)(三口烧瓶或三颈瓶也给分)
冷凝回流冰醋酸(2分)(缺少冰醋酸也给分,见错不给分)
(2)温度过低反应速率太慢,温度过高冰醋酸挥发太快(2分)
(不全给1分,见错不给分)
(3)防止滤液冷却结晶,减少产品损失(2分)(合理即给分,见错不给分)
(4)抑制醋酸铜水解,提高产品纯度和产率(2分)(合理即给分,见错不给分)
(5)蓝色变无色(1分)(有半分钟内溶液颜色不再变化也给分)
(6)2Cu2++4I-===I +2CuI↓(2分)
2
(无沉淀符号扣1分,写错或未配平不给分)
62cV 125m
(7) 或 或 (2分)(见错不给分)
125m49cV
17.(14分)
(1) (1分)(见错不给分)
(2)①SiO 、TiO (1分)(漏写或多写、写错均不给分)
2 2
②反应温度、酸的浓度、接触面积(或颗粒大小)、固液比、浸取时间等(2分)
(任意两个均给2分,一个给1分,写错不给分)
(3)①ScR +3OH-===Sc(OH) ↓+3R-(2分)
3 3
(无沉淀符号扣1分,写错或未配平不给分)
②向反萃液中加入适量的酸后分液(1分)(写盐酸或硫酸均给分,无分液也给分)
(4)1(1分) 8×10-6a(2分)(见错不给分)
(5)进一步分离杂质(铁),提高产品纯度(2分)(合理即给分)
(6)2Sc (C O ) +3O 2Sc O +12CO (2分)
2 2 4 3 2 2 3 2
1(高温条件也给分,没有反应条件扣1分,写错、没有配平均不给分)
18.(13分)
(1)酰胺基(1分)(写酰胺键或肽键均不给分,错别字不给分)
(2)消去反应(1分)(只写消去或写错均不给分)
(3)氯甲酸乙酯(1分)(一氯甲酸乙酯也给分,见错不给分)
(4)①C H NOCl(2分)(见错不给分,不考虑N、O、Cl顺序)
14 10
② (2分)(见错不给分)
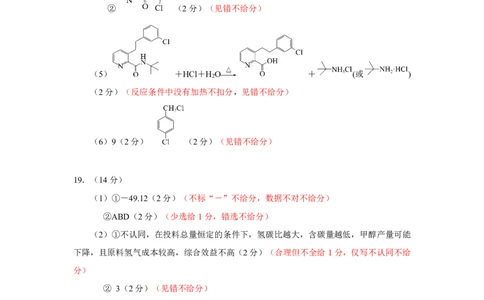
(5) +HCl+H O + (或 )
2
(2分)(反应条件中没有加热不扣分,见错不给分)
(6)9(2分) (2分)(见错不给分)
19.(14分)
(1)①-49.12(2分)(不标“-”不给分,数据不对不给分)
②ABD(2分)(少选给1分,错选不给分)
(2)①不认同,在投料总量恒定的条件下,氢碳比越大,含碳量越低,甲醇产量可能
下降,且原料氢气成本较高,综合效益不高(2分)(合理但不全给1分,仅写不认同不给
分)
② 3(2分)(见错不给分)
(3)① b(2分)(见错不给分)
② (2分)(2.67无小括号也给分,见错不给分)
③ 升温平衡逆向移动,温度过高还会造成催化剂选择性或活性下降(2分)
(考虑催化剂因素不考虑平衡移动也给2分,只考虑平衡移动给1分)
21解析 血液透析属于胶体的渗析,是物理变化。
2解析 聚氯乙烯中添加的塑化剂对人体有害。
3解析 A项,VSEPR还包括S的一对孤对电子,C项,每个Cl原子外还有3对未成键的
电子,D项,Fe2+先失去的是最外层的2个电子,第3层还有14个电子。
4解析 B项,滴定终点为CH COONa,水解显碱性,故选择在碱性条件下变色的指示剂酚
3
酞,C项,乙炔也能被酸性KMnO 氧化,D项,NaClO溶液具有漂白性,会使pH试纸褪
4
色,可使用pH计测量。
5解析 D项,Si为+4价,O为-2价,离子符号应为Si O 6-。
2 7
6解析 A项,共有羧基,酯基,(酚)羟基,酰胺基4种含氧官能团,B项,乙酰水杨酸中
有羧基,能与NaHCO 溶液反应放出CO 气体,C项,乙酰水杨酸和乙酰氨基酚都有酸性,
3 2
对肠胃有刺激性,合成贝诺酯可以消除药物的酸性,D项,贝诺酯水解后生成1mol
(消耗2molNaOH)、2molCH COOH(消耗2molNaOH)和1mol
3
(消耗1molNaOH),共消耗5molNaOH。
7解析 C项,产物中的FeS能溶于强酸,离子方程式为2Fe3++H S===2Fe2++S↓+2H+。
2
8解析 D项,金刚石和C 中均有共价键,金刚石的硬度与共价键有关,而C 与范德华
60 60
力有关。
9解析 根据题干信息,可推测X、Y、Z和W分别为Ca、Al、Si和N。A项,Si的氧化
物不能作半导体材料,而是其单质Si,B项,NH 的价层电子对数是3+1=4,故分子构型
3
为三角锥形,C项,氯化钙可以用作融雪剂的主要原因包括其吸湿性、降低水的冰点以及溶
解过程中放热等特性,D项,Al O 的离子键的成份只有41%,按共价晶体处理。
2 3
10解析 分析图像,N侧H 中H元素化合价升高,失电子,故M侧得电子,化合价降低,
2
另外,题干中有CO 转化为HCO-,故应有O 参与反应,反应方程式为4CO +O +2H O
2 3 2 2 2 2
+4e-===4HCO-,HCO-再通过阴离子交换膜进入N侧,反应方程式为H +2HCO--2e-===
3 3 2 3
2H O+2CO ,C项,未说明CO 处于标况下。
2 2 2
11解析 C项,没有将储氢后的氢原子算在晶胞中计算。
12解析 A项,a电极Fe元素化合价降低,得电子,为阴极,与电源负极相连,B项,淡
化池中,Na+通过离子交换膜1向左移动,故1为阳膜,SO2-通过离子交换膜2向右移动,
4
故2为阴膜,双极膜中的H+向左移动,OH-向右移动,浓缩池2右边池中的Na+通过离子
交换膜3向左移动,故3为阳膜,故浓缩池1中产生的是H SO ,浓缩池2中产生的是NaOH。
2 4
13解析 A项,芳香烃只含碳氢元素,B项,(b)结构比(a)结构少了2个H原子,故M为
+2价,C项,由于形成了16中心的共轭结构,故N原子都为sp2杂化,D项,酞菁(a)分
子中,8个C各提供1个电子,6个不带H的N原子各提供1个电子,2个带H的N原子
各提供2个电子,共18个电子。
14解析 A项,银镜反应需要水浴加热,不能加热煮沸,C项,反应的本质是Fe3++3SCN
- Fe(SCN) ,与KCl的浓度无关,D项,若发生的是消去反应也有浅黄色沉淀,并不能
3
3说明发生的是水解反应。
15解析 A项,取X=0时,三条线在Y轴上的截距分别约为0.7,1.3和2.8,故K 分别为
a
10-0.7,10-1.3和10-2.8,由于Cl原子越多,吸电子效应越大,其对应的羧酸酸性越强,故Ⅰ,
Ⅱ和Ⅲ分别对应的X= 、 和 ,
C项,滴加至pH=7时,较强酸消耗的n(NaOH)更多,即CCl COOH,D项,完全中和时
3
生成三种等浓度的钠盐,分别为CH ClCOONa、CHCl COONa和CCl COONa,阴离子水解
2 2 3
程度逐渐减小,剩余阴离子浓度逐渐增大。
16解析 (7)
列式可得结果。
17解析 (4)每萃取1次剩余2%,萃取3次为(2%)3 × a=8×10-6a。
18解析 (6) 、 (另一个Cl有邻间对3种)、 (ABC模型有6种),
共有10种,去掉B自身,还有9种。
19解析 (1)ΔH=-0.51×6.02×1023/mol×1.6×10-19J×10-3kJ/J=-49.12kJ·mol-1
(2)②在恒压恒容条件下,相当于起始加入的量相等,可以按1mol来处理,若氢碳比为2时,
相当于CO 有1/3mol,CHOH的产量为1/3mol×3.04%≈1.01×10-2mol,当氢碳比为3、5
2 3
和7时按上述算法,可得当氢碳比为3时,其产量最高。
(3)H 与CO 投料比为3,可设H 为3mol,CO 为1mol,起始压强为4Mpa,相当于每
2 2 2 2
1mol气体所占分压为1Mpa。根据图中数据可知,CO 的转化率为15%,CH OH的选择性
2 3
为60%,其生成量为1×15%×60%=0.09mol,CO的生成量为1×15%×40%=0.06mol。
n(CO ) =1-0.09-0.06=0.85mol,n(H ) =3-0.27-0.06=2.67mol,n(CH OH) =0.09mol,
2 平 2 平 3 平
n(H O) =0.09+0.06=0.15mol,代入平衡表达式中即可。
2 平
4