文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:75 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第 1 章-第 2 章第 2 节(人教版 2019 选择性必修 1)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 O-16
第Ⅰ卷(选择题 共 42 分)
一、选择题:本题共 14 个小题,每小题 3 分,共 42 分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.“能源”是人们生活中不可或缺的一部分,下列属于利用化学能与热能的转化的过程是
过程
选项 A.太阳能热水器烧水 B.燃油汽车行驶
过程
选项 C.锂电池供电 D.水力发电
A.A B.B C.C D.D
【答案】B
【详解】A.太阳能烧水是将太阳能转换为热能,不属于化学能与热能的转化,A 错误;
B.燃油汽车行驶是化学能转化为热能,热能再转化为动能,属于化学能与热能的转化,B 正确;
C.锂电池是一种以锂金属或锂合金为负极材料,使用非水电解质溶液的二次电池,属于化学能与电能
/的转化,C 错误;
D.水力发电是将水能转换为电能,不属于化学能与热能的转化,D 错误;
故选 B。
2.下列关于能量变化的说法正确的是
A.“冰,水为之,而寒于水”说明相同质量的水和冰相比较,冰的能量高
B.已知,C(s,石墨)=C(s,金刚石)△H>0,则金刚石比石墨稳定
C.灼热的碳与 CO 反应既是吸热反应,又是氧化还原反应
2
D.放热反应都不需要加热,吸热反应都需要加热才能发生
【答案】C
【详解】A.冰融化为水需要吸热,故水的能量比冰高,A 错误;
B.由 C(s,石墨)=C(s,金刚石)△H>0 可知,石墨转化为金刚石需要吸热,故金刚石的能量高,能量越
高的物质越不稳定,B 错误;
C.C+CO 2CO 是吸热反应,反应中 C 的化合价发生变化,是氧化还原反应,C 正确;
2
D.有的放热反应刚开始也需要加热反应才能进行,如 2Na+O Na O ,有的吸热反应常温下也能发生,
2 2 2
如 NH Cl 晶体与 Ba(OH) ·8H O 晶体的反应,D 错误;
4 2 2
故选 C。
3.下列事实不能用勒夏特列原理解释的是
A.实验室新制氯水经光照后颜色变浅
B.夏天打开冰镇可乐瓶盖时产生大量泡沫
C.反应 2HI(g) H (g)+I (g)达到平衡后,缩小容器体积加压,气体颜色加深
2 2
D.合成氨工业
⇌
中采用高压有利于提高原料的平衡转化率
【答案】C
【详解】A.新制的氯水在光照条件下颜色变浅,由于次氯酸光照分解生成盐酸和氧气,次氯酸的浓度
减小,氯气与水反应平衡正向移动,颜色变浅,能用勒夏特列原理,A 不符合题意;
B.可乐瓶中存在可逆过程 CO
2
(g)+H
2
O⇌H
2
CO
3
(aq),打开可乐瓶盖后,减小压强,该平衡逆向移动,观
察到有大量泡沫逸出,能用勒夏特列原理解释,B 不符合题意;
C.反应 2HI(g)⇌H
2
(g)+I
2
(g)达到平衡后,缩小容器体积加压后颜色变深,浓度增大,但平衡没有移动,
不能用勒夏特列原理,C 符合题意;
D.工业上合成氨存在平衡 ,是气体分子数减小的反应,增大压强,平衡正向移动,
可以提高氨气的产量,能用勒夏特列原理解释,D 不符合题意;
/答案为 C。
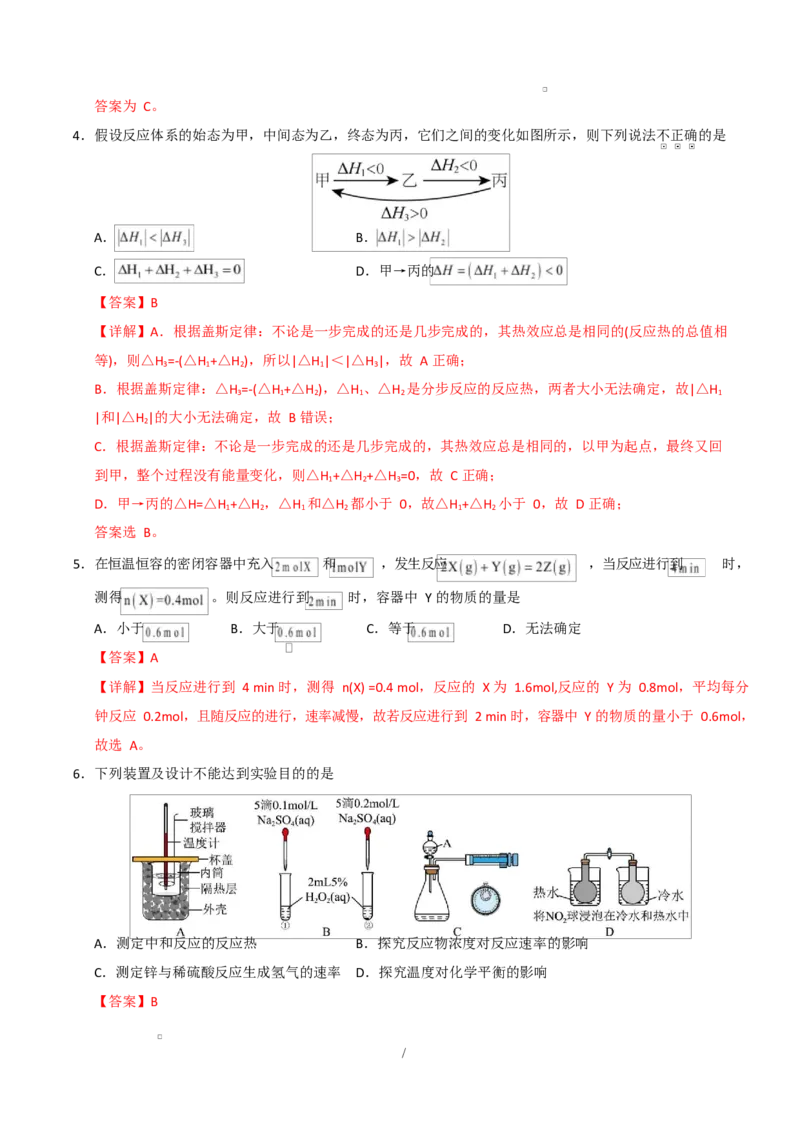
4.假设反应体系的始态为甲,中间态为乙,终态为丙,它们之间的变化如图所示,则下列说法不正确的是
A. B.
C. D.甲→丙的
【答案】B
【详解】A.根据盖斯定律:不论是一步完成的还是几步完成的,其热效应总是相同的(反应热的总值相
等),则△H =-(△H +△H ),所以|△H |<|△H |,故 A 正确;
3 1 2 1 3
B.根据盖斯定律:△H =-(△H +△H ),△H 、△H 是分步反应的反应热,两者大小无法确定,故|△H
3 1 2 1 2 1
|和|△H |的大小无法确定,故 B 错误;
2
C.根据盖斯定律:不论是一步完成的还是几步完成的,其热效应总是相同的,以甲为起点,最终又回
到甲,整个过程没有能量变化,则△H +△H +△H =0,故 C 正确;
1 2 3
D.甲→丙的△H=△H +△H ,△H 和△H 都小于 0,故△H +△H 小于 0,故 D 正确;
1 2 1 2 1 2
答案选 B。
5.在恒温恒容的密闭容器中充入 和 ,发生反应 ,当反应进行到 时,
测得 。则反应进行到 时,容器中 Y 的物质的量是
A.小于 B.大于 C.等于 D.无法确定
【答案】A
【详解】当反应进行到 4 min 时,测得 n(X) =0.4 mol,反应的 X 为 1.6mol,反应的 Y 为 0.8mol,平均每分
钟反应 0.2mol,且随反应的进行,速率减慢,故若反应进行到 2 min 时,容器中 Y 的物质的量小于 0.6mol,
故选 A。
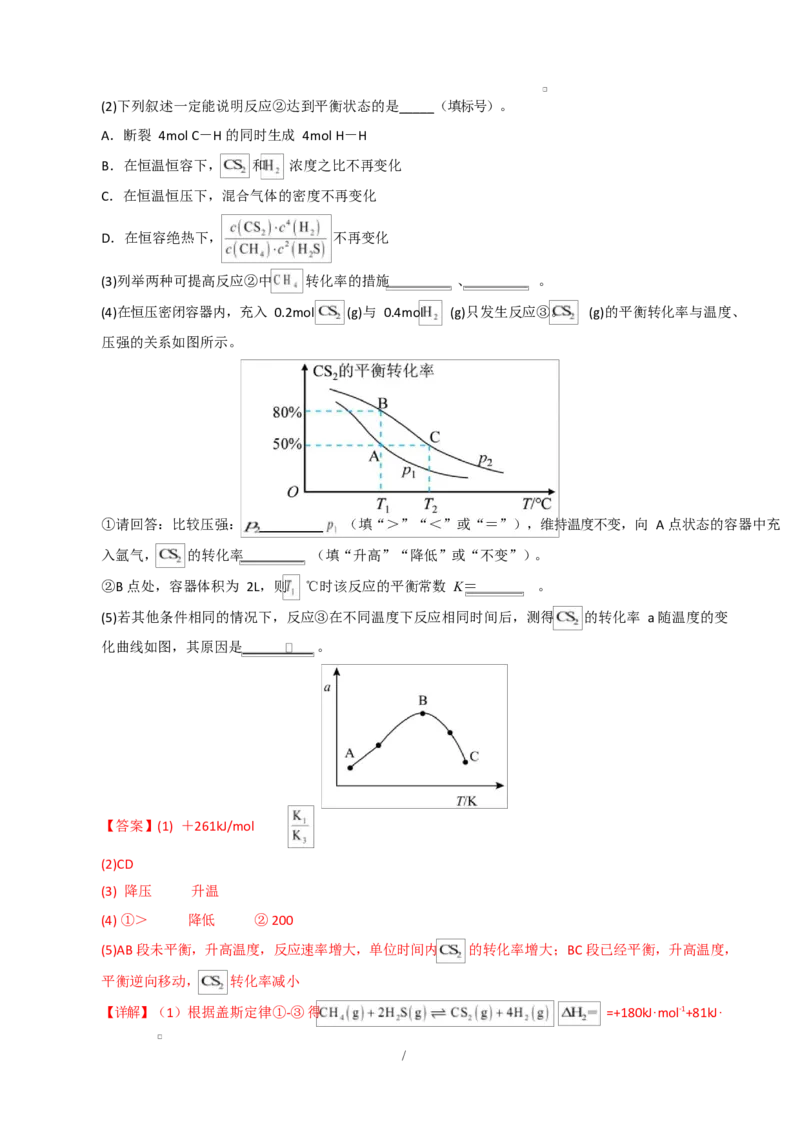
6.下列装置及设计不能达到实验目的的是
A.测定中和反应的反应热 B.探究反应物浓度对反应速率的影响
C.测定锌与稀硫酸反应生成氢气的速率 D.探究温度对化学平衡的影响
【答案】B
/【详解】A.此装置中,内外桶中间有隔热层,内外桶口与杯盖相平,吻合度高,有温度计、环形玻璃
搅拌棒,则装置的保温效果好,最高温度的测定准确,A 正确;
B.实验通过改变 Na SO 的浓度探究浓度对反应速率的影响,若 Na SO 是反应物则正确,若 Na SO 作
2 4 2 4 2 4
为催化剂或反应无关的物质,其浓度变化不会影响反应速率,B 错误;
C.锌与稀硫酸反应,测定相同时间内产生的氢气体积,或者产生相同体积氢气所用的时间,可测定平
均反应速率,C 正确;
D.NO 呈红棕色,N O 呈无色,依据热水中圆底烧瓶内气体的颜色与冷水中圆底烧瓶内气体的颜色的
2 2 4
深浅,可确定平衡移动的方向,从而确定温度对化学平衡的影响,D 正确;
故选 B。
7.国家主席习近平在第七十五届联合国大会上庄严宣布,中国将力争 2030 年前实现碳达峰、2060 年前实
现碳中和。恒温恒容时,按体积比 1:1 向密闭容器中投入 CO 与 ,发生反应:
。下列不能判断反应达到平衡的是
A.平均相对分子质量不再变化 B.单位时间生成 与 CO 的体积相等
C.CO 体积分数不再变化 D.混合气体密度不再变化
【答案】D
【详解】A.反应前后均为气体,质量守恒,平均相对分子质量 ,即 不变,总物质的量从
反应前的 3mol(1mol CO + 2mol )变为 1mol (假设完全反应), 变,平均相对分子质
量也会变化,当平均相对分子质量不再变化时,反应达到平衡,A 正确;
B.根据方程式可知: ,平衡时正、逆反应速率相等,生成 CH₃OH 的速率(正反应)等
于生成 CO 的速率(逆反应),B 正确;
C.CO 的物质的量随反应减少,气体总物质的量也减少。达平衡时 CO 的物质的量与总气体物质的量均
稳定, 体积分数不再变化即达到平衡,C 正确;
D. ,反应前后总质量守恒(均为气体,质量不变),且体积恒容,因此密度始终不变,D
不能判断反应达到平衡;
故选 D。
8.反应物(S)转化为产物(P)的能量与反应历程的关系如图所示。下列有关说法错误的是
/A.该反应为放热反应 B.增大 X 的用量,反应历程不变
C.X 提高了反应物(S)的转化率 D. 为该反应的决速步骤
【答案】C
【分析】从图中可以看出,该反应反应物总能量大于生成物总能量,为放热反应;反应前后 X 的性质未
变,属于催化剂,改变了反应的途径,降低了反应的活化能,增大反应速率;
【详解】A.从图中可以看出,该反应反应物总能量大于生成物总能量,为放热反应,故 A 正确;
B.催化剂可以降低活化能,提高反应速率,与用量多少无关,增大用量,反应历程不变,故 B 正确;
C.X 为催化剂,催化剂只能改变反应速率,不能提高转化率,故 C 错误;
D.如图,该反应分为三步进行,其中 的活化能最大,反应速率最慢,为该反应的决速步
骤,故 D 正确;
故选 C。
9.在恒容密闭容器中,加入 1mol CO 和 1mol 发生反应: ,一定温
度下,达到平衡时测得 ,下列说法不正确的是
A.在该温度下,反应的平衡常数
B.在平衡后的容器中,继续加入 1mol CO,重新达到平衡后,所得平衡常数增大
C.CO 的平衡转化率为 50%
D.平衡时 为 0.5mol
【答案】B
【详解】A.设容器的体积为 V,由题干的数据可知,平衡时各种组分的物质的量都为 0.5mol,K=
= =1,故 A 正确;
B.平衡常数只与温度有关,温度不改变,平衡常数不变,故 B 错误;
C.由题干可知,消耗的 CO 为 0.5mol,CO 的平衡转化率为 =50%,故 C 正确;
/D.达到平衡时测得 ,消耗的 H O 为 0.5mol,故平衡时 为 0.5mol,故 D 正确;
2
答案选 B。
10.下列关于有效碰撞理论与影响速率因素之间关系正确的是
A.增大反应物浓度,可以提高活化分子百分数,从而提高反应速率
B.加入催化剂可以降低活化能,活化分子百分数虽然没变,但可以加快反应速率
C.升高温度,反应物分子的能量增加,增加了活化分子的百分数,从而提高反应速率
D.只要增大压强,就可提高单位体积内活化分子数,从而提高反应速率
【答案】C
【详解】A.增大反应物浓度,增大单位体积内活化分子个数,活化分子百分数不变,故 A 错误;
B.催化剂能降低反应所需活化能,增大活化分子百分数,增大化学反应速率,不改变平衡移动,反应
物转化率不变,故 B 错误;
C.升高温度,活化分子百分数增大,则化学反应速率加快,故 C 正确;
D.对于气体反应来说,压缩体积增大压强,增大单位体积内活化分子个数,活化分子有效碰撞几率增
大,反应速率加快,对固体反应来说,增大压强无影响,故 D 错误;
故选:C。
11.在密闭容器中发生如下反应: 。其他条件不变时,改变某一条件对上述反应的
影响,得到下列图像(图中 p 表示压强,T 表示温度,n 表示物质的量,α表示平衡转化率)。下列分析正
确的是
A.如图 1 反应: 此反应的ΔH>0
B.如图 1 反应:若 p >p ,则 a+bT
1 2
D.如图 3 反应:t 时刻改变的条件可能是加入了催化剂或增大了压强
1
【答案】D
【详解】A.由图 1 可知,P 时,升高温度,A 的转化率降低,平衡逆向移动,则正反应为放热反应,
1
正反应ΔH<0,A 错误;
B.由图 1 可知,若 p >p ,向 T 轴作垂线,温度相等,增大压强,则 A 的转化率升高,平衡正向移动,
1 2
说明正向是气体物质的量减小的反应,则 a+b>c,B 错误;
/C.由图 2 可知,T P ,维持温度不变,向 A 点状态的容器中充入氩气,
2 2 1
容器体积增大,相当于减压,平衡逆向移动,CS 的转化率降低;
2
②B 点处,CS 的平衡转化率为 80%,列出三段式:
2
容器体积为 2L,则 T ℃时该反应的平衡常数 K= =200。
1
(5)AB 段未平衡,升高温度,反应速率增大,单位时间内 的转化率增大;BC 段已经平衡,升高
温度,平衡逆向移动, 转化率减小。
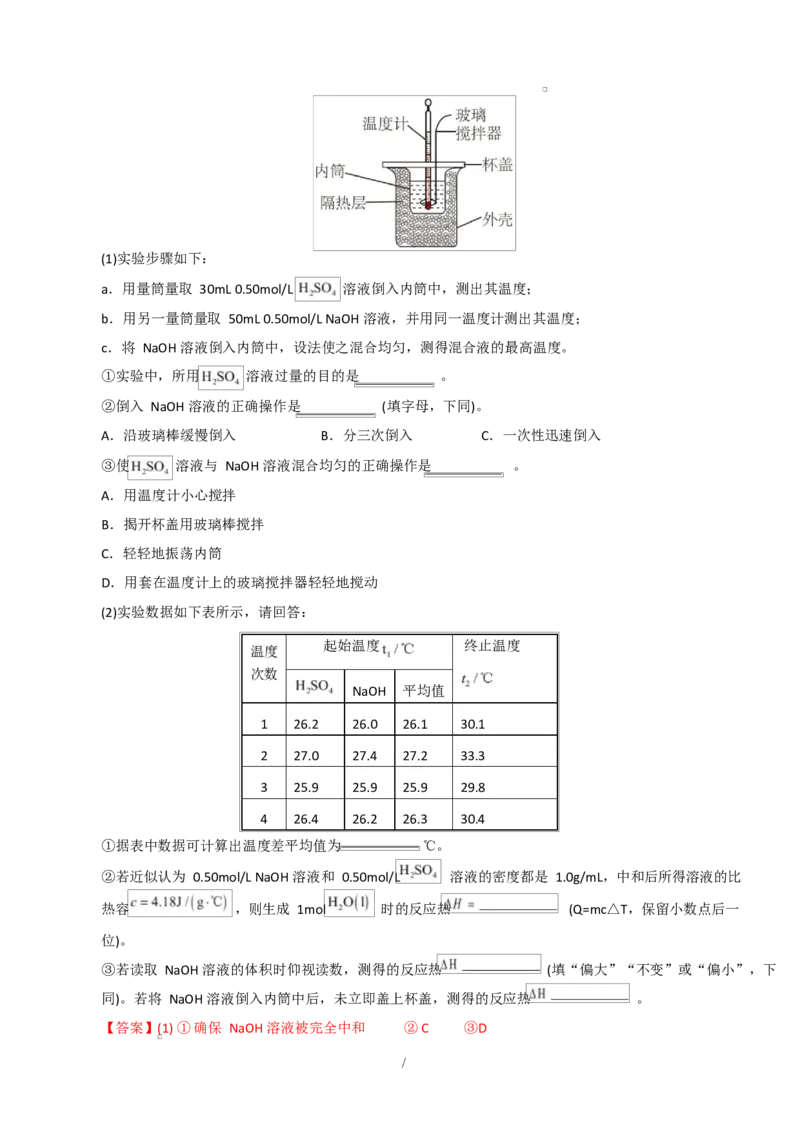
16.(14 分)某实验小组用 0.50mol/L NaOH 溶液和 0.50mol/L 溶液进行反应热的测定,实验装置如
右图所示。
/(1)实验步骤如下:
a.用量筒量取 30mL 0.50mol/L 溶液倒入内筒中,测出其温度;
b.用另一量筒量取 50mL 0.50mol/L NaOH 溶液,并用同一温度计测出其温度;
c.将 NaOH 溶液倒入内筒中,设法使之混合均匀,测得混合液的最高温度。
①实验中,所用 溶液过量的目的是 。
②倒入 NaOH 溶液的正确操作是 (填字母,下同)。
A.沿玻璃棒缓慢倒入 B.分三次倒入 C.一次性迅速倒入
③使 溶液与 NaOH 溶液混合均匀的正确操作是 。
A.用温度计小心搅拌
B.揭开杯盖用玻璃棒搅拌
C.轻轻地振荡内筒
D.用套在温度计上的玻璃搅拌器轻轻地搅动
(2)实验数据如下表所示,请回答:
起始温度 终止温度
温度
次数
NaOH 平均值
1 26.2 26.0 26.1 30.1
2 27.0 27.4 27.2 33.3
3 25.9 25.9 25.9 29.8
4 26.4 26.2 26.3 30.4
①据表中数据可计算出温度差平均值为 ℃。
②若近似认为 0.50mol/L NaOH 溶液和 0.50mol/L 溶液的密度都是 1.0g/mL,中和后所得溶液的比
热容 ,则生成 1mol 时的反应热 (Q=mc△T,保留小数点后一
位)。
③若读取 NaOH 溶液的体积时仰视读数,测得的反应热 (填“偏大”“不变”或“偏小”,下
同)。若将 NaOH 溶液倒入内筒中后,未立即盖上杯盖,测得的反应热 。
【答案】(1) ①确保 NaOH 溶液被完全中和 ②C ③D
/(2) ①4.0 ② ③偏小 偏大
【分析】中和热的测定实验,一种溶液的浓度稍过量,并且混合时两种溶液快速倒入,并用玻璃搅拌
器搅拌混合均匀,使其充分反应,不断地读取数据,当温度下降时停止读数。
【详解】(1)①实验中,所用 溶液过量可以保证氢氧化钠完全反应,故答案为:确保 NaOH 溶
液被完全中和;
②倒入 NaOH 溶液的正确操作是一次迅速倒入,使其充分反应,避免分次倒入,有热量的损失,故答
案为:C;
③A.不能用温度计小心搅拌,用环形玻璃搅拌器搅拌,故 A 错误;
B.不能揭开杯盖用玻璃棒搅拌,应盖上硬纸板搅拌,故 B 错误;
C.不能轻轻地振荡内筒,应用环形玻璃搅拌棒搅拌,故 C 错误;
D.用套在温度计上的玻璃搅拌器上下轻轻地搅动,故 D 正确;
综上所述,答案为:D;
(2)①4 次实验的温度差分别为:4℃,6.1℃,3.9℃,4.1℃,因此实验 2 中的数据是无效的,应该舍
去,所以温度差的平均值为(4℃+3.9℃+4.1℃)÷3=4℃;
②50mL 0.50mol/L 氢氧化钠与 30mL0.50mol/L 硫酸溶液进行中和反应,硫酸是过量的,则生成水的物质
的量为 0.05L×0.50mol/L=0.025mol,溶液的质量为:80ml×1g/ml=80g,温度变化的平均值为△T=4℃,则
生成 0.025mol 水放出的热量为 Q=mc△T=80g×4.18J/(g·℃)×4.0℃=1337.6J,即 1.3376kJ,所以实验测得
的中和热 ;故答案为−53.5kJ/mol;
③若读取 NaOH 溶液的体积时仰视读数,则其体积偏大,反应放出的热多,测得的反应热 偏小;若
将 NaOH 溶液倒入内筒中后,未立即盖上杯盖,会造成热量流失,测得的反应热 偏大。
17.(15 分)等质量的铁与过量的盐酸在不同的实验条件下进行反应。
组别 对应曲线 反应温度/℃ 铁的状态
1 35 粉末状
2 3.2 35 粉末状
3 3.2 35 块状
4 35 块状
测得在不同时间(t)内产生气体体积(V)的数据如图所示。
/回答下列问题:
(1)盐酸 (填“是电解质”“是非电解质”或“既不是电解质也不是非电解质”),原因为 。
(2)该反应的化学方程式为 。
(3)结合图像,由第 1 组和第 2 组实验数据可知,第 1 组实验中 (填“>”“<”或“=”)3.2,判断的理
由为 。
(4)在上述四组实验中(等质量的铁粉,不考虑盐酸的挥发):
①消耗盐酸体积最多的是第 (填“1”“2”“3”或“4”)组,原因为 。
②四组实验中,主要讨论 和 对反应速率的影响。
【答案】(1) 既不是电解质也不是非电解质 盐酸属于混合物,电解质为化合物
(2)
(3) > 接触面积和物质的状态均相同,图中可判断出第 1 组反应速率大于第 2 组反应速率,故
(4) ①4 生成氢气的体积相同,接触面积和物质的状态均相同,第 3 组反应速率大于第 4 组反应速
率,故 ,则消耗盐酸体积最多 ②浓度 接触面积
【详解】(1)盐酸属于混合物,电解质为化合物,所以盐酸既不是电解质也不是非电解质。
(2)铁和盐酸反应生成氯化亚铁和氢气,该反应的化学方程式为 。
(3)根据对比实验的单一变量原则,结合图像第 1 组速率快于第 2 组,且两组数据其他条件相同,故
第 1 组实验中 >3.2,判断的理由为接触面积和物质的状态均相同,图中可判断出第 1 组反应速率大于
第 2 组反应速率,故 。
(4)①四组数据生成相同体积的氢气,消耗 HCl 的物质的量相同,故消耗盐酸体积最多的是第 4 组,
原因为生成氢气的体积相同,接触面积和物质的状态均相同,第 3 组反应速率大于第 4 组反应速率,
故 ,则消耗盐酸体积最多。
②结合四组的实验数据,1、2 和 3、4 组的浓度不同,2、3 组的接触面积不同,故四组实验中,主要
讨论浓度和接触面积对反应速率的影响。
18.(14 分)含氮物质在自然界中有着广泛的分布和形态。
(1)已知: 反应 I. ;
/反应Ⅱ. 。
则反应 2NO(g)+O
2
(g)⇌2NO
2
(g) 。
(2)若反应 2NO
2
(g)⇌N
2
O
4
(g)在体积为 1L 的恒容密闭容器中进行,保持温度不变,达到平衡后,向反应
容器中再充入少量 NO ,重新达到平衡后和原平衡相比,NO 的体积分数 (填“增大”、“减小”或“不
2 2
变”)。
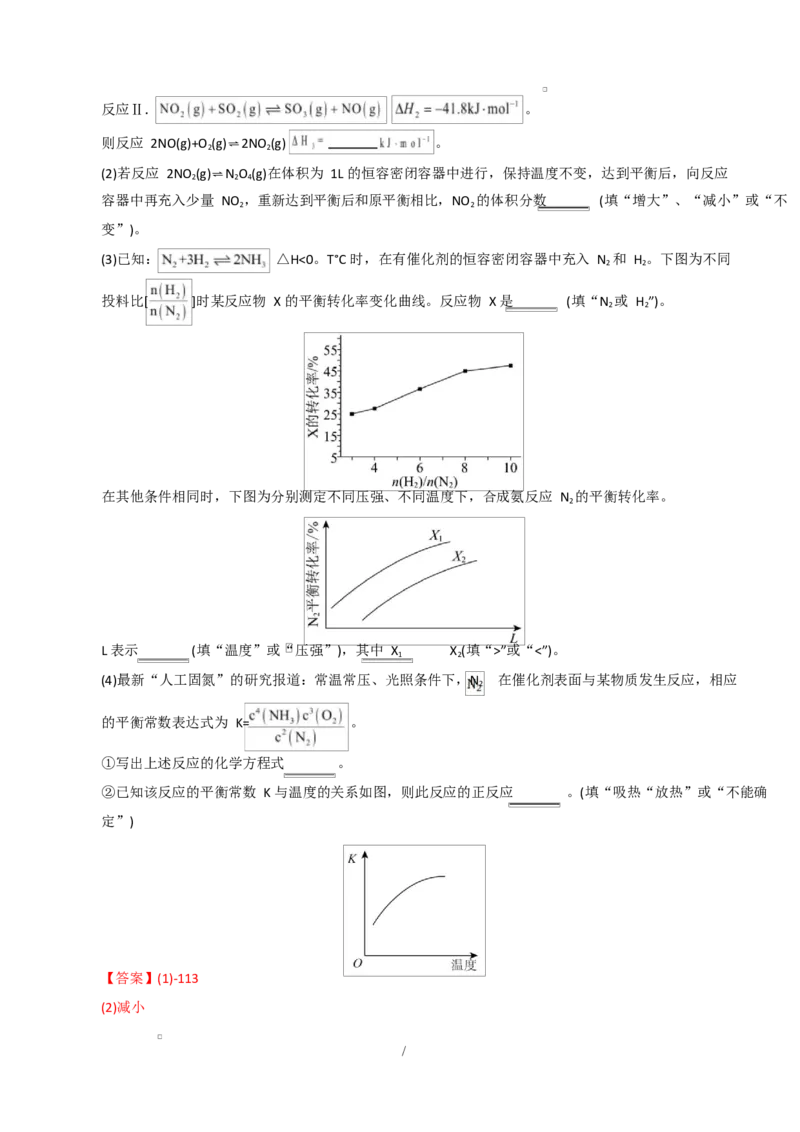
(3)已知: △H<0。T°C 时,在有催化剂的恒容密闭容器中充入 N 和 H 。下图为不同
2 2
投料比[ ]时某反应物 X 的平衡转化率变化曲线。反应物 X 是 (填“N 或 H ”)。
2 2
在其他条件相同时,下图为分别测定不同压强、不同温度下,合成氨反应 N 的平衡转化率。
2
L 表示 (填“温度”或“压强”),其中 X X (填“>”或“<”)。
1 2
(4)最新“人工固氮”的研究报道:常温常压、光照条件下,N 在催化剂表面与某物质发生反应,相应
2
的平衡常数表达式为 K= 。
①写出上述反应的化学方程式 。
②已知该反应的平衡常数 K 与温度的关系如图,则此反应的正反应 。(填“吸热“放热”或“不能确
定”)
【答案】(1)-113
(2)减小
/(3) N 压强 <
2
(4) ①2N (g)+6H O(l) 4NH (g)+3O (g) ② 吸热
2 2 3 2
【详解】(1)根据盖⇌斯定律,反应 I-2×反应Ⅱ得反应 2NO(g)+O
2
(g)⇌2NO
2
(g)
;
(2)反应为气体分子数减小的反应,达到平衡后,向反应容器中再充入少量 NO ,相当于增大压强,
2
重新达到平衡后,在原平衡基础上平衡正向移动,则 NO 的体积分数减小;
2
(3)若增大氢气的投料,平衡正向移动,氢气自身的平衡转化率降低,促使氮气的平衡转化率升高,
所以反应物 X 表示 N ;
2
反应为气体分子数减小的放热反应;恒温增大压强,平衡正向移动;正反应放热,升高温度平衡逆向
移动;随 L 值增大,N 的平衡转化率增大,说明平衡正向移动,则 L 表示压强,X 表示温度,温度越高,
2
N 的平衡转化率越低,则 X