文档内容
2025-2026 学年高二化学上学期第一次月考卷
(考试时间:90 分钟 试卷满分:100 分)
注意事项:
1.本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准考证号
填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用 2B 铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:选择性必修一第一章(鲁科版)。
5.难度系数:0.65
6.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 S 32 Cl 35.5 Cu 64
第Ⅰ卷(选择题 共 54 分)
一、选择题:本题共 18 个小题,每小题 3 分,共 54 分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1.下列设备工作时,将化学能转化为热能的是
A B C D
太阳能集热器 锂离子电池 燃气灶 电风扇
A.A B.B C.C D.D
【答案】C
【详解】A.太阳能集热器工作时将光能转化为热能,A 不符合题意;
B.锂离子电池是化学电池,工作时将化学能转化为电能,B 不符合题意;
C.燃气灶工作时将化学能转化为热能,C 符合题意;
D.电风扇工作时将电能转化为机械能,D 不符合题意;
故选 C。
2.某化学反应由两步反应 A→B→C 构成,A、B、C 分别为三种物质,该反应中能量曲线如图所示,下列
叙述正确的是
/A.A→C 为放热反应,所以不需要任何条件
B.A 比 C 更稳定
C.破坏 B 中化学键吸收的能量低于形成 C 中新化学键释放的能量,所以 B→C 为放热反应
D.A→B 中化学能转化为热能
【答案】C
【详解】A.反应是吸热还是放热与反应条件无关,但反应的发生需要提供起始条件,A 错误;
B.根据图中信息,A 的总能量高于 C,能量越低越稳定,故 C 比 A 更稳定,B 错误;
C.由图可知 B 的总能量高于 C 的总能量,B→C 为放热反应,即破坏反应物 B 中化学键吸收能量要低
于形成 C 中新化学键时放出的能量,C 正确;
D.A→B 为吸热反应,可以看成是热能转化为化学能,D 错误;
故选 C。
3.热化学方程式 的意义是
A. 二氧化硫气体和 氧气反应生成 三氧化硫气体放出 热量
B. 二氧化硫气体和 氧气反应生成 三氧化硫气体放出 热量
C. 二氧化硫气体和 氧气反应生成 三氧化硫气体吸收 热量
D.上述说法都不正确
【答案】B
【详解】热化学方程式的ΔH 表示反应物完全转化为生成物时的能量变化,
表示 2mol SO (g)和 1mol O(g)完全生成 2mol SO (g)时放出
2 2 3
197kJ 的热量,故选 B。
4.一些烷烃的燃烧热如下表所示:
化合物 燃烧热ΔH/(kJ·mol-1) 化合物 燃烧热ΔH/(kJ·mol-1)
甲烷 -891.0 正丁烷 -2878.0
乙烷 -1560.8 异丁烷 -2869.6
丙烷 -2221.5 异戊烷 -3531.3
下列说法正确的是
A.正戊烷的燃烧热ΔH 大约是-3540kJ·mol-1
/B.热稳定性:正丁烷>异丁烷
C.乙烷完全燃烧的热化学方程式:2C H(g)+7O(g)=4CO (g)+6HO(g) ΔH=-1560.8kJ·mol-1
2 6 2 2 2
D.相同质量的烷烃,碳的质量分数越大,完全燃烧放出的热量越多
【答案】A
【详解】A.正戊烷和异戊烷互为同分异构体,由表格中正丁烷、异丁烷的燃烧热比较可知,互为同分
异构体的化合物,支链多的燃烧放出热量少,根据正丁烷和丙烷的燃烧热推断一个 基团对燃烧热的
贡献约为 ,故正戊烷的燃烧热约为
,与题中数据大约相等,A 正确;
B.正丁烷燃烧热绝对值大于异丁烷,说明正丁烷能量更高,稳定性更差,因此热稳定性:正丁烷<异丁
烷,B 错误;
C.燃烧热指的是 1 mol 物质完全燃烧,且生成液态水,则表示乙烷燃烧的热化学方程式为 C H(g)+
2 6
O(g)=2CO (g)+3HO(l) △H= -1560.8 kJ·mol-1,C 错误;
2 2 2
D.碳质量分数越大,氢含量越少,由于氢燃烧放热更多(如甲烷每克放热约 55.7 kJ/g,乙烷约 52.0 kJ/g),
碳质量分数大的烷烃单位质量放热更少,D 错误;
故选 A。
5.下列图示与对应的叙述不相符的是
A.(a)图可表示 Ba(OH) •8H O 与 NH Cl 反应的能量变化
2 2 4
B.通过(b)图可知石墨比金刚石稳定
C.由(c)图可知,若在密闭容器中加入 和 充分反应放出的热量为
D.由(d)图可知,A 与 C 的能量差为:
【答案】C
【详解】A.Ba(OH) •8H O 与 NH Cl 的反应为吸热反应,(a)图中反应物的总能量小于生成物的总能量,
2 2 4
表示的反应为吸热反应,则(a)图可表示 Ba(OH) •8H O 与 NH Cl 反应的能量变化,A 不符合题意;
2 2 4
B.物质具有的能量越低,稳定性越强,通过(b)图可知,石墨的能量低于金刚石的能量,则石墨比金刚
石稳定,B 不符合题意;
C.由(c)图可知,若反应过程中消耗了 1molO (g)和 2molSO (g),同时生成 2molSO (g),反应放热(a-b)
2 2 3
kJ,而 SO (g)与 O(g)的反应为可逆反应,当在密闭容器中加入 1molO (g)和 2molSO (g),充分反应后生
2 2 2 2
成的 SO (g)小于 2mol,所以放出的热量小于(a-b)kJ,C 符合题意;
3
/D.由(d)图可知,总反应(A→C)可视为经两步反应得到,则总反应的 ,则
,所以 A 与 C 的能量差为 ,D 不符合题意;
故选 C。
6.下列说法或表示方法中正确的是
A.在一定温度和压强下,将 0.5mol 和 1.5mol 置于密闭容器中充分反应生成 ,放出热量
19.3kJ,则其热化学方程式为 (g)+3 (g)⇌2
B.101kPa 时, 的摩尔燃烧焓为 ,则表示氢气摩尔燃烧焓的热化学方程式为:
C.由“C(石墨)=C(金刚石) ”可知,金刚石比石墨稳定
D.已知中和热为 ,则反应
【答案】B
【详解】A. 在一定温度和压强下,合成氨反应是可逆反应,将 0.5mol 和 1.5mol 置于密闭容器中
充分反应生成 ,放出热量 19.3kJ,则实际消耗氮气小于 0.5mol,难以计算反应的焓变,A 错误;
B. 101kPa 时, 的摩尔燃烧焓为 ,则表示氢气摩尔燃烧焓的热化学方程式中氢气的
化学计量数为 1,即: ,B 正确;
C.由“C(石墨)=C(金刚石) ”可知,金刚石能量比等量石墨能量高,金刚石不如石墨
稳定,C 错误;
D.在稀溶液中,强酸和强碱反应生成 1mol 水时所放出 57.3kJ 的热量,生成硫酸钡沉淀也会放热,则
反应 ,D 错误;
答案选 B。
7.电池在生活中随处可见,下列装置能构成原电池的是
A. B. C. D.
【答案】D
【分析】构成原电池需要满足四个条件:一是有两个活泼性不同的电极,且电极具有导电性;二是存在
能导电的电解质溶液;三是电极与电解质溶液接触,且通过导线等形成闭合回路;四是能发生自发的氧
化还原反应。这四个条件缺一不可,共同保证原电池能将化学能转化为电能并持续工作。
【详解】A.该装置中,两个电极相同,碳单质不能与氯化铜溶液反应,所以不能构成原电池,故 A 错
误;
/B.该装置中,酒精是非电解质,所以不能构成原电池,故 B 错误;
C.该装置没有外电路,因此没有形成闭合回路,故 C 错误;
D.该装置符合原电池的构成条件,铝单质能与氢氧化钠溶液反应,但是镁不能反应,因此 Al 作负极,
Mg 作正极,该装置能将化学能转化为电能,故 D 正确;
故答案选 D。
8.根据实验现象,下列判断正确的是
装置
现象 金属 A 不断溶解形成二价金属离子 C 极质量增加 A 极有气泡产生
A.装置甲中正极的电极反应式是
B.装置乙中正极的电极反应式是
C.装置丙中溶液的 不变
D.四种金属活动性由强到弱的顺序是
【答案】B
【详解】A.金属 A 不断溶解形成二价金属离子,则装置甲中负极的电极反应式是 ,A 错
误;
B.C 极质量增加,则装置乙中正极铜离子得电子生成铜,其电极反应式是 ,B 正确;
C.装置丙中,A 极有气泡产生,则 A 极溶液中的氢离子得电子生成氢气, 减小,溶液的 增大,
C 错误;
D.装置甲中 A 为负极,则金属活动性: ,装置乙中 C 为正极,则金属活动性: ,装置丙中
A 为正极,则金属活动性: ,故四种金属活动性由强到弱的顺序是 ,D 错误;
故答案为:B。
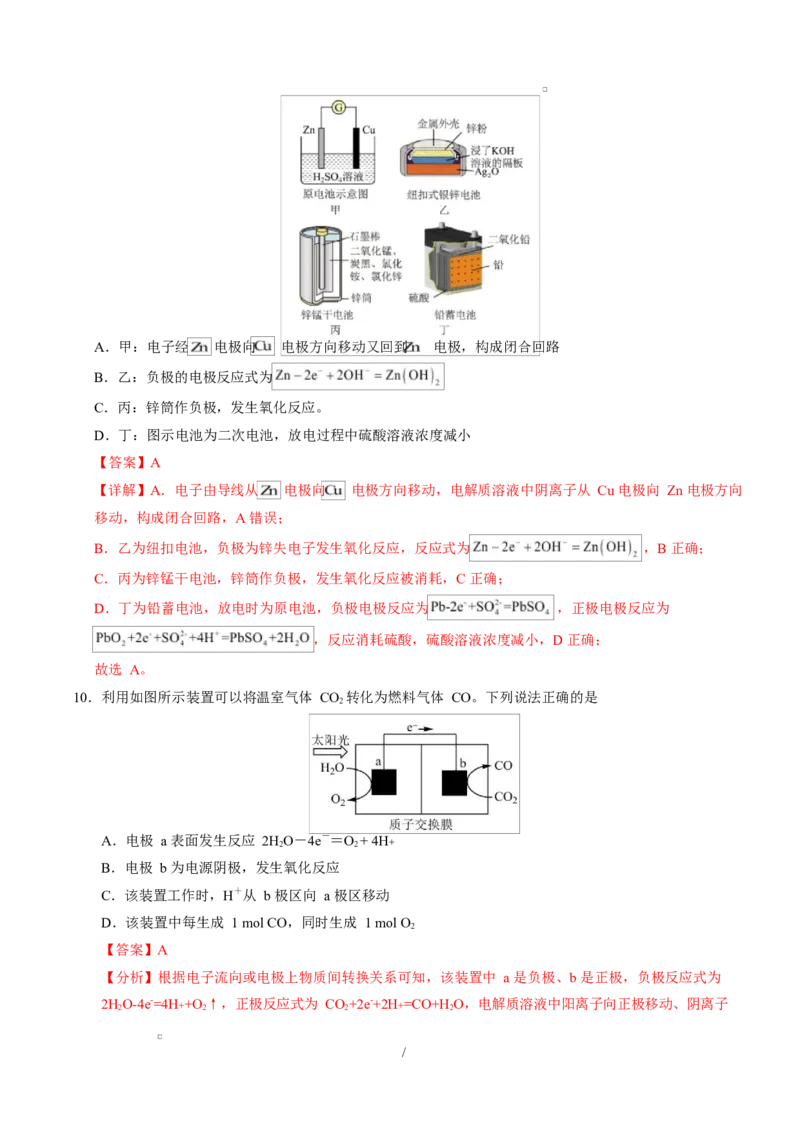
9.化学电源在日常生活和高科技领域中都有广泛应用。下列说法不正确的是
/A.甲:电子经 电极向 电极方向移动又回到 电极,构成闭合回路
B.乙:负极的电极反应式为
C.丙:锌筒作负极,发生氧化反应。
D.丁:图示电池为二次电池,放电过程中硫酸溶液浓度减小
【答案】A
【详解】A.电子由导线从 电极向 电极方向移动,电解质溶液中阴离子从 Cu 电极向 Zn 电极方向
移动,构成闭合回路,A 错误;
B.乙为纽扣电池,负极为锌失电子发生氧化反应,反应式为 ,B 正确;
C.丙为锌锰干电池,锌筒作负极,发生氧化反应被消耗,C 正确;
D.丁为铅蓄电池,放电时为原电池,负极电极反应为 ,正极电极反应为
,反应消耗硫酸,硫酸溶液浓度减小,D 正确;
故选 A。
10.利用如图所示装置可以将温室气体 CO 转化为燃料气体 CO。下列说法正确的是
2
A.电极 a 表面发生反应 2H
2
O-4e-=O
2
+ 4H+
B.电极 b 为电源阴极,发生氧化反应
C.该装置工作时,H+从 b 极区向 a 极区移动
D.该装置中每生成 1 mol CO,同时生成 1 mol O
2
【答案】A
【分析】根据电子流向或电极上物质间转换关系可知,该装置中 a 是负极、b 是正极,负极反应式为
2H
2
O-4e-=4H++O
2
↑,正极反应式为 CO
2
+2e-+2H+=CO+H
2
O,电解质溶液中阳离子向正极移动、阴离子
/移向负极,据此分析解答。
【详解】A.由分析可知,a 电极表面发生反应 2H
2
O-4e-=O
2
+ 4H+ ,故 A 项说法正确;
B.由分析可知,b 是正极,即电源阴极,电极上发生还原反应,故 B 项说法错误;
C.电解质溶液中阳离子向正极移动,即 H+ 从 a 极区向 b 极区移动,故 C 项说法错误;
D.该装置中每生成 1 mol CO,转移 2 mol e-,根据负极电极反应可知,同时会生成 0.5 mol O,故 D
2
项说法错误;
故答案为 A。
11.一种铜催化铝硫二次电池的工作原理如图所示,放电时的电池反应为
。下列说法错误的是
A.放电时, 作正极,发生还原反应
B.放电时,负极反应式为:
C.充电时,每生成 ,有 通过阳离子交换膜
D.充电时,阳极质量增加,阴极质量减少
【答案】D
【分析】由图示结合电池放电总反应可知,该电池放电时,Al 为负极,电极反应式为
,Cu/Cu S 为正极,电极反应式为 ;充电时,Al 为阴极,电
x
极反应式为 ,Cu/Cu S 为阳极,电极反应式为 。
x
【详解】A.由分析可知,放电时, 作正极,发生得电子的还原反应,A 正确;
B.由分析可知,放电时,负极反应式为: ,B 正确;
C.充电时,阳极的反应为: ,每生成 ,转移 ,故有 通过
阳离子交换膜,C 正确;
D.充电时,由电极反应式可知,阴极生成 Al,阳极由 Cu 转化为 Cu S,两电极的质量均增加,D 错误;
x
故选 D。
12.某同学欲完成反应:2HCl+2Ag=2AgCl+H ↑,设计了下列四个实验,你认为可行的是
2
/A.A B.B C.C D.D
【答案】C
【详解】电解池中阳极发生氧化反应,阴极发生还原反应,根据电解总反应方程式可知:Ag 元素化合
价升高,发生氧化反应,故 Ag 与电源正极相连,电解质为盐酸,阴极氢离子得电子生成氢气,发生还
原反应,满足条件的为 C。
答案选 C。
13.宏观—微观—符号是化学的三重表征,下列化学符号表征正确的是
A.用铁作阳极电解氯化镁溶液:
B.铜片上电镀银总反应(银作阳极,硝酸银溶液作电镀液): (阳极) (阴极)
C.铅蓄电池充电时阳极电极反应式:
D.用 溶液做导电性实验,灯泡发光:
【答案】B
【详解】A.铁作阳极时,阳极反应为 Fe 被氧化为 Fe2+,阴极水得到电子发生还原反应生成氢气和氢
氧根,镁离子、亚铁离子和氢氧根生成沉淀,A 错误;
B.电镀银时,阳极 Ag 溶解为 Ag+ ,阴极 Ag+ 还原为 Ag,总反应正确表征了 Ag 的转移,B 正确;
C.铅蓄电池充电时阳极反应为 PbSO 转化为 PbO : ,C 错误;
4 2
D.CuCl 离解为 Cu2+和 Cl-是自发过程,无需电解条件,电离方程式: ,D 错误;
2
故选 B。
14.港珠澳大桥的设计使用寿命达 120 年,施工中对桥体钢构件采用了多种防腐蚀方法。下列分析错误的
是
A.防腐蚀原理主要是避免发生反应:2Fe+O+2HO=2Fe(OH)
2 2 2
B.钢构件表面喷涂环氧树脂涂层,是为了隔绝空气、水等,防止形成原电池
C.采用外加电流阴极保护法时需直接在钢构件上安装锌块
D.钢构件可采用不锈钢材料以减缓电化学腐蚀
/【答案】C
【详解】A.防腐蚀原理是避免钢铁发生吸氧腐蚀,总反应为 2Fe+O +2H O=2Fe(OH) ,A 正确;
2 2 2
B.环氧树脂涂层隔绝空气和水,防止形成原电池,B 正确;
C.外加电流阴极保护法需通过外部电源使钢构件成为阴极,无需安装锌块(锌块用于牺牲阳极法),
C 错误;
D.不锈钢通过合金化增强抗腐蚀能力,D 正确;
故答案为 C。
15.钢铁在潮湿空气中的电化学腐蚀基本化学原理如下图所示。下列说法不正确的是
A.Fe、C 构成原电池的外电路 B.钢铁表面可发生反应:
C.吸氧腐蚀与析氢腐蚀可先后发生 D.利用电化学腐蚀可测定空气中氧气的含量
【答案】D
【详解】A.钢铁在潮湿的空气中会发生电化学腐蚀,从图中可以看出,Fe 失去电子,电子通过外电
路流向 C,所以 Fe、C 构成原电池的外电路,A 正确;
B.在钢铁表面,O 得电子生成 OH-,若此时溶液中溶有 CO,则可与 OH-反应生成 等,从而发
2 2
生反应: ,B 正确;
C.钢铁在潮湿的空气中,开始时电解质溶液的酸性较强,可能发生析氢腐蚀,随着反应进行,溶液酸
性减弱,可能会发生吸氧腐蚀,所以吸氧腐蚀与析氢腐蚀可先后发生,C 正确;
D.电化学腐蚀过程中,氧气的消耗量难以准确测量和控制,且会受到多种因素的干扰,不能准确利用
电化学腐蚀测定空气中氧气的含量,D 不正确;
故选 D。
16.一种新型高温可充电电池的构造如图所示,其电池活性物质为 Na 和 S。下列说法正确的是
/A.放电时石墨 b 上发生的反应为
B.外电路中每通过 1mol 电子,有 0.5molNa+ 通过含 Na+ 的导体
C.放电时,电流的传导方向为石墨 b→外电路→石墨 a→固体电解质→石墨 b
D.闭合 K,可将化学能转化为电能
2
【答案】C
【分析】放电时钠在负极上反应,所以石墨 a 为负极,电极反应式为: ,石墨 b 为正极,
硫得到电子,正极电极反应式为 ,充电时,在阳极上发生失电子的氧化反应,电
极反应式为: ,阴极发生还原反应,电极反应为 ,据此分析;
【详解】A.石墨 b 为正极,硫得到电子,正极电极反应式为 ,A 错误;
B.外电路中每通过 1mol 电子,有 1molNa+ 通过含 Na+ 的导体,B 错误;
C.放电时,电流由正极流向负极,传导方向为石墨 b→外电路→石墨 a→固体电解质→石墨 b,C 正确;
D.外加电源为电池充电,可将电能转化为化学能,D 错误;
故选 C。
17.下列是冬季使用的某一“暖宝宝”贴的标签。以下叙述错误的是
品名:一次性使用取暖片
成分:铁粉、活性炭、水、木粉、食盐等
用法:使用之前将其真空包装外袋撕开。取出内袋,轻轻揉
搓,贴在内衣外层。
注意事项:1.避免真空塑料包装袋被破坏,造成产品失效。
2.可持续 10 小时均匀放热。
A.暖宝宝发热的原理主要是利用铁生锈放热
B.铁生锈后反应产物的主要成分是四氧化三铁
C.暖宝宝需接触空气才会发热
D.食盐能加快“暖宝宝”中铁生锈的速度
【答案】B
【详解】A.“暖宝宝”发热的原理主要是利用铁生锈放热,铁生锈是缓慢的氧化反应,A 项正确;
B.铁生锈后反应产物的主要成分是 Fe O,B 项错误;
2 3
/C.铁生锈需要空气,“暖宝宝”需接触空气才会发热,C 项正确;
D.食盐的主要成分为氯化钠,吸水后能与铁和其中的碳,构成原电池,能加快“暖宝宝”中铁生锈的速
度,D 项正确;
故选 B。
18.我国科学家在光电催化—化学耦合烟气脱硫并实现 CO 的资源化利用与电能储存的研究中取得重大突
2
破,其工作原理如图所示。下列说法正确的是
A.电极 a 的电极反应式:
B.装置 A 食盐水中 质量分数:x%<y%
C.离子交换膜 N 为阴离子交换膜
D.每吸收 1molSO ,理论上装置 B 的总质量增加 62g
2
【答案】D
【分析】装置 B 中,d 极 2Fe2+-2e-=2Fe3+,作原电池的负极;c 极 2H++2e-=H
2
↑,作原电池的正极,则
装置 B 为原电池。装置 A 为电解池,a 极与电源的负极相连,作电解池的阴极,在该电极,CO 得电
2
子产物与电解质反应生成 CO 和 ,电极反应式为 3CO+2e-+H O=CO+2 ;b 极与电源正极相
2 2
连,为电解池的阳极,食盐水中的 Cl-失电子生成 Cl,电极反应式为 2Cl--2e-=Cl↑。装置 A 中,左侧
2 2
透过离子交换膜 M 进入中间盛有 NaHCO
3
溶液室,右侧 Na+ 透过离子交换膜 N 进入中间盛有
NaHCO 溶液室,使 NaHCO 溶液由稀变浓,食盐水由浓变稀;离子交换膜 M 为阴膜,离子交换膜 N
3 3
为阳膜。
【详解】A.由分析可知,电极 a 为阴极,CO 得电子产物与电解质反应生成 CO 和 ,电极反应
2
式:3CO+2e-+H O=CO+2 ,A 不正确;
2 2
B.装置 A 中,食盐水中 Cl-失电子生成 Cl
2
从溶液中逸出,Na+ 透过阳离子交换膜 N 进入中间 NaHCO
3
溶液室,从而使 NaCl 溶液由浓变稀,所以 NaCl 质量分数:x%>y%,B 不正确;
C.由分析可知,Na+ 能透过离子交换膜 N,所以离子交换膜 N 为阳离子交换膜,C 不正确;
D.在装置 B 内,SO
2
-2e-+2H
2
O= +4H+ ,在 c 极 2H++2e-=H
2
↑,每吸收 1molSO
2
,同时生成 1molH
2
,则理论上装置 B 的总质量增加 1mol×64g/mol-1mol×2g/mol=62g,D 正确;
/故选 D。
第 II 卷(非选择题 共 46 分)
二、非选择题(本大题包含 4 小题,共 46 分)
19.(8 分)完成下列热化学方程式:
(1)已知 AX 的熔点和沸点分别为-93.6℃和 76℃,AX 的熔点为 167℃。室温时 AX 与气体 X 反应生
3 5 3 2
成 1molAX ,放出热量 123.8 kJ。该反应的热化学方程式为 。
5
(2)2g (g)燃烧生成 (g)放热 242kJ,1mol (l)蒸发吸热 44kJ, 燃烧热的热化学方程式
为 。
(3)晶体硅(熔点 1410℃)是良好的半导体材料。由粗硅制纯硅过程如下:
Si(粗) SiCl SiCl (纯) Si(纯)
4 4
在上述由 SiCl 制纯硅的反应中,测得每生成 1.12 kg 纯硅需吸收 a kJ 热量,写出该反应的热化学方程
4
式: 。
(4)汽车发动机工作时会引发 N 和 O 反应,其能量变化示意图如下:
2 2
写出该反应的热化学方程式: 。
【答案】(1)
(2)
(3)
(4)
【详解】(1)由题目信息可知,常温时 AX 为液体,AX 为固体,该反应的热化学方程式为:
3 5
;
(2)燃烧热是在 101 kPa 时,1 mol 物质完全燃烧生成指定产物时所放出的热量;2g (g)(为
1mol)燃烧生成 1mol (g)放热 242kJ,1mol (l)蒸发吸热 44kJ,则 1mol (g)液化变
为 1mol (l)放热 44kJ,故 1mol (g)燃烧生成 1mol (l)放热 242kJ+44kJ=286kJ,故 燃
烧热的热化学方程式为: ;
(3)生成 1.12ꢀ kg 硅,吸收 aꢀ kJ 热量,则生成 1ꢀmol(28g)硅,吸收 x kJ 热量,故:
/,解得 x=0.025a,热化学方程式为 ;
(4)该反应为: ,反应热等于反应物的总键能减去生成物的总键能,
故 , 热 化 学 方 程 式 为 :
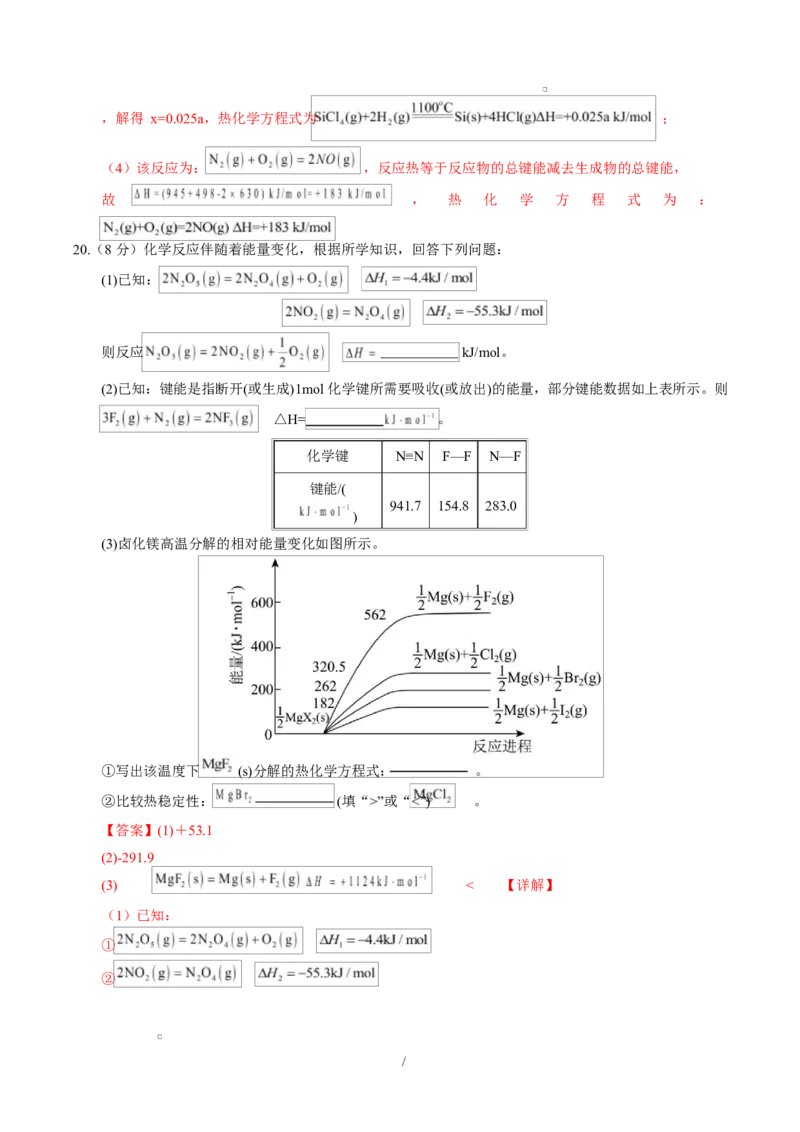
20.(8 分)化学反应伴随着能量变化,根据所学知识,回答下列问题:
(1)已知:
则反应 kJ/mol。
(2)已知:键能是指断开(或生成)1mol 化学键所需要吸收(或放出)的能量,部分键能数据如上表所示。则
△H= 。
化学键 N≡N F—F N—F
键能/(
941.7 154.8 283.0
)
(3)卤化镁高温分解的相对能量变化如图所示。
①写出该温度下 (s)分解的热化学方程式: 。
②比较热稳定性: (填“>”或“<”) 。
【答案】(1)+53.1
(2)-291.9
(3) < 【详解】
(1)已知:
①
②
/由盖斯定律, ①-②得反应 ,故
;
(2)反应焓变=反应物键能总和-生成物键能总和;该反应ΔH=3×154.8 +941.7 -6×283.0
=-291.9 ;
(3)①根据化合反应生成卤化镁的相对能量变化图,0.5mol 氟化镁固体的能量为 0 kJ,0.5mol 固态镁
单质和 0.5mol 气态 F 能量和为 562kJ,故该温度下 MgF (s)分解生成 Mg 和 F 能量升高,是吸热反应,
2 2 2
热化学方程式为 ;
②能量越低越稳定,故热稳定性:MgBr (s)