文档内容
微信公众号:【高中精品资料君】
2024 届明日之星高考化学精英模拟卷 【河南版】
可能用到的相对原子质量:H—1、C—12、O—16、K—39、Cr—52、Fe—56、Br—80
一、选择题:本题共 7小题,每小题 6分,共 42分。在每小题给出的四个选项中,只有一项
符合题目要求的。
1.化学与人类的生活密切相关。下列叙述正确的是( )
A.漂白粉与洁厕灵(含有盐酸)混合使用,可提高漂白效果
B.生活中常见的生铁和熟铁是组成相同、结构不同的铁单质
C.醋酸纤维、黏胶纤维、碳纤维以及光导纤维都属于高分子材料
D.“美人首饰侯王印,尽是沙中浪底来”,可知古人用沉降法得到黄金
2.我国科学家在国际上首次实现人工合成淀粉,部分流程如图所示。
下列说法错误的是( )
A.X与Y中C原子的杂化方式不同
B.Y分子中所有原子共平面
C.X、Y都有毒,X沸点高于Y
D.DHA属于羧酸,能发生取代反应,不能发生加成反应
3.X、Y、Z、W为原子序数依次增大的短周期元素,由它们可组成一种新型共价化合物
X Z WYWX Z ,W原子的质子数等于X与Y的原子序数之和。下列说法正确的是
2 5 3 2 5 3
( )
A.原子半径:Z>Y>X B.第一电离能:Y>W>X
C.Z的单质具有较强的还原性 D.W、Y可组成一种具有导光性的物质
4.《Jourmal of Energy Chemistry》报导了我国科学家设计CO 熔盐捕获与转化装置,该装置
2
可耦合光伏组件实现绿色转化。下列有关说法错误的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
A.CO 被熔盐捕获的过程中会生成CO2和C O2
2 3 2 5
B.X极电极反应式为2CO 3O2 4e C O2 O
2 2 5 2
C.Y极连接光伏电池的负极
D.若光伏电池有1mol电子输出,可捕获标准状况下 5.6LCO
2
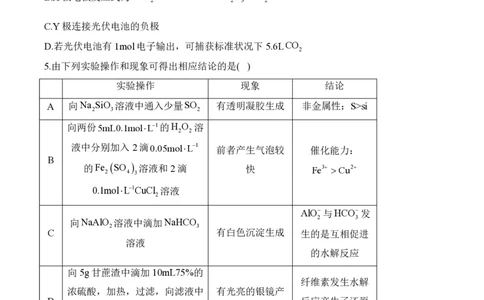
5.由下列实验操作和现象可得出相应结论的是( )
实验操作 现象 结论
A 向Na SiO 溶液中通入少量SO 有透明凝胶生成 非金属性:S>si
2 3 2
向两份5mL0.1molL1的H O 溶
2 2
液中分别加入2滴0.05molL1
前者产生气泡较 催化能力:
B
的Fe SO 溶液和2滴 快 Fe3 Cu2
2 4 3
0.1molL1CuCl 溶液
2
AlO与HCO发
2 3
向NaAlO 溶液中滴加NaHCO
2 3
C 有白色沉淀生成 生的是互相促进
溶液
的水解反应
向5g甘蔗渣中滴加 10mL75%的
纤维素发生水解
浓硫酸,加热,过滤,向滤液中 有光亮的银镜产
D 反应产生了还原
加入固体NaOH,至pH=9,再 生
性糖
加入2mL银氨溶液,水浴加热
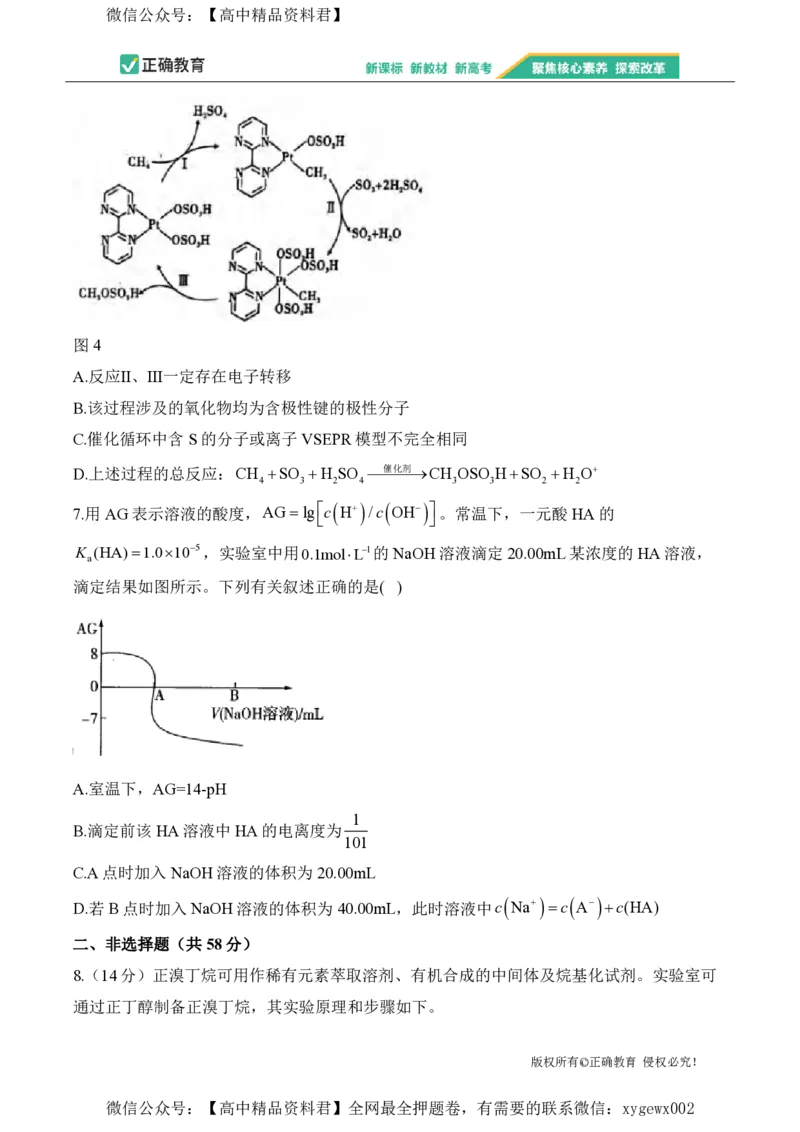
6.一种含Pt催化剂活化甲烷中碳氢键的反应机理如图4所示。下列说法错误的是( )
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
图4
A.反应Ⅱ、Ⅲ一定存在电子转移
B.该过程涉及的氧化物均为含极性键的极性分子
C.催化循环中含S的分子或离子VSEPR模型不完全相同
D.上述过程的总反应:CH SO H SO 催化剂CH OSO HSO H O
4 3 2 4 3 3 2 2
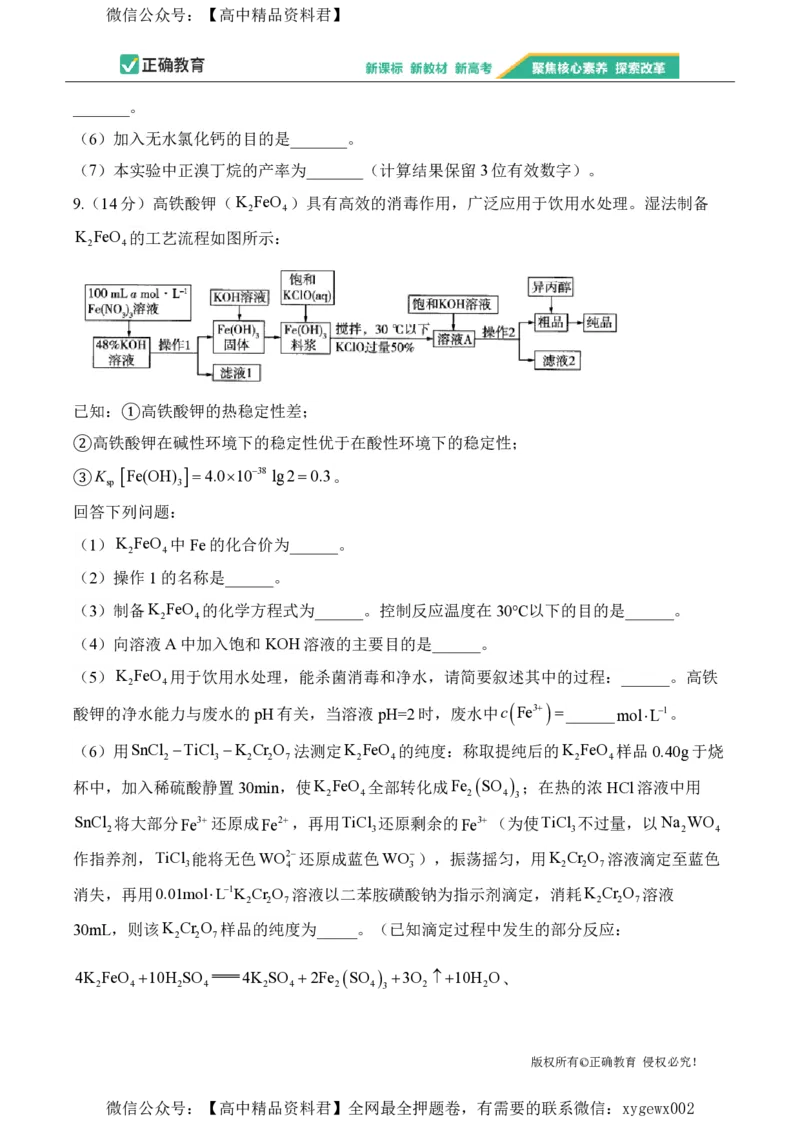
7.用AG表示溶液的酸度,AG lgc H /c OH。常温下,一元酸HA的
K (HA)1.0105,实验室中用0.1molL1的NaOH溶液滴定20.00mL某浓度的HA溶液,
a
滴定结果如图所示。下列有关叙述正确的是( )
A.室温下,AG=14-pH
1
B.滴定前该 HA溶液中HA的电离度为
101
C.A点时加入NaOH溶液的体积为20.00mL
D.若B点时加入NaOH溶液的体积为40.00mL,此时溶液中c
Na
c
A
c(HA)
二、非选择题(共 58分)
8.(14分)正溴丁烷可用作稀有元素萃取溶剂、有机合成的中间体及烷基化试剂。实验室可
通过正丁醇制备正溴丁烷,其实验原理和步骤如下。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
已知:醇类、醚类和烯烃可溶于浓硫酸,其他相关信息如下表。
名称 相对分子质量 沸点/℃ 密度/(gcm3) 溶解性
正丁醇 74 117.7 0.8 微溶于水
正溴丁烷 137 101.6 1.3 难溶于水
实验原理
△
主反应:NaBrH SO 浓 NaHSO HBr
2 4 4
CH CH CH CH OHHBr△CH CH CH CH BrH O
3 2 2 2 3 2 2 2 2
△
副反应:2HBrH SO 浓 SO Br 2H O
2 4 2 2 2
CH CH CH CH OH浓硫酸CH CH CHCH H O
3 2 2 2 △ 3 2 2 2
2CH CH CH CH OH浓硫酸CH CH CH CH O正丁醚H O
3 2 2 2 △ 3 2 2 2 2 2
实验步骤
①在装有冷凝管的圆底烧瓶中加入 15mL水,然后缓慢加入20mL浓硫酸,冷却至室温后,
再加入13mL正丁醇,混合后加入 15g溴化钠,充分振荡,加入几粒沸石,加热回流半小
时。②待反应液冷却后,将反应所得混合液体加入另一蒸馏装置中,蒸馏得到正溴丁烷粗产
品。
③将粗产品转入分液漏斗,用 10mL水洗涤,将所得有机层转入另一干燥的分液漏斗中,用
5mL浓硫酸洗涤,分去硫酸层后,有机层依次用水、饱和碳酸氢钠溶液、水洗涤。
④将上述有机层转入干燥的锥形瓶,加入无水氯化钙后再次蒸馏,收集99~103℃的馏分,最
终得到产品9.6mL。
回答下列问题:
(1)在步骤①的反应装置中应选用_______(填“直形”或“球形”)冷凝管,在冷凝管的上面
用橡胶管连接一个漏斗,倒置于盛有NaOH溶液的烧杯中,目的是_______。
(2)蒸馏得到正溴丁烷粗产品时,判断正溴丁烷是否完全蒸出的方法是_______。
(3)若正溴丁烷粗产品呈红棕色,可加入适量的饱和NaHSO 溶液除去杂质,反应的离子方
3
程式为_______。
(4)在步骤③中加入浓硫酸洗涤的作用是_______。
(5)粗产品用浓硫酸洗涤后,不直接用饱和碳酸氢钠溶液洗涤而要先用水洗涤的原因是
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
_______。
(6)加入无水氯化钙的目的是_______。
(7)本实验中正溴丁烷的产率为_______(计算结果保留3位有效数字)。
9.(14分)高铁酸钾(K FeO )具有高效的消毒作用,广泛应用于饮用水处理。湿法制备
2 4
K FeO 的工艺流程如图所示:
2 4
已知:①高铁酸钾的热稳定性差;
②高铁酸钾在碱性环境下的稳定性优于在酸性环境下的稳定性;
③K Fe(OH) 4.01038 lg20.3。
sp 3
回答下列问题:
(1)K FeO 中Fe的化合价为______。
2 4
(2)操作1的名称是______。
(3)制备K FeO 的化学方程式为______。控制反应温度在30℃以下的目的是______。
2 4
(4)向溶液A中加入饱和KOH溶液的主要目的是______。
(5)K FeO 用于饮用水处理,能杀菌消毒和净水,请简要叙述其中的过程:______。高铁
2 4
酸钾的净水能力与废水的pH有关,当溶液pH=2时,废水中c
Fe3
______molL1。
(6)用SnCl TiCl K Cr O 法测定K FeO 的纯度:称取提纯后的K FeO 样品0.40g于烧
2 3 2 2 7 2 4 2 4
杯中,加入稀硫酸静置30min,使K FeO 全部转化成Fe SO ;在热的浓HCl溶液中用
2 4 2 4 3
SnCl 将大部分Fe3还原成Fe2,再用TiCl 还原剩余的Fe3(为使TiCl 不过量,以Na WO
2 3 3 2 4
作指养剂,TiCl 能将无色WO2还原成蓝色WO),振荡摇匀,用K Cr O 溶液滴定至蓝色
3 4 3 2 2 7
消失,再用0.01molL1K Cr O 溶液以二苯胺磺酸钠为指示剂滴定,消耗K Cr O 溶液
2 2 7 2 2 7
30mL,则该K Cr O 样品的纯度为_____。(已知滴定过程中发生的部分反应:
2 2 7
4K FeO 10H SO 4K SO 2Fe SO 3O 10H O、
2 4 2 4 2 4 2 4 3 2 2
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
Cr O2 6Fe2 14H 6Fe3 2Cr3 7H O)
2 7 2
10.(15分)乙烯的产量是衡量一个国家石油化工发展水平的标志,近几年各国都加大了乙烯
的制备的研发力度。回答下列问题:
(1)乙烷分解法
已知CO的燃烧热为283kJmol1。以C H 和CO 为原料可以协同制取C H 和CO,发生的
2 6 2 2 4
反应如下:
反应1:2C H (g)O (g)2C H (g)2H O(g) H 212kJmol1
2 6 2 2 4 2
反应2:H (g)CO (g)CO(g)H O(g) H 41kJmol1
2 2 2
①C H (g)C H (g)H (g)的H _____kJmol1。
2 6 2 4 2
②恒温条件下,下列能够提高反应C H (g)C H (g)H (g)中乙烯产率的措施有_____
2 6 2 4 2
(填标号)。
A.保持体积不变,通入氮气
B.保持压强不变,通入乙烷
C.保持体积不变,通入乙烷
D.及时分离出氢气
③恒温恒压(100kPa)下,在密闭容器中通入乙烷和稀有气体,平衡时各组分的体积分数分
别为:乙烷5%、氢气20%、乙烯20%。该温度下反应C H (g)C H (g)H (g)的平衡
2 6 2 4 2
常数K =____kPa(用物质的平衡分压代替平浓度,平衡分压=总压强×体积分数)。
p
(2)二氧化碳转化法
反应原理为2CO (g)6H (g)C H (g)4H O(g)。在体积固定的密闭容器中,加入一定
2 2 2 4 2
量的CO 与H 和催化剂,一段时间内测得二氧化碳的浓度变化如图1所示。在相同时间段
2 2
内,测得乙烯的体积分数随温度变化如图2所示。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
①由图 1可知,0~8min用乙烯表示的平均反应速率为_______molL1min1。
②图 2中,a、b、c三点表示的平均化学平衡常数由大到小的顺序为;b点的反应速率v
正
______v (填“<“>”或“=”)。
逆
③b点后乙烯的体积分数随温度升高逐渐减小的原因可能是______、______。
④实验测定,反应中,v k c2CO c6H ,v k cCH CH c4H O(k 、
正 正 2 2 逆 逆 2 2 2 正
k 为速率常数,只与温度有关),精确实验表明,达到平衡时k 的值为k 的2倍,则该反
逆 逆 正
应的平衡常数K=_____。
11.(15分)PTP1B(蛋白酪氨酸磷酸酶 1B)是蛋白酪氨酸磷酸酶家族的主要成员之一,在
胰岛素信号传导中起着重要的负调控作用,F是一种具有 PTP抑制活性的溴代天然海洋产
物,其合成路线如下:
已知:
回答下列问题:
(1)F的分子式为______,E中含氧官能团的名称是______。
(2)已知B有3种不同化学环境的氢原子,且个数比为3:1:1,则B的结构简式为
______。
(3)C→D的反应类型为______,D中第一电离能最大的元素是______。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
(4)写出反应A+B→C的化学方程式______。
(5)A有多种同分异构体,其中满足下列条件的芳香族化合物有种。
Ⅰ.1mol该物质最多消耗3molNa、2molNaOH、1molNaHCO
3
Ⅱ.红外光谱法测定后发现结构中无甲基
上述芳香族化合物核磁共振氢谱有9组峰的结构简式为______。
(6)二苯甲酮( )是一种定香剂,参照上述合成路线设计以苯为原料合成
二苯甲酮的合成路线(其他试剂任选)______。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
答案以及解析
1.答案:D
解析:漂白粉的有效成分次氯酸钙与洁厕灵(含有盐酸)混合,会发生氧化还原反应生成有
毒的氯气,漂白效果变差,两者不能混合使用,A错误;生铁和熟铁均属于合金,不是铁的
单质,B错误;光导纤维的主要成分是二氧化硅,不属于高分子材料,C错误;“尽是沙中浪
底来”,从中可以得出古人从沙子中得到黄金的方法为沉降法,D正确。
2.答案:D
解析:根据题图可知X中C原子的杂化方式是sp3,Y中C原子的杂化方式是sp2,A正确;
甲醛含有碳氧双键,双键是平面结构,所以四个原子共平面,B正确;甲醇与甲醛都有毒,
甲醇分子间存在氢键,因此其沸点高于甲醛,C正确;DHA的结构简式为
HOCH COCH OH,无羧基,不属于羧酸,DHA分子含有羟基,能发生取代反应,含有羧
2 2
基,能发生加成反应,D错误。
3.答案:D
解析:同周期主族元素,从左到右原子半径依次减小,则C、O、F的原子半径大小顺序为
C>O>F,A错误;同周期主族元素,从左到右元素的第一电离能呈增大趋势,同主族元素,
从上到下元素的第一电离能依次减小,则C、O、Si的第一电离能的大小顺序为O>C>Si,B
错误;位于元素周期表右上角的氟元素的非金属性最强,单质具有很强的氧化性,C错误;
二氧化硅具有导光性,D正确。
4.答案:B
解析:根据图示可知本装置是电解池。A项,CO 与熔盐反应生成CO2和C O2,正确;B
2 3 2 5
项,生成的C O2和CO2分别在X、Y两极放电,其中X极电极反应式是
2 5 3
2C O2 4e 4CO O ,错误;C项,Y极电极反应式是CO2 4e C3O2,Y
2 5 2 2 3
是阴极,连接光伏电池的负极,正确;D项,由上述分析可知总反应是CO CO ,每
2 2
转移4mol电子,捕获1molCO ,故若光伏电池有1mol电子输出,则可捕获0.25molCO ,
2 2
在标准状况下体积是5.6L,正确。
5.答案:D
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
解析:将SO 通入Na SiO 溶液中,发生反应Na SiO SO H O H SiO Na SO ,
2 2 3 2 3 2 2 2 3 2 3
说明H SO 的酸性强于H SiO 的,但H SO 不是硫元素的最高价含氧酸,故无法通过此实验
2 3 2 3 2 3
比较硫、硅元素非金属性的强弱,A错误;虽然c Fe3 c Cu2 ,两个实验cH O 也相
2 2
同,但由于阴离子种类不相同,则不能比较Fe3和Cu2的催化能力,B错误;向NaAlO 溶
2
液中滴加NaHCO 溶液,发生反应AlO HCO H O Al(OH) CO2,该反应是一个
3 2 3 2 3 3
“夺氢反应”,即AlO夺取HCO电离出的H,不属于互相促进的水解反应,C错误;甘蔗渣
2 3
的主要成分为纤维素,在75%的浓硫酸、加热条件下,会发生水解反应,其水解产物能发生
银镜反应,说明有还原性糖生成,D正确。
6.答案:B
解析:A,反应Ⅰ、Ⅱ过程中有 S元素化合价发生改变,发生的是氧化还原反应,故一定有电
子转移,A正确;
B.该过程涉及的氧化物有SO 、SO ,SO 为含极性键的极性分子,SO 为含极性键的非极性
2 3 2 3
分子,B错误;
C.SO 、SO 中S原子的价层电子对数都为3,二者 VSEPR模型均为平面三角形;而SO2子
2 3 4
中S的价层电子对数为 4,VSEPR模型为四面体形,故催化循环中S的VSEPR模型不完全
相同,C正确;
D.根据反应机理图,上述过程的总反应为
CH SO H SO 催化剂CH OSO HSO H O,D正确;
4 3 2 4 3 3 2 2
本题选B。
7.答案:B
解析:
AG lgc H /c OH lgc Hlgc OH pH(pOH)pH14pH142pH
,A错误。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
8.(14分)答案:(1)球形(1分);吸收挥发出的溴化氢、溴蒸气和SO ,防止污染空气
2
(1分)
(2)观察蒸馏烧瓶中正溴丁烷有机层是否完全消失,若完全消失,说明正溴丁烷完全蒸出
(2分)
(3)Br HSO H O 2Br SO2 3H(2分)
2 3 2 4
(4)除去杂质正丁醇、正丁醚、1-丁烯(2分)
(5)先用水洗可以洗去大部分残留的硫酸,否则硫酸会消耗较多的碳酸氢钠,且会产生较多
的二氧化碳,导致分液漏斗内压强增大,洗涤时会有液体冲出,造成产品损失(2分)
(6)除去产品中的水(2分)
(7)64.8%(2分)
解析:(1)用于冷凝回流的冷凝管是球形冷凝管。NaOH溶液的作用是吸收未反应的HBr和
副反应生成的溴蒸气、SO ,防止污染空气。
2
(2)观察蒸馏烧瓶中正溴丁烷有机层是否完全消失,若完全消失,说明正溴丁烷完全蒸出。
或将新收集到的馏出液加入装有蒸馏水的试管中,若无分层现象,说明正溴丁烷完全蒸出。
(3)根据发生的副反应可知,红棕色的杂质是Br ,故反应的离子方程式为
2
Br HSO H O 2Br SO2 3H。
2 3 2 4
(4)根据已知信息醇类、醚类和烯烃可溶于浓硫酸知,加入浓硫酸洗涤的作用是除去未反应
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
的正丁醇及副产物正丁醚、1-丁烯。
(5)因为刚用浓硫酸洗涤过的产品中还含有较多硫酸,若直接用饱和碳酸氢钠溶液洗涤,会
消耗较多的碳酸氢钠,且会有较多的二氧化碳产生,导致分液漏斗内压强增大,洗涤时会有
液体冲出,造成产品损失。
(6)加入无水氯化钙的目的是除去产品中的水。
(7)根据关系CH CH CH CH OH~CH CH CH CH Br可知,理论上
3 2 2 2 3 2 2 2
0.813
mCH CH CH CH Br 137g,实际上mCH CH CH CH Br9.61.3g,正溴丁烷
3 2 2 2 74 3 2 2 2
9.61.3g
100%64.8%
的产率= 0.813 。
137g
74
9.(14分)答案:(1)+6(1分)
(2)过滤(1分)
(3)2Fe(OH) 3KClO4KOH 2K FeO 3KCl5H O(2分);防止温度过高时
3 2 4 2
K FeO 分解(1分)
2 4
(4)增大K的浓度,促进K FeO 从溶液中析出(1分)
2 4
(5)K FeO 具有强氧化性,能将病菌氧化变性(2分);K FeO 的还原产物Fe3水解生成
2 4 2 4
的Fe(OH) 胶体具有较大的表面积,可吸附水中的悬浮物,起到净水作用(2分);0.04(2
3
分)
(6)89.1%(2分)
解析:(1)化合物中各元素化合价代数和为0,则K FeO 中Fe的化合价为+6。
2 4
(2)操作1后得到固体和滤液,则操作1是过滤。
(3)分析流程可知操作2分离出K FeO 粗品,则
2 4
Fe(OH) KClOKOHK FeO KClH O,依据氧化还原反应方程式的配平原则配平
3 2 4 2
即可。结合已知信息①高铁酸钾的热稳庭性差,控制反应温度在30℃以下是为了防止温度过
高时K FeO 分解。
2 4
(4)饱和KOH溶液可增大K的浓度,促进K FeO 从溶液中析出。
2 4
(5)K FeO 具有强氧化性,能将病菌氧化变性,起到杀菌作用;K FeO 的还原产物Fe2水
2 4 2 4
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
解生成的Fe(OH) 胶体具有较大的表面积,可吸附水中的悬浮物,起到净水作用。当溶液
3
K 1014
pH=2时,常温下,c OH W molL1 1012molL1 ,
c H 102
K Fe(OH) 4.01038
c Fe3 sp 3 molL1 0.04molL1
。
c3 OH 10123
(6)结合题意得:6K FeO ~6Fe3 ~6Fe2 ~ K Cr O ,K FeO 的样品的纯度为
2 4 2 2 7 2 4
301030.016198
100%=89.1%。
0.40
10.(15分)答案:(1)①+136(1分);②D(1分);③80(1分)
(2)①0.025(2分);②a>b>c(2分);>(2分);③温度升高,催化剂的活性降低,反
应速率降低(2分);温度升高,发生其他副反应(2分);④0.5(2分)
1
解析:(1)H
212 41283
kJmol1 136kJmol1。②A项保持体积不变,通入
2
氮气,对平衡无影响;B项保持压强不变,通入乙烷,各组分体积分数不变,产率不变;C
项保持体积不变,通入乙烷,等于加压,平衡逆向移动,乙烯产率减小;D项及时分离出氢
气,平衡正向移动,乙烯产率增大。③根据题意,
pC H 100kPa5%5kPa,pC H 100kPa20%20kPa,pH 100kPa20%20kPa
2 6 2 4 2
pC H pH 2020
,K 2 4 2 kPa 80kPa。
p pC H 5
2 6
(2)①根据图1,0~8min,cCO (0.80.4)molL1 0.4molL1,
2
0.4molL1
vCO 0.05molL1min1,故用乙烯表示的平均反应速率为0.025
2 8min
molL1min1。②根据图 2中,平衡时的体积分数曲线,可知温度升高乙烯的体积分数减
小,该反应为放热反应,温度升高,化学平衡常数减小;b点乙烯体积分数小于乙烯在该温
度下的平衡体积分数,故反应正向进行,v v 。③b点后乙烯的体积分数随温度升高逐渐
正 逆
减小的原因可能为温度升高,催化剂的活性降低,反应速率降低;有机反应复杂,温度升
高,有其他副反应发生。④达到平衡时,v v ,故
正 逆
c4H OcC H k
k c2CO c6H k cC H c4H O,K 2 2 4 正 0.5。
正 2 2 逆 2 4 2 c6H c2CO k
2 2 逆
11.(15分)答案:(1)C H BrO (1分);酮羧基、醚键(1分)
13 7 3 5
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
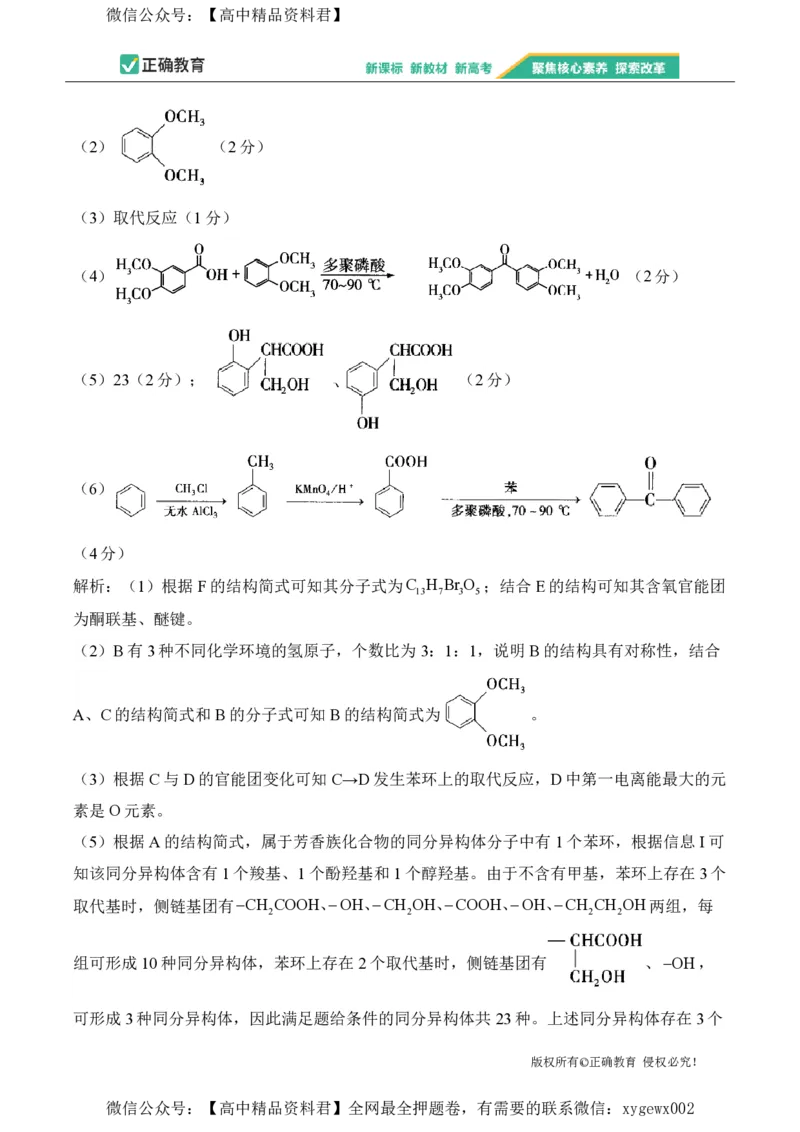
(2) (2分)
(3)取代反应(1分)
(4) (2分)
(5)23(2分); (2分)
(6)
(4分)
解析:(1)根据F的结构简式可知其分子式为C H BrO ;结合E的结构可知其含氧官能团
13 7 3 5
为酮联基、醚键。
(2)B有3种不同化学环境的氢原子,个数比为3:1:1,说明B的结构具有对称性,结合
A、C的结构简式和B的分子式可知B的结构简式为 。
(3)根据C与D的官能团变化可知C→D发生苯环上的取代反应,D中第一电离能最大的元
素是O元素。
(5)根据A的结构简式,属于芳香族化合物的同分异构体分子中有 1个苯环,根据信息I可
知该同分异构体含有1个羧基、1个酚羟基和1个醇羟基。由于不含有甲基,苯环上存在3个
取代基时,侧链基团有CH COOH、OH、CH OH、COOH、OH、CH CH OH两组,每
2 2 2 2
组可形成10种同分异构体,苯环上存在2个取代基时,侧链基团有 、OH,
可形成3种同分异构体,因此满足题给条件的同分异构体共23种。上述同分异构体存在3个
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
取代基时,核磁共振氢谱均有8组峰,存在2个取代基且处于邻位和间位时,核磁共振氢谱
有9组峰,符合题给条件的结构简式为 。
(6)参照合成C的反应可知合成二苯甲酮需要苯和苯甲酸,由苯可合成苯甲酸,先根据已
知信息将苯转化为甲苯,再将甲苯氧化成苯甲酸,可设计合成路线如下:
。
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002微信公众号:【高中精品资料君】
版权所有©正确教育 侵权必究!
微信公众号:【高中精品资料君】全网最全押题卷,有需要的联系微信:xygewx002