文档内容
让更多的孩子得到更好的教育
中考总复习:盐 化学肥料(提高)
撰稿:熊亚军 审稿:李伟
【巩固练习】
一、 选择题 (每小题只有一个选项符合题意)
1.某星期天,小明同学回家发现自家田里的小麦出现大面积倒伏现象,就向父母提出了一条合理化建议:
明年应在小麦生长期增施抗倒伏的化肥。你认为增施的化肥应是( )
A.KCl B.CO(NH) C.NHNO D.Ca(HPO)
2 2 4 3 2 4 2
2.镧(La)是一种活动性比锌更强的元素,它的氧化物的化学式为LaO;La(OH) 是不溶于水的碱,而
2 3 3
LaCl、La(NO) 都可溶于水。由此判断下列几组物质不能直接反应制取LaCl 的是( )
3 3 3 3
A.LaO 和HCl B.La(OH) 和HCl C.NaCl和La(OH) D.La和HCl
2 3 3 3
3.如果将物质按单质、氧化物、酸、碱、盐、有机物分类,下图中甲、乙、丙是三种不同类别的物质,且相连
物质间均能发生化学反应。
下列说法符合图示要求的是( )
A.当甲为氯化铵时,X可以为氢氧化钾
B.当甲、乙、丙分别为酸、碱、盐时,X一定不可能为碳酸钠
C.当X为氧气时,甲、乙、丙可以为氢气、红磷、葡萄糖
D.当X为稀盐酸时,甲、乙、丙可以为铜、氢氧化铜、硝酸银
4.只需用水就能直接鉴别的一组物质是( )
A.NaSO、CuSO、CaCO B.AgCl、BaSO、CuSO
2 4 4 3 4 4
C.NaCl、CaCl、BaCl D.BaCl、AgCl、CaCO
2 2 2 3
5.如图所示是某同学鉴别NHHCO、NHCl、KCl三种化肥的过程,其中试剂甲和试剂乙可能是( )
4 3 4
A.甲:熟石灰;乙:稀盐酸
B.甲:水;乙:氢氧化钠溶液
C.甲:氢氧化钠溶液;乙:氯化钠溶液
D.甲:稀盐酸;乙:氯化钠溶液
6.探究中和反应是否发生的方法有多种。小明同学进行了以下四个实验,并用如图所示图像分别描述了
实验过程中的现象。其中,依据图示现象不能判断中和反应一定发生的是( )
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第1页 共7页让更多的孩子得到更好的教育
A.在稀盐酸中加氯化铜,然后向其中逐滴加入NaOH溶液
B.在NaOH溶液中加入CaCO,然后向其中逐滴加入稀盐酸
3
C.在NaOH溶液中加入CuO,然后向其中逐滴加入稀硫酸
D.在NaOH溶液中加入Ba(NO),然后向其中逐滴加入稀硫酸
3 2
7.为从废铜屑中得到较纯的单质铜,某探究小组设计了如图所示的方案:
则下列说法正确的是( )
A.若X是Fe,第③步反应还应有氯化铁生成
B.X还可以是Zn,但不能是Ag
C.直接用废铜屑进行②③步操作也能达到实验目的
D.向第②步反应后的溶液中加入硝酸银溶液,若有白色沉淀产生,即证明盐酸过量
8.(2012江苏)能大量共存且形成无色溶液的一组离子是( )
A.Cu2+、SO2-、H+ B.CI-、NH+、OH-
4 4
C.Ba2+ 、 SO2-、NO- D.Na+、K+、NO-
4 3 3
二、 选择题 (每小题有二个或两个以上选项符合题意)
9.对于化学反应:A+B=C+D,下列说法中错误的是( )
A.若A、B为化合物,该反应一定是复分解反应
B.若A、C为单质,B、D为化合物,该反应一定是置换反应
C.若A为可溶性碱,B为可溶性盐,则C和D可能是两种沉淀物
D.若C、D为盐和水,该反应一定是中和反应
10.甲、乙两工厂排出的废水澄清透明,分别含有K+、Ba2+、Cu2+、OH-、CO2-、NO-六种离子中的三种不同的
3 3
离子,已知甲厂废水明显呈碱性。若两厂单独排放都会造成严重的污染;若将两厂的废水按一定比例混合,
沉淀后废水会变成只含一种溶质的无色澄清溶液,此溶质可做化肥。下列关于废水的分析中,正确的是(
)
A.甲厂排放的废水中含有K+、Ba2+、OH-三种离子
B.甲厂排放的废水中含有K+、OH-、CO2-三种离子
3
C.可做化肥的溶质为KNO
3
D.可做化肥的溶质为KCO
2 3
三、填空题
11.现有:①CuCl;②Fe(NO);③KSO;④NaCO;⑤NaOH;⑥Ba(NO);⑦锌粒。根据下表所列实验现象,
2 3 3 2 4 2 3 3 2
判断是哪两种物质发生的反应,把物质的编号和有关化学方程式填入表格内。
混合编号 实验现象 化学方程式
( )+( ) 白色沉淀,滴加硝酸沉淀不消失
( )+( ) 白色沉淀,滴加硝酸沉淀消失
( )+( ) 蓝色沉淀
( )+( ) 红褐色沉淀
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第2页 共7页让更多的孩子得到更好的教育
( )+( ) 锌表面生成红色物质
12.某粗盐样品中含有杂质氯化镁、氯化钙。小林设计了如图所示提纯方案:
(1)若先除去氯化镁,再除去氯化钙,则:①试剂a的化学式是________,试剂b的化学式是________。
②指出操作c的名称:________。
③操作过程中加入适量稀盐酸时,可能发生反应的化学方程式是 ,
。
(2)用下图所示装置进行过滤时,向过滤器内倾注液体的正确方法是________。
A.倾注时,玻璃棒插入过滤器中心
B.倾注时,玻璃棒下端靠在过滤器内任意位置
C.倾注时,玻璃棒下端靠在过滤器内三层滤纸一边
四、实验探究题
13.小李通过学习知道:NaCO、NaHCO 均能与盐酸反应,NaCO 溶液还会与石灰水反应。
2 3 3 2 3
[产生疑问] NaHCO 溶液也能与石灰水发生反应吗?如果能反应,生成物可能是什么?
3
[查阅资料] 已知Ca(HCO) 能溶于水,碳酸氢盐在碱溶液中会生成碳酸盐。
3 2
[进行实验] 小李将NaHCO 溶液与石灰水混合,结果产生白色沉淀。此白色沉淀是________,证明
3
NaHCO 溶液与Ca(OH) 溶液也能发生反应。
3 2
为了进一步了解生成的含钠化合物是什么物质,继续探究。
[作出猜想]①只有NaOH; ②有NaCO 和NaOH;③________。
2 3
[实验与结论]
步骤1:取少量上述实验后的上层清液于试管中,再滴加足量的CaCl 溶液(中性),观察到产生白色
2
沉淀,由此可知生成的含钠化合物中一定含有________。
步骤2:将步骤1中反应后的混合物过滤,往滤液中先滴加几滴酚酞溶液,再滴加足量的稀盐酸,观察
到溶液颜色变化情况为________,整个实验过程中无气泡产生,由此可知猜想②成立。
NaHCO 与Ca(OH) 反应的化学方程式为 。
3 2
14.某校化学兴趣小组进行了“复分解反应发生条件的实验探究活动”(用到HSO、Ba(NO)、NaOH、KCO
2 4 3 2 2 3
四种溶液)。他们对实验后的废液成分进行了探究。
取废液少许,测得其pH为12。
[提出问题] 废液中除含OH-外,还含有哪些离子呢?
[理论分析] 废液是由四种盐混合而成的。这四种盐电离出的八种离子(H+、SO2-、Ba2+、NO-、Na+、OH
4 3
-、K+、CO2-)之间会相互发生反应。废液的pH为12,显碱性,所以一定不存在的一种离子是________;有
3
三种离子在任何条件下都会存在,它们是NO-,K+和________。
3
[猜想与假设]
甲同学:另外可能还含有SO2-、CO2-。
4 3
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第3页 共7页让更多的孩子得到更好的教育
乙同学:另外可能还含有Ba2+。
丙同学:另外可能还含有Ba2+、SO2-、CO2-。
4 3
以上甲、乙、丙三位同学的假设中,________同学的假设一定不成立,原因是________。
15.实验室有一瓶化肥的标签已脱落,只知道它是NHC1、(NH)SO、NHHCO 和尿素[CO(NH)]中的一种。
4 4 2 4 4 3 2 2
请你完成以下探究:
[猜想]
猜想①:该化肥是NHCl;猜想②:该化肥是________;猜想③:该化肥是NHHCO;猜想④:该化肥是尿
4 4 3
素。
[实验探究]
(1)取少量样品在研钵中与熟石灰研磨,有刺激性气味的气体放出,证明猜想________不成立;写出
其中一种化肥发生该反应的化学方程式: 。
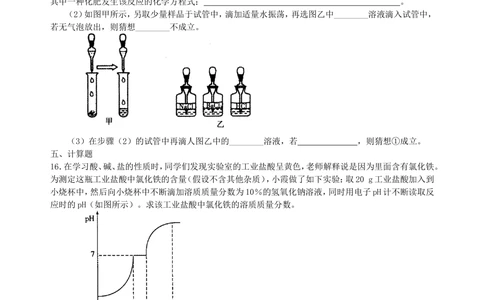
(2)如图甲所示,另取少量样品于试管中,滴加适量水振荡,再选图乙中________溶液滴入试管中,
若无气泡放出,则猜想________不成立。
(3)在步骤(2)的试管中再滴人图乙中的________溶液,若 ,则猜想①成立。
五、计算题
16.在学习酸、碱、盐的性质时,同学们发现实验室的工业盐酸呈黄色,老师解释说是因为里面含有氯化铁。
为测定这瓶工业盐酸中氯化铁的含量(假设不含其他杂质),小霞做了如下实验:取20 g工业盐酸加入到
小烧杯中,然后向小烧杯中不断滴加溶质质量分数为10%的氢氧化钠溶液,同时用电子pH计不断读取反
应时的pH(如图所示)。求该工业盐酸中氯化铁的溶质质量分数。
【答案与解析】
1.【答案】A
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第4页 共7页让更多的孩子得到更好的教育
【解析】钾肥能促进作物生长,增强作物的抗倒伏能力。
2.【答案】C
【解析】本题主要考查对于复分解反应发生条件的理解。A和B中的两种物质相互交换成分后有水生成,
符合复分解反应的条件,所以可以;La的活动性比锌更强,所以可以直接和酸反应生成LaCl;而C中的
3
NaCl和La(OH) 相互交换成分后是NaOH和LaCl,即没有沉淀,也没有水和气体生成,所以不会发生反应,
3 3
故选C。
3.【答案】A
【解析】A中氯化铵可与氢氧化钾反应放出氨气,氢氧化钾属于碱,乙和丙可选择非金属氧化物(如二氧
化碳等)和酸(盐酸、硫酸等),故A正确;B中三种物质可分别为盐酸(或硫酸等)、氢氧化钡(或氢氧化钙
等)、氯化钙(或氯化钡、硝酸钙等),这些物质都可以与碳酸钠反应,故X也可以是碳酸钠,B错误;C中氢
气和红磷都属于单质,不符合题意,C错误;D中铜与盐酸不反应,故D错误。
4.【答案】A
【解析】记住盐的溶解性和一些特殊离子在溶液中的颜色是解题的关键。A选项中NaSO 溶液无色,
2 4
CuSO 溶液显蓝色,CaCO 不溶于水,可以鉴别。B选项中AgCl和BaSO 均是不溶于水的白色物质,C选项中
4 3 4
的3种物质均能溶于水形成无色溶液,D选项中的AgCl、CaCO 均不溶于水。
3
5.【答案】A
【解析】加入试剂甲后,产生有氨味气体的物质有NHHCO、NHCl,说明加入的试剂甲是碱,与NH+结合后
4 3 4 4
产生氨气,故B、D错误;NHHCO 与NHCl中含有相同的NH+,区分它们只能从HCO-与Cl-着手选择试剂乙,
4 3 4 4 3
加入乙后NHHCO 产生了气泡,说明乙与HCO-结合有气体产生,此气体一定是CO,故加入的乙是酸,C不
4 3 3 2
符合。
6.【答案】D
【解析】A中加入NaOH溶液,NaOH先与盐酸反应,当NaOH与稀盐酸恰好反应完后,NaOH才与CuCl 反应
2
产生沉淀;B中加入稀盐酸,盐酸先与NaOH反应,当盐酸与NaOH恰好反应完后,再与CaCO 反应产生气体;
3
C中加入稀硫酸,稀硫酸先与NaOH反应,当硫酸与NaOH恰好反应完后,再与CuO反应生成CuSO,使溶液
4
颜色变蓝,并逐渐加深。A,B,C图示现象恰好与反应情况完全相符,所以可以根据图示现象判断一定发生
了中和反应。D图中,向D中滴加稀硫酸,稀硫酸就会与Ba(NO) 反应产生沉淀,随着稀硫酸量的增加,沉
3 2
淀增多,当Ba(NO) 反应完后,沉淀就不再增多,在这里沉淀量的变化情况与NaOH是否和稀硫酸反应没
3 2
有必然的关系,故不能用图示现象判断中和反应是否发生。
7.【答案】B
【解析】若X是Fe,反应的生成物是铜和氯化亚铁;由于铜不能与盐酸反应,故直接用废铜屑进行②③
步操作不能达到实验目的;第②步反应后的溶液中有氯离子,加入硝酸银溶液后会产生白色沉淀,据此现
象不能判断盐酸过量。
8.【答案】D
【解析】首先排除A,铜离子呈蓝色。NH+和OH-反应生成氨气,故B中离子不能大量共存。Ba2+和SO2-反应
4 4
生成白色沉淀,故C中离子不能大量共存。D中离子能共存且溶液为无色,故选D。
9.【答案】A、D
【解析】复分解反应不但要求反应物是两种化合物,而且要具备两种化合物相互交换成分这一基本特征,
例如,CO+2NaOH=NaCO+HO,此反应不是复分解反应,故A错误;置换反应的特征是一种化合物和一种单
2 2 3 2
质反应,生成另一种单质和另一种化合物, B 正确;C 项表述也是正确的,例如,
Ba(OH)+CuSO=Cu(OH)↓+BaSO↓;中和反应不但强调生成物是盐和水,更强调反应物必须是酸和碱,如
2 4 2 4
HCl+NaOH=NaCl+HO,而像金属氧化物和酸的反应以及非金属氧化物和碱的反应,尽管生成物都是盐和水
2
但都不属于中和反应。
10.【答案】BC
【解析】离子间的共存问题,其实质是复分解反应能否发生的问题,离子能共存的条件是复分解反应不
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第5页 共7页让更多的孩子得到更好的教育
能发生的条件。甲厂废水呈碱性,说明OH-在甲厂废水中。因为Cu2+不能与OH-共存,因此Cu2+存在于乙厂
废水中。CO2-不能与Cu2+共存,所以CO2-在甲厂废水中。Ba2+不能与CO2-共存,所以Ba2+应该在乙厂废水
3 3 3
中。因此甲厂废水中含有OH-,CO2-两种阴离子,所以K+应该在甲厂废水中。乙厂废水中含有Cu2+,Ba2+两
3
种阳离子,则NO-应该在乙厂废水中。
3
11.【答案】③ ⑥ KSO+Ba(NO)=BaSO↓+2KNO
2 4 3 2 4 3
④ ⑥ NaCO+Ba(NO)=BaCO↓+2NaNO
2 3 3 2 3 3
① ⑤ CuCl+2NaOH=Cu(OH)↓+2NaCl
2 2
② ⑤ Fe(NO)+3NaOH=Fe(OH)↓+3NaNO
3 3 3 3
① ⑦ CuCl+Zn=ZnCl+Cu
2 2
【解析】解题的关键是记住某些物质的特殊性质,如AgC1、BaSO 都不溶于硝酸,Fe(OH) 为不溶于水的红
4 3
褐色固体,Cu(OH) 为不溶于水的蓝色固体。
2
12.【答案】
(1)①NaOH NaCO ②蒸发结晶
2 3
③NaOH+HCl=NaCl+HO,NaCO+2HCl=2NaCl+HO+CO↑
2 2 3 2 2
(2)C
【解析】(1)除去氯化镁,需引入OH-,但要保证不引入其他杂质离子,即阳离子为Na+,故试剂为氢氧化
钠;同理,除去氯化钙要引入碳酸钠。从食盐溶液中获得精盐晶体应采用蒸发溶剂的方法。溶液中存在剩
余的氢氧化钠和碳酸钠,加入盐酸可将它们除去。(2)向过滤器中倾倒液体时要用玻璃棒引流,并将玻璃
棒靠在三层滤纸处。
13.【答案】[进行实验] CaCO(或碳酸钙)
3
[作出猜想]只有NaCO
2 3
[实验与结论] NaCO 溶液先由无色变成红色,再由红色变成无色
2 3
Ca(OH)+NaHCO=CaCO↓+NaOH+HO
2 3 3 2
【解析】由题意知,Ca(HCO) 在碱溶液(氢氧化钙)中会生成白色沉淀CaCO;分析Ca(OH) 和NaHCO 反
3 2 3 2 3
应后含钠的化合物可能为NaOH或NaCO 或两者的混合物;当加入CaCl 时,有白色沉淀(CaCO)生成,则
2 3 2 3
含钠化合物为NaCO;因滤液显碱性,加入酚酞时溶液显红色,随着盐酸的加入,溶液的红色逐渐褪去,直
2 3
至无色。
14.【答案】[理论分析] H+ Na+
[猜想与假设] 丙 Ba2+与SO2-、CO2-不能共存
4 3
【解析】[理论分析]由于废液pH为12,呈碱性,所以一定不存在的离子是H+;由于NO2-、K+和Na+不会
3
与溶液中的其他离子反应,所以这三种离子在任何条件下都会存在。
[猜想与假设]丙同学的假设一定不成立,原因是Ba2+与SO2-、CO2-不能共存,它们能发生反应生成BaSO
4 3 4
和BaCO 两种沉淀。
3
15.【答案】(1)[猜想](NH)SO(或硫酸铵)
4 2 4
[实验探究](1)④ 2NHCl+Ca(OH)=CaCl+2HO+2NH↑
4 2 2 2 3
[或(NH)SO+Ca(OH)=CaSO+2HO+2NH↑或NHHCO+Ca(OH)=CaCO+2HO+NH↑]
4 2 4 2 4 2 3 4 3 2 3 2 3
(2)HC1(或盐酸) ③
(3)BaCl(或氯化钡) 无白色沉淀
2
【解析】含有NH+的化肥与熟石灰研磨时会放出有刺激性气味的NH,而尿素则没有这种性质;NHHCO
4 3 4 3
与盐酸混合时会放出CO ,(NH)SO 溶液与BaCl 溶液混合会生成BaSO 白色沉淀,而NHCl溶液与BaCl
2 4 2 4 2 4 4 2
溶液混合无沉淀生成。
16.【答案】
解:根据图中信息可知:
与氯化铁反应的氢氧化钠溶液的质量为22 g-16 g=6 g
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第6页 共7页让更多的孩子得到更好的教育
设:20 g该工业盐酸中氯化铁的质量为x。
FeCl + 3NaOH=Fe(OH)↓+3NaCl
3 3
162.5 120
x 6 g×10%
x≈0.82g
该工业盐酸中氯化铁的质量分数为
答:该工业盐酸中氯化铁的质量分数为4.1%。
地址:北京市西城区新德街20号4层 电话:010-82025511 传真:010-82079687 第7页 共7页