文档内容
石嘴山市第一中学 2025-2026 学年第一学期高三年级
月考 化学试题
一、单选题
1. 材料是人类赖以生存和发展的物质基础,下列说法正确的是
A. 岩彩壁画颜料所用贝壳粉,主要成分属于硅酸盐
B. 油画颜料调和剂所用核桃油,属于有机高分子
C. 竹胎漆画颜料赭石的主要成分氧化铁,耐酸、碱
D. 尼龙 66 由己二酸和己二胺缩聚合成,强度高、韧性好
【答案】D
【解析】
【详解】A.贝壳粉主要成分为碳酸钙,属于碳酸盐而非硅酸盐,A 错误;
B.核桃油属于油脂,相对分子质量较小,不属于有机高分子,B 错误;
C.氧化铁( )易与酸反应生成盐和水,不耐酸,C 错误;
D.尼龙 66 由己二酸和己二胺缩聚形成聚酰胺,具有高强度和高韧性,D 正确;
故选 D。
2. 诗词既能赋情,也能承载科学。下列古诗词中不涉及氧化还原反应的是
A. 野火烧不尽,春风吹又生——(唐·白居易《草·赋得古原草送别》)
B. 朱门酒肉臭,路有冻死骨——(唐·杜甫《自京赴奉先县咏怀五百字》)
C. 遥知不是雪,为有暗香来——(北宋·王安石《梅花》)
D. 何意百炼钢,化为绕指柔——(西晋·刘琨《重赠卢谌》)
【答案】C
【解析】
【详解】A.野火烧草涉及燃烧反应,碳和氧的化合价变化,属于氧化还原反应,A 错误;
B.酒肉腐败是有机物分解,涉及氧化反应,存在化合价变化,属于氧化还原反应,B 错误;
C.暗香来是分子扩散的物理过程,无化学变化,不涉及氧化还原反应,C 正确;
D.百炼钢是碳被氧化的过程,碳的化合价升高,属于氧化还原反应,D 错误;
故答案选 C。
3. 下列陈述 I 与陈述 II 不存在因果关系的是
第 1页/共 19页选项 陈述 I 陈述 II
A 稳定性: 键能:H-O>H-S
B 沸点:乙醇>乙醛 相对分子质量:乙醇>乙醛
酸性:
C 电负性:F>Cl
碱性:
D 金属性:Na>Mg
A. A B. B C. C D. D
【答案】B
【解析】
【详解】A.氢化物分子中共价键的键能越大,说明共价键越强,分子越稳定,由氢氧键的键能强于氢硫键
可知,水分子的稳定性强于硫化氢,故 A 正确;
B.乙醇能形成分子间氢键,乙醛不能形成分子间氢键,所以乙醇的分子间作用力强于乙醛,沸点高于乙醛,
故 B 错误;
C.氟原子和氯原子都是吸电子基,氟元素 电负性大于氯元素,则三氟乙酸分子的羧基中氢氧键的极性强
于三氯乙酸,电离出氢离子的能力强于三氯乙酸,酸性强于三氯乙酸,故 C 正确;
D.金属元素的金属性越强,最高价氧化物对应水化物的碱性越强,钠元素的金属性强于镁元素,则氢氧化
钠的碱性强于氢氧化镁,故 D 正确;
故选 B。
4. 为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下, 中原子的数目为
B. 所含中子的数目为
C. 粉和足量 完全反应,转移电子的数目为
D. 乙酸与足量乙醇反应,生成乙酸乙酯分子的数目为
第 2页/共 19页【答案】B
【解析】
【详解】A.标准状况下, 不是气体,不能用气体摩尔体积计算原子数,A 错误;
B. 的中子数为 14−6=8, 含 个中子,B 正确;
C.32 g Cu(0.5 mol)与 S 反应生成 ,每 1 mol Cu 转移 1 mol 电子,总转移电子数为 0.5 ,C 错
误;
D.酯化反应为可逆反应, 乙酸与足量乙醇反应无法完全生成 0.1 mol 乙酸乙酯,D 错误;
故答案选 B。
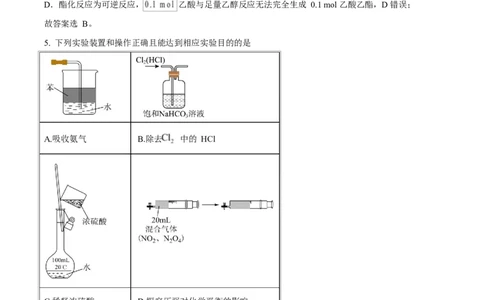
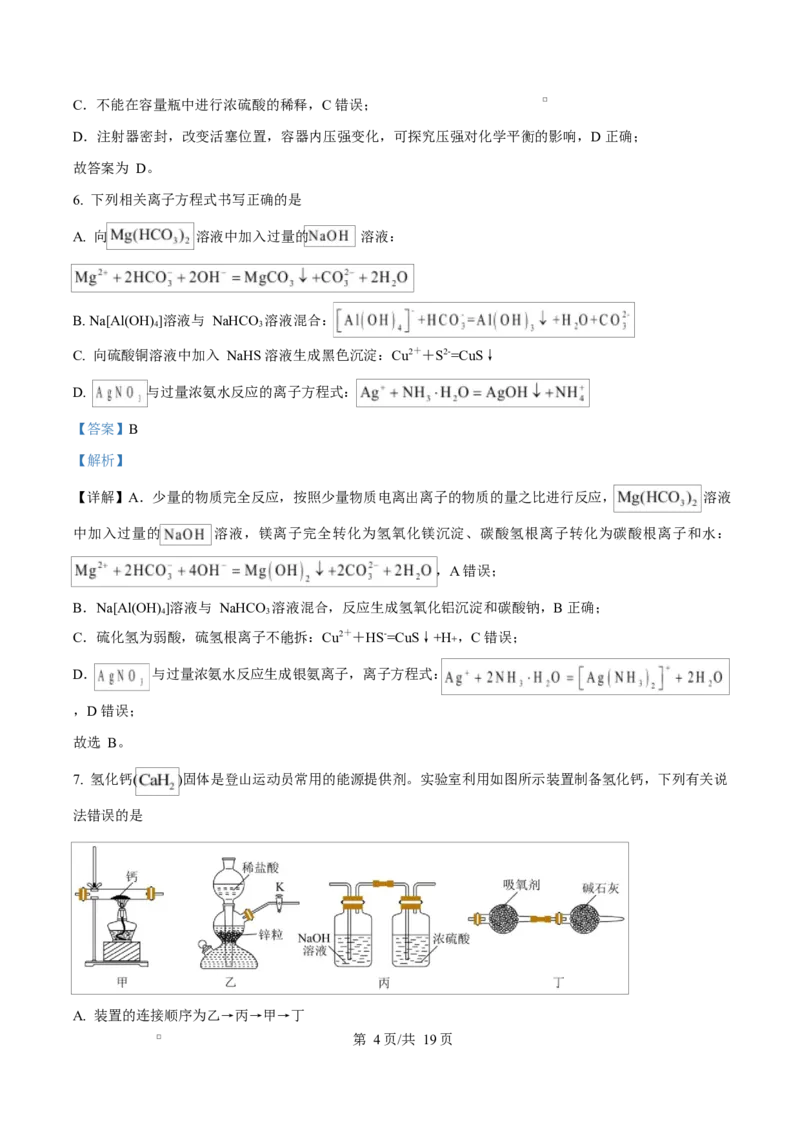
5. 下列实验装置和操作正确且能达到相应实验目的的是
A.吸收氨气 B.除去 中的 HCl
C.稀释浓硫酸 D.探究压强对化学平衡的影响
A. A B. B C. C D. D
【答案】D
【解析】
【详解】A.氨气极易溶于水,将氨气直接通入水中会发生倒吸,A 错误;
B.氯化氢与碳酸氢钠反应生成二氧化碳,引入新杂质,达不到除杂目的,B 错误;
第 3页/共 19页C.不能在容量瓶中进行浓硫酸的稀释,C 错误;
D.注射器密封,改变活塞位置,容器内压强变化,可探究压强对化学平衡的影响,D 正确;
故答案为 D。
6. 下列相关离子方程式书写正确的是
A. 向 溶液中加入过量的 溶液:
B. Na[Al(OH) ]溶液与 NaHCO 溶液混合:
4 3
C. 向硫酸铜溶液中加入 NaHS 溶液生成黑色沉淀:Cu2++S2-=CuS↓
D. 与过量浓氨水反应的离子方程式:
【答案】B
【解析】
【详解】A.少量的物质完全反应,按照少量物质电离出离子的物质的量之比进行反应, 溶液
中加入过量的 溶液,镁离子完全转化为氢氧化镁沉淀、碳酸氢根离子转化为碳酸根离子和水:
,A 错误;
B.Na[Al(OH)]溶液与 NaHCO 溶液混合,反应生成氢氧化铝沉淀和碳酸钠,B 正确;
4 3
C.硫化氢为弱酸,硫氢根离子不能拆:Cu2++HS-=CuS↓+H+ ,C 错误;
D. 与过量浓氨水反应生成银氨离子,离子方程式:
,D 错误;
故选 B。
7. 氢化钙( )固体是登山运动员常用的能源提供剂。实验室利用如图所示装置制备氢化钙,下列有关说
法错误的是
A. 装置的连接顺序为乙→丙→甲→丁
第 4页/共 19页B. 装置丁作用是防止外界空气中的水蒸气及氧气与钙或 CaH 反应
2
C. 实验时,应先点燃硬质玻璃管下方 酒精灯,再通氢气
D. 若使甲装置中 20.0g 钙完全转化为氢化钙,则需氢气的体积大于 11.2L(标准状况)
【答案】C
【解析】
【分析】甲装置属于发生装置,装置乙制备氢气,装置丙净化氢气,装置丁防止空气中进入装置甲中,据
此解答。
【详解】A.根据以上分析可知装置的连接顺序为乙→丙→甲→丁,A 正确;
B.钙是活泼的金属,极易和氧气、水等反应,所以装置丁作用是防止外界空气中的水蒸气及氧气与钙或
CaH 反应,B 正确;
2
C.氢气是可燃性气体,需要验纯,所以实验时,应先通氢气,排尽装置中的空气并验纯后,再点燃硬质玻
璃管下方的酒精灯,C 错误;
D.由于需要氢气排尽装置中的空气,所以实际需要氢气的量大于理论值,即若使甲装置中 20.0g 钙完全转
化为氢化钙,则需氢气的体积大于 11.2L(标准状况),D 正确;
答案选 C。
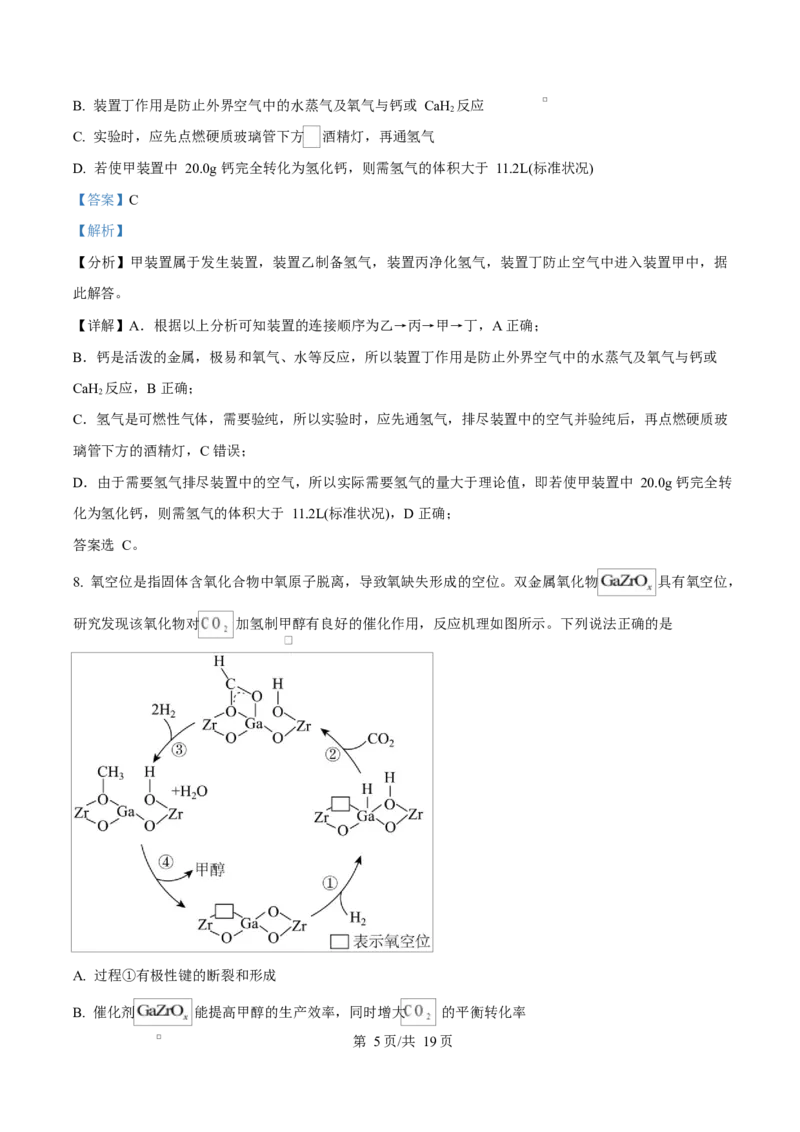
8. 氧空位是指固体含氧化合物中氧原子脱离,导致氧缺失形成的空位。双金属氧化物 具有氧空位,
研究发现该氧化物对 加氢制甲醇有良好的催化作用,反应机理如图所示。下列说法正确的是
A. 过程①有极性键的断裂和形成
B. 催化剂 能提高甲醇的生产效率,同时增大 的平衡转化率
第 5页/共 19页C. 氧空位的存在有利于捕获
D. 催化过程中,Ga 元素的化合价未发生变化
【答案】C
【解析】
【详解】A.过程①为 H 与催化剂作用,断裂 H-H 非极性键,形成 O-H 极性键,只涉及非极性键断裂和极
2
性键形成,无极性键断裂,A 错误;
B.催化剂能加快反应速率,提高生产效率,但不影响化学平衡,不能增大 CO 的平衡转化率,B 错误;
2
C.氧空位(□)可通过吸附或结合 CO 分子(如 CO 中的 O 原子填补空位),有利于捕获 CO,C 正确;
2 2 2
D.CO 加氢制甲醇为氧化还原反应(C 从+4→-2,H 从 0→+1),Ga 作为催化剂可能参与电子转移,化合
2
价发生变化后再生,D 错误;
故选 C。
9. 用 和侯氏制碱工艺联合制 ,同时 、 循环利用的主要物质转化如下。下列说法
正确的是
A. ①中应向 溶液先通入 ,再通入
B. ②中可使用蒸发结晶的方法获得 固体
C. 电解 的溶液可以制得 和
D. 理论上①中消耗的 与③中生成的 不相等
【答案】D
【解析】
【分析】向饱和食盐水先通入溶解度大的氨气、再通入二氧化碳,二氧化碳与氨化的饱和食盐水反应生成
碳酸氢钠沉淀和氯化铵,过滤得到碳酸氢钠固体和含有氯化铵的滤液(步骤①);向滤液中加入氯化钠固体,
降低氯化铵固体的溶解度使氯化铵固体析出,过滤得到母液和氯化铵固体(步骤②);将氯化铵固体溶于水,
第 6页/共 19页向其中加入碳酸镁,反应生成氯化镁、氨气和二氧化碳(步骤③)。
【详解】A.二氧化碳微溶于水,氨气极易溶于水,饱和食盐水中先通入的气体为氨气,通氨气后再通二氧
化碳,可增大二氧化碳的溶解度,故 A 错误;
B.NH Cl 受热易分解,不能通过蒸发结晶的方法获得 NH Cl 固体,故 B 错误;
4 4
C.电解 MgCl 溶液产生氯气、氢气和氢氧化镁,故 C 错误;
2
D.①中反应方程式为 NH +CO +NaCl+HO=NH Cl+NaHCO ↓, ,③中反应方程式为 MgCO
3 2 2 4 3 3
+2NHCl=MgCl +2NH↑+CO ↑+H O, ,故 D 正确;
4 2 3 2 2
故答案为 D。
10. 下列物质的性质与用途不具有对应关系的是
A. 金属钠具有强还原性,可与 反应制取 Ti
B. 铁粉能与 反应,可用作食品保存的吸氧剂
C. 溶液具有碱性,可用于环境消毒
D. 聚合硫酸铁能水解并形成胶体,可用于净水
【答案】C
【解析】
【详解】A.钠的强还原性使其能还原 TiCl 制取 Ti,A 正确;
4
B.铁粉与 O 反应消耗氧气,符合吸氧剂原理,B 正确;
2
C.NaClO 的消毒主要依赖 HClO 的强氧化性,而非碱性,性质与用途无直接关联,C 错误;
D.水解形成胶体吸附杂质是净水的关键,D 正确;
故选 C。
11. 有关下列实验装置能达到实验目的的是
第 7页/共 19页A. 甲装置:0.1000mol/L 的标准 溶液滴定未知浓度 溶液
B. 乙装置:启停自如地制备
C. 丙装置:观察钾元素的焰色
D. 丁装置:检验 中是否混有
【答案】D
【解析】
【详解】A.高锰酸钾溶液可以氧化橡胶,不能选图中的碱式滴定管,应选择酸式滴定管,A 错误;
B.过氧化钠为粉末,与水接触后不能分离,不能关闭活塞使反应停止,B 错误;
C.观察 K 的焰色需要透过蓝色钴玻璃,不能直接观察,C 错误;
D.酸性高锰酸钾可与二氧化硫反应从而除去二氧化硫,品红溶液可以检验二氧化硫是否除尽,如果品红不
褪色,澄清石灰水变浑浊即可说明二氧化碳的存在,D 正确;
故答案选 D。
12. 标准状态下,CH=CHCH(g)与 HCl(g)反应生成 CHCHCICH (g)和 CHCHCHCl(g)的反应历程如图所
2 3 3 3 3 2 2
示。下列说法正确的是
A.
B. 其他条件不变,加入适量 Cl-(g)可以有效加快历程 I、Ⅱ
C. 选择性: >
D. 历程 I 第一步反应的热化学方程式为:
【答案】C
【解析】
【详解】A. 为反应物总能量, 、 分别为历程Ⅰ、Ⅱ产物的能量,因两产物能量不同( ),
第 8页/共 19页则 ,A 错误;
B.历程Ⅰ、Ⅱ的决速步为碳正离子中间体的形成( 进攻双键), 不参与该步反应,加入 对反
应速率无显著影响,B 错误;
C.历程Ⅰ生成 ,中间体为稳定的仲碳正离子( ),活化能低;历程Ⅱ生成
,中间体为不稳定的伯碳正离子( ),活化能高。活化能低的反应优先进
行,故选择性 > ,C 正确;
D.历程Ⅰ第一步反应的热化学方程式为:
,D 错误;
故选 C
13. 25℃时,用 0.1 KOH 溶液滴定同浓度的 溶液, 被滴定分数 与 pH 值、
微粒分布分数 [ ,X 表示 、 或 ]的关系如图所示,下
列说法正确的是
A. 25℃时, 第二步电离平衡常数
B. 点对应的 pH 值约为 2
C. 点溶液中:
D. 、 两点溶液中水的电离程度:
【答案】D
第 9页/共 19页【解析】
【详解】A.HA 的第二步电离平衡常数 = 。当δ(HA⁻)=δ(A²⁻)时,c(HA-) =c(A2-),则
2
=c(H⁺),此时 pH= 。图像中 HA⁻与 A2⁻分布分数曲线交点(c 点)对应的 pH 约为 7,故
,A 错误;
B.根据图像估算 (a 点 pH≈4),
(c 点 pH≈7),则 ,
由 e 点可知 ,则 ,B 错误;
C.c 点时,HA 被滴定分数为 1.5,此时溶液中溶质为等物质的量的 KHA 和 KA,根据物料守恒,2c
2 2
(K⁺)=3[c(H
2
A)+c(HA⁻)+c(A2⁻)],所以 2c(K⁺)>3c(HA⁻),c 点溶液中,c(HA⁻)=c(A2⁻),pH=7,c(H+)=c(OH-),
根据电荷守恒,c(K⁺)+c(H+)=c(OH-)+c(HA⁻)+2c(A2⁻),所以 c(K⁺)=3c(HA⁻),C 错误;
D.c 点为 HA⁻与 A2⁻共存溶液,d 点 A2⁻浓度更大(滴定分数更高)。A2⁻水解促进水的电离,浓度越大对水
电离的促进作用越强,故水的电离程度 c < d,D 正确;
故选 D。
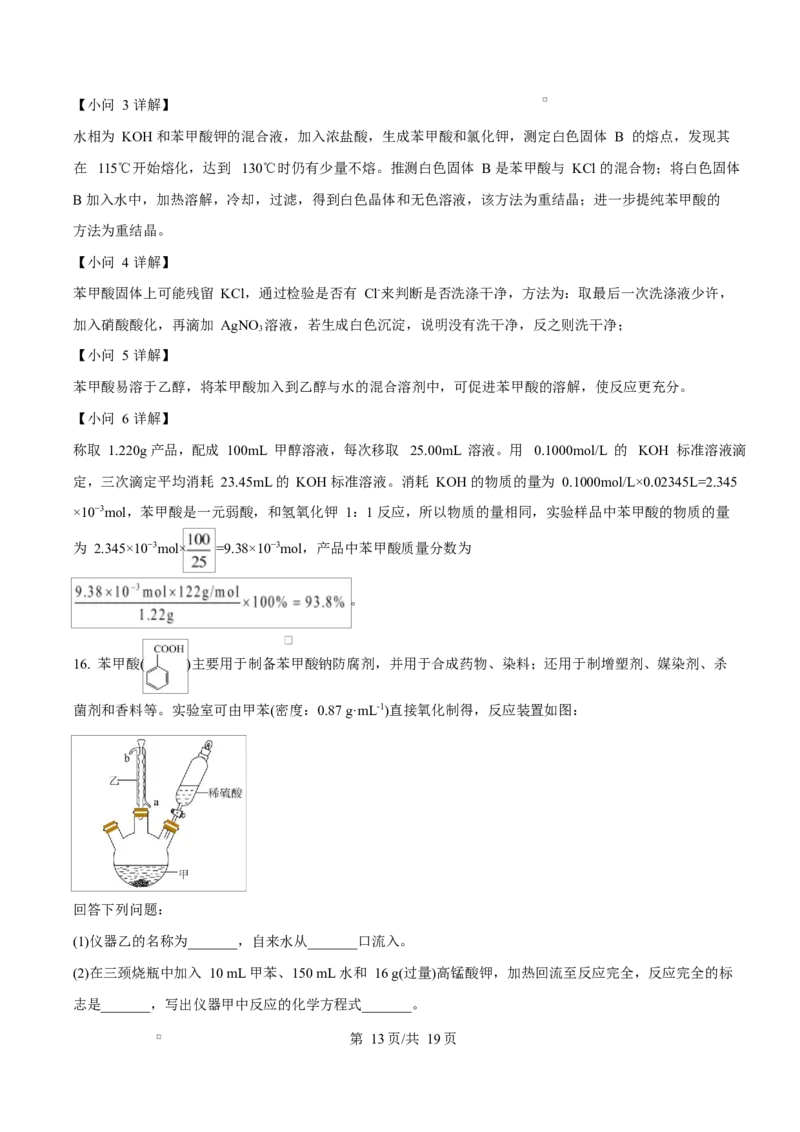
14. 甲、乙、丙三种有机物在一定条件下可实现下列转化,下列有关说法错误的是
A. 甲是一种具有两性的芳香烃
B. 乙在工业生产中可用作抗氧化剂
C. 可用碳酸氢钠溶液检验甲是否完全反应
D. 1mol 丙最多能与 7molH 发生加成反应
2
【答案】A
【解析】
【详解】A.甲的结构中含有羧基和氨基,具有两性,但芳香烃仅含 C、H 元素,而甲含 N、O 元素,不属
于芳香烃,故 A 错误;
第 10页/共 19页B.乙含多个酚羟基,酚羟基易被氧化,可作为抗氧化剂,故 B 正确;
C.甲含羧基,能与 NaHCO 反应生成 CO 气体,丙中无羧基不反应,可用 NaHCO 溶液检验甲是否完全
3 2 3
反应,故 C 正确;
D.丙含 2 个苯环和 1 个羰基,所以 1mol 丙最多与 7mol H₂加成,故 D 正确;
选 A。
二、非选择题
15. 苯甲酸广泛应用于制药和化工行业,实验室可通过甲苯氧化制苯甲酸。
反应原理:
制备装置及相关信息:
苯甲酸
相对分子质量 122
熔点 122.4℃
25℃:
0.3g
水中溶解度
95℃:
6.9g
实验方法:将甲苯和 KMnO 溶液加热回流一段时间后停止反应,按如下流程分离出苯甲酸和回收未反应的
4
甲苯。
第 11页/共 19页(1)制备装置中仪器 a 的名称为_______,主要作用是_______。
(2)操作Ⅰ为_______,操作Ⅱ为_______,无水 NaSO 的作用是_______,无色液体 A 是_______。
2 4
(3)测定白色固体 B 的熔点,发现其在 115℃开始熔化,达到 130℃时仍有少量不熔。推测白色固体 B
是苯甲酸与 _______的混合物,进一步提纯苯甲酸的方法为_______。
(4)提纯时,往往要洗涤苯甲酸,检验苯甲酸是否洗涤干净的操作是 _______。
(5)将苯甲酸加入到乙醇与水的混合溶剂中,充分溶解后,加入 Cu(OH) 搅拌,过滤,滤液静置一段时间,
2
可获得有机合成常用的催化剂苯甲酸铜,混合溶剂中乙醇的作用是_______ 。
(6)称取 1.220g 产品,配成 100mL 甲醇溶液,每次移取 25.00mL 溶液。用 0.1000mol/L 的 KOH 标准
溶液滴定,三次滴定平均消耗 23.45mL 的 KOH 标准溶液。产品中苯甲酸质量分数为_______(保留三位有效
数字)。
【答案】(1) ①. 球形冷凝管 ②. 冷凝回流
(2) ①. 分液 ②. 蒸馏 ③. 除水 ④. 甲苯
(3) ①. KCl ②. 重结晶
(4)取最后一次洗涤液少许,加入硝酸酸化,再滴加 AgNO 溶液,若生成白色沉淀,说明没有洗干净,反
3
之则洗干净
(5)苯甲酸易溶于乙醇,将苯甲酸加入到乙醇与水的混合溶剂中,可促进苯甲酸的溶解,使反应更充分
(6)93.8%
【解析】
【分析】一定量的甲苯和适量的 KMnO 溶液在 100℃反应一段时间后停止反应,按如图流程分离出苯甲酸
4
和回收未反应的甲苯,苯甲酸能溶于水,甲苯不溶于水,互不相溶的液体采用分液方法分离,有机相中含
有甲苯、水相中含有苯甲酸钾,有机相中的甲苯采用蒸馏方法得到无色液体 A,A 是甲苯;水相为 KOH 和
苯甲酸钾的混合液,加入浓盐酸,经蒸发浓缩、冷却结晶、过滤得白色固体 B 为苯甲酸和 KCl 的混合物。
【小问 1 详解】
根据装置图,制备装置中仪器 a 的名称为球形冷凝管,主要作用是冷凝回流。
【小问 2 详解】
操作Ⅰ把有机层和水层分开,则操作Ⅰ为分液;操作Ⅱ为有机相中分离出甲苯,方法为蒸馏,无水 NaSO
2 4
干燥剂,作用是除水,无色液体 A 是甲苯。
第 12页/共 19页【小问 3 详解】
水相为 KOH 和苯甲酸钾的混合液,加入浓盐酸,生成苯甲酸和氯化钾,测定白色固体 B 的熔点,发现其
在 115℃开始熔化,达到 130℃时仍有少量不熔。推测白色固体 B 是苯甲酸与 KCl 的混合物;将白色固体
B 加入水中,加热溶解,冷却,过滤,得到白色晶体和无色溶液,该方法为重结晶;进一步提纯苯甲酸的
方法为重结晶。
【小问 4 详解】
苯甲酸固体上可能残留 KCl,通过检验是否有 Cl-来判断是否洗涤干净,方法为:取最后一次洗涤液少许,
加入硝酸酸化,再滴加 AgNO 溶液,若生成白色沉淀,说明没有洗干净,反之则洗干净;
3
【小问 5 详解】
苯甲酸易溶于乙醇,将苯甲酸加入到乙醇与水的混合溶剂中,可促进苯甲酸的溶解,使反应更充分。
【小问 6 详解】
称取 1.220g 产品,配成 100mL 甲醇溶液,每次移取 25.00mL 溶液。用 0.1000mol/L 的 KOH 标准溶液滴
定,三次滴定平均消耗 23.45mL 的 KOH 标准溶液。消耗 KOH 的物质的量为 0.1000mol/L×0.02345L=2.345
×10−3mol,苯甲酸是一元弱酸,和氢氧化钾 1:1 反应,所以物质的量相同,实验样品中苯甲酸的物质的量
为 2.345×10−3mol× =9.38×10−3mol,产品中苯甲酸质量分数为
。
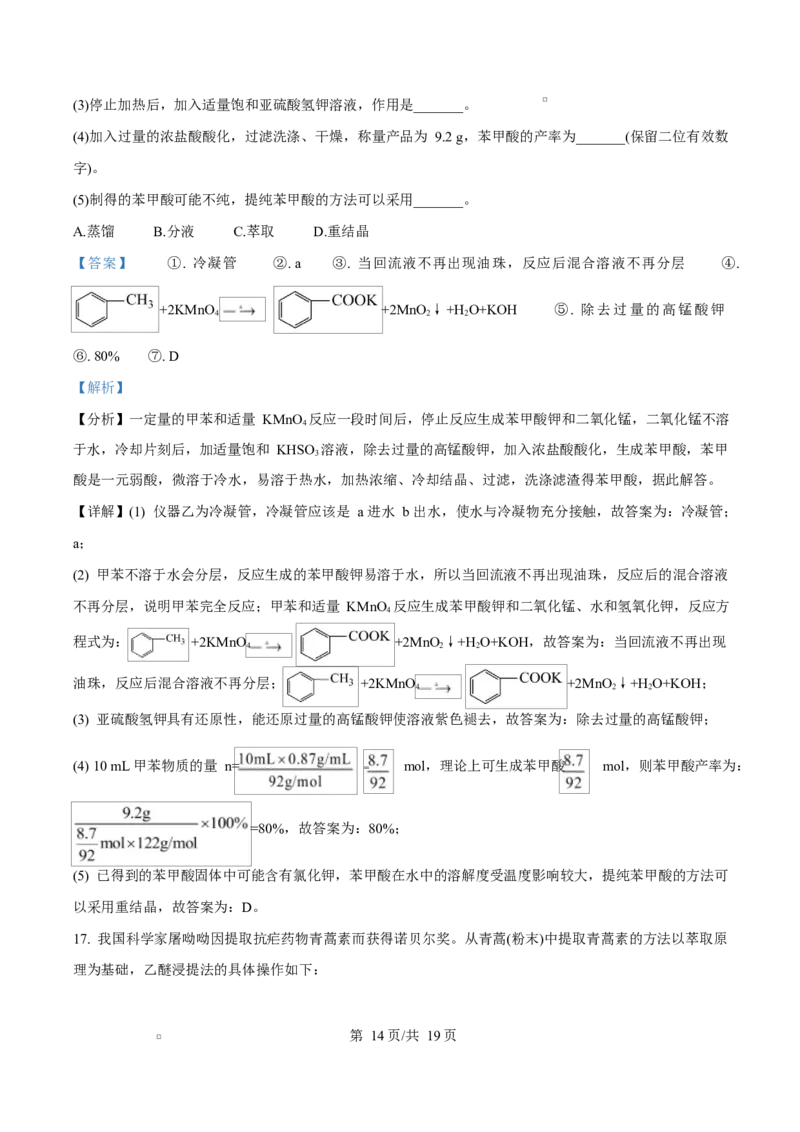
16. 苯甲酸( )主要用于制备苯甲酸钠防腐剂,并用于合成药物、染料;还用于制增塑剂、媒染剂、杀
菌剂和香料等。实验室可由甲苯(密度:0.87 g·mL-1)直接氧化制得,反应装置如图:
回答下列问题:
(1)仪器乙的名称为_______,自来水从_______口流入。
(2)在三颈烧瓶中加入 10 mL 甲苯、150 mL 水和 16 g(过量)高锰酸钾,加热回流至反应完全,反应完全的标
志是_______,写出仪器甲中反应的化学方程式_______。
第 13页/共 19页(3)停止加热后,加入适量饱和亚硫酸氢钾溶液,作用是_______。
(4)加入过量的浓盐酸酸化,过滤洗涤、干燥,称量产品为 9.2 g,苯甲酸的产率为_______(保留二位有效数
字)。
(5)制得的苯甲酸可能不纯,提纯苯甲酸的方法可以采用_______。
A.蒸馏 B.分液 C.萃取 D.重结晶
【答案】 ①. 冷凝管 ②. a ③. 当回流液不再出现油珠,反应后混合溶液不再分层 ④.
+2KMnO +2MnO↓+H O+KOH ⑤. 除去过量的高锰酸钾
4 2 2
⑥. 80% ⑦. D
【解析】
【分析】一定量的甲苯和适量 KMnO 反应一段时间后,停止反应生成苯甲酸钾和二氧化锰,二氧化锰不溶
4
于水,冷却片刻后,加适量饱和 KHSO 溶液,除去过量的高锰酸钾,加入浓盐酸酸化,生成苯甲酸,苯甲
3
酸是一元弱酸,微溶于冷水,易溶于热水,加热浓缩、冷却结晶、过滤,洗涤滤渣得苯甲酸,据此解答。
【详解】(1) 仪器乙为冷凝管,冷凝管应该是 a 进水 b 出水,使水与冷凝物充分接触,故答案为:冷凝管;
a;
(2) 甲苯不溶于水会分层,反应生成的苯甲酸钾易溶于水,所以当回流液不再出现油珠,反应后的混合溶液
不再分层,说明甲苯完全反应;甲苯和适量 KMnO 反应生成苯甲酸钾和二氧化锰、水和氢氧化钾,反应方
4
程式为: +2KMnO +2MnO↓+H O+KOH,故答案为:当回流液不再出现
4 2 2
油珠,反应后混合溶液不再分层; +2KMnO +2MnO↓+H O+KOH;
4 2 2
(3) 亚硫酸氢钾具有还原性,能还原过量的高锰酸钾使溶液紫色褪去,故答案为:除去过量的高锰酸钾;
(4) 10 mL 甲苯物质的量 n= = mol,理论上可生成苯甲酸 mol,则苯甲酸产率为:
=80%,故答案为:80%;
(5) 已得到的苯甲酸固体中可能含有氯化钾,苯甲酸在水中的溶解度受温度影响较大,提纯苯甲酸的方法可
以采用重结晶,故答案为:D。
17. 我国科学家屠呦呦因提取抗疟药物青蒿素而获得诺贝尔奖。从青蒿(粉末)中提取青蒿素的方法以萃取原
理为基础,乙醚浸提法的具体操作如下:
第 14页/共 19页已知:青蒿素为白色针状晶体,易溶于乙醇、乙醚、苯和汽油等有机溶剂,不溶于水,熔点为 156~157℃,
沸点为 389.9℃,热稳定性差。屠呦呦团队经历了使用不同溶剂和不同温度的探究过程,实验结果如下:
溶剂 水 乙醇 乙醚
沸点/℃ 100 78 35
几乎
提取效率 35% 95%
为 0
(1)用水作溶剂,提取无效 原因可能是___________。
(2)研究发现,青蒿素分子中的某个基团对热不稳定。分析用乙醚作溶剂,提取效率高于乙醇的原因是
___________。
(3)下列说法不正确的是___________。
A. 粉碎的目的是增大青蒿与乙醚的接触面积,提高青蒿素浸取率
B. 操作 I 需要用到玻璃仪器有漏斗、玻璃棒、烧杯
C. 操作Ⅱ蒸馏时最好选用水浴加热
D. 操作Ⅲ的主要过程为加水溶解、蒸发浓缩、冷却结晶、过滤
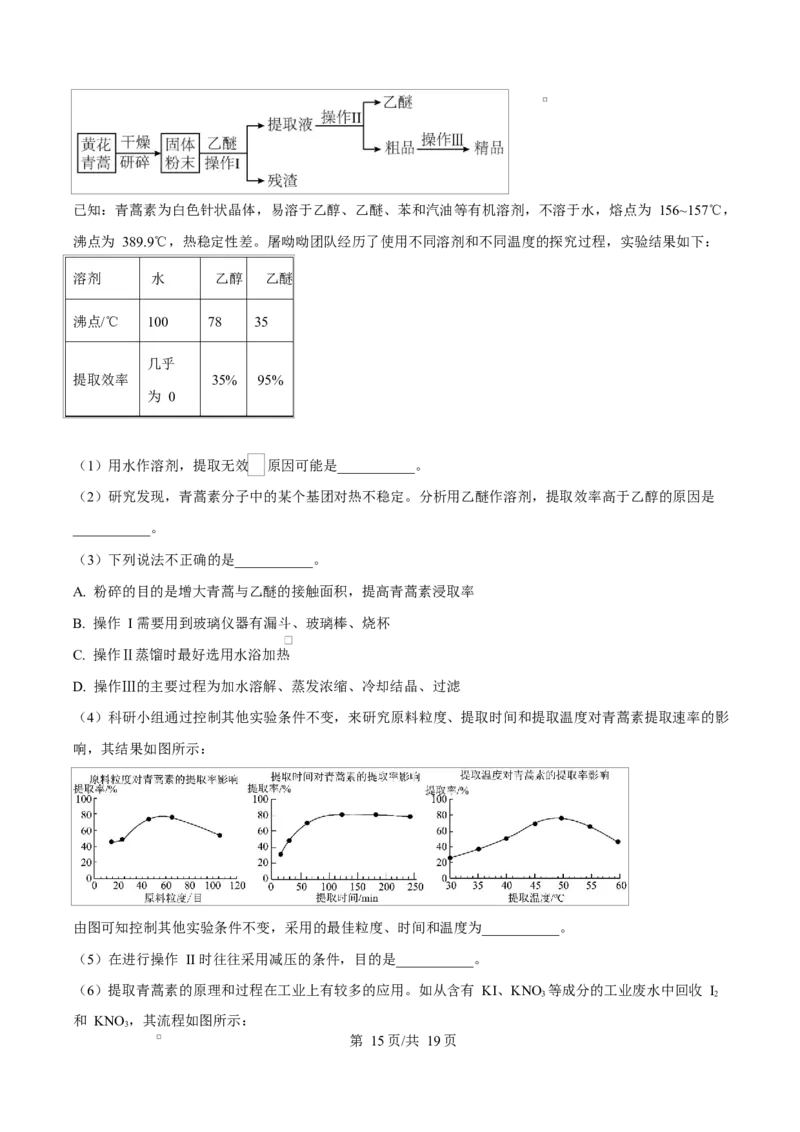
(4)科研小组通过控制其他实验条件不变,来研究原料粒度、提取时间和提取温度对青蒿素提取速率的影
响,其结果如图所示:
由图可知控制其他实验条件不变,采用的最佳粒度、时间和温度为___________。
(5)在进行操作 II 时往往采用减压的条件,目的是___________。
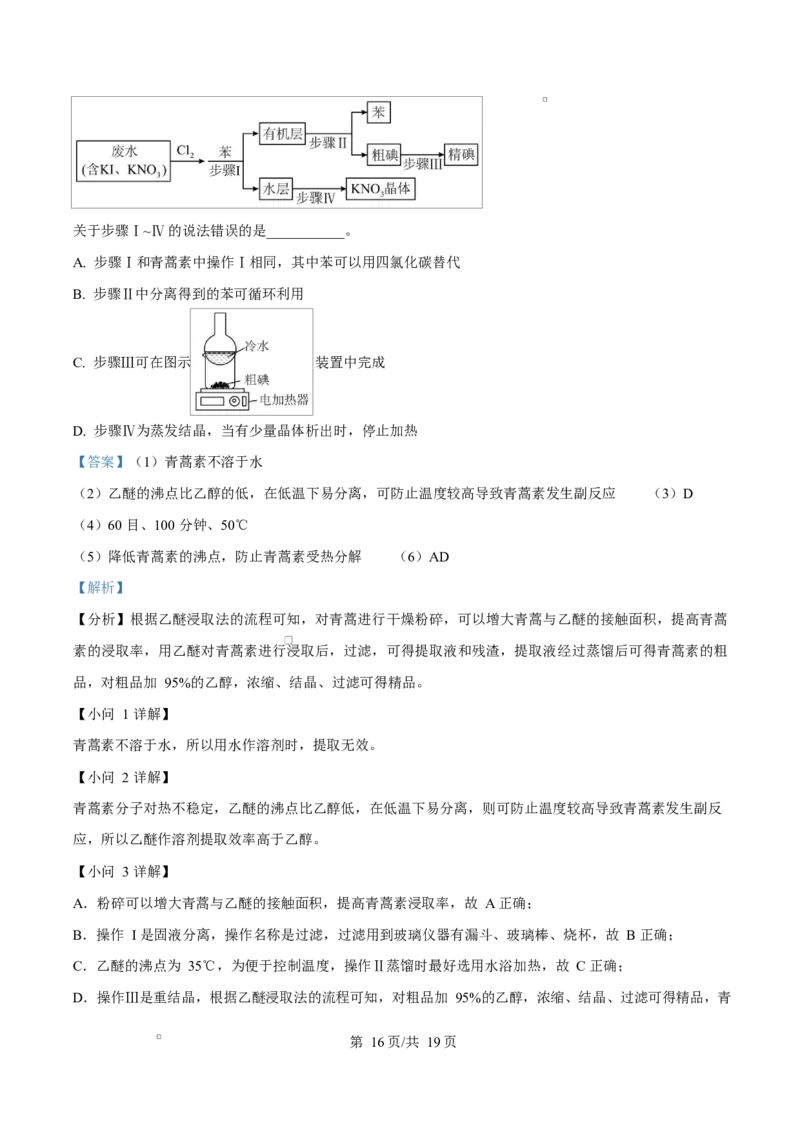
(6)提取青蒿素的原理和过程在工业上有较多的应用。如从含有 KI、KNO 等成分的工业废水中回收 I
3 2
和 KNO,其流程如图所示:
3
第 15页/共 19页关于步骤Ⅰ~Ⅳ的说法错误的是___________。
A. 步骤Ⅰ和青蒿素中操作Ⅰ相同,其中苯可以用四氯化碳替代
B. 步骤Ⅱ中分离得到的苯可循环利用
C. 步骤Ⅲ可在图示 装置中完成
D. 步骤Ⅳ为蒸发结晶,当有少量晶体析出时,停止加热
【答案】(1)青蒿素不溶于水
(2)乙醚的沸点比乙醇的低,在低温下易分离,可防止温度较高导致青蒿素发生副反应 (3)D
(4)60 目、100 分钟、50℃
(5)降低青蒿素的沸点,防止青蒿素受热分解 (6)AD
【解析】
【分析】根据乙醚浸取法的流程可知,对青蒿进行干燥粉碎,可以增大青蒿与乙醚的接触面积,提高青蒿
素的浸取率,用乙醚对青蒿素进行浸取后,过滤,可得提取液和残渣,提取液经过蒸馏后可得青蒿素的粗
品,对粗品加 95%的乙醇,浓缩、结晶、过滤可得精品。
【小问 1 详解】
青蒿素不溶于水,所以用水作溶剂时,提取无效。
【小问 2 详解】
青蒿素分子对热不稳定,乙醚的沸点比乙醇低,在低温下易分离,则可防止温度较高导致青蒿素发生副反
应,所以乙醚作溶剂提取效率高于乙醇。
【小问 3 详解】
A.粉碎可以增大青蒿与乙醚的接触面积,提高青蒿素浸取率,故 A 正确;
B.操作 I 是固液分离,操作名称是过滤,过滤用到玻璃仪器有漏斗、玻璃棒、烧杯,故 B 正确;
C.乙醚的沸点为 35℃,为便于控制温度,操作Ⅱ蒸馏时最好选用水浴加热,故 C 正确;
D.操作Ⅲ是重结晶,根据乙醚浸取法的流程可知,对粗品加 95%的乙醇,浓缩、结晶、过滤可得精品,青
第 16页/共 19页蒿素不溶于水,不能用水溶解青蒿素粗品,故 D 错误;
故选 D。
【小问 4 详解】
由图可知控制其他实验条件不变,粒度为 60 目时青蒿素提取率最高,提取时间为 100min 时提取率达到最
大值,提取温度为 50℃时青蒿素提取率最高,所以采用的最佳粒度、时间和温度为 60 目、100min、50℃。
【小问 5 详解】
青蒿素热稳定性差,在进行操作 II 时往往采用减压的条件是因为:降低青蒿素的沸点,防止青蒿素受热分
解。
【小问 6 详解】
A.由分析可知,步骤Ⅰ是萃取操作,青蒿素中操作Ⅰ为过滤,故 A 错误;
B.步骤Ⅱ分离得到的苯可在步骤 I 中循环使用,故 B 正确;
C.受热时碘升华变为碘蒸气,遇到盛有冷水的烧瓶,会在烧瓶外壁又凝华析出,从而达到提纯碘的目的,
故 C 正确;
D.由于硝酸钾溶解度随温度变化幅度较大,故制备硝酸钾晶体,应采用蒸发浓缩,冷却结晶的方法,而不
是蒸发结晶,故 D 错误;
故选 AD。
18. 乙酰水杨酸(阿司匹林)是目前常用药物之一,实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如
下:
水杨酸 醋酸酐 乙酰水杨酸
熔点/℃ 157~159 -72~-74 135~138
相对密度/(g·cm-3) 1.44 1.10 1.35
相对分子质量 138 102 180
实验过程: 100 mL 锥形瓶中加入水杨酸 6.9 g 及醋酸酐 10 mL,充分摇动使固体完全溶解。缓慢滴加 0.5
mL 浓硫酸后加热,维持瓶内温度在 70℃ 左右,充分反应。稍冷后进行如下操作:
①在不断搅拌下将反应后的混合物倒入 100 mL 冷水中,析出固体,过滤;
第 17页/共 19页②所得结晶粗品加入 50 mL 饱和碳酸氢钠溶液,溶解、过滤;
③滤液用浓盐酸酸化后冷却、过滤得固体;
④固体经纯化得白色的乙酰水杨酸晶体 5.4 g;
回答下列问题:
(1)该合成反应中应采用___________加热(填字母)。
A. 热水浴 B. 酒精灯 C. 煤气灯 D. 电炉
(2)①中需使用冷水,目的是___________。
(3)②中饱和碳酸氢钠的作用是___________,以便过滤除去难溶杂质。
(4)④采用的纯化方法为___________。
(5)本实验的产率是___________%。
【答案】(1)A (2)充分析出乙酰水杨酸固体(结晶)
(3)生成可溶的乙酰水杨酸钠
(4)重结晶 (5)60
【解析】
【分析】水杨酸与醋酸酐在浓硫酸作用下水浴加热至 70℃左右,发生取代反应,生成乙酰水杨酸。
【小问 1 详解】
该反应的温度应控制在 70℃左右,所以应采用热水浴加热,故答案为:A;
【小问 2 详解】
温度降低,乙酰水杨酸晶体的溶解度减小,所以操作①中使用冷水的目的是降低乙酰水杨酸的溶解度,使
其充分结晶析出;
【小问 3 详解】
②中饱和 NaHCO 的作用是与乙酰水杨酸反应生成乙酰水杨酸钠,乙酰水杨酸钠能溶于水,以便过滤除去
3
其他难溶性杂质;
【小问 4 详解】
乙酰水杨酸的溶解度随温度变化较大,故可利用重结晶的方法来纯化得到乙酰水杨酸晶体;
【小问 5 详解】
由表中及题中数据分析可知,加入的水杨酸少量,6.9g 水杨酸的物质的量为 0.05mol,由方程式 (水
杨酸)+(CH CO) O (乙酰水杨酸)+CH COOH 可知,1mol 水杨酸与过量醋酸酐反应生
3 2 3
第 18页/共 19页成 1mol 乙酰水杨酸,则 0.05mol 水杨酸参与反应得到 0.05mol 乙酰水杨酸,其质量为 0.05mol×180g/mol=9.0g,
所以乙酰水杨酸的产率为 ×100%=60%。
第 19页/共 19页