文档内容
高途高中·化学
点睛卷
2024
湖南省
1-------------------------------- 高途高中化学点睛卷 -----------------------------------
绝密 启用前
【高途】2023 年湖南省普通高中学业水平选择性考试模拟测试卷
化学
本试卷共10页,18题,满分100分,考试用时75分钟
可能用到的相对原子质量:H—1 C—12 N—14 O—16 B—11 F—19 Mn—55 Zn—65 S—32
一、选择题:本题共 14小题,共 42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1. 化学科技的进步,理应得到人类的密切关注。下列说法中正确的是
A.新型半导体“单层聚合C60 ”是新型有机高分子材料
B.无铅储能陶瓷铌酸银(AgNbO3 )基陶瓷属于传统无机非金属材料
C.全氟烷(PFAS)被列入新的污染物检测标准,是因为其难以降解且有毒性
D.无定型碳酸钙水通道技术将CaCO3 •H2O转化为CaCO3 ,此过程为物理变化
2. 下列化学用语或图示不正确的是
A.1﹣丁烯的实验式:CH2
B.SO 2-的VSEPR模型:
3
C.基态Cr原子的价层电子排布式:3d54s1
D.HCl分子中σ键的形成:
3. 室温下,下列实验方案不能达到实验目的的是
选项 实验方案 实验目的
A 向浓度均为0.01mol•L ﹣1的NaCl、NaI混合溶液中滴加几滴AgNO3 证明Ksp (AgCl)>Ksp (AgI)
溶液,观察沉淀的颜色
B 用pH计测量氢氟酸、盐酸的pH,比较溶液pH的大小 证明HF是弱电解质
C 向含有少量乙酸的乙酸乙酯中加入稍过量的饱和碳酸钠溶液,振荡 提纯含有少量乙酸的乙酸乙
后静置分液 酯
D 向盛有SO2 水溶液的试管中滴加几滴品红溶液,振荡,再加热试管, 证明SO2 具有漂白作用
观察溶液的颜色变化
A.A B.B C.C D.D
2-------------------------------- 高途高中化学点睛卷 -----------------------------------
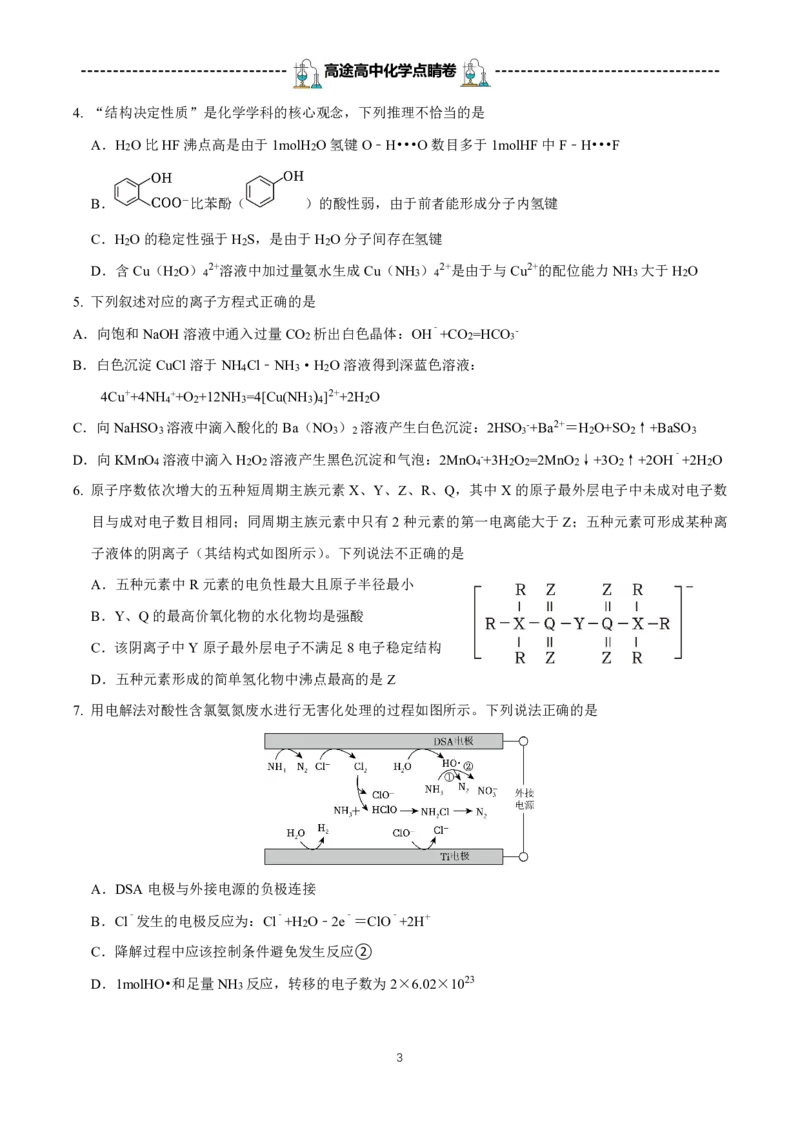
4. “结构决定性质”是化学学科的核心观念,下列推理不恰当的是
A.H2O比HF沸点高是由于1molH2O氢键O﹣H•••O数目多于1molHF中F﹣H•••F
B. 比苯酚( )的酸性弱,由于前者能形成分子内氢键
C.H2O的稳定性强于H2S,是由于H2O分子间存在氢键
D.含Cu(H2O)
4
2+溶液中加过量氨水生成Cu(NH3 )
4
2+是由于与Cu2+的配位能力NH3 大于H2O
5. 下列叙述对应的离子方程式正确的是
A.向饱和NaOH溶液中通入过量CO2 析出白色晶体:OH ﹣ +CO2=HCO
3
-
B.白色沉淀CuCl溶于NH4Cl﹣NH3 ·H2O溶液得到深蓝色溶液:
4Cu++4NH
4
++O2+12NH3=4[Cu(NH3 ) 4]2++2H2O
C.向NaHSO3 溶液中滴入酸化的Ba(NO3 )
2
溶液产生白色沉淀:2HSO
3
-+Ba2+=H2O+SO2 ↑+BaSO3
D.向KMnO4 溶液中滴入H2O2 溶液产生黑色沉淀和气泡:2MnO
4
-+3H2O2=2MnO2 ↓+3O2 ↑+2OH ﹣ +2H2O
6. 原子序数依次增大的五种短周期主族元素X、Y、Z、R、Q,其中X的原子最外层电子中未成对电子数
目与成对电子数目相同;同周期主族元素中只有2种元素的第一电离能大于Z;五种元素可形成某种离
子液体的阴离子(其结构式如图所示)。下列说法不正确的是
A.五种元素中R元素的电负性最大且原子半径最小
B.Y、Q的最高价氧化物的水化物均是强酸
C.该阴离子中Y原子最外层电子不满足8电子稳定结构
D.五种元素形成的简单氢化物中沸点最高的是Z
7. 用电解法对酸性含氯氨氮废水进行无害化处理的过程如图所示。下列说法正确的是
A.DSA电极与外接电源的负极连接
B.Cl ﹣发生的电极反应为:Cl ﹣ +H2O﹣2e ﹣=ClO ﹣ +2H+
C.降解过程中应该控制条件避免发生反应②
D.1molHO•和足量NH3 反应,转移的电子数为2×6.02×1023
3-------------------------------- 高途高中化学点睛卷 -----------------------------------
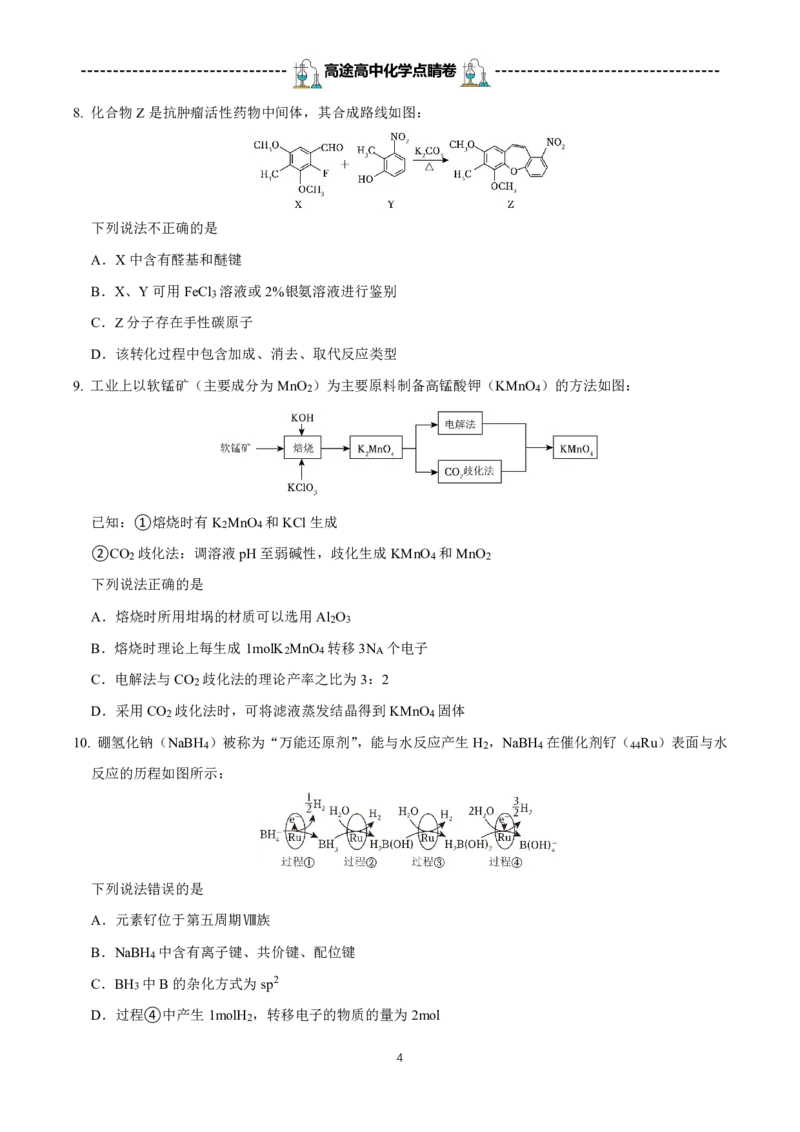
8. 化合物Z是抗肿瘤活性药物中间体,其合成路线如图:
下列说法不正确的是
A.X中含有醛基和醚键
B.X、Y可用FeCl3 溶液或2%银氨溶液进行鉴别
C.Z分子存在手性碳原子
D.该转化过程中包含加成、消去、取代反应类型
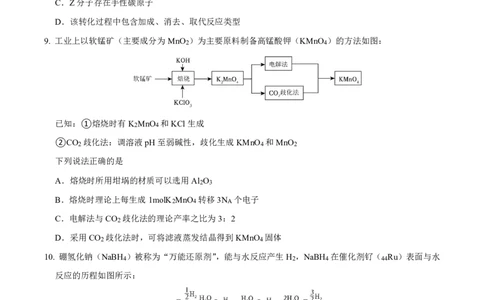
9. 工业上以软锰矿(主要成分为MnO2 )为主要原料制备高锰酸钾(KMnO4 )的方法如图:
已知:①熔烧时有K2MnO4 和KCl生成
②CO2 歧化法:调溶液pH至弱碱性,歧化生成KMnO4 和MnO2
下列说法正确的是
A.熔烧时所用坩埚的材质可以选用Al2O3
B.熔烧时理论上每生成1molK2MnO4 转移3NA 个电子
C.电解法与CO2 歧化法的理论产率之比为3:2
D.采用CO2 歧化法时,可将滤液蒸发结晶得到KMnO4 固体
10. 硼氢化钠(NaBH4 )被称为“万能还原剂”,能与水反应产生H2 ,NaBH4 在催化剂钌( 44Ru)表面与水
反应的历程如图所示:
下列说法错误的是
A.元素钌位于第五周期Ⅷ族
B.NaBH4 中含有离子键、共价键、配位键
C.BH3 中B的杂化方式为sp2
D.过程④中产生1molH2 ,转移电子的物质的量为2mol
4-------------------------------- 高途高中化学点睛卷 -----------------------------------
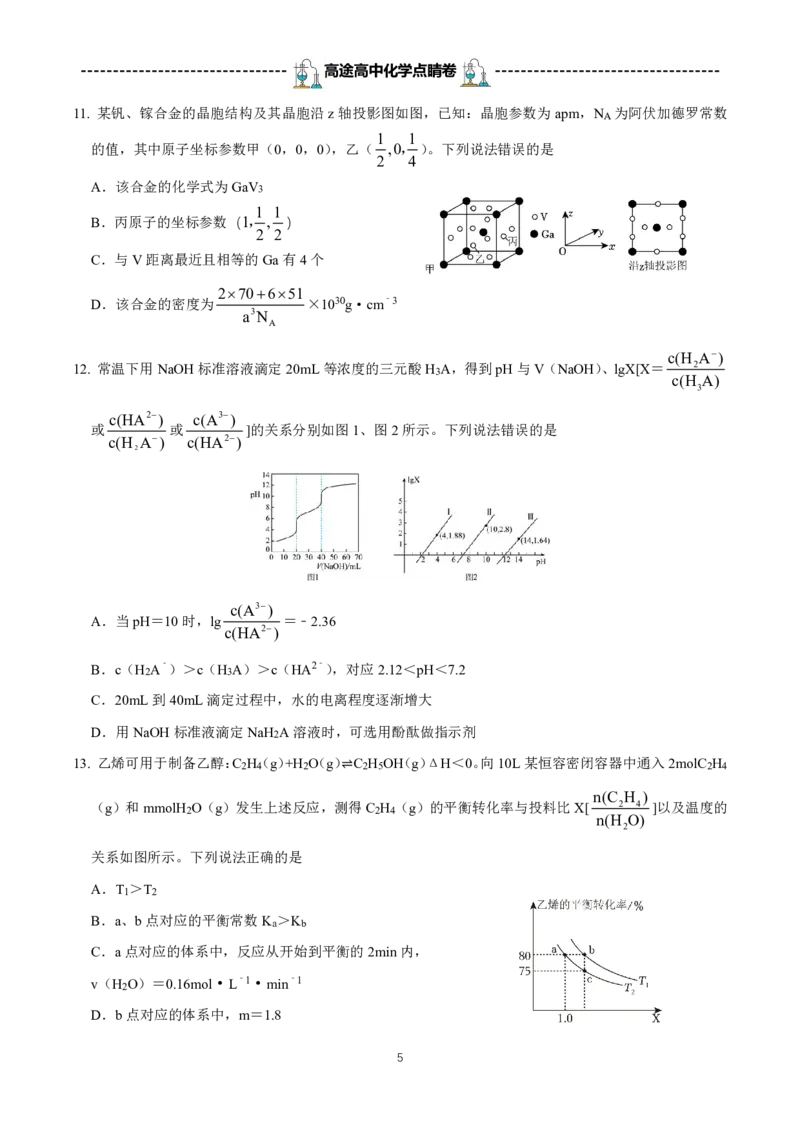
11. 某钒、镓合金的晶胞结构及其晶胞沿z轴投影图如图,已知:晶胞参数为apm,NA 为阿伏加德罗常数
1 1
的值,其中原子坐标参数甲(0,0,0),乙( ,0,)。下列说法错误的是
2 4
A.该合金的化学式为GaV3
1 1
B.丙原子的坐标参数(1,, )
2 2
C.与V距离最近且相等的Ga有4个
270651
D.该合金的密度为 ×1030g·cm ﹣3
a3N
A
c(H A)
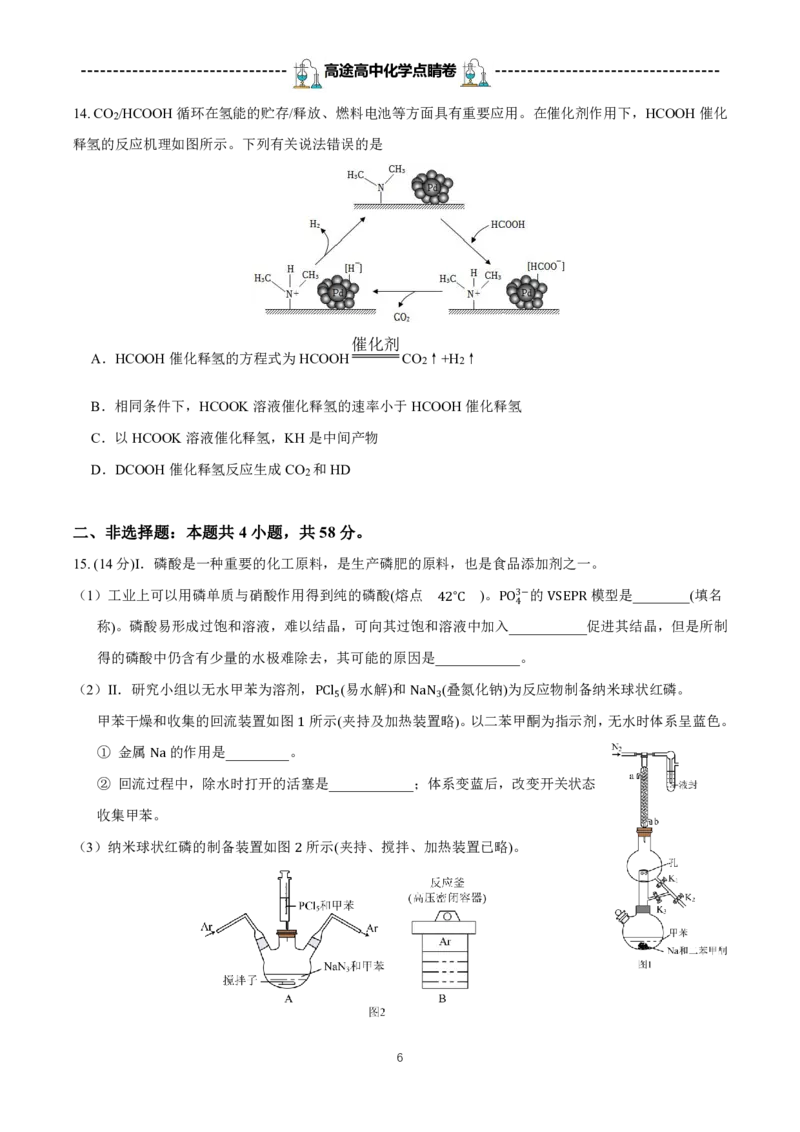
12. 常温下用NaOH标准溶液滴定20mL等浓度的三元酸H3A,得到pH与V(NaOH)、lgX[X= 2
c(H A)
3
c(HA2) c(A3)
或 或 ]的关系分别如图1、图2所示。下列说法错误的是
c(H A) c(HA2)
2
c(A3)
A.当pH=10时,lg =﹣2.36
c(HA2)
B.c(H2A ﹣)>c(H3A)>c(HA2﹣),对应2.12<pH<7.2
C.20mL到40mL滴定过程中,水的电离程度逐渐增大
D.用NaOH标准液滴定NaH2A溶液时,可选用酚酞做指示剂
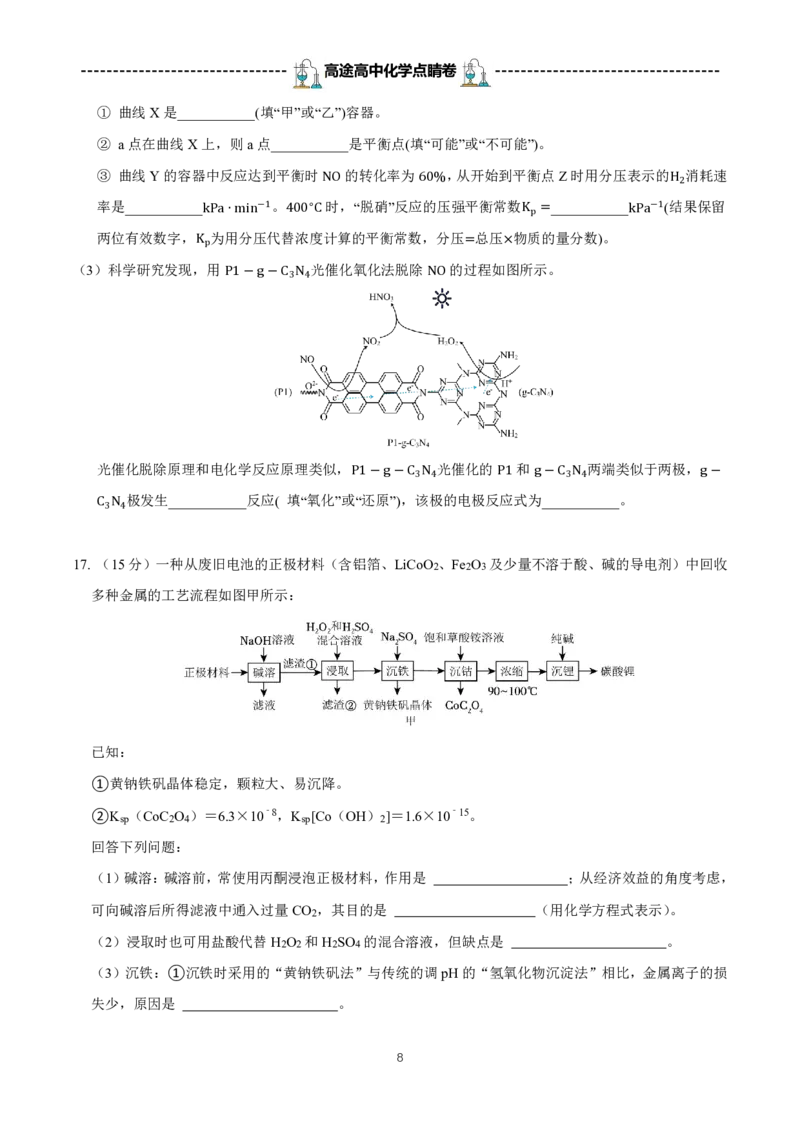
13. 乙烯可用于制备乙醇:C2H( 4 g)+H2O(g) C2H5OH(g)ΔH<0。向10L某恒容密闭容器中通入2molC2H4
⇌ n(C H )
(g)和mmolH2O(g)发生上述反应,测得C2H4 (g)的平衡转化率与投料比X[ 2 4 ]以及温度的
n(H O)
2
关系如图所示。下列说法正确的是
A.T1 >T2
B.a、b点对应的平衡常数Ka >Kb
C.a点对应的体系中,反应从开始到平衡的2min内,
v(H2O)=0.16mol · L ﹣1· min ﹣1
D.b点对应的体系中,m=1.8
5-------------------------------- 高途高中化学点睛卷 -----------------------------------
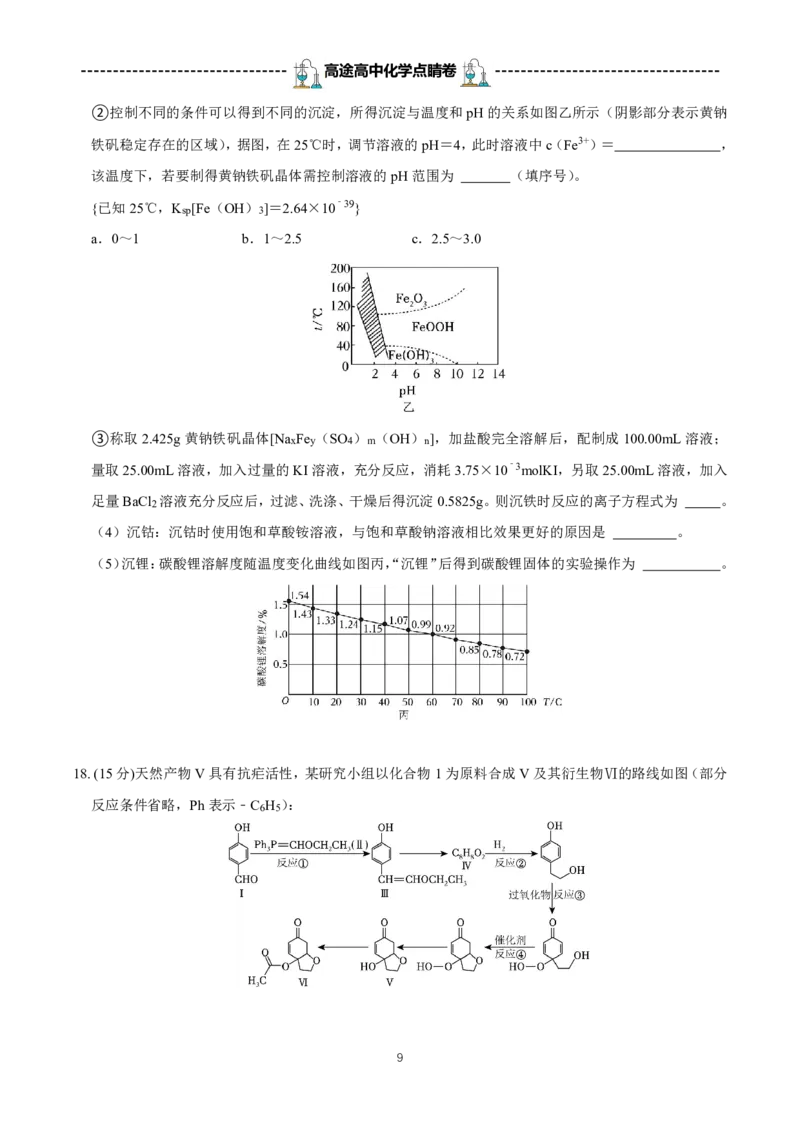
14.CO2/HCOOH循环在氢能的贮存/释放、燃料电池等方面具有重要应用。在催化剂作用下,HCOOH催化
释氢的反应机理如图所示。下列有关说法错误的是
催化剂
A.HCOOH催化释氢的方程式为HCOOH CO2 ↑+H2 ↑
B.相同条件下,HCOOK溶液催化释氢的速率小于HCOOH催化释氢
C.以HCOOK溶液催化释氢,KH是中间产物
D.DCOOH催化释氢反应生成CO2 和HD
二、非选择题:本题共 4小题,共 58分。
15.(14分)I.磷酸是一种重要的化工原料,是生产磷肥的原料,也是食品添加剂之一。
(1)工业上可以用磷单质与硝酸作用得到纯的磷酸(熔点 )。 的 模型是________(填名
∘ 3−
称)。磷酸易形成过饱和溶液,难以结晶,可向其过饱 和4溶2液C中加入PO_4_____V_S_E_P_R_促进其结晶,但是所制
得的磷酸中仍含有少量的水极难除去,其可能的原因是____________。
(2)Ⅱ.研究小组以无水甲苯为溶剂, (易水解)和 (叠氮化钠)为反应物制备纳米球状红磷。
甲苯干燥和收集的回流装置如图 所PC示l5 (夹持及加热N装aN置3略)。以二苯甲酮为指示剂,无水时体系呈蓝色。
① 金属 的作用是_________。1
② 回流过Na程中,除水时打开的活塞是____________;体系变蓝后,改变开关状态
收集甲苯。
(3)纳米球状红磷的制备装置如图 所示(夹持、搅拌、加热装置已略)。
2
6-------------------------------- 高途高中化学点睛卷 -----------------------------------
① 在氩气保护下,反应物在装置 中混匀后转入装置 ,于 加热 小时,反应物完全反应,其
∘
化学方程式为_________________;A用氩气赶走空气的目B的是2_8_0__C______1_2______。
②经冷却、离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是___________、
__________。
16.(14分)含 的烟气需要处理后才能排放。
(1)氢气催化NO还原含 的烟气,发生“脱硝”反应:
NO
。一定条件下,加入 的体积分数对该反
−1
应2N平O衡g时+含2氮H物 2 质g ⇌ 的N体 2 积g分+数2的H2 影O响g如Δ图H所=示−:605kJ∙mol H2
① 随着 体积分数增加, 中 被还原的价态逐渐降低。当 的体积分数在
−3 −3
时, H的2转化率基本为 NO ,N而 和 的体积分数仍呈增H2加趋势,其可能0原.5因×是10___~__0_.7_5__×__1。0
② 已N知O:Ⅰ. 100% N2 NH3
−1
Ⅱ. 4NH3 g +5O2 g = 4NO g +6H2O g ΔH = −1025kJ∙mol
−1
图中2H2减g少+的O原2因g是=2与H2O反g 应Δ生H成= −4,84写k出J∙该mo反l应的热化学方程式:___________。
(2)某科N研2 小组研究了 N2与H2反应生成NH和3 的转化过程。在起始温度为 时,将
∘
通入甲、乙两个N恒O容密H闭2 容器中,N甲2 为N绝H热3过程、乙为恒温过程,两反4应00体C系的压强n随NO时间:n的H变2 化=
1曲:2线如图所示。
7-------------------------------- 高途高中化学点睛卷 -----------------------------------
① 曲线X是___________(填“甲”或“乙”)容器。
② a点在曲线X上,则a点___________是平衡点(填“可能”或“不可能”)。
③ 曲线Y的容器中反应达到平衡时 的转化率为 ,从开始到平衡点Z时用分压表示的 消耗速
率是___________ 。 N时O,“脱硝”反应6的0%压强平衡常数 ___________ (结H2果保留
−1 ∘ −1
两位有效数字, kP为a用∙m分in压代替40浓0度C计算的平衡常数,分压 总压 物K质p =的量分数)。 kPa
(3)科学研究发现,Kp用 光催化氧化法脱除 的过=程如×图所示。
P1−g−C3N4 NO
光催化脱除原理和电化学反应原理类似, 光催化的 和 两端类似于两极,
极发生___________反应( 填“氧化”或P“1还−原g”−),C该3N极4 的电极反P应1式为g_−__C_ 3 _N_ 4 _____。 g−
C3N4
17. (15分)一种从废旧电池的正极材料(含铝箔、LiCoO2 、Fe2O3 及少量不溶于酸、碱的导电剂)中回收
多种金属的工艺流程如图甲所示:
已知:
①黄钠铁矾晶体稳定,颗粒大、易沉降。
②Ksp (CoC2O4 )=6.3×10 ﹣8,Ksp[Co(OH) 2]=1.6×10 ﹣15。
回答下列问题:
(1)碱溶:碱溶前,常使用丙酮浸泡正极材料,作用是 ;从经济效益的角度考虑,
可向碱溶后所得滤液中通入过量CO2 ,其目的是 (用化学方程式表示)。
(2)浸取时也可用盐酸代替H2O2 和H2SO4 的混合溶液,但缺点是 。
(3)沉铁:①沉铁时采用的“黄钠铁矾法”与传统的调pH的“氢氧化物沉淀法”相比,金属离子的损
失少,原因是 。
8-------------------------------- 高途高中化学点睛卷 -----------------------------------
②控制不同的条件可以得到不同的沉淀,所得沉淀与温度和pH的关系如图乙所示(阴影部分表示黄钠
铁矾稳定存在的区域),据图,在25℃时,调节溶液的pH=4,此时溶液中c(Fe3+)= ,
该温度下,若要制得黄钠铁矾晶体需控制溶液的pH范围为 (填序号)。
{已知25℃,Ksp[Fe(OH) 3]=2.64×10 ﹣39}
a.0~1 b.1~2.5 c.2.5~3.0
③称取2.425g黄钠铁矾晶体[NaxFey (SO4 )
m
(OH) n],加盐酸完全溶解后,配制成100.00mL溶液;
量取25.00mL溶液,加入过量的KI溶液,充分反应,消耗3.75×10 ﹣3molKI,另取25.00mL溶液,加入
足量BaCl2 溶液充分反应后,过滤、洗涤、干燥后得沉淀0.5825g。则沉铁时反应的离子方程式为 。
(4)沉钴:沉钴时使用饱和草酸铵溶液,与饱和草酸钠溶液相比效果更好的原因是 。
(5)沉锂:碳酸锂溶解度随温度变化曲线如图丙,“沉锂”后得到碳酸锂固体的实验操作为 。
18.(15分)天然产物V具有抗疟活性,某研究小组以化合物1为原料合成V及其衍生物Ⅵ的路线如图(部分
反应条件省略,Ph表示﹣C6H5 ):
9-------------------------------- 高途高中化学点睛卷 -----------------------------------
已知:
(1)化合物Ⅰ中含氧官能团有 (写名称)。
(2)反应①的方程式可表示为:Ⅰ+Ⅱ=Ⅲ+Z,化合物Z的分子式为 。
(3)化合物Ⅳ能发生银镜反应,其结构简式为 。
(4)反应②③④中属于还原反应的有 ,属于加成反应的有 。
(5)化合物Ⅵ的芳香族同分异构体中,同时满足如下条件的有 种,写出其中任意一种的结构简
式: 。条件:
a)能与NaHCO3 反应;
b)最多能与2倍物质的量的NaOH反应;
c)能与3倍物质的量的Na发生放出H2 的反应;
d)核磁共振氢谱确定分子中有6个化学环境相同的氢原子;
e)不含手性碳原子(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子)。
(6)根据上述信息,写出以苯酚的一种同系物及HOCH2CH2Cl为原料合成 的路线 (需注明
反应条件)。
10-------------------------------- 高途高中化学点睛卷 -----------------------------------
【高途】2023年湖南省普通高中学业水平选择性考试模拟测试卷
化学·参考答案
一、选择题:本题共 14小题,共 42分。在每小题给出的四个选项中,只有一项是符合题目
要求的。
1. 【答案】C
【分析】A.高分子化合物的相对分子质量在一万以上;
B.陶瓷、玻璃、水泥属于传统无机非金属材料;
C.全氟烷(PFAS)被列人新的污染物检测标准,是因为其难以降解且有毒性;
D.有新物质生成的过程为化学变化。
【解答】解:A.C60 是无机单质,不是有机高分子材料,故A错误;
B.无铅储能陶瓷铌酸银(AgNbO3 )基陶瓷属于新型无机非金属材料,故B错误;
C.全氟烷(PFAS)被列人新的污染物检测标准,是因为其难以降解且有毒性,故C正确;
D.CaCO3 •H2O转化为CaCO3 的过程有新物质生成,为化学变化,故D错误;
故选:C。
2. 【答案】B
【解答】解:A.2﹣丁烯的分子式为C4H8 ,实验式为CH2 ,故A正确;
B.SO 2-中S原子价层电子对个数为4,含一对孤电子,SO 2-的VSEPR模型为正四面体结构,故B错误;
3 3
C.基态Cr原子的核电荷数为24,原子的价层电子排布式:3d54s1,故C正确;
D.HCl分子中σ键的形成是氢原子s电子和氯原子的3p电子形成一对共用电子对,形成σ键,σ键的形
成过程为: ,故D正确;
故选:B。
3. 【答案】B
【解答】解:A.向浓度均为0.01mol•L ﹣1的NaCl、NaI混合溶液中滴加几滴AgNO3 溶液,溶度积常数
小的先生成沉淀,根据沉淀的颜色判断溶度积常数大小,能实现实验目的,故A错误;
B.HF、HCl的物质的量浓度相对大小未知,不能根据溶液的pH值相对大小判断HF为弱电解质,不能
实现实验目的,故B正确;
C.饱和Na2CO3 能和CH3COOH反应生成CH3COONa和CO2 、H2O,降低乙酸乙酯的溶解度,所以可
以用饱和碳酸钠溶液除去乙酸乙酯中的乙酸,能实现实验目的,故C错误;
D.品红溶液具有漂白性,但其漂白性不稳定,受热易恢复原来的颜色,操作正确,能实现实验目的,
11-------------------------------- 高途高中化学点睛卷 -----------------------------------
故D错误;
故选:B。
4. 【答案】C
【解答】解:A.H2O比HF沸点高是由于H2O形成的氢键数目多,故A正确。
B.水杨酸电离后的离子( )能形成分子内氢键,分子内氢键的形成会使该微粒中酚羟基上的氢
离子更难电离出H+,导致 的酸性比苯酚的酸性弱,故B正确;
C.氢键与物质的稳定性无关,H2O的稳定性强于H2S,是因为H﹣O比H﹣S键牢固,故C错误;
D.N的电负性小于O的电负性,配位能力NH3 大于H2O,向Cu(H
2
O)
4
2+中加过量氨水生成Cu(NH
3
)
4
2+,
故D正确;
故选:C。
5. 【答案】D
【解答】解:A.向饱和NaOH溶液中通入过量CO2 析出白色晶体,离子方程式为:Na++OH ﹣ +CO2 ═
NaHCO3 ↓,故A错误;
B.沉淀在离子方程式书写时不能拆,离子方程式为:+4CuCl+4NH
4
++O2+12NH3 ═4[Cu(NH3 )
4]2++2H2O+4Cl ﹣,故B错误;
C.硝酸具有强氧化性,,能将HSO -氧化为SO 2-,SO 2-继续与Ba2+反应生成难溶于酸的硫酸钡沉淀,
3 4 4
离子方程式为:2NO
3
-+3HSO
3
-+3Ba2+=H++H2O+2NO↑+3BaSO4 ↓,故C错误;
D.向KMnO4 溶液中滴入H2O2 溶液产生黑色沉淀和气泡:2MnO
4
-+3H2O2=2MnO2 ↓+3O2 ↑+2OH ﹣ +2H2O,
故D正确;
故选:D。
6. 【答案】C
【分析】X的原子最外层电子中未成对电子数目与成对电子数目相同,X为C元素;同周期主族元素中
只有2种元素的第一电离能大于Z,Z为O元素,则Y为N元素;由阴离子结构可知,R为F元素,Q
为S元素,以此分析解答。
【解答】解:A.由分析可知,F元素的电负性最大且原子半径最小,故A正确;
B.N、S的最高价氧化物的水化物分别为HNO3 、H2SO4 ,均是强酸,故B正确;
C.在阴离子结构中,N原子分别和两个硫原子共用一对电子,同时因为是阴离子再得到一个电子,N
最外层本身有五个电子,这样正好构成八电子稳定结构,达到稳定结构,故C错误;
D.五种元素形成的简单氢化物中分别为CH4 、NH3 、H2O、HF、H2S,其中NH3 、H2O、HF可形成分
12-------------------------------- 高途高中化学点睛卷 -----------------------------------
子间氢键,H2O形成的氢键最多,沸点最高,故D正确;
故选:C。
7. 【答案】C
【解答】解:A.NH3 在DSA电极转化为N2 ,氮元素从﹣3价升高为0价,被氧化,该电极是电解池的
阳极,与外接电源的正极相连,故A错误;
B.Cl ﹣在DSA电极表面转化为Cl2 电极反应式为:2Cl ﹣﹣2e ﹣=Cl2 ↑,故B错误;
C.反应②中NH3 转化为NO
3
-,没有达到氨氮废水无害化处理的目的,则降解过程中应该控制条件避免
发生反应②,故C正确;
D.反应中一个HO•可得到一个电子,1molHO•完全反应时转移的电子数为6.02×1023,故D错误;
故选:C。
8. 【答案】C
【解答】解:A.根据图知,X中含有醛基和醚键,故A正确;
B.含有酚羟基的有机物能和氯化铁溶液发生显色反应,含有醛基的有机物能和银氨溶液发生银镜反应,
Y能和氯化铁发生显色反应,X和氯化铁溶液不发生显色反应,X能和银氨溶液发生银镜反应,Y不能
和银氨溶液发生银镜反应,所以X、Y可用FeCl3 溶液或2%银氨溶液进行鉴别,故B正确;
C.连接4个不同原子或原子团的碳原子为手性碳原子,根据图知,Z中不含手性碳原子,故C错误;
D.X和Y反应生成Z时,酚羟基中的H原子被苯基取代生成醚键,X中醛基和Y苯环上的氢原子发生
加成反应生成醇羟基,然后醇羟基发生消去反应生成Z中碳碳双键,所以该转化过程中包含加成、消去、
取代反应类型,故D正确;
故选:C。
9. 【答案】C
【解答】解:A.焙烧时环境为碱性,不可以选择氧化铝,故A错误;
△
B.熔烧时发生反应3MnO2+6KOH+KClO3 3K2MnO4+KCl+3H2O结合方程式可知,1molK2MnO4 转移
2NA 个电子,故B错误;
C.“电解法”阳极上发生反应:MnO 2--e-=MnO -,锰酸根离子全部转换为高锰酸根。CO2歧化反应为:
4 4
3K2MnO4+2CO
2
=2KMnO
4
+2K
2
CO
3
+MnO
2
,有2/3的锰酸根离子转化为高锰酸根离子,两者的理论产率
之比为3:2,C正确;
D.采用CO2 歧化法时,滤液的主要成分为KHCO3和KMnO4,因为有碳酸氢钾所以不能蒸发结晶,会有
碳酸钾杂质,故D错误;
13-------------------------------- 高途高中化学点睛卷 -----------------------------------
故选:C。
10. 【答案】D
【解答】解:A.第四周期的最后一种元素是36号,元素钌为44号元素位于第五周期第VIII族,故A
正确;
B.NaBH4 是离子化合物,钠离子和[BH
4
]-间存在离子键,[BH
4
]-中硼与其中3个氢形成共价键,与一个
氢形成配位键,故B正确;
C.BH3 分子中B原子的价层电子对数为3,B的杂化方式为sp2杂化,故C正确;
3
D.从图中可以看出,过程④中发生反应HB(OH) 2+2H2O+e ﹣=B(OH)
4
-+ H2 ↑,则产生1molH2 ,转
2
2
移电子的物质的量为 mol,故D错误;
3
故选:D。
11. 【答案】B
1
【解答】解:A.Ga位于顶点和体心,V位于面心,该晶胞中Ga的个数为1+8× =2、V的个数为12
8
1
× =6,所以Ga、V的个数之比为2:6=1:3,则该合金的化学式为GaV3 ,故A正确;
2
1 1 1 1
B.由信息可知,丙原子在x、y、z轴上的投影分别是1、 、 ,则丙原子的坐标参数(1, , ),
4 2 4 2
故B错误;
C.晶胞中距离Ga最近且相等的V有12个,距离V最近且相等的Ga有4个,故C正确;
1 1
D.该晶胞中Ga的个数为1+8× =2、V的个数为12× =6,相当于含有2个“GaV3 ”,晶胞体积为
8 2
M
2
m N 270651
(a×10 ﹣10cm)3,则合金的密度为 = A = ×1030g cm ﹣3,故D正确;
V V a3N ⋅
A
故选:B。
12. 【答案】B
c(H A) K c(HA2) K c(A3) K
【分析】lg 2 =lg a1 ,lg =lg a2 ,lg =lg a3 ,当pH相同时,即
c(H A) c(H) c(H A) c(H) c(HA2) c(H)
3 2
c(H A) c(HA2) c(A3)
c(H+)相等,由于Ka1 >Ka2 >Ka3 ,则有lg 2 >lg >lg ,故曲线I、Ⅱ、Ⅲ分
c(H A) c(H A) c(HA2)
3 2
c(H A) c(HA2) c(A3)
别表示lg 2 、lg 、lg 与pH关系;图1中滴定过程依次发生反应H3A+NaOH
c(H A) c(H A) c(HA2)
3 2
14-------------------------------- 高途高中化学点睛卷 -----------------------------------
=NaH2A+H2O、NaH2A+NaOH=Na2HA+H2O、Na2HA+NaOH=Na3A+H2O。
c(A3) c(A3) K
【解答】解:A.曲线Ⅲ表示lg 与pH关系,当pH=14时,lg =lg a3 =1.64,则
c(HA2) c(HA2) c(H)
c(A3) K 1012.36
Ka3 =101.64×10 ﹣14=10 ﹣12.36,当pH=10时,lg =lg a3 =lg =﹣2.36,故A正确;
c(HA2) c(H) 1010
c(H A) K c(H A) K
B. 2 = a1 >1时,c(A2H ﹣)>c(H3A),由曲线I可知,当pH=4时,lg 2 =lg a1
c(H A) c(H) c(H A) c(H)
3 3
=1.88,则 Ka1 =101.88×10 ﹣4=10 ﹣2.12,故 c(H+)<10 ﹣2.12mol/L,则 pH=﹣lgc(H+)>2.12,
c(H A) c(HA2) c(HA2) K K
2 × = = a1 × a2 <1时,c(H3A)>c(AH2﹣),由曲线Ⅱ可知,当
c(H A) c(H A) c(H A) c(H) c(H)
3 2 3
c(HA2) K
pH=10时,lg =lg a2 =2.8,故Ka2 =102.8×10 ﹣10=10 ﹣7.2,即c(2 H+)>Ka1×Ka2 =10 ﹣2.12×10
c(H A) c(H)
2
﹣7.2=10 ﹣9.34,则c(H+)>10 ﹣4.66,则pH=﹣lgc(H+)<4.66,故B错误;
C.加入20mLNaOH溶液时,溶液中溶质为NaH2A,加入40mLNaOH溶液时,溶液中溶质为Na2HA,
溶液中HA ﹣离子浓度增大,H2A ﹣浓度减小,HA ﹣水解程度比H2A ﹣水解程度大,故20mL到40mL滴定
过程中,水的电离程度逐渐增大,故C正确;
D.滴定终点pH处于指示剂变色范围内,Na3A溶液呈碱性,能用酚酞做指示剂,故D正确;
故选:B。
13. 【答案】D
【解答】解:A.该反应为放热反应,投料比相同,升高温度,平衡逆向移动,C2H4 (g)的平衡转化率
减小,b、c点的投料比相同,b的转化率高,所以T1 温度低,故A错误;
B.该反应为放热反应,升高温度,平衡逆向移动,则平衡常数减小,所以Ka <Kb ,故B错误;;
C.a点时X=1.0,此时C2H4 (g)与H2O(g)的物质的量相等,即m=2,据图中信息列化学平衡三段
式,
C2H4 (g)+H2O(g) C2H5OH(g)
起始/mol 2 2 ⇌ 0
转化/mol 1.6 1.6 1.6
平衡/mol 0.4 0.4 1.6
1.6mol
容器容积为10L,反应时间是2min,故v(H2O)= =0.08mol/(L•min),故C错误;
10L2min
15-------------------------------- 高途高中化学点睛卷 -----------------------------------
D.a、c点对应的平衡常数相等,b、c点对应的体系起始通入的反应物的物质的量相等,将c点对应体
系列化学平衡三段式,
C2H4 (g)+H2O(g) C2H5OH(g)
起始/mol 2 m ⇌ 0
转化/mol 1.5 1.5 1.5
平衡/mol 0.5 m﹣1.5 1.5
1.6 1.5
c(C H OH) 10 10
K= 2 5 ,解得m=1.8,故D正确;
c(C H )c(H O) 0.4 0.4 0.5 m1.5
2 4 2
10 10 10 10
故选:D。
14. 【答案】B
催化剂
【分析】由图可知,HCOOH催化释氢生成二氧化碳和氢气,反应的方程式为:HCOOH CO2 ↑
+H2 ↑,HCOOH催化释氢反应的机理中有H ﹣离子生成,根据总反应方程式可知,DCOOH催化释氢反
应生成CO2 和HD,以此做题。
催化剂
【解答】解:A.由图可知HCOOH催化释氢生成二氧化碳和氢气,反应的方程式为:HCOOH CO2
↑+H2 ↑,故A正确;
B.若将弱电解质HCOOH替换为强电解质HCOOK,HCOOK在溶液中快速电离有利于提高释放氢气的速
率,相同条件下,HCOOK溶液催化释氢的速率大于HCOOH催化释氢,故B错误;
C.由图可知,HCOOH 催化释氢反应的机理中有H ﹣离子生成,若将弱电解质HCOOH 替换为强电解质
HCOOK,HCOOK在溶液中快速电离出的K+能与H ﹣反应生成KH,KH与水反应生成的氢氧化钾和氢
气,KH是中间产物,故C正确;
D.根据总反应方程式可知,DCOOH催化释氢反应生成CO2 和HD,故D正确;
故选:B。
二、非选择题:本题共 4小题,共 58分。
15.(14分)【分析】利用苯来干燥甲苯,通过回流得到的水与钠反应,二苯甲酮为指示剂,无水时体系
呈蓝色,改变开关状态收集甲苯,将甲苯、五氯化磷、 在 气氛围中充分混合后转入装置 中,
在反应釜中于 加热 小时使其充分反应。 NaN3 Ar B
∘
(1)【答案】四2面8体0 C形 磷1酸2 晶体 磷酸分子与水分子能形成氢键
16-------------------------------- 高途高中化学点睛卷 -----------------------------------
【解析】 中心原子价层电子对数为 ,其 模型是四面体形。磷酸易形成过饱和溶液,
3−
难以结晶P,O可4以引入晶种来促进溶液中的4磷+酸0结=晶4析出V,S可EP向R其过饱和溶液中加入磷酸晶体促进其结晶,
磷酸分子含有羟基,容易与水分子形成氢键,因此磷酸具有较强的吸水性,所制得的磷酸中仍含有少量
的水极难除去。
(2)【答案】干燥甲苯 、
【解析】① 金属钠与水 能K1发生K3反应,因此金属 的作用是干燥甲苯。
② 回流过程中,水要回流到烧瓶中,因此除水时Na打开的活塞是 、 ;体系变蓝后,改变开关状态
收集甲苯。 K1 K3
(3)【答案】 防止五氯化磷遇空气中的水蒸气而发生
∘
280 C
水解 甲苯 10NaN 氯 3 化 + 钠 2PCl5 ������������ 2P+15N2 ↑+10NaCl
【解析】① 在氩气保护下,反应物在装置 中混匀后转入装置 ,于 加热 小时,反应物完
∘
全反应,五氯化磷和 反应生成红磷、氮A气和氯化钠,其反应B的化学28方0程C 式为: 12
NaN3
;由于五氯化磷易水解,为防止五氯化磷遇见空气中
∘
280 C
1 的 0 水 Na 蒸 N3 气 + 发 2 生 PC 水 l5 解,������因����此�� 用 2 氩 P 气 + 赶 15 走 N2 空 ↑ 气 + 。 10NaCl
② 根据反应可知,得到的产物上沾有甲苯和氯化钠,用乙醇洗去甲苯,用水洗去氯化钠。
16.(14分)(1)【答案】 较少时, 主要被还原为 (或 价含氮化合物等)(合理即可)
H2 NO N2O +1
−1
N【 2 解g析+】3①H2 根g 据⇌ 2题N中H3 信g息,ΔH随=着−氢9气2.5体k积J∙分mo数l的增加, 中被还原的价态逐渐降低,根据图像可知,
当氢气的体积分数在 时, 转化N率O基本为 ,而氮气和氨气的体积分数仍
−3 −3
呈增加趋势, 中 0显.5×10价,~0.7中5×1显00价,NO 中 显 价,10因0%此当氢气较少时, 被还原为
的 价化合N物O或 N ;+2 N2 N NH3 N −3 NO
N +1 N2OⅡ Ⅰ
② 根据盖斯定律可知, 脱硝反应,推出
×5− −484×5+1025
; − N2 g +3H2 g ⇌ 2NH3 g ΔH=( 2 +
2
(620)5【)答kJ/案m】ol甲=−可92能.50k.J1/1m0o.l12
【解析】① 该过程发生的两个反应都是物质的量减少的放热反应,恒温恒容状态下,随着时间的进行,
气体物质的量减小,压强降低,而绝热容器中,虽然气体物质的量减小,但温度升高,气体压强增大,
因此根据图像可知,X为绝热容器,Y为恒温容器;
② 因为反应为放热,甲绝热容器内反应体系温度升过高,反应速率快,先达到平衡,温度升高,平衡
17-------------------------------- 高途高中化学点睛卷 -----------------------------------
左移,平衡时压强增大,因此点a可能已达到平衡;
③ 曲线Y是恒温过程的乙容器,恒温容器中反应达到平衡时 的转化率为 ,开始时体系总压强
为 , , , N,O 60%
9kPa n NO :n H2 =1:2 p NO =3kPa p H2 =6kPa
初始量 2NO( 3 g) + 2 H2 6 (g) ⇌ N2 0 (g)+2 H0 2O(g)
反应量/kPa 1.8 0.9 1.8
平衡量/kPa 3×0.60 4.2-3x 0.9-x 1.8
/kPa 1.2
反应量 N x 2(g)+3 3 H x 2(g)⇌ 2NH 2x 3(g)
平衡量/kPa 2x
平衡压强/为kPa ,则 ,从开始到平衡时用分压表示的氢气消耗速率时
kPa
(1.8+3×0.5)
7.1kPa x=0.5 =
;平衡时 、 、 30 min 、
0.11kPa/min p NO =1.2kPa p H2 = 4.2−1.5 kPa=2.7kPa p H2O =1.8kPa p N2 =
, ;
N 2 H 2
p( 2)∙p ( 2O) 0.4×(1.8) −1
( 0 3 .9 )【 − 答 0.5 案 k 】 P 还 a= 原 0.4kPa Kp = p 2 ( H 2)∙p 2(N O) = (2.7) 2 ×(1.2) 2 =0.12kPa
+ −
【解析】 极 氧O2气+得2H电子+,2e发生=还H2原O2反应,电极反应式为 。
+ −
17.(15分g)【−答C3案N4】(1)除去废旧电池正极材料表面的油污;NaAlOO 2 2++C2OH 2+2+H2 2Oe==Al(H2 OOH 2)
3
↓+NaHCO3
(2)HCl作还原剂,氧化产物为Cl2 ,Cl2 有毒,污染环境
(3)①调节pH时Fe3+会生成氢氧化铁胶体,会吸附溶液中的金属离子
②2.64×10 ﹣9mol/L;c
③Na++3Fe3++2SO
4
2-+6H2O=NaFe3 (SO4 )
2
(OH)
6
↓+6H+
(4)草酸钠溶液相比,饱和草酸铵溶液的碱性更弱,可以防止沉钴时生成氢氧化钴沉淀
(5)趁热过滤
【解答】解:(1)碱溶前,常用丙酮浸泡正极材料的目的是除去废旧电池正极材料表面的油污:由思路
分析可知,碱溶后的滤液中含有NaAlO2 ,通入过量CO2 的目的是生成Al(OH)
3
沉淀,进而回收铝,
对应的化学方程式为NaAlO2+CO2+2H2O=Al(OH)
3
↓+NaHCO3 ,
故答案为:除去废旧电池正极材料表面的油污;NaAlO2+CO2+2H2O=Al(OH)
3
↓+NaHCO3 ;
(2)用H2O2 和H2SO4 的混合溶液浸取滤渣①的作用是将Co(Ⅲ)还原为Co(Ⅱ),则H2O2 作还原剂,
若用盐酸代替H2O2 和H2SO4 的混合溶液,则HCl作还原剂,氧化产物为Cl2 ,Cl2 有毒,污染环境,
18-------------------------------- 高途高中化学点睛卷 -----------------------------------
故答案为:HCl作还原剂,氧化产物为Cl2 ,Cl2 有毒,污染环境;
(3)①由于黄钠铁矾晶体稳定、颗粒大、易沉降,而调节pH时Fe3+会生成氢氧化铁胶体,会吸附溶液
中的金属离子,所以沉铁时采用的“黄钠铁矾法”与传统的通过调节溶液pH的“氢氧化物沉淀法”相
比,溶液中的金属离子的损失少,
故答案为:调节pH时Fe3+会生成氢氧化铁胶体,会吸附溶液中的金属离子;
②在 25℃时,调节溶液的 pH=4,由图乙可知,溶液中 Fe3+以 Fe(OH)
3
的形式存在,此时
K
c(OH) w 1010mol/L ,由Ksp[Fe(OH) ]=c(Fe3+)×c3(OH-),代入数据得c(Fe3+)=2.64×10-9mol/L;
c(H) 3
由图乙可知,该温度下,若要制得黄钠铁矾晶体需控制溶液的pH范围为2.5~3.0,
故答案为:2.64×10 ﹣9mol/L;c;
③由题意得有关反应的离子方程式为2Fe3++2I-=2Fe2++I ,定量关系式为Fe3+~I ﹣,25.00mL溶液中,n
2
(Fe3+)=n(I ﹣)=3.75×10 ﹣3mol,加入足量BaCl2 溶液充分反应后,过滤、洗涤、干燥后得沉淀0.5825g,
沉淀为硫酸钡,对应的BaSO4 的物质的量为2.5×10 ﹣3mol,则25.00mL溶液中,n(SO
4
2-)=2.5×10 ﹣3mol,
即100.00mL溶液中含有n(Fe3+)=3.75×10 ﹣3mol×4=0.015mol,n(SO 2-)=0.01mol,设2.425g样品中钠离
4
子的物质的量为n(Na+),氢氧根离子的物质的量为n(OH ﹣),根据质量守恒得2.425g﹣0.015mol×56g
mol
﹣1﹣0.01mol×96g
mol
﹣1=n(Na+)×23g
mol
﹣1+n(OH ﹣)×17g
mol
﹣1,根据电荷守恒得
⋅ ⋅ ⋅ ⋅
0.015mol×3+n(Na+)×1=0.01mol×2+n(OH ﹣)×1,解得n(Na+)=0.005mol,n(OH ﹣)=0.03mol,
则x:y:m:n=1:3:2:6,即黄钠铁矾晶体的化学式为NaFe3 (SO4 )
2
(OH)
6
,沉铁时反应的离子
方程式为Na++3Fe3++2SO
4
2-+6H2O=NaFe3 (SO4 )
2
(OH)
6
↓+6H+,
故答案为:Na++3Fe3++2SO
4
2-+6H2O=NaFe3 (SO4 )
2
(OH)
6
↓+6H+。
(4)沉钴时采用饱和草酸铵溶液将钴元素转化为CoC2O4 沉淀,与草酸钠溶液相比,饱和草酸铵溶液的
碱性更弱,可以防止沉钴时生成氢氧化钴沉淀,
故答案为:草酸钠溶液相比,饱和草酸铵溶液的碱性更弱,可以防止沉钴时生成氢氧化钴沉淀;
(5)由题图丙可知,碳酸锂的溶解度随温度升高而降低,由此得出沉锂后得到碳酸锂固体的实验操作为
趁热过滤,
故答案为:趁热过滤。
18.(15分)【答案】(1)酚羟基、醛基;
(2)C18H15OP;
(3) ;
19-------------------------------- 高途高中化学点睛卷 -----------------------------------
(4)②;②④;
(5)10; ;
(6) 。
【分析】I中醛基上的O原子被取代生成III,根据反应条件知,反应②为加成反应,根据反应②产物
的结构简式及IV分子式知,IV能发生有机反应,则IV含有酯基,IV为 ,反应③为氧
化反应,反应④中碳碳双键发生加成反应,V发生酯化反应生成VI;
(6)以苯酚的一种同系物及HOCH2CH2Cl为原料合成 ,根据“ ”知,合成
的苯酚的同系物为 , 及HOCH2CH2Cl发生信息中的反应生成 ,
发生水解反应生成 , 发生反应④类型的反应生成 。
【解答】解:(1)化合物Ⅰ中含氧官能团有酚羟基、醛基,
故答案为:酚羟基、醛基;
(2)反应①的方程式可表示为:Ⅰ+Ⅱ=Ⅲ+Z,根据I、II、III的结构简式知,II中的CHOCH2CH3 被
I中的O原子取代,则Z为Ph3P=O,则化合物Z的分子式为C18H15OP,
故答案为:C18H15OP;
(3)通过以上分析知,IV为 ,
故答案为: ;
(4)反应②③④中属于还原反应的有②,属于加成反应的有②④,
故答案为:②;②④;
(5)化合物Ⅵ的不饱和度是5,VI的芳香族同分异构体中含有苯环,苯环的不饱和度是4,同分异构体
同时满足如下条件:
20-------------------------------- 高途高中化学点睛卷 -----------------------------------
条件:a)能与NaHCO3 反应,说明含有﹣COOH,根据其不饱和度知,不含酯基或碳碳双键;
b)最多能与2倍物质的量的NaOH反应,说明含有1个酚羟基;
c)能与3倍物质的量的Na发生放出H2 的反应,说明含有1个醇羟基;
d)核磁共振氢谱确定分子中有6个化学环境相同的氢原子,说明含有2个甲基;
e)不含手性碳原子(手性碳原子是指连有4个不同的原子或原子团的饱和碳原子),其取代基有3个,
分别为﹣COOH、酚﹣OH、 ,如果﹣COOH、酚﹣OH相邻, 有4种排列方式;如果﹣COOH、
酚﹣OH相间, 有4种排列方式;如果﹣COOH、酚﹣OH相对, 有2种排列方式,所以符合条
件的同分异构体有10种,其中一种结构简式为 ,
故答案为:10; ;
(6)以苯酚的一种同系物及HOCH2CH2Cl为原料合成 ,根据“ ”知,合
成 的苯酚的同系物为 , 及 HOCH2CH2Cl 发生信息中的反应生成 ,
发生水解反应生成 , 发生反应④类型的反应生成 ,
其合成路线为 。
故答案为: 。
21