文档内容
专题55 化学平衡常数及计算
1.【2022年重庆卷】两种酸式碳酸盐的分解反应如下。某温度平衡时总压强分别为p 和p。
1 2
反应1:NH HCO (s) NH (g)+HO(g)+CO(g) p=3.6×104Pa
4 3 3 2 2 1
反应2:2NaHCO (s) NaCO(s)+HO(g)+CO(g) p=4×103Pa
3 2 3 2 2 2
该温度下,刚性密闭容器中放入NH HCO 和NaCO 固体,平衡后以上3种固体均大量存在。下列说法错
4 3 2 3
误的是
A.反应2的平衡常数为4×106Pa2 B.通入NH ,再次平衡后,总压强增大
3
C.平衡后总压强为4.36×105Pa D.缩小体积,再次平衡后总压强不变
【答案】B
【解析】A.反应2的平衡常数为 ,A正确;B.刚性密闭容
器,温度不变平衡常数不变,再次达平衡后,容器内各气体分压不变,总压强不变,B错误;C.
, ,
, ,所以总压强为:
,C正确;D.达平衡后,缩小体积,平衡逆向移动,温度不变,
平衡常数不变,再次平衡后总压强不变,D正确;故选B。
2.【2021年江苏卷】N 是合成氨工业的重要原料,NH 不仅可制造化肥,还能通过催化氧化生产HNO;
2 3 3
HNO 能溶解Cu、Ag等金属,也能与许多有机化合物发生反应;在高温或放电条件下,N 与O 反应
3 2 2
生成NO,NO进一步氧化生成NO 。2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1。大气中过量的NO
2 2 2 x
和水体中过量的NH 、NO 均是污染物。通过催化还原的方法,可将烟气和机动车尾气中的NO转化
为N,也可将水体中的NO -转化为N。对于反应2NO(g)+O (g) 2NO (g),下列说法正确的是
2 3 2 2 2
A.该反应的ΔH<0,ΔS<0
B.反应的平衡常数可表示为K=
C.使用高效催化剂能降低反应的焓变
D.其他条件相同,增大 ,NO的转化率下降
【答案】A【解析】A.2NO(g)+O (g)=2NO (g) ΔH=-116.4kJ·mol-1,反应气体物质的量减少,ΔS<0,故A正确;
2 2
B.2NO(g)+O (g) 2NO (g)反应的平衡常数可表示为K= ,故B错误;C.使用高效
2 2
催化剂,反应的焓变不变,故C错误;D.其他条件相同,增大 ,NO的转化率增大,故D错
误;选A。
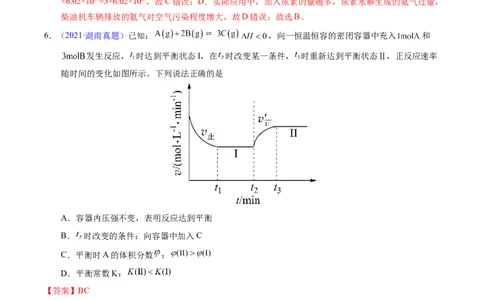
3.【2022年上海卷】向体积为1L的容器中充入4molA,发生反应: ,不同温度下
的平衡常数与达到平衡时B的物质的量如下:
温度
K 4 1
x y
/mol
下列说法正确的是
A.容器中气体的平均摩尔质量不变时,该反应达到平衡
B. 时,若平衡时剩余2molA,则C必为气体
C. 时,当反应达到平衡后,容器内剩余A的物质的量为3mol
D. 时,若容器的体积变为2L,则平衡时 mol
【答案】D
【解析】A.如果C不是气体,则容器内的气体只有B,气体的平均摩尔质量始终为B的摩尔质量,如果
C为气体,由于B、C均为生成物,且物质的量之比始终为2∶1,则容器中气体的平均摩尔质量为
,始终为定值,因此容器内气体的平均摩尔质量不变时,无法判断该反应是否达到平衡,
A错误;B. 时,若平衡时剩余2 mol A,则生成了2 mol B和1 mol C,容器内B的浓度为2 mol·L
,若C为气体,则C的浓度为1 mol·L ,平衡常数 ,符合题目条件,若C不是气
体,则 ,也符合题目条件,故C不一定是气体,B错误;C.T₂时,反应达到平衡后容
器内剩余3 mol A,则生成了1 mol B和0.5 mol C,若C不是气体,则 ,符合题目条件,
若C为气体,则 ,与题目条件不符,C错误;D. 时,容器体积变为2 L,由
于平衡常数只与温度有关,所以平衡常数保持不变,又因为 或 ,
所以需要 保持不变,则平衡时 mol,D正确;故答案选D。
4.【2022年辽宁卷】某温度下,在 恒容密闭容器中 发生反应 ,有关数
据如下:时间段/ 产物Z的平均生成速率/
0~2 0.20
0~4 0.15
0~6 0.10
下列说法错误的是
A. 时,Z的浓度大于
B. 时,加入 ,此时
C. 时,Y的体积分数约为33.3%
D. 时,X的物质的量为
【答案】B
【解析】A.反应开始一段时间,随着时间的延长,反应物浓度逐渐减小,产物Z的平均生成速率逐渐减
小,则 内Z的平均生成速率大于 内的,故 时,Z的浓度大于 ,A正
确; B. 时生成的Z的物质的量为 , 时生成的Z的
物质的量为 ,故反应在 时已达到平衡,设达到平衡时生了
,列三段式:
根据 ,得 ,则Y的平衡浓度为 ,Z的平衡浓度为 ,平衡常数
, 时Y的浓度为 ,Z的浓度为 ,加入 后Z
的浓度变为 , ,反应正向进行,故 ,B错误;
C.反应生成的Y与Z的物质的量之比恒等于1∶2,反应体系中只有Y和Z为气体,相同条件下,体
积之比等于物质的量之比, ,故Y的体积分数始终约为33.3%,C正确;D.由B项分析可
知 时反应处于平衡状态,此时生成Z为 ,则X的转化量为 ,初始X的物质的量为
,剩余X的物质的量为 ,D正确;故答案选B。
5.【2022年江苏卷】用尿素水解生成的 催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,下列说法正确的是
A.上述反应
B.上述反应平衡常数C.上述反应中消耗 ,转移电子的数目为
D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小
【答案】B
【解析】A.由方程式可知,该反应是一个气体分子数增大的反应,即熵增的反应,反应△S>0,故A错
误;B.由方程式可知,反应平衡常数 ,故B正确;C.由方程式可知,反
应每消耗4mol氨气,反应转移12mol电子,则反应中消耗1mol氨气转移电子的数目为3mol×4×
×6.02×1023=3×6.02×1023,故C错误;D.实际应用中,加入尿素的量越多,尿素水解生成的氨气过量,
柴油机车辆排放的氨气对空气污染程度增大,故D错误;故选B。
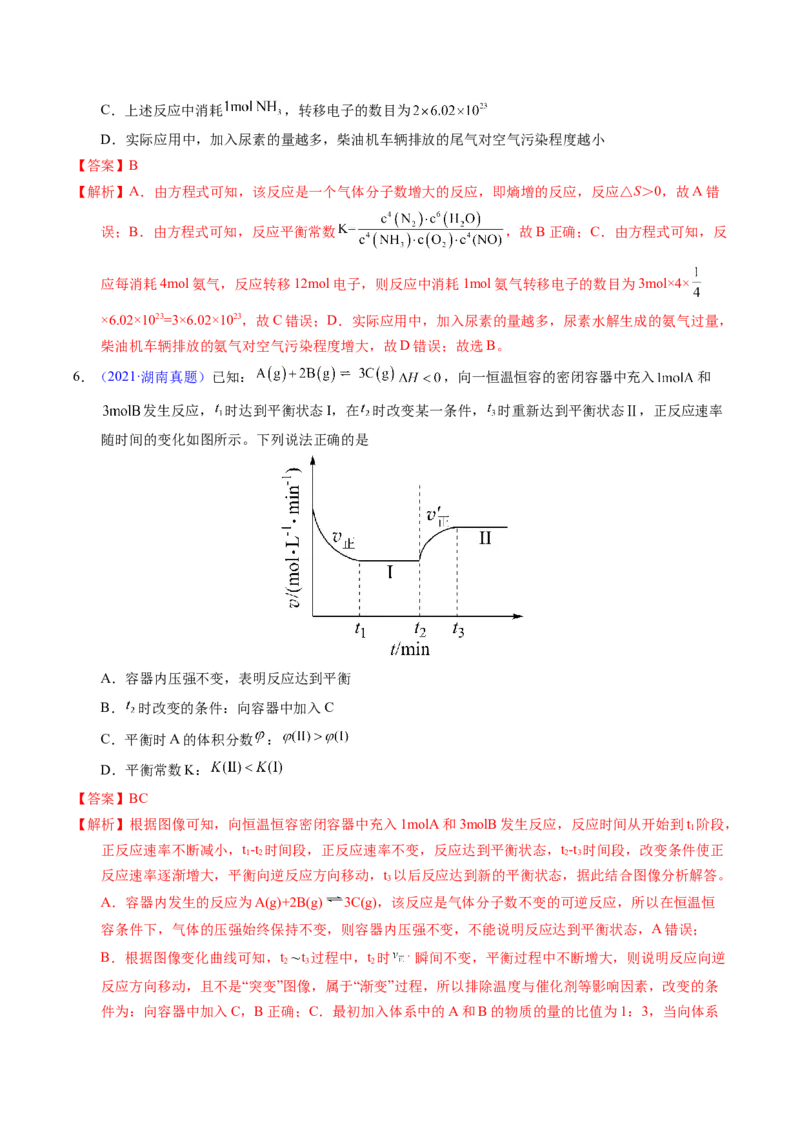
6.(2021·湖南真题)已知: ,向一恒温恒容的密闭容器中充入 和
发生反应, 时达到平衡状态I,在 时改变某一条件, 时重新达到平衡状态Ⅱ,正反应速率
随时间的变化如图所示。下列说法正确的是
A.容器内压强不变,表明反应达到平衡
B. 时改变的条件:向容器中加入C
C.平衡时A的体积分数 :
D.平衡常数K:
【答案】BC
【解析】根据图像可知,向恒温恒容密闭容器中充入1molA和3molB发生反应,反应时间从开始到t 阶段,
1
正反应速率不断减小,t-t 时间段,正反应速率不变,反应达到平衡状态,t-t 时间段,改变条件使正
1 2 2 3
反应速率逐渐增大,平衡向逆反应方向移动,t 以后反应达到新的平衡状态,据此结合图像分析解答。
3
A.容器内发生的反应为A(g)+2B(g) 3C(g),该反应是气体分子数不变的可逆反应,所以在恒温恒
容条件下,气体的压强始终保持不变,则容器内压强不变,不能说明反应达到平衡状态,A错误;
B.根据图像变化曲线可知,t t 过程中,t 时 ,瞬间不变,平衡过程中不断增大,则说明反应向逆
2 3 2
反应方向移动,且不是“突变”图像,属于“渐变”过程,所以排除温度与催化剂等影响因素,改变的条
件为:向容器中加入C,B正确;C.最初加入体系中的A和B的物质的量的比值为1:3,当向体系中加入C时,平衡逆向移动,最终A和B各自物质的量增加的比例为1:2,因此平衡时A的体积分
数 (II)> (I),C正确;D.平衡常数K与温度有关,因该反应在恒温条件下进行,所以K保持不变,
D错误。故选BC。
7.(2020·浙江高考真题)5mL0.1mol⋅L-1KI溶液与1mL0.1mol⋅L-1FeCl
溶液发生反应:
3
2Fe3+ (aq)+2I- (aq)⇌2Fe2+ (aq)+I (aq),达到平衡。下列说法不正确的是( )
2
A.加入苯,振荡,平衡正向移动
B.经苯2次萃取分离后,在水溶液中加入KSCN,溶液呈血红色,表明该化学反应存在限度
C.加入FeSO 固体,平衡逆向移动
4
c2(Fe2+)
D.该反应的平衡常数K=
c2(Fe3+)×c2(I-)
【答案】D
【解析】A.加入苯振荡,苯将I 萃取到苯层,水溶液中c(I)减小,平衡正向移动,A正确;B.将
2 2
5mL0.1mol/LKI溶液与1mL0.1mol/LFeCl 溶液混合,参与反应的Fe3+与I-物质的量之比为1:1,反应后
3
I-一定过量,经苯2次萃取分离后,在水溶液中加入KSCN溶液呈血红色,说明水溶液中仍含有Fe3+,
即Fe3+没有完全消耗,表明该化学反应存在限度,B正确;C.加入FeSO 固体溶于水电离出Fe2+,c
4
c2(Fe2+)⋅c(I )
(Fe2+)增大,平衡逆向移动,C正确;D.该反应的平衡常数K= 2 ,D错误;答案
c2(Fe3+)⋅c2(I-)
选D。
8.(2020·浙江高考真题)一定温度下,在2 L的恒容密闭容器中发生反应 。
反应过程中的部分数据如下表所示:
n/mol
t/min
0 2.0 2.4 0
5 0.9
10 1.6
15 1.6
下列说法正确的是( )
A.0~5 min用A表示的平均反应速率为
B.该反应在10 min后才达到平衡
C.平衡状态时,
D.物质B的平衡转化率为20%
【答案】C【解析】A.v(C)= ,同一反应反应中反应速率之比等于计量数之比,
3v(A)=v(C),所以v(A)= ,错误;B.15min时,n(B)=1.6mol,消耗了
2.4mol-1.6mol=0.8mol,根据方程式可知这段时间内消耗A的物质的量为0.4mol,所以15min时,
n(A)=1.6mol,与10min时A的物质的量相同,说明10~15min这段时间内平衡没有移动,但无法确定
是10min时达到平衡,还是10min前已经达到平衡,错误;C.根据B选项分析可知平衡时消耗的B
为0.8mol,根据方程式可知生成C的物质的量为1.2mol,浓度为 ,正确;
D.物质B的平衡转化率为 ,错误;故答案为C。
9.(2017·浙江高考真题)已知:N(g)+3H(g) 2NH (g) △H=-92kJ/mol。起始反应物为 和 ,
2 2 3
物质的量之比为1:3,且总物质的量不变,在不同压强和温度下,反应达到平衡时,体系中 的物
质的量分数如下表:
温度
400℃ 450℃ 500℃ 600℃
压强
20MPa 0.387 0.274 0.189 0.088
30MPa 0.478 0.359 0.260 0.129
下列说法正确的是
A.体系中 的物质的量分数越大,则正反应速率越大
B.反应达到平衡时, 和 的转化率之比为1∶1
C.反应达到平衡时,放出的热量均为92.4kJ
D.600℃,30MPa下反应达到平衡时,生成 的物质的量最多
【答案】B
【解析】A.体系中 的物质的量分数越大,不能表示正反应速率越大,如20MPa,500℃时 的物
质的量分数大于30MPa,600℃时 的物质的量分数,但温度和压强均为后者大,反应速率后者快,
错误;B.根据方程式,反应的氮气和氢气的物质的量之比为1:3,起始反应物中 和 的物质的
量之比为1:3,因此反应达到平衡时, 和 的转化率之比1:1,正确;C.无法确定反应的氮气
和氢气的物质的量,因此无法计算平衡时放出的热量,错误;D.根据表格数据,反应物的总物质的
量不变时, 的物质的量分数越大,生成 的物质的量越多,则400℃,30MPa下反应达到平衡时,生成 的物质的量最多,错误;故选B。
10.(2015·天津高考真题)某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:
X(g)+m Y(g) 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体
系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A.m=2
B.两次平衡的平衡常数相同
C.X与Y的平衡转化率之比为1:1
D.第二次平衡时,Z的浓度为0.4 mol·L-1
【答案】D
【解析】A.某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y
(g) 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入
1molZ(g),则可等效为两等效平衡体系合,在合并瞬间X、Y、Z的体积分数不变,但单位体积内
体系分子总数增多,依据勒夏特列原理平衡应朝使单位体积内分子总数减小方向移动,但再次达到平
衡后,X、Y、Z的体积分数不变,则说明m+1=3,故m=2,正确;B.同一化学反应的平衡常数只与
温度有关,两次平衡温度不变,故两次平衡的平衡常数相同,正确;C.m=2,起始量X与Y之比为
1:2,则反应过程中由方程式可知反应的X与Y之比为1:2,故X与Y的平衡转化率之比为1:1,正确;
D.m=2,则该反应为反应前后气体总量不变的反应,故第二次平衡时Z的物质的量为:
4mol×10%=0.4mol,故Z的浓度为0.4mol÷2L=0.2mol/L,项错误;本题选D。
11.(2015·重庆高考真题)羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。
在恒容密闭容器中,将CO和HS混合加热并达到下列平衡:
2
CO(g)+H S(g) COS(g)+H (g) K=0.1
2 2
反应前CO物质的量为10mol,平衡后CO物质的量为8mol。下列说法正确的是
A.升高温度,HS浓度增加,表明该反应是吸热反应
2
B.通入CO后,正反应速率逐渐增大
C.反应前HS物质的量为7mol
2
D.CO的平衡转化率为80%
【答案】C
【解析】A.升高温度,HS浓度增加,说明平衡逆向移动,则该反应是放热反应,A错误;B.通入CO
2
后,CO浓度增大,正反应速率瞬间增大,又逐渐减小,B错误;C.根据
CO(g)+H S(g) COS(g)+H (g) K=0.1
2 2
起始物质的量(mol) 10 n 0 0
变化物质的量(mol) 2 2 2 2
平衡物质的量(mol) 8 n-2 2 2
设该容器的体积为V,根据K=0.1,列关系式得 [(2÷V)×(2÷V))÷[(8÷V)×(n-2)÷V]=0.1,解得
n=7,C正确;
D.根据上述数据,CO的平衡转化率为2mol÷10mol×100%=20%,D错误;答案选C。12.(2014·四川高考真题)在10 L恒容密闭容器中充入X(g)和Y(g),发生反应X(g) + Y(g) M(g) +
N(g),所得实验数据如下表:
起始时物质的量/
平衡时物质的量/mol
实验
mol
温度/℃
编号
n(X) n(Y) n(M)
① 700 0.40 0.10 0.090
② 800 0.10 0.40 0.080
③ 800 0.20 0.30 a
④ 900 0.10 0.15 b
下列说法正确的是
A.实验①中,若5 min时测得n(M)=0.050 mol,则0至5 min时间内,用N表示的平均反应速率
υ(N)=1.0×10-2 mol/(L·min)
B.实验②中,该反应的平衡常数K=2.0
C.实验③中,达到平衡时,X的转化率为60%
D.实验④中,达到平衡时,b>0.060
【答案】C
【解析】A.实验①中,若5min时测得n(M)=0.050mol,浓度是0.0050mol/L,根据反应的化学方程式可
知,同时生成的N的物质的量浓度也是0.0050mol/L,因此0至5min时间内,用N表示的平均反应速
率υ(N)=0.0050mol/L÷5min=1.0×10-3mol/(L·min),错误;B、实验②中,平衡时M的浓度是
0.0080mol/L,同时生成的N的浓度是0.0080mol/L,消耗X与Y的浓度均是0.0080mol/L,因此平衡时
X和Y的浓度分别为0.01mol/L-0.0080mol/L=0.002mol/L,0.04mol/L-0.0080mol/L=0.032mol/L,因
此反应的平衡常数K=(0.0080×0.0080)÷(0.002×0.032)=1,错误;C.根据反应的化学方程式可知,如果
X的转化率为60%,则
X(g)+Y(g) M(g)+N(g)
起始浓度(mol/L) 0.020 0.030 0 0
转化浓度(mol/L) 0.012 0.012 0.012 0.012
平衡浓度(mol/L)0.008 0.018 0.012 0.012
温度不变,平衡常数不变,则K=(0.0120×0.0120)÷(0.008×0.018)=1,即反应达到平衡状态,因此最终平衡
时X的转化率为60%。正确;
D.700℃时
X(g)+Y(g) M(g)+ N(g)
起始浓度(mol/L) 0.040 0.010 0 0
转化浓度(mol/L) 0.009 0.009 0.009 0.009
平衡浓度(mol/L) 0.0310 0.001 0.009 0.009则该温度下平衡常K=(0.009×0.009)÷(0.031×0.001)=2.6>1,这说明升高温度平衡常数减小,即平衡向逆反
应方向移动,因此正方应是放热反应。若容器④中温度也是800℃,由于反应前后体积不变,则与③
相比④平衡是等效的,因此最终平衡时M的物质的量b=0.5a=0.06。当温度升高到900℃时平衡向逆
反应方向移动,因此b<0.060,错误;答案选C。
13.(2008·海南高考真题)X、Y、Z三种气体,取X和Y按1:1的物质的量之比混合,放入密闭容器中
发生如下反应:X+2Y 2Z ,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质
的量之比为3:2,则Y的转化率最接近于( )
A.33% B.40% C.50% D.65%
【答案】D
【解析】假设X和Y物质的量为1mol,达到平衡时消耗X物质的量为amol,则:
X+2Y 2Z
起始量(mol)1 1 0
转化量(mol)a 2a 2a
平衡量(mol)1-a 1-2a 2a
根据题意有:(1-a+1-2a):2a =3:2 ,a= ,Y的转化率= ×100%=67%,最接近65%,
答案选D。
14.(2013·四川高考真题)在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生
反应X(g)+Y(g) 2Z(g) △H < 0,一段时间后达到平衡,反应过程中测定的数据如下表:
t/min 2 4 7 9
n(Y)/mol 0.12 0.11 0.10 0.10
下列说法正确的是
A.反应前2min的平均速率ν(Z)=2.0×10-3mol·L-1·min-1
B.其他条件不变,降低温度,反应达到新平衡前ν(逆)> ν(正)
C.该温度下此反应的平衡常数K=1.44
D.其他条件不变,再充入0.2molZ,平衡时X的体积分数增大
【答案】C
【解析】A、v(Y)=(0.16-0.12)mol÷10L÷2min=0.002mol·L-1min-1,则v(Z)= 0.004mol·L-1min-1,错误;B、
降温,平衡正向移动,则达新平衡前,v(正)>v(逆),错误;
C、 X(g)+Y(g) 2Z(g) △H < 0
起始 0.16 0.16 0
变化 0.06 0.06 0.12
平衡 0.10 0.10 0.12K= =1.44,正确;
D、由于该反应是气体体积不变的反应,则达平衡时与原平衡等效,平衡时X的体积分数不变,错误;
答案选C。
15.(2014·上海高考真题)只改变一个影响因素,平衡常数K与化学平衡移动的关系叙述错误的是
A.K值不变,平衡可能移动 B.K值变化,平衡一定移动
C.平衡移动,K值可能不变 D.平衡移动,K值一定变化
【答案】D
【解析】A、平衡常数只与温度有关系,温度不变平衡也可能发生移动,则K值不变,平衡可能移动,A
正确;B、K值变化,说明反应的温度一定发生了变化,因此平衡一定移动,B正确;C、平衡移动,
温度可能不变,因此K值可能不变,C正确;D、平衡移动,温度可能不变,因此K值不一定变化,
D不正确,答案选D。
16.(2010·北京高考真题)某温度下,H(g)+CO(g) HO(g)+CO(g)的平衡常数 。该温度下在
2 2 2 2
甲、乙、丙三个恒容密闭容器中,
起始浓度 甲 乙 丙
c(H)/mol L-1 0.010 0.020 0.020
2
c(CO)/mol L-1 0.010 0.010 0.020
2
投入H(g)和CO(g),其起始浓度如表所示。下列判断不正确的是( )
2 2
A.平衡时,乙中CO 的转化率大于60%
2
B.平衡时,甲中和丙中H 的转化率均是60%
2
C.平衡时,丙中c(CO)是甲中的2倍,是0.012mol/L
2
D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢
【答案】C
【解析】A.设甲容器中平衡时反应掉的二氧化碳的浓度为xmol/L,根据K= =2.25,得
x=0.006,所以CO 的转化率为60%,H 的转化率也是60%,在乙容器中相当于是甲容器中增加了
2 2
H,CO 的转化率增大,不选;B.设甲容器中平衡时反应掉的氢气的浓度为xmol/L,根据K=
2 2
=2.25,得x=0.006,所以H 的转化率是60%,又甲和丙为等效平衡,所以甲中和丙中H
2 2
的转化率均是60%,不选;C.由A的分析可知,平衡时甲容器中c(CO)是0.004mol/L,而甲和丙为
2
等效平衡,但丙的起始浓度为甲的两倍,所以平衡时,丙中c(CO)是0.008mol/L,选;D.根据浓度
2
越大反应速率越快可知,反应开始时,丙中的反应物浓度最大,所以反应速率最快,甲中的反应物浓度最小,所以反应速率最慢,不选;综上所述,故选C。
17.(2009·宁夏高考真题)在一定温度下,反应 H
2
(g)+ X
2
(g)⇌HX(g)的平衡常数为10,若将
1.0mol的HX(g)通入体积为1.0L的密闭容器中,在该温度时HX(g)的最大分解率接近于
A.5% B.17% C.25% D.33%
【答案】B
【解析】由一定温度下,反应 H(g)+ X(g) HX(g)的平衡常数为10,
2 2
则相同条件下HX分解的化学反应的平衡常数为 ,设HX分解的物质的量为x,则
HX(g)⇌ H
2
(g)+ X
2
(g)
开始 1.0mol/L 0 0
转化 mol/L mol/L mol/L
平衡 (1﹣x)mol/L mol/L mol/L
故 = ,
解得x=0.17mol,
该温度时HX(g)的最大分解率为 ×100%=17%,故选B。
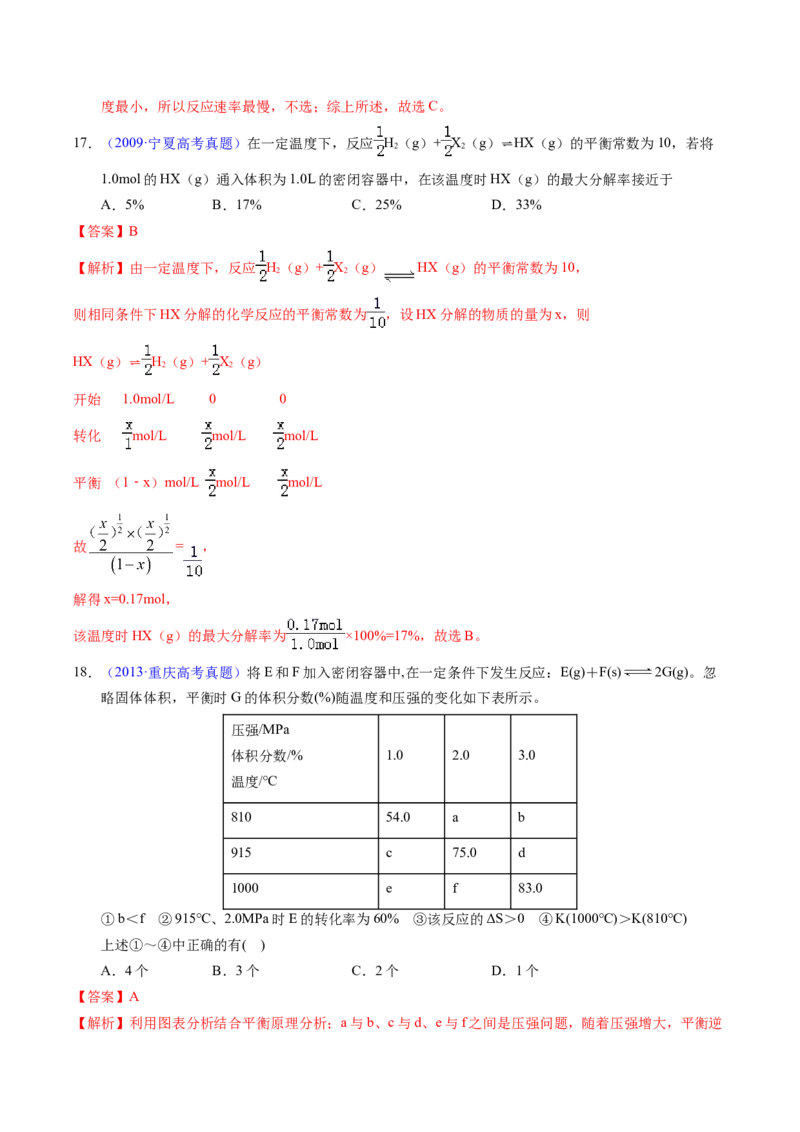
18.(2013·重庆高考真题)将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽
略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示。
压强/MPa
体积分数/% 1.0 2.0 3.0
温度/℃
810 54.0 a b
915 c 75.0 d
1000 e f 83.0
①b<f ②915℃、2.0MPa时E的转化率为60% ③该反应的ΔS>0 ④K(1000℃)>K(810℃)
上述①~④中正确的有( )
A.4个 B.3个 C.2个 D.1个
【答案】A
【解析】利用图表分析结合平衡原理分析;a与b、c与d、e与f之间是压强问题,随着压强增大,平衡逆向移动,G的体积分数减小,b<a,c>75%,e>83%;c、e是温度问题,随着温度升高,G的体积分
数增大,所以正反应是一个吸热反应,所以,K(1000℃)>K(810℃),④正确;f的温度比b的
高,压强比b的小,所以b<f,①正确;设E的起始量为amol,转化率为x,则平衡时G的量为
2ax,由题意得 =75%,解得x=0.6,α=60%,②正确;该反应是一个气体分子增大的反应,
属于熵增反应,所以③正确;答案选A。
19.(2011·江苏高考真题)700℃时,向容积为2L的密闭容器中充入一定量的CO和HO,发生反应:
2
CO(g)+HO(g) CO(g)+H(g),反应过程中测定的部分数据见下表(表中t>t)
2 2 2 1 2
反应时间/min n(CO)/mol HO/ mol
2
0 1.20 0.60
t 0.80
1
t 0.20
2
下列说法正确的是
A.反应在tmin内的平均速率为v(H )=0.40/t mol·L-1·min-1
1 2 1
B.保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH O,到达平衡时,n(CO)=0.40
2 2
mol。
C.保持其他条件不变,向平衡体系中再通入0.20molHO,与原平衡相比,达到新平衡时CO转化率
2
增大,HO的体积分数减小。
2
D.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
【答案】B
【解析】
A.则v(H )=0.20 mol·L-1/ t min,错误;选项B保持其他条件不变,相当于只是将两反应物交换,但量不变,
2 1
所以达相同的平衡态,故正确;C.再通入0.20molHO,平衡右移,则:达到新平衡时CO转化率增
2
大,但HO的转化率减小,故HO的体积分数应增大,错误;D、计算,得:K(700℃)=
2 2
(0.20×0.20)/(0.40×0.10)="1" ,而K(800℃)= 0.64,说明温度升高,K值减小,平衡右移,则
逆向是吸热的,错误
20.(2009·天津高考真题)人体血液内的血红蛋白(Hb)易与O 结合生成HbO ,因此具有输氧能力,CO吸
2 2
入肺中发生反应:CO+HbO O+HbCO,37 ℃时,该反应的平衡常数K=220。HbCO的浓度达
2 2
到HbO 浓度的0.02倍,会使人智力受损。据此,下列结论错误的是
2A.CO与HbO 反应的平衡常数K=
2
B.人体吸入的CO越多,与血红蛋白结合的O 越少
2
C.当吸入的CO与O 浓度之比大于或等于0.02时,人的智力才会受损
2
D.把CO中毒的病人放入高压氧仓中解毒,其原理是使上述平衡向逆反应方向移动
【答案】C
【解析】A.根据化学方程式可知平衡常数表达式为K= ,正确;B.c(CO)增大,
CO+HbO O+HbCO平衡正向移动,正确;C.K= =220,当 =0.02时,
2 2
此时 = =9×10-5,错误;D.增大c(O),使CO+HbO O+HbCO平衡逆向移动解毒,
2 2 2
正确。综上所述,本题正确答案为C。
21.(2008·北京高考真题)工业上制备纯硅反应的热化学方程式如下:SiCl (g)+2H(g) Si(s)
4 2
+4HCl(g);ΔH=+QkJ·mol-1(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应,下
列叙述正确的是( )
A.反应过程中,若增大压强能提高SiCl 的转化率
4
B.若反应开始时SiCl 为1mol,则达平衡时,吸收热量为QkJ
4
C.反应至4min时,若HCl浓度为0.12mol·L-1,则H 反应速率为0.03mol·L-1·min-1
2
D.当反应吸收热量为0.025QkJ时,生成的HCl通入100mL1mol·L-1的NaOH溶液恰好反应
【答案】D
【解析】A.该反应是反应前后气体分子数增大的反应,增大压强,平衡向逆反应方向移动,SiCl 的转化
4
率减小,A错误;B.该反应是可逆反应,达平衡时,吸收热量小于QkJ,B错误;C.速率之比等于
反应系数之比,v(H)= v(HCl)= ,C错误;D.由方程式可
2
知,当反应吸收热量为0.025QkJ时,生成的HCl的物质的量为 ,
100mL1mol·L-1的NaOH的物质的量为0.1mol,二者物质的量相等,恰好反应,D正确;故答案为:
D。
22.【2022年湖南卷】2021年我国制氢量位居世界第一,煤的气化是一种重要的制氢途径。回答下列问题:
(1)在一定温度下,向体积固定的密闭容器中加入足量的 和 ,起始压强为 时,发
生下列反应生成水煤气:
Ⅰ.
Ⅱ.①下列说法正确的是_______;
A.平衡时向容器中充入惰性气体,反应Ⅰ的平衡逆向移动
B.混合气体的密度保持不变时,说明反应体系已达到平衡
C.平衡时 的体积分数可能大于
D.将炭块粉碎,可加快反应速率
②反应平衡时, 的转化率为 ,CO的物质的量为 。此时,整个体系_______(填“吸
收”或“放出”)热量_______kJ,反应Ⅰ的平衡常数 _______(以分压表示,分压=总压×物质
的量分数)。
【答案】(1) BD 吸收 31.2
【解析】
(1)①A.在恒温恒容条件下,平衡时向容器中充入情性气体不能改变反应混合物的浓度,因此反应Ⅰ
的平衡不移动,A说法不正确;
B.在反应中有固体C转化为气体,气体的质量增加,而容器的体积不变,因此气体的密度在反应过程中
不断增大,当混合气体的密度保持不变时,说明反应体系已达到平衡,B说法正确;
C.若C(s)和HO(g)完全反应全部转化为CO(g)和H(g),由C(s)+ 2H O(g) = CO(g)+ 2H (g)可知,H 的体
2 2 2 2 2 2 2
积分数的极值为 ,由于可逆反应只有一定的限度,反应物不可能全部转化为生成物,因此,平衡时
H 的体积分数不可能大于 ,C说法不正确;
2
D.将炭块粉碎可以增大其与HO(g)的接触面积,因此可加快反应速率,D说法正确;
2
综上所述,相关说法正确的是BD。
②反应平衡时,HO(g)的转化率为50%,则水的变化量为0.5mol,水的平衡量也是0.5mol,由于CO的物
2
质的量为0.1mol,则根据O原子守恒可知CO 的物质的量为0.2mol,生成0.2mol CO 时消耗了0.2mol
2 2
CO,故在反应Ⅰ实际生成了0.3molCO。根据相关反应的热化学方程式可知,生成0.3mol CO要吸收
热量39.42kJ ,生成0.2mol CO 要放出热量8.22kJ此时,因此整个体系吸收热量
2
39.42kJ-8.22kJ=31.2kJ;由H原子守恒可知,平衡时H 的物质的量为0.5mol,CO的物质的量为
2
0.1mol,CO 的物质的量为0.2mol,水的物质的量为0.5mol,则平衡时气体的总物质的量为
2
0.5mol+0.1mol+0.2mol+0.5mol=1.3mol,在同温同体积条件下,气体的总压之比等于气体的总物质的量
之比,则平衡体系的总压为0.2MPa 1.3=0.26MPa,反应I(C(s)+HO(g) CO(g)+H(g))的平衡常
2 2
数K = 。
p
23.【2022年河北卷】氢能是极具发展潜力的清洁能源,以氢燃料为代表的燃料电池有良好的应用前景。
(2)工业上常用甲烷水蒸气重整制备氢气,体系中发生如下反应。
Ⅰ.Ⅱ.
①下列操作中,能提高 平衡转化率的是_______ (填标号)。
A.增加 用量 B.恒温恒压下通入惰性气体
C.移除 D.加入催化剂
②恒温恒压条件下, 和 反应达平衡时, 的转化率为 , 的物
质的量为 ,则反应Ⅰ的平衡常数 _______ (写出含有A.b的计算式;对于反应
, ,x为物质的量分数)。其他条件不变,
起始量增加到 ,达平衡时, ,平衡体系中 的物质的量分数为
_______(结果保留两位有效数字)。
【答案】
(2) BC
【解析】
(2)①A.增加CH (g)用量可以提高HO(g)的转化率,但是CH(g)平衡转化率减小,A不符合题意;
4 2 4
B.恒温恒压下通入惰性气体,相当于减小体系压强,反应混合物中各组分的浓度减小,反应Ⅰ的化学平
衡正向移动,能提高CH(g)平衡转化率,B符合题意;
4
C.移除CO(g),减小了反应混合物中CO(g)的浓度,反应Ⅰ的化学平衡正向移动,能提高CH(g)平衡转化
4
率,C符合题意;
D.加入催化剂不能改变平衡状态,故不能提高CH(g)平衡转化率,D不符合题意;
4
综上所述,上述操作中,能提高CH(g)平衡转化率的是BC;
4
②恒温恒压条件下,1 mol CH (g)和1 mol H O(g)反应达平衡时,CH (g)的转化率为α,CO (g)的物质的
4 2 4 2
量为b mol,则转化的CH (g)为α mol,剩余的CH (g)为(1-α )mol,根据C元素守恒可知,CO(g)的
4 4
物质的量为(α-b)mol,根据H和O守恒可知,HO(g)的物质的量为(1-α-b )mol,H(g)的物质的量为
2 2
(3α+b )mol,则反应混合物的总物质的量为(2α+2 )mol,平衡混合物中,CH(g)、HO(g)、 CO(g) 、
4 2
H(g)的物质的量分数分别为 、 、 、 ,因此,反应I的平衡常数K=
2 x
;其他条件不变,HO(g)起始量增加到5mol,达平衡时,a
2
=0.90,b =0.65,则平衡时,CH (g)为0.1mol,根据C元素守恒可知,CO(g)的物质的量为
4
0.25mol,,根据H和O守恒可知,HO(g)的物质的量为(5-0.90-0.65 )mol=3.45mol,H(g)的物质的量
2 2
为(3α+b )mol=3.35mol,平衡混合物的总物质的量为(2α+6 )mol=7.8mol,平衡体系中H(g)的物质的量
2
分数为 ;24.(2021·湖南真题)氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两
种方法由氨气得到氢气。
方法I:氨热分解法制氢气
相关化学键的键能数据
化学键
键能 946 436.0 390.8
一定温度下,利用催化剂将 分解为 和 。回答下列问题:
(1)反应 _______ ;
(2)已知该反应的 ,在下列哪些温度下反应能自发进行?_______(填标号)
A.25℃ B.125℃ C.225℃ D.325℃
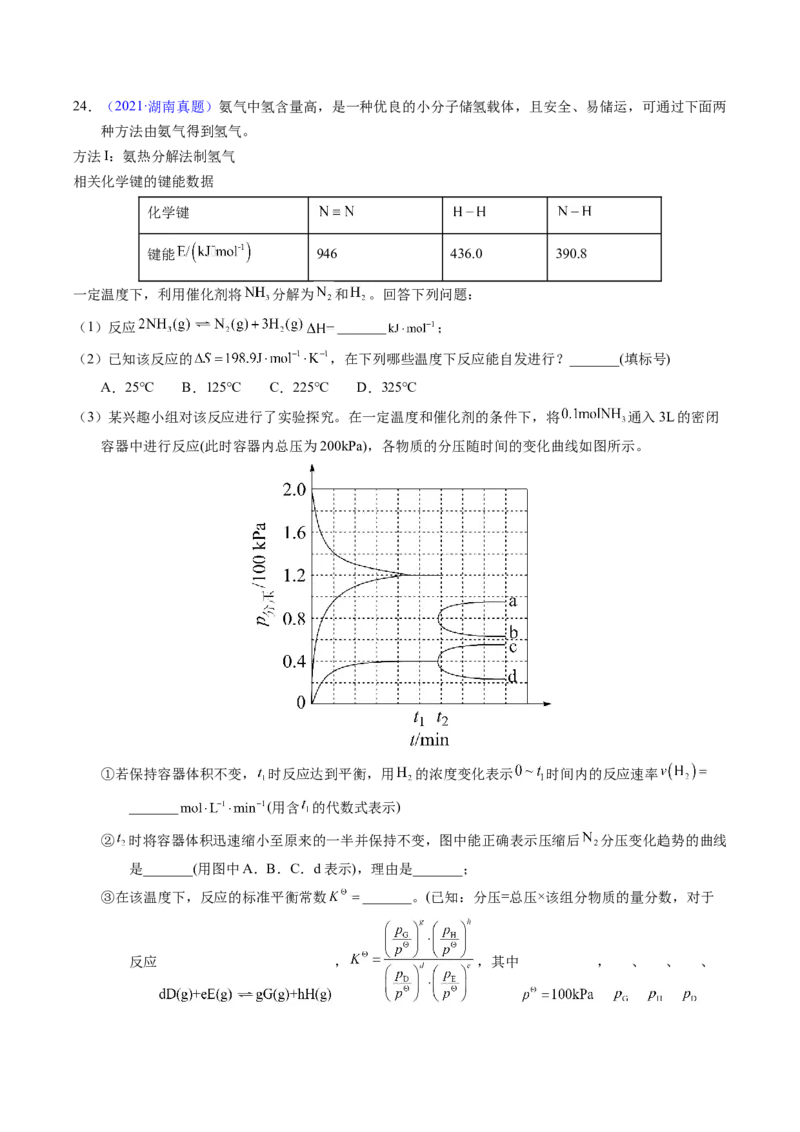
(3)某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将 通入3L的密闭
容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。
①若保持容器体积不变, 时反应达到平衡,用 的浓度变化表示 时间内的反应速率
_______ (用含 的代数式表示)
② 时将容器体积迅速缩小至原来的一半并保持不变,图中能正确表示压缩后 分压变化趋势的曲线
是_______(用图中A.B.C.d表示),理由是_______;
③在该温度下,反应的标准平衡常数 _______。(已知:分压=总压×该组分物质的量分数,对于
反应 , ,其中 , 、 、 、为各组分的平衡分压)。
【答案】
(1)+90.8
(2)CD
(3)① ②b 开始体积减半,N 分压变为原来的2倍,随后由于加压平衡逆向移动,N
2 2
分压比原来2倍要小 ③0.48
【解析】
(1) 根据反应热=反应物的总键能-生成物的总键能,2NH (g) N(g)+3H(g), H=390.8kJ mol-1 -
3 2 2
(946 kJ mol-1+436.0kJ mol-1 )= +90.8kJ mol-1,故答案为:+90.8;
(2)若反应自发进行,则需 H-T S<0,T> = =456.5K,即温度应高于(456.5-
273)℃=183.5℃,CD符合,故答案为:CD;
(3)①设t 时达到平衡,转化的NH 的物质的量为2x,列出三段式:
1 3
根据同温同压下,混合气体的物质的量等于体积之比, = ,解得x=0.02mol, (H )=
2
= mol L-1 min-1,故答案为: ;
②t 时将容器体积压缩到原来的一半,开始N 分压变为原来的2倍,随后由于加压平衡逆向移动,N 分压
2 2 2
比原来2倍要小,故b曲线符合,故答案为:b;开始体积减半,N 分压变为原来的2倍,随后由于加
2
压平衡逆向移动,N 分压比原来2倍要小;
2
③由图可知,平衡时,NH 、N、H 的分压分别为120 kPA.40 kPA.120 kPa,反应的标准平衡常数 =
3 2 2
=0.48,故答案为:0.48;
25.(2021·河北真题)当今,世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用
技术,降低空气中二氧化碳含量成为研究热点。
(2)雨水中含有来自大气的CO,溶于水中的CO 进一步和水反应,发生电离:
2 2
①CO(g)=CO (aq)
2 2
②CO(aq)+H O(l)=H+(aq)+HCO (aq)
2 2
25℃时,反应②的平衡常数为K 。
2
溶液中CO 的浓度与其在空气中的分压成正比(分压=总压×物质的量分数),比例系数为
2
ymol•L-1•kPa-1,当大气压强为pkPa,大气中CO(g)的物质的量分数为x时,溶液中H+浓度为
2________mol•L-1(写出表达式,考虑水的电离,忽略HCO 的电离)
(3)105℃时,将足量的某碳酸氢盐(MHCO )固体置于真空恒容容器中,存在如下平衡:2MHCO (s)
3 3
MCO(s)+HO(g)+CO(g)。上述反应达平衡时体系的总压为46kPa。
2 3 2 2
保持温度不变,开始时在体系中先通入一定量的CO(g),再加入足量MHCO (s),欲使平衡时体系中
2 3
水蒸气的分压小于5kPa,CO(g)的初始压强应大于________kPa。
2
【答案】
(2)
(3)100.8
【解析】
(2)由题可知,①CO(s) CO(aq),②CO(aq)+H O(l) H+(aq)+HC (aq),K = ,又
2 2 2 2 2
因为p(CO)=p(kPa) x,则c(CO)=y(mol•L-1•kPa-1)p(CO )=p x y mol/L,在忽略HC 的电离时,
2 2 2
c(H+)=c(HC ),所以可得c(H+)= ,故答案为: ;
(3)2MHCO (s) MCO(s)+HO(g)+ CO (g),等温等容条件下,压强之比等于物质的量之比,可用分压
3 2 3 2 2
表示物质的量浓度,平衡常数K = = =529kPa2。温度不变化学平衡常数K 不变,
p p
设平衡时,平衡体系中CO 的分压为x,则K= = 529kPa2, = kPa=105.8kPa,CO 的
2 2
初始压强等于平衡压强减去碳酸氢盐分解产生的CO 的分压,即CO(g)的初始压强应大于
2 2
105.8kPa-5kPa=100.8kPa,故答案为:100.8;
26.(2012·海南高考真题)已知A(g)+B(g) C(g)+D(g)反应的平衡常数和温度的关系如下:
|温度/ ℃ 700 900 830 1000 1200
平衡常数 1.7 1.1 1.0 0.6 0.4
回答下列问题:
(1)该反应的平衡常数表达式K=____________,△H____0(填“<”“ >”“ =”);
(2)830℃时,向一个5 L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反
应速率v(A)=0.003 mol·L-1·s-1。则6s时c(A)=_____mol·L-1, C的物质的量为______mol;若反应经一
段时间后,达到平衡时A的转化率为_____,如果这时向该密闭容器中再充入1 mol氩气,平衡时A
的转化率为_________;
(3)判断该反应是否达到平衡的依据为______(填正确选项前的字母):
a.压强不随时间改变 b.气体的密度不随时间改变c.c(A)不随时间改变 d.单位时间里生成C和D的物质的量相等
(4)1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数的值为_____________。
【答案】(1)[c(C)c(D)]/[c(A)c(B)] < (2)0.022 0.09 80% 80% (3)c (4)
2.5
【解析】
(1)A(g)+B(g) C(g)+D(g)反应的平衡常数表达式为K=[c(C)c(D)]/[c(A)c(B)];700℃时,平衡常数为
1.7,1000℃时,平衡常数为0.6,故温度越高,平衡常数越小,说明此反应为放热反应,即△H<0;
(2)反应初始6s内A的平均反应速率v(A)=0.003mol•L-1•s-1,则6s时
△n(A)=0.003mol•L-1•s-1×6s×5L=0.09mol,故A剩余物质的量为:n(A)=0.2mol-0.09mol=0.11mol,则6s
时c(A)= =0.022mol/L,根据方程式可知,消耗A0.09mol时,生成C的物质的量为
0.09mol;
设平衡时A的浓度变化量为x,则:
A(g)+B(g) C(g)+D(g)
开始(mol/L):0.04 0.16 0 0
变化(mol/L):x x x x
平衡(mol/L):0.04-x 0.16-x x x
故 =1,解得x=0.032,所以平衡时A的转化率为 ×100%=80%,此时C
的物质的量为0.032mol/L×5L=0.16mol;如果这时向该密闭容器中再充入1mol氩气,体积不变,平衡
没有移动, A的转化率仍为80%;
(3) a.因气体反应物与生成物系数不变,压强始终不随时间改变 ,故a错误;
b.气体的质量不变,体积不变,气体的密度始终不变,故b错误;
c.c(A)不随时间改变,说明反应物或生成物的量一定,是平衡状态,故c正确;
d.单位时间里生成C和D的物质的量相等,此时不一定是平衡状态,故d错误,
答案为c;
(4)由图表知1200℃时反应A(g)+B(g) C(g)+D(g)的平衡常数的值为0.4,则C(g)+D(g) A(g)+B(g)
的平衡常数为 =2.5。
27.(2014·山东高考真题)研究氨氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
2NO (g)+NaCl(s) NaNO (s)+ClNO(g) K ΔH<0(Ⅰ)
2 3 1 1
2NO(g)+Cl(g) 2ClNO(g) K ΔH<0(Ⅱ)
2 2 2
(1)4NO (g)+2NaCl(s) 2NaNO (s)+2NO(g)+Cl(g)的平衡常数K=_______(用K、K 表示)。
2 3 2 1 2
(2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2 L恒容密闭容器中加入0.2 mol NO和0.1 mol
Cl,10 min时反应(Ⅱ)达到平衡。测得10 min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后n(Cl )=
2 2________mol,NO的转化率α =________。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时
1
NO的转化率α ________α (填“>”“<”或“=”),平衡常数K______(填“增大”“减小”或“不
2 1 2
变”)。若要使K 减小,可采取的措施是________。
2
【答案】(1) (2)2.5×10-2 75% > 不变 升高温度
【解析】
(1)由化学平衡常数的概念写出K=c(ClNO)/c2(NO ),K=c2(ClNO)/[c2(NO)·c(Cl )],反应4NO (g)
1 2 2 2 2
+2NaCl(s) 2NaNO (s)+2NO(g)+Cl(g)的平衡常数K=[ c2(NO)·c(Cl )]/c4(NO )= 。
3 2 2 2
(2)反应起始到平衡时转化的ClNO物质的量为7.5×10-3mol•L-1•min-1 10min 2L=0.15mol,用三段式计算
2NO(g)+Cl(g) 2ClNO(g)
2
n(起始)(mol) 0.2 0.1 0
n(转化)(mol) 0.15 0.075 0.15
n(平衡)(mol) 0.05 0.025 0.15
则平衡后n(Cl)=0.025mol。NO的转化率a=0.15mol 0.2mol=0.75。该反应的正反应为气体分子数减小
2 1
的反应,该反应若在其他条件不变,恒压条件下进行,相当于在恒容条件下达到平衡后,增大压强,
平衡正向移动,平衡时NO的转化率增大,a a。平衡常数只与温度有关,温度不变平衡常数不变,
2 1
K 不变。要使K 减小只能改变温度,由于该反应的正反应为放热反应,所以使K 减小只能升高温度。
2 2 2
28.(2019·海南高考真题)由 羟基丁酸生成 丁内酯的反应如下:HOCH CHCHCOOH
2 2 2
+H O
2
在298K下, 羟基丁酸水溶液的初始浓度为 ,测得 丁内酯的浓度随时间变化的数据
如表所示。回答下列问题:
21 50 80 100 120 160 220
0.024 0.050 0.071 0.081 0.090 0.104 0.116 0.132
(1)该反应在50~80min内的平均反应速率为_____ 。
(2)120min时 羟基丁酸的转化率为______。
(3)298K时该反应的平衡常数 _____。
(4)为提高 羟基丁酸的平衡转化率,除适当控制反应温度外,还可采取的措施是______。
【答案】(1)0.0007 (2)0.5(50%) (3) (4)将 丁内酯移走
【解析】(1) υ= = =0.0007mol/(L·min);
(2)在120min时反应产生的 丁内酯的物质的量浓度0.090mol/L,则反应消耗的 羟基丁酸的浓度
为0.090mol/L,由于反应开始时 羟基丁酸的浓度0.180mol/L,所以 羟基丁酸的转化率为
=50%;
(3)298K的摄氏温度为25℃,水为液态,则此时该反应的平衡常数K= =
= ;
(4)为提高 羟基丁酸的平衡转化率,使化学平衡正向移动,除适当控制反应温度外,还可采取的措施
是及时分离出 丁内酯。
29.(2017·全国高考真题)近期发现,HS是继NO、CO之后的第三个生命体系气体信号分子,它具有参
2
与调节神经信号传递、舒张血管减轻高血压的功能。回答下列问题:
(3)HS与CO 在高温下发生反应:HS(g)+CO(g) COS(g) +HO(g)。在610 K时,将0.10 mol CO 与
2 2 2 2 2 2
0.40 mol HS充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
2
①HS的平衡转化率 =_______%,反应平衡常数K=________。
2
②在620 K重复试验,平衡后水的物质的量分数为0.03,HS的转化率 _____ ,该反应的
2
H_____0。(填“>”“<”或“=”)
③向反应器中再分别充入下列气体,能使HS转化率增大的是________(填标号)
2
A.HS B.CO C.COS D.N
2 2 2
【答案】(3)①2.5 2.8×10–3 ②> > ③B
【解析】
(3)设反应的HS物质的量为x,由题意列三段式得:
2
因为反应平衡后水的物质的量分数为0.02,所以 =0.02,解得x=0.01;①HS的
2
平衡转化率α =0.01÷0.40×100%=2.5%;反应平衡常数K= = ≈2.849×10-3(或2.8×10-3或
1
2.85×10-3)。
②由已知,升温,水的物质的量分数增大,所以升温时平衡正向移动,故α >α ,ΔH>0。
2 1③A项,再充入HS,平衡正向移动,使CO 转化率增大,根据化学平衡移动原理,HS的转化率减小,
2 2 2
故A错误;B项,再充入CO,平衡正向移动,在不改变HS初始量的前提下,使HS转化率增大,
2 2 2
故B正确;C项,再充入COS,平衡逆向移动,使HS的转化率减小,故C错误;D项,再充入N,
2 2
与该反应无关,平衡不移动,HS的转化率不变,故D错误。综上选B。
2
30.(2016·海南高考真题)顺-1,2-二甲基环丙烷和反-1,2-二甲基环丙烷可发生如下转化:
该反应的速率方程可表示为:v =k c 和v =k c ,k 和k 在一定温度时为常数,分
(正) (正) (顺) (逆) (逆) (反) (正) (逆)
别称作正,逆反应速率常数。回答下列问题:
(1)已知:t 温度下, , ,该温度下反应的平衡常数值K=_____;该反应
1 1
的活化能E(正)小于E(逆),则 ________0(填“小于”“等于”或“大于”)。
a a
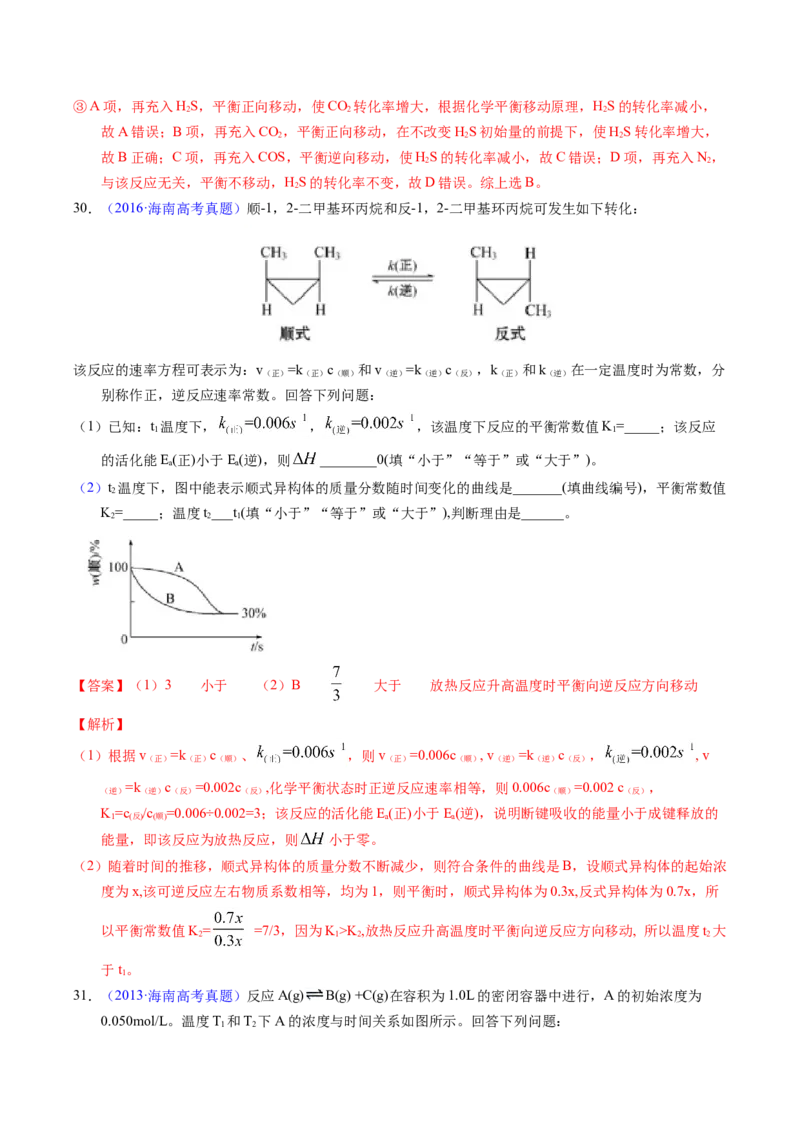
(2)t 温度下,图中能表示顺式异构体的质量分数随时间变化的曲线是_______(填曲线编号),平衡常数值
2
K=_____;温度t___t(填“小于”“等于”或“大于”),判断理由是______。
2 2 1
【答案】(1)3 小于 (2)B 大于 放热反应升高温度时平衡向逆反应方向移动
【解析】
(1)根据v =k c 、 ,则v =0.006c , v =k c , , v
(正) (正) (顺) (正) (顺) (逆) (逆) (反)
=k c =0.002c ,化学平衡状态时正逆反应速率相等,则0.006c =0.002 c ,
(逆) (逆) (反) (反) (顺) (反)
K=c /c =0.006÷0.002=3;该反应的活化能E(正)小于E(逆),说明断键吸收的能量小于成键释放的
1 (反) (顺) a a
能量,即该反应为放热反应,则 小于零。
(2)随着时间的推移,顺式异构体的质量分数不断减少,则符合条件的曲线是B,设顺式异构体的起始浓
度为x,该可逆反应左右物质系数相等,均为1,则平衡时,顺式异构体为0.3x,反式异构体为0.7x,所
以平衡常数值K= =7/3,因为K>K ,放热反应升高温度时平衡向逆反应方向移动, 所以温度t 大
2 1 2 2
于t。
1
31.(2013·海南高考真题)反应A(g) B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为
0.050mol/L。温度T 和T 下A的浓度与时间关系如图所示。回答下列问题:
1 2(1)上述反应的温度T___ T,平衡常数K(T)___K(T )。(填“大于”、“小于” 或“等于”)
1 2 1 2
(2)若温度T 时,5min后反应达到平衡,A的转化率为70%,则:
2
①平衡时体系总的物质的量为_______。
②反应的平衡常数K=______。
③反应在0~5min区间的平均反应速率v(A)=_______。
【答案】(1)小于 小于 (2)①0.085mol ②0.082mol/L ③0.007mol/(L·min)
【解析】
(1)由图可知,温度为T 时反应先达到平衡状态,温度越高,反应速率越快,达到平衡所需的时间越短,
2
所以T 小于T;据图可知,温度为T 时c(A)小,说明升高温度平衡正向移动,所以正反应为吸热
1 2 2
反应,温度越高K值越大,故答案为小于;小于;
(2) A(g) B(g)+C(g)
起始浓度:0.050 0 0
变化浓度:0.035 0.035 0.035
平衡浓度:0.015 0.035 0.035
①平衡时体系总的物质的量为=(0.015+0.035+0.035)mol/L×1L=0.085mol;
②K= =0.082mol/L;
③反应在0~5min区间的平均反应速率v(A)= =0.007mol/(L•min);
32.(2014·海南高考真题)(9分)硝基苯甲酸乙酯在OH-存在下发生水解反应:ONC HCOOC H+OH-
2 6 4 2 5
ONC HCOO-+C HOH.两种反应物的初始浓度均为0.050mol/L,15 ℃时测得:
2 6 4 2 5
ONC HCOOC H 的转化率α随时间变化的数据如表所示。回答下列问题:
2 6 4 2 5
t/s 0 120 180 240 330 30 600 700 800
α/% 0 33.0 41.8 48.8 58.0 69.0 70.4 71.0 71.0
(1)列式计算该反应在120~180s与180~240s区间的平均反应速率_______、__________。比较两者大
小可得到的结论是_______________________。
(2)列式计算15 ℃时该反应的平衡常数_________________。
(3)为提高ONC HCOOC H 的平衡转化率,除可适当控制反应温度外,还可以采取的措施有_________
2 6 4 2 5
(要求写出两条)。【答案】(1) ;
.随着反应的的进行,反应物的浓度
降低,反应速率减慢 (2) 或 ;
(3)增加OH-的浓度,移去产物。
【解析】
(1)根据题意结合表格的数据可知在120~180s内的反应速率是
。在180~240s内的反应速率是
由反应速率的数值可以看出:随着
反应的的进行,反应物的浓度降低,反应速率减慢。
(2)在15 ℃时该反应的平衡常数是 ;(3)为提高ONC HCOOC H 的平衡
2 6 4 2 5
转化率,除可适当控制反应温度外,还可以采取的措施有增加其它反应物浓度的方法或减小生成物浓
度的方法。因此对该反应来说,就是可采取增大OH-的浓度,移去产物的方法。