文档内容
专题58 弱电解质的电离
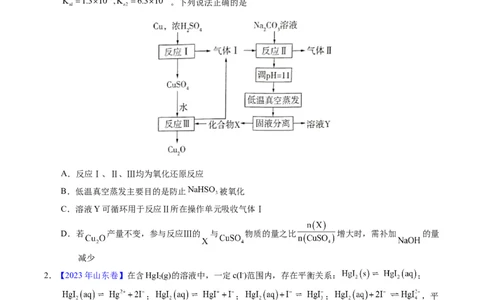
1.【2023年山东卷】一种制备 的工艺路线如图所示,反应Ⅱ所得溶液 在3~4之间,反应Ⅲ需及
时补加 以保持反应在 条件下进行。常温下, 的电离平衡常数
。下列说法正确的是
A.反应Ⅰ、Ⅱ、Ⅲ均为氧化还原反应
B.低温真空蒸发主要目的是防止 被氧化
C.溶液Y可循环用于反应Ⅱ所在操作单元吸收气体Ⅰ
D.若 产量不变,参与反应Ⅲ的 与 物质的量之比 增大时,需补加 的量
减少
2.【2023年山东卷】在含HgI (g)的溶液中,一定c(I-)范围内,存在平衡关系: ;
2
; ; ; ,平
衡常数依次为 。已知 、 , 、 随
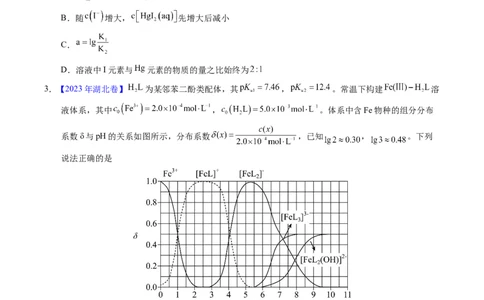
的变化关系如图所示,下列说法错误的是A.线 表示 的变化情况
B.随 增大, 先增大后减小
C.
D.溶液中I元素与 元素的物质的量之比始终为
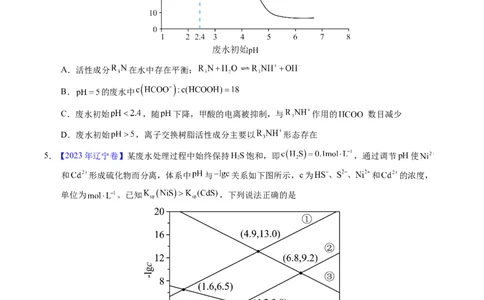
3.【2023年湖北卷】 为某邻苯二酚类配体,其 , 。常温下构建 溶
液体系,其中 , 。体系中含Fe物种的组分分布
系数δ与pH的关系如图所示,分布系数 ,已知 , 。下列
说法正确的是
A.当 时,体系中
B.pH在9.5~10.5之间,含L的物种主要为
C. 的平衡常数的lgK约为14
D.当 时,参与配位的
4.【2023年1月浙江卷】甲酸 是重要的化工原料。工业废水中的甲酸及其盐,通过离子交换树脂(含固体活性成分 ,R为烷基)因静电作用被吸附回收,其回收率(被吸附在树脂上甲酸根的物质
的量分数)与废水初始 关系如图(已知甲酸 ),下列说法不正确的是
A.活性成分 在水中存在平衡:
B. 的废水中
C.废水初始 ,随 下降,甲酸的电离被抑制,与 作用的 数目减少
D.废水初始 ,离子交换树脂活性成分主要以 形态存在
5.【2023年辽宁卷】某废水处理过程中始终保持HS饱和,即 ,通过调节pH使
2
和 形成硫化物而分离,体系中 与 关系如下图所示,c为 和 的浓度,
单位为 。已知 ,下列说法正确的是
A. B.③为 与 的关系曲线
C. D.
6.【2022年福建卷】探究醋酸浓度与电离度 关系的步骤如下,与相关步骤对应的操作或叙述正确的步骤 操作或叙述
A Ⅰ.用 标准溶液标定醋酸溶液浓度 滴定时应始终注视滴定管中的液面
B Ⅱ.用标定后的溶液配制不同浓度的醋酸溶液 应使用干燥的容量瓶
C Ⅲ.测定步骤Ⅱ中所得溶液的 应在相同温度下测定
D Ⅳ.计算不同浓度溶液中醋酸的电离度
计算式为
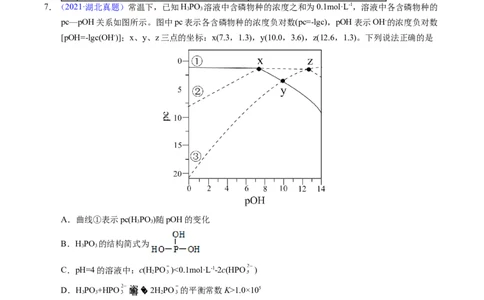
7.(2021·湖北真题)常温下,已知HPO 溶液中含磷物种的浓度之和为0.1mol·L-1,溶液中各含磷物种的
3 3
pc—pOH关系如图所示。图中pc表示各含磷物种的浓度负对数(pc=-lgc),pOH表示OH-的浓度负对数
[pOH=-lgc(OH-)];x、y、z三点的坐标:x(7.3,1.3),y(10.0,3.6),z(12.6,1.3)。下列说法正确的是
A.曲线①表示pc(HPO )随pOH的变化
3 3
B.HPO 的结构简式为
3 3
C.pH=4的溶液中:c(H PO )<0.1mol·L-1-2c(HPO )
2
D.HPO +HPO 2HPO 的平衡常数K>1.0×105
3 3 2
8.【2022年湖北卷】根据酸碱质子理论,给出质子 的物质是酸,给出质子的能力越强,酸性越强。
已知: , ,下列酸性强弱顺序正确的是
A. B.
C. D.
9.【2022年海南卷】NaClO溶液具有漂白能力,已知25℃时,K=(HClO)=4.0×10-8。下列关于NaClO溶
a
液说法正确的是
A.0.01mol/L溶液中,c(ClO-)<0.01mol/LB.长期露置在空气中,释放Cl,漂白能力减弱
2
C.通入过量SO ,反应的离子方程式为SO +ClO-+H O=HSO +HClO
2 2 2
D.25℃,pH=7.0的NaClO和HClO的混合溶液中,c(HClO)>c(ClO-)=c(Na+)
10.【2022年全国乙卷】常温下,一元酸 的 。在某体系中, 与 离子不能穿过
隔膜,未电离的 可自由穿过该膜(如图所示)。
设溶液中 ,当达到平衡时,下列叙述正确的是
A.溶液Ⅰ中
B.溶液Ⅱ中的HA的电离度 为
C.溶液Ⅰ和Ⅱ中的 不相等
D.溶液Ⅰ和Ⅱ中的 之比为
11.【2022年6月浙江卷】关于反应 ,达到平衡后,
下列说法不正确的是
A.升高温度,氯水中的 减小
B.氯水中加入少量醋酸钠固体,上述平衡正向移动, 增大
C.取氯水稀释, 增大
D.取两份氯水,分别滴加 溶液和淀粉KI溶液,若前者有白色沉淀,后者溶液变蓝色,可以
证明上述反应存在限度
12.【2022年6月浙江卷】 时,苯酚 的 ,下列说法正确的是
A.相同温度下,等 的 和 溶液中,
B.将浓度均为 的 和 溶液加热,两种溶液的 均变大
C. 时, 溶液与 溶液混合,测得 ,则此时溶液中
D. 时, 的 溶液中加少量 固体,水的电离程度变小
13.(2021.6·浙江真题)某同学拟用 计测定溶液 以探究某酸HR是否为弱电解质。下列说法正确的
是A.25℃时,若测得 溶液 ,则HR是弱酸
B.25℃时,若测得 溶液 且 ,则HR是弱酸
C.25℃时,若测得HR溶液 ,取该溶液 ,加蒸馏水稀释至 ,测得 ,
则HR是弱酸
D.25℃时,若测得NaR溶液 ,取该溶液 ,升温至50℃,测得 , ,则HR是弱
酸
14.(2020·全国高考真题)二氧化碳的过量排放可对海洋生物的生存环境造成很大影响,其原理如下图所
示。下列叙述错误的是
A.海水酸化能引起 浓度增大、 浓度减小
B.海水酸化能促进CaCO 的溶解,导致珊瑚礁减少
3
C.CO 能引起海水酸化,其原理为 H++
2
D.使用太阳能、氢能等新能源可改善珊瑚的生存环境
15.(2020·北京高考真题)室温下,对于1L0.1mol•L-1醋酸溶液。下列判断正确的是
A.该溶液中CHCOO-的粒子数为6.02×1022
3
B.加入少量CHCOONa固体后,溶液的pH降低
3
C.滴加NaOH溶液过程中,n(CHCOO-)与n(CHCOOH)之和始终为0.1mol
3 3
D.与NaCO 溶液反应的离子方程式为CO +2H+=H O+CO↑
2 3 2 2
16.(2020·浙江高考真题)下列说法不正确的是( )
A. 的溶液不一定呈碱性
B.中和pH和体积均相等的氨水、 溶液,所需 的物质的量相同
C.相同温度下,pH相等的盐酸、 溶液中, 相等
D.氨水和盐酸反应后的溶液,若溶液呈中性,则
17.(2019·浙江高考真题)下列属于强电解质的是
A.硫酸钡 B.食盐水 C.二氧化硅 D.醋酸18.(2019·全国高考真题)设N 为阿伏加德罗常数值。关于常温下pH=2的HPO 溶液,下列说法正确的
A 3 4
是
A.每升溶液中的H+数目为0.02N
A
B.c(H+)= c( )+2c( )+3c( )+ c(OH−)
C.加水稀释使电离度增大,溶液pH减小
D.加入NaH PO 固体,溶液酸性增强
2 4
19.(2019·天津高考真题)某温度下, 和 的电离常数分别为 和 。
将 和体积均相同的两种酸溶液分别稀释,其 随加水体积的变化如图所示。下列叙述正确的是
( )
A.曲线Ⅰ代表 溶液
B.溶液中水的电离程度:b点>c点
C.从c点到d点,溶液中 保持不变(其中 、 分别代表相应的酸和酸根离
子)
D.相同体积a点的两溶液分别与 恰好中和后,溶液中 相同
20.(2018·浙江高考真题)下列说法不正确的是
A.测得0.1 mol·L-1的一元酸HA溶液pH=3.0,则HA一定为弱电解质
B.25℃时,将0.1 mol·L-1的NaOH溶液加水稀释100倍,所得溶液的pH=11.0
C.25℃时,将0.1 mol·L-1的HA溶液加水稀释至pH=4.0,所得溶液c(OH-)=1×10-10 mol·L-1
D.0.1 mol·L-1的HA溶液与0.1 mol·L-1的NaOH溶液等体积混合,所得溶液pH一定等于7.0
21.(2018·浙江高考真题)相同温度下,关于盐酸和醋酸两种溶液的比较,下列说法正确的是
A.pH相等的两溶液中:c(CHCOOˉ)=c(Clˉ)
3
B.分别中和pH相等、体积相等的两溶液,所需NaOH的物质的量相同
C.相同浓度的两溶液,分别与金属镁反应,反应速率相同
D.相同浓度的两溶液,分别与NaOH固体反应后呈中性的溶液中(忽略溶液体积变化):c(CHCOOˉ)
3
=c(Clˉ)
22.(2018·天津高考真题)LiH PO 是制备电池的重要原料。室温下,LiH PO 溶液的pH随c
2 4 2 4 初始(HPO –)的变化如图1所示,HPO 溶液中HPO –的分布分数δ随pH的变化如图2所示,[
2 4 3 4 2 4
]下列有关LiH PO 溶液的叙述正确的是
2 4
A.溶液中存在3个平衡
B.含P元素的粒子有HPO –、HPO 2–、PO 3–
2 4 4 4
C.随c (HPO –)增大,溶液的pH明显变小
初始 2 4
D.用浓度大于1 mol·L-1的HPO 溶液溶解LiCO,当pH达到4.66时,HPO 几乎全部转化为
3 4 2 3 3 4
LiH PO
2 4
23.(2013·上海高考真题)HS水溶液中存在电离平衡HS H++HS-和HS- H++S2-。若向HS溶液
2 2 2
中
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO 气体,平衡向左移动,溶液pH值增大
2
C.滴加新制氯水,平衡向左移动,溶液pH值减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
24.(2015·全国高考真题)浓度均为0.10mol/L、体积均为V 的MOH和ROH溶液,分别加水稀释至体积
0
V,pH随 的变化如图所示,下列叙述错误的是( )
A.MOH的碱性强于ROH的碱性
B.ROH的电离程度:b点大于a点C.若两溶液无限稀释,则它们的c(OH-)相等
D.当 =2时,若两溶液同时升高温度,则 增大
25.(2016·浙江高考真题)常温下,关于pH相等的盐酸和醋酸溶液(两溶液的OH-浓度也相等),下列说
法正确的是( )
A.c(HCl)>c(CH COOH)
3
B.c(Cl-)=c(CHCOO-)
3
C.等体积的盐酸和醋酸溶液分别与足量的Zn完全反应,盐酸产生的H 多
2
D.用相同浓度的NaOH溶液分别与等体积的盐酸和醋酸溶液恰好反应完全,盐酸消耗的NaOH溶液
体积多
26.(2016·上海高考真题)能证明乙酸是弱酸的实验事实是
A.CHCOOH溶液与Zn反应放出H
3 2
B.0.1 mol/L CH COONa溶液的pH大于7
3
C.CHCOOH溶液与NaCO 反应生成CO
3 3 2
D.0.1 mol/L CH COOH溶液可使紫色石蕊变红
3
27.(2014·全国高考真题)一定温度下,下列溶液的离子浓度关系式正确的是
A.pH=5的HS溶液中,c(H+)= c(HS-)=1×10-5mol·L-1
2
B.pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1
C.pH=2的HC O 溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC O-)
2 2 4 2 4
D.pH相同的①CHCOO Na②NaHCO ③NaClO三种溶液的c(Na+):①>②>③
3 3
28.(2011·全国高考真题)将浓度为0.1mol·L-1HF溶液加水不断稀释,下列各量始终保持增大的是
A.c(H+) B.K(HF) C. D.
a
29.(2015·海南高考真题)下列曲线中,可以描述乙酸(甲, Ka=1.8×10-5)和一氯乙酸(乙,
Ka=1.4×10-3)在水中的电离度与浓度关系的是()
A B C D
30.(2012·重庆高考真题)下列叙述正确的是( )
A.盐酸中滴加氨水至中性,溶液中溶质为氯化铵
B.稀醋酸加水稀释,醋酸电离程度增大,溶液的pH减小
C.饱和石灰水中加入少量CaO,恢复至室温后溶液的pH不变
D.沸水中滴加适量饱和FeCl 溶液,形成带电的胶体,导电能力增强
331.(2013·上海高考真题)部分弱酸的电离平衡常数如下表:
弱酸 HCOOH HCN HCO
2 3
电离平衡常数(25℃) K=1.77×10-4 K=4.9×10-10 K =4.3×10-7 K =5.6×10-11
i i i1 i2
下列选项错误的是
A.2CN-+H O+CO→2HCN+CO 2-
2 2 3
B.2HCOOH+CO 2-→2HCOO-+H O+CO↑
3 2 2
C.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
D.等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者大于后者
32.(2011·山东高考真题)室温下向10mL pH=3的醋酸溶液中加入水稀释后,下列说法正确的是
A.溶液中导电粒子的数目减少
B.溶液中 不变
C.醋酸的电离程度增大,C(H+)亦增大
D.再加入10mlpH=11的NaOH溶液,混合液pH=7
33.(2013·福建高考真题)室温下,对于0.10 mol·L-1的氨水,下列判断正确的是
A.与AlCl 溶液反应发生的离子方程式为 Al3++3OH-=Al(OH) ↓
3 3
B.加水稀释后,溶液中c(NH +)c(OH-)变大
4
C.用HNO 溶液完全中和后,溶液不显中性
3
D.其溶液的pH=13
34.(2014·浙江高考真题)氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯
气-氯水体系中存在以下平衡关系:
Cl(g) Cl(aq) K =10-1.2
2 2 1
Cl(aq)+ HO HClO + H++Cl-K=10-3.4
2 2 2
HClO H++ ClO-Ka=?
其中Cl(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是( )
2
A.Cl(g)+ H O 2H++ ClO-+ Cl-K=10-10.9
2 2
B.在氯处理水体系中,c(HClO) + c(ClO-) =c(H+)-c(OH-)
C.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时好
D.氯处理饮用水时,在夏季的杀菌效果比在冬季差35.(2017·浙江高考真题)为证明醋酸是弱电解质,下列方法不正确的是( )
A.测定0.1 mol·L-1醋酸溶液的pH
B.测定0.1 mol·L-1CHCOONa溶液的酸碱性
3
C.比较浓度均为0.1 mol·L-1盐酸和醋酸溶液的导电能力
D.比较相同物质的量浓度的NaOH溶液和醋酸溶液恰好反应完全时消耗两溶液的体积
36.(2016·浙江高考真题)关于常温下浓度均为0.1 mol·L-1 的盐酸和醋酸溶液,下列说法正确的是
A.醋酸溶液的pH小于盐酸
B.醋酸的电离方程式:CHCOOH=CHCOO-+H+
3 3
C.c(CHCOOH)+c(CHCOO-)=c(Cl-)
3 3
D.0.1 mol·L-1 的醋酸溶液与等物质的量浓度、等体积的氢氧化钠溶液混合后:c(H+)>c(OH-)
37.(2014·上海高考真题)25℃时,甲、乙两烧杯均盛有5mLpH=3的某一元酸溶液,向乙烧杯中加水稀
释至pH=4。下列关于甲烧杯和稀释后的乙烧杯中的溶液的描述中,不正确的是
A.溶液的体积:10V ≤V
甲 乙
B.水电离出的OH-浓度:10c(OH-) =c(OH-)
甲 乙
C.若分别用等浓度的NaOH溶液完全中和,所得溶液的pH:甲≤乙
D.若分别与5mLpH=11的NaOH溶液反应,所得溶液的pH:甲≤乙
38.(2013·海南高考真题)0.1mol·L-1HF溶液的pH=2,则该溶液中有关浓度关系式不正确的是( )
A.c(H+)>c(F-) B.c(H+)>c(HF) C.c(OH-)<c(HF) D.c(HF)>c(F-)
39.(2010·全国高考真题)下列关于电解质溶解的正确判断是
A.在pH=12的溶液中, 可以常量共存
B.在pH=0的溶液中, 、 、 、 可以常量共存
C.由0.1 mol· 一元碱BOH溶液的pH=10,可推知BOH溶液存在BOH = +
D.由 0.1 mol· 一元酸HA溶液的pH=3,可推知NaA溶液存在A-+H O HA+OH-
2
40.(2010·重庆高考真题)pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的
关系如下图所示。分别滴加NaOH溶液(c=0.1 mol·L-1)至pH=7。消耗NaOH溶液的体积为V、V 则
x y
( )
A.x为弱酸,VV
x y x y
C.y为弱酸,VV
x y x y