文档内容
专题93 工艺流程——物质分离提纯
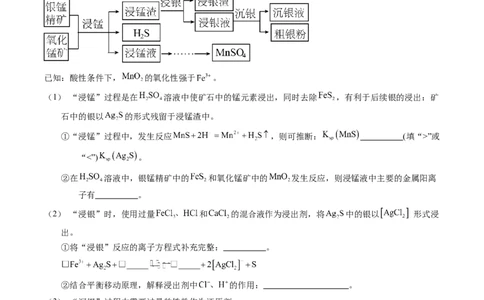
1.【2023年北京卷】以银锰精矿(主要含 、 、 )和氧化锰矿(主要含 )为原料联合提取
银和锰的一种流程示意图如下。
已知:酸性条件下, 的氧化性强于 。
(1) “浸锰”过程是在 溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出:矿
石中的银以 的形式残留于浸锰渣中。
①“浸锰”过程中,发生反应 ,则可推断: (填“>”或
“<”) 。
②在 溶液中,银锰精矿中的 和氧化锰矿中的 发生反应,则浸锰液中主要的金属阳离
子有 。
(2) “浸银”时,使用过量 和 的混合液作为浸出剂,将 中的银以 形式浸
出。
①将“浸银”反应的离子方程式补充完整: 。
②结合平衡移动原理,解释浸出剂中 的作用: 。
(3) “沉银”过程中需要过量的铁粉作为还原剂。
①该步反应的离子方程式有 。
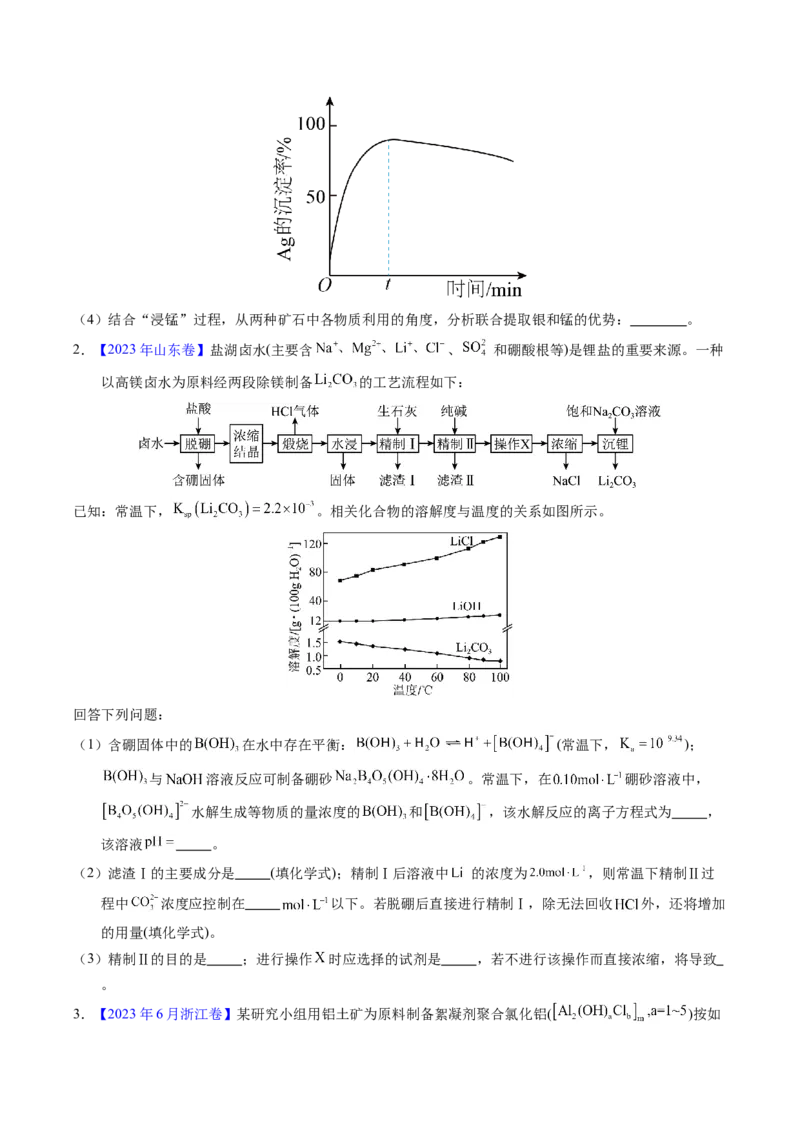
②一定温度下, 的沉淀率随反应时间的变化如图所示。解释 分钟后 的沉淀率逐渐减小的原因:
。(4)结合“浸锰”过程,从两种矿石中各物质利用的角度,分析联合提取银和锰的优势: 。
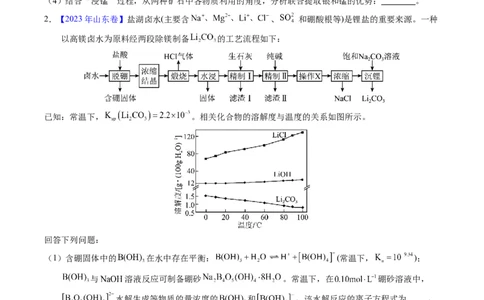
2.【2023年山东卷】盐湖卤水(主要含 、 和硼酸根等)是锂盐的重要来源。一种
以高镁卤水为原料经两段除镁制备 的工艺流程如下:
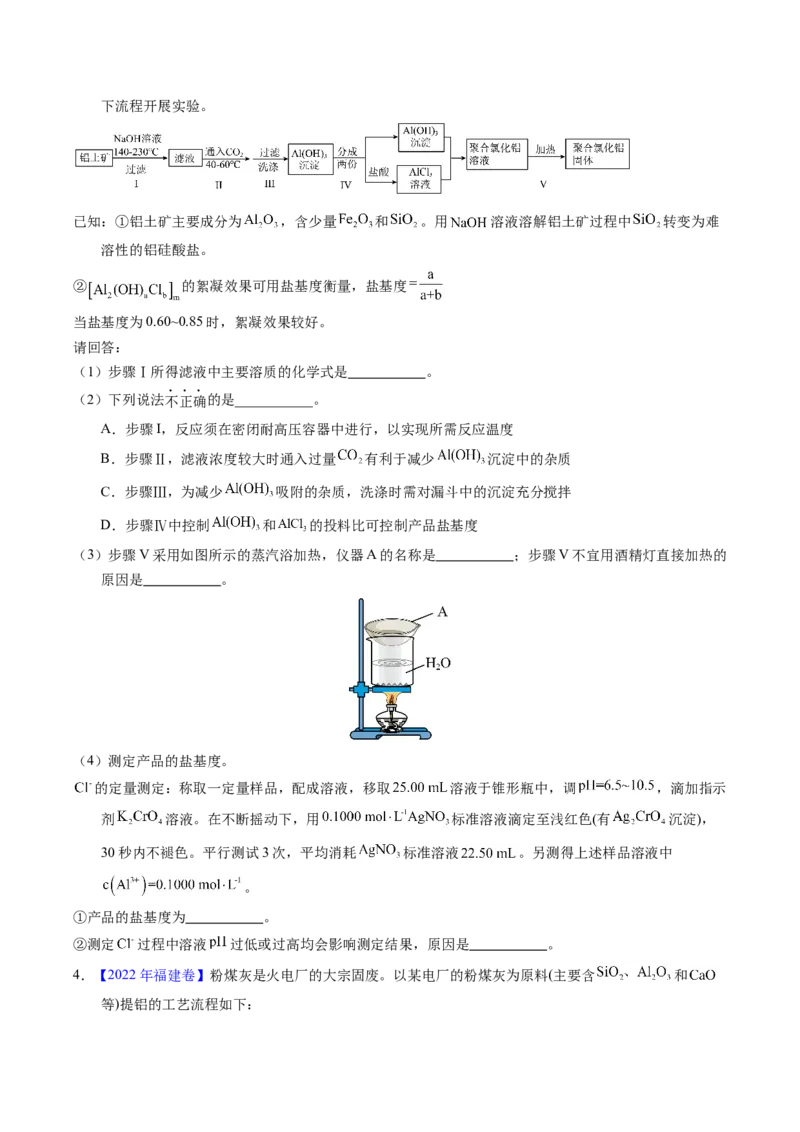
已知:常温下, 。相关化合物的溶解度与温度的关系如图所示。
回答下列问题:
(1)含硼固体中的 在水中存在平衡: (常温下, );
与 溶液反应可制备硼砂 。常温下,在 硼砂溶液中,
水解生成等物质的量浓度的 和 ,该水解反应的离子方程式为 ,
该溶液 。
(2)滤渣Ⅰ的主要成分是 (填化学式);精制Ⅰ后溶液中 的浓度为 ,则常温下精制Ⅱ过
程中 浓度应控制在 以下。若脱硼后直接进行精制Ⅰ,除无法回收 外,还将增加
的用量(填化学式)。
(3)精制Ⅱ的目的是 ;进行操作 时应选择的试剂是 ,若不进行该操作而直接浓缩,将导致
。
3.【2023年6月浙江卷】某研究小组用铝土矿为原料制备絮凝剂聚合氯化铝( )按如下流程开展实验。
已知:①铝土矿主要成分为 ,含少量 和 。用 溶液溶解铝土矿过程中 转变为难
溶性的铝硅酸盐。
② 的絮凝效果可用盐基度衡量,盐基度
当盐基度为0.60~0.85时,絮凝效果较好。
请回答:
(1)步骤Ⅰ所得滤液中主要溶质的化学式是 。
(2)下列说法不正确的是___________。
A.步骤I,反应须在密闭耐高压容器中进行,以实现所需反应温度
B.步骤Ⅱ,滤液浓度较大时通入过量 有利于减少 沉淀中的杂质
C.步骤Ⅲ,为减少 吸附的杂质,洗涤时需对漏斗中的沉淀充分搅拌
D.步骤Ⅳ中控制 和 的投料比可控制产品盐基度
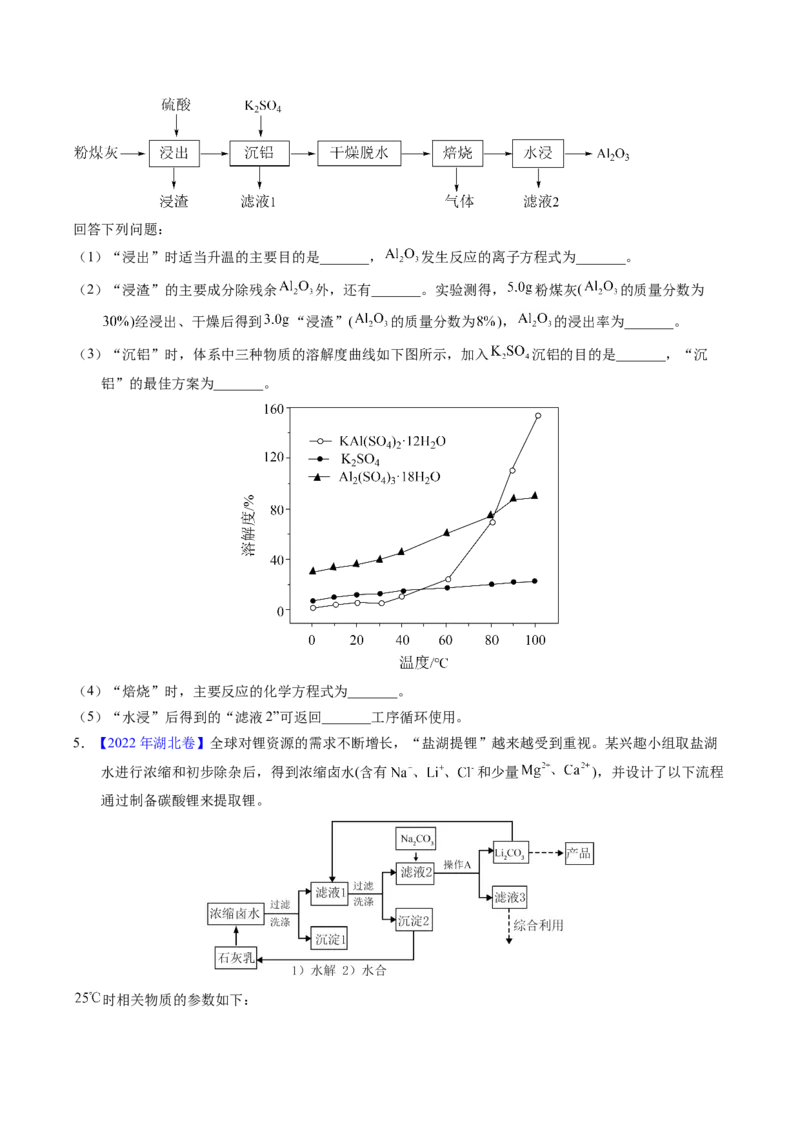
(3)步骤V采用如图所示的蒸汽浴加热,仪器A的名称是 ;步骤V不宜用酒精灯直接加热的
原因是 。
(4)测定产品的盐基度。
的定量测定:称取一定量样品,配成溶液,移取 溶液于锥形瓶中,调 ,滴加指示
剂 溶液。在不断摇动下,用 标准溶液滴定至浅红色(有 沉淀),
30秒内不褪色。平行测试3次,平均消耗 标准溶液 。另测得上述样品溶液中
。
①产品的盐基度为 。
②测定 过程中溶液 过低或过高均会影响测定结果,原因是 。
4.【2022年福建卷】粉煤灰是火电厂的大宗固废。以某电厂的粉煤灰为原料(主要含 和
等)提铝的工艺流程如下:回答下列问题:
(1)“浸出”时适当升温的主要目的是_______, 发生反应的离子方程式为_______。
(2)“浸渣”的主要成分除残余 外,还有_______。实验测得, 粉煤灰( 的质量分数为
)经浸出、干燥后得到 “浸渣”( 的质量分数为 ), 的浸出率为_______。
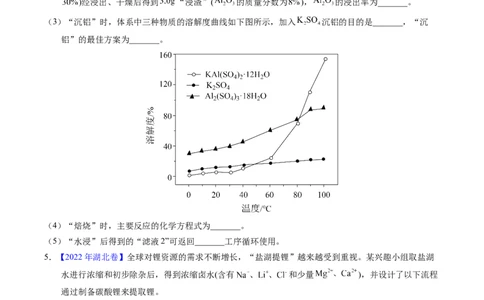
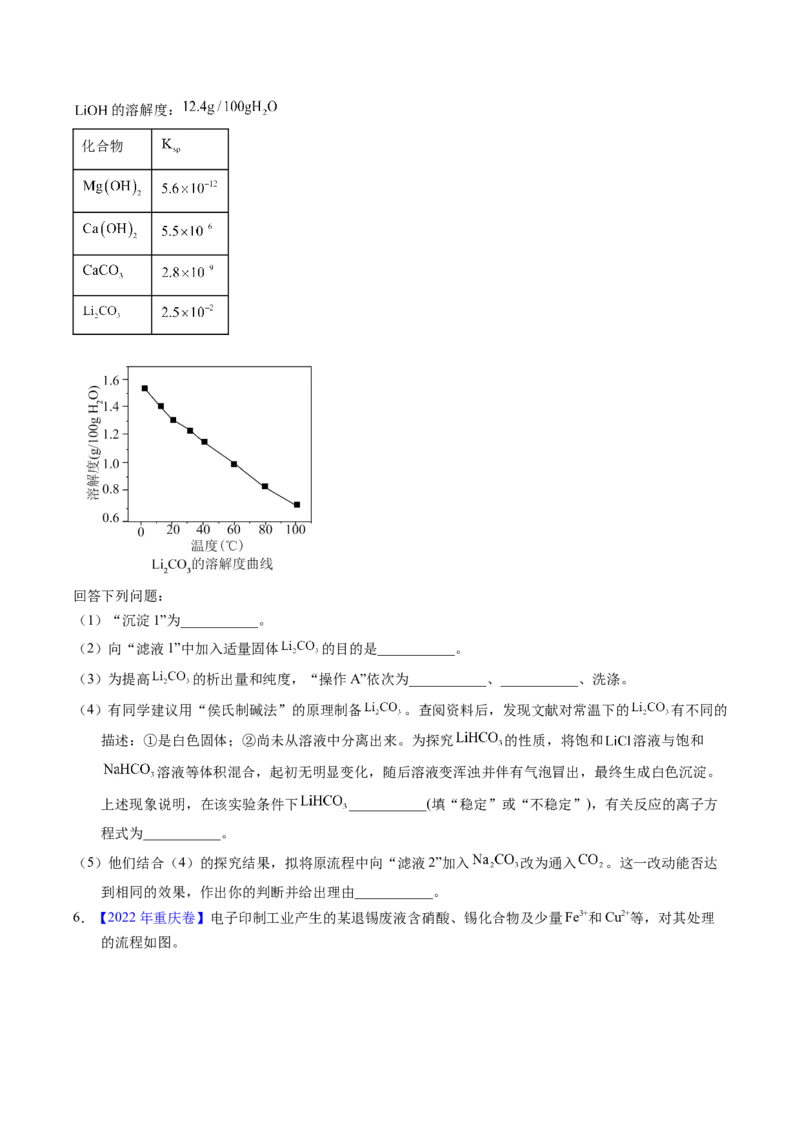
(3)“沉铝”时,体系中三种物质的溶解度曲线如下图所示,加入 沉铝的目的是_______,“沉
铝”的最佳方案为_______。
(4)“焙烧”时,主要反应的化学方程式为_______。
(5)“水浸”后得到的“滤液2”可返回_______工序循环使用。
5.【2022年湖北卷】全球对锂资源的需求不断增长,“盐湖提锂”越来越受到重视。某兴趣小组取盐湖
水进行浓缩和初步除杂后,得到浓缩卤水(含有 和少量 ),并设计了以下流程
通过制备碳酸锂来提取锂。
时相关物质的参数如下:的溶解度:
化合物
回答下列问题:
(1)“沉淀1”为___________。
(2)向“滤液1”中加入适量固体 的目的是___________。
(3)为提高 的析出量和纯度,“操作A”依次为___________、___________、洗涤。
(4)有同学建议用“侯氏制碱法”的原理制备 。查阅资料后,发现文献对常温下的 有不同的
描述:①是白色固体;②尚未从溶液中分离出来。为探究 的性质,将饱和 溶液与饱和
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。
上述现象说明,在该实验条件下 ___________(填“稳定”或“不稳定”),有关反应的离子方
程式为___________。
(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入 改为通入 。这一改动能否达
到相同的效果,作出你的判断并给出理由___________。
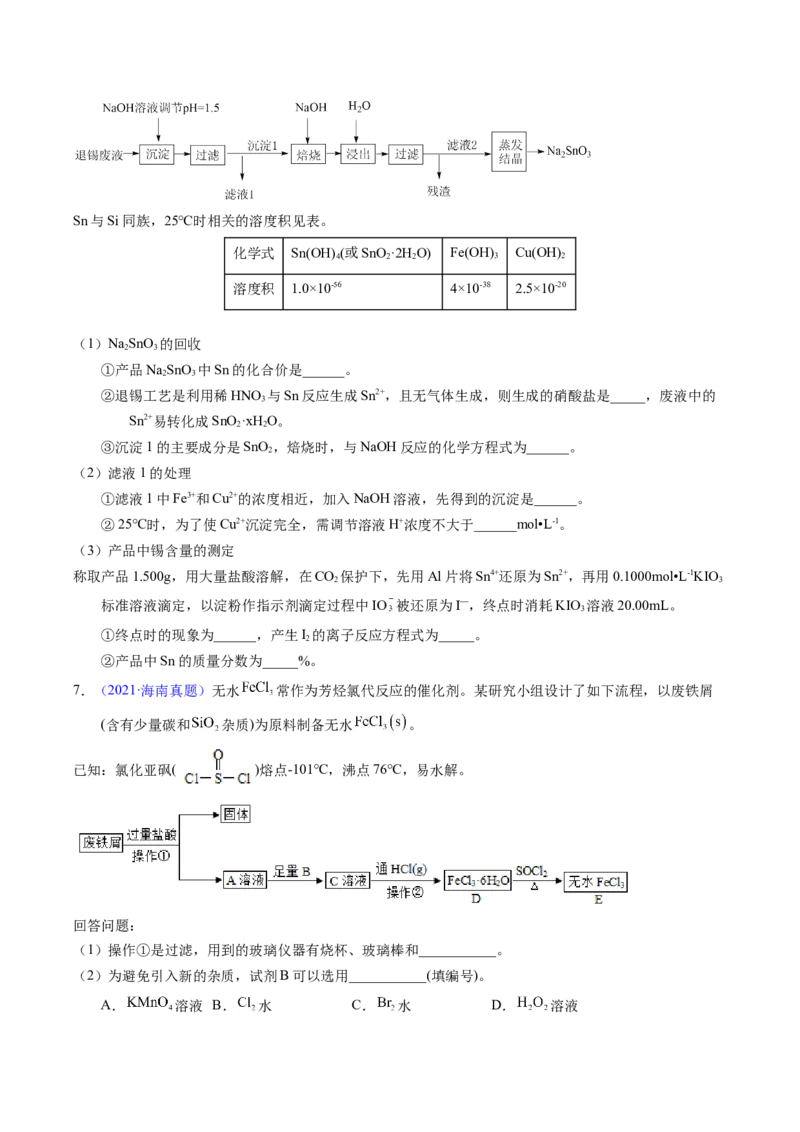
6.【2022年重庆卷】电子印制工业产生的某退锡废液含硝酸、锡化合物及少量Fe3+和Cu2+等,对其处理
的流程如图。Sn与Si同族,25℃时相关的溶度积见表。
化学式 Sn(OH)(或SnO ·2H O) Fe(OH) Cu(OH)
4 2 2 3 2
溶度积 1.0×10-56 4×10-38 2.5×10-20
(1)NaSnO 的回收
2 3
①产品NaSnO 中Sn的化合价是______。
2 3
②退锡工艺是利用稀HNO 与Sn反应生成Sn2+,且无气体生成,则生成的硝酸盐是_____,废液中的
3
Sn2+易转化成SnO ·xH O。
2 2
③沉淀1的主要成分是SnO ,焙烧时,与NaOH反应的化学方程式为______。
2
(2)滤液1的处理
①滤液1中Fe3+和Cu2+的浓度相近,加入NaOH溶液,先得到的沉淀是______。
②25℃时,为了使Cu2+沉淀完全,需调节溶液H+浓度不大于______mol•L-1。
(3)产品中锡含量的测定
称取产品1.500g,用大量盐酸溶解,在CO 保护下,先用Al片将Sn4+还原为Sn2+,再用0.1000mol•L-1KIO
2 3
标准溶液滴定,以淀粉作指示剂滴定过程中IO 被还原为I—,终点时消耗KIO 溶液20.00mL。
3
①终点时的现象为______,产生I 的离子反应方程式为_____。
2
②产品中Sn的质量分数为_____%。
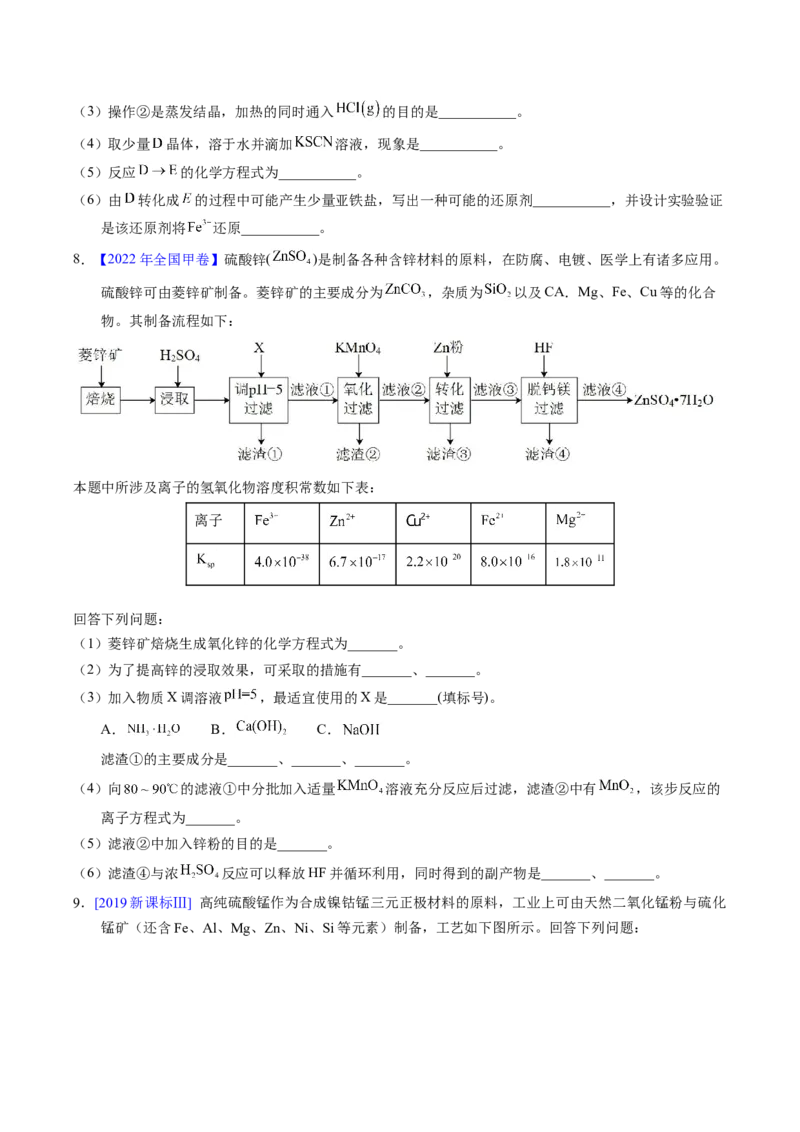
7.(2021·海南真题)无水 常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑
(含有少量碳和 杂质)为原料制备无水 。
已知:氯化亚砜( )熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和___________。
(2)为避免引入新的杂质,试剂B可以选用___________(填编号)。
A. 溶液 B. 水 C. 水 D. 溶液(3)操作②是蒸发结晶,加热的同时通入 的目的是___________。
(4)取少量 晶体,溶于水并滴加 溶液,现象是___________。
(5)反应 的化学方程式为___________。
(6)由 转化成 的过程中可能产生少量亚铁盐,写出一种可能的还原剂___________,并设计实验验证
是该还原剂将 还原___________。
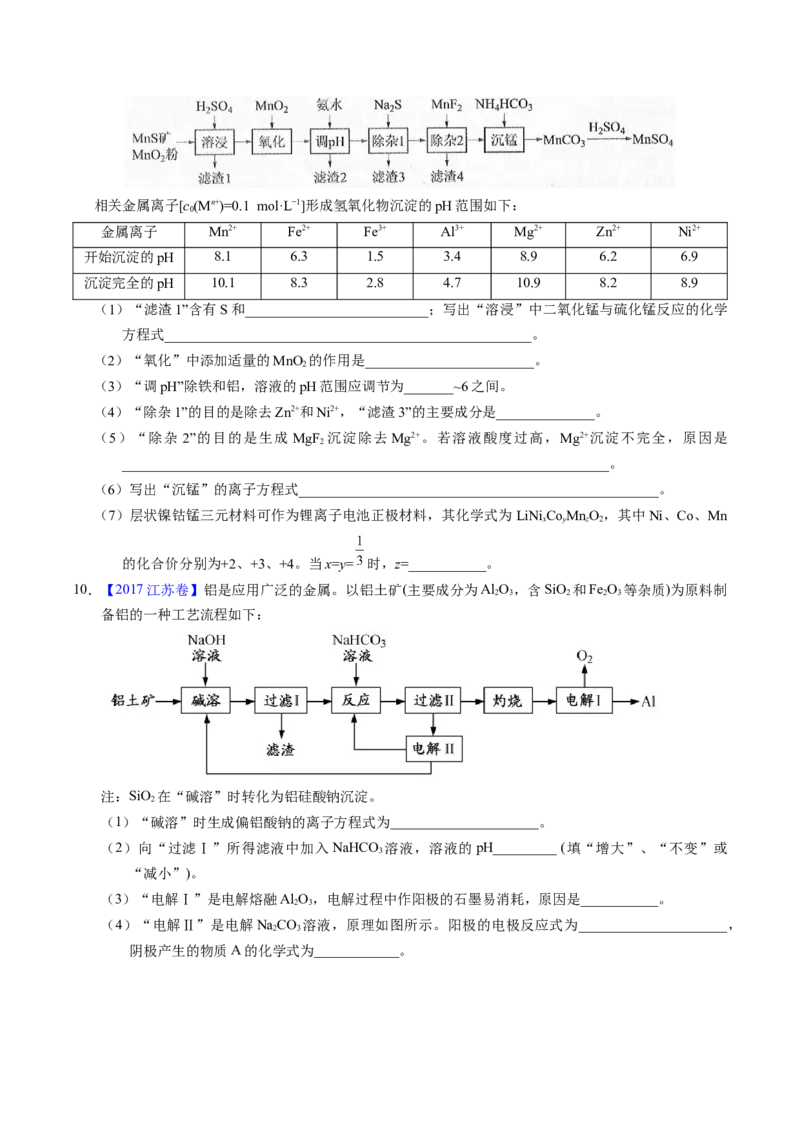
8.【2022年全国甲卷】硫酸锌( )是制备各种含锌材料的原料,在防腐、电镀、医学上有诸多应用。
硫酸锌可由菱锌矿制备。菱锌矿的主要成分为 ,杂质为 以及CA.Mg、Fe、Cu等的化合
物。其制备流程如下:
本题中所涉及离子的氢氧化物溶度积常数如下表:
离子
回答下列问题:
(1)菱锌矿焙烧生成氧化锌的化学方程式为_______。
(2)为了提高锌的浸取效果,可采取的措施有_______、_______。
(3)加入物质X调溶液 ,最适宜使用的X是_______(填标号)。
A. B. C.
滤渣①的主要成分是_______、_______、_______。
(4)向 的滤液①中分批加入适量 溶液充分反应后过滤,滤渣②中有 ,该步反应的
离子方程式为_______。
(5)滤液②中加入锌粉的目的是_______。
(6)滤渣④与浓 反应可以释放HF并循环利用,同时得到的副产物是_______、_______。
9.[2019新课标Ⅲ] 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化
锰矿(还含Fe、Al、Mg、Zn、Ni、Si等元素)制备,工艺如下图所示。回答下列问题:相关金属离子[c(Mn+)=0.1 mol·L−1]形成氢氧化物沉淀的pH范围如下:
0
金属离子 Mn2+ Fe2+ Fe3+ Al3+ Mg2+ Zn2+ Ni2+
开始沉淀的pH 8.1 6.3 1.5 3.4 8.9 6.2 6.9
沉淀完全的pH 10.1 8.3 2.8 4.7 10.9 8.2 8.9
(1)“滤渣1”含有S和__________________________;写出“溶浸”中二氧化锰与硫化锰反应的化学
方程式____________________________________________________。
(2)“氧化”中添加适量的MnO 的作用是________________________。
2
(3)“调pH”除铁和铝,溶液的pH范围应调节为_______~6之间。
(4)“除杂1”的目的是除去Zn2+和Ni2+,“滤渣3”的主要成分是______________。
(5)“除杂 2”的目的是生成 MgF 沉淀除去 Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
2
_____________________________________________________________________。
(6)写出“沉锰”的离子方程式___________________________________________________。
(7)层状镍钴锰三元材料可作为锂离子电池正极材料,其化学式为LiNiCoMnO ,其中Ni、Co、Mn
x y z 2
的化合价分别为+2、+3、+4。当x=y= 时,z=___________。
10.【2017江苏卷】铝是应用广泛的金属。以铝土矿(主要成分为Al O ,含SiO 和Fe O 等杂质)为原料制
2 3 2 2 3
备铝的一种工艺流程如下:
注:SiO 在“碱溶”时转化为铝硅酸钠沉淀。
2
(1)“碱溶”时生成偏铝酸钠的离子方程式为_____________________。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO 溶液,溶液的pH_________ (填“增大”、“不变”或
3
“减小”)。
(3)“电解Ⅰ”是电解熔融Al O,电解过程中作阳极的石墨易消耗,原因是___________。
2 3
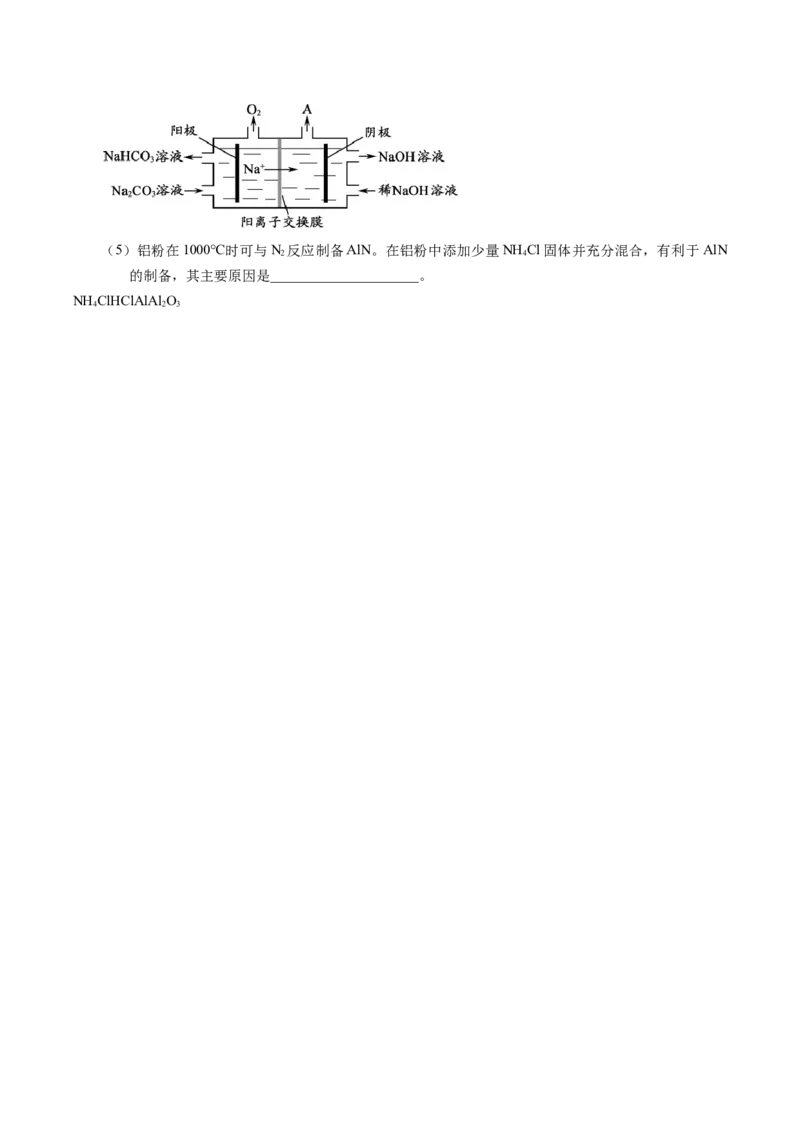
(4)“电解Ⅱ”是电解NaCO 溶液,原理如图所示。阳极的电极反应式为_____________________,
2 3
阴极产生的物质A的化学式为____________。(5)铝粉在1000℃时可与N 反应制备AlN。在铝粉中添加少量NH Cl固体并充分混合,有利于AlN
2 4
的制备,其主要原因是_____________________。
NH ClHClAlAl O
4 2 3