文档内容
2024 年甘肃高考化学试题
一、单选题
1.下列成语涉及金属材料的是
A.洛阳纸贵 B.聚沙成塔 C.金戈铁马 D.甘之若饴
【答案】C
【详解】A.纸的主要成分是纤维素,不是金属材料,A错误;
B.沙的主要成分是硅酸盐,不是金属材料,B错误;
C.金和铁都是金属,C正确;
D.甘之若饴意思是把它看成像糖那样甜,糖类是有机物,不是金属材料,D错误;
故选C。
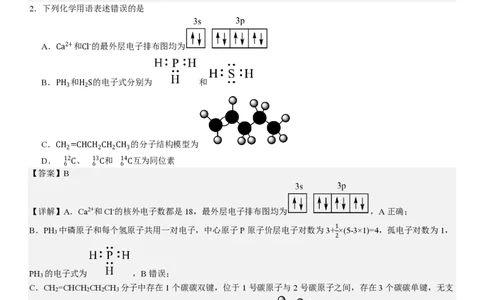
2.下列化学用语表述错误的是
A. 和 的最外层电子排布图均为
2+ -
Ca Cl
B. 和 的电子式分别为 和
PH3 H2S
C. 的分子结构模型为
D. CH2= 、 CHCH2C 和 H2CH3 互为同位素
【答案】B12 13 14
6 C 6 C 6 C
【详解】A.Ca2+和Cl-的核外电子数都是18,最外层电子排布图均为 ,A正确;
B.PH 中磷原子和每个氢原子共用一对电子,中心原子P原子价层电子对数为3+ ×(5-3×1)=4,孤电子对数为1,
3
1
2
PH 的电子式为 ,B错误;
3
C.CH =CHCH CH CH 分子中存在1个碳碳双键,位于1号碳原子与2号碳原子之间,存在3个碳碳单键,无支
2 2 2 3
链,且氢原子半径小于碳原子半径,其分子结构模型表示为 ,C正确;
D. 、 和 是质子数相同、中子数不同的碳原子,是碳元素的不同核素,互为同位素,D正确;
故选12B。 13 14
6C 6C 6C
3.化学与生活息息相关,下列对应关系错误的是
物质 性质 用途
A 次氯酸钠 氧化性 衣物漂白
B 氢气 可燃性 制作燃料电池
C 聚乳酸 生物可降解性 制作一次性餐具D 活性炭 吸附性 分解室内甲醛
A.A B.B C.C D.D
【答案】D
【详解】A.次氯酸钠有强氧化性,从而可以做漂白剂,用于衣物漂白,A正确;
B.氢气是可燃气体,具有可燃性,能被氧气氧化,可以制作燃料电池,B正确;
C.聚乳酸具有生物可降解性,无毒,是高分子化合物,可以制作一次性餐具,C正确;
D.活性炭有吸附性,能够有效吸附空气中的有害气体、去除异味,但无法分解甲醛,D错误;
故选D。
4.下列措施能降低化学反应速率的是
A.催化氧化氨制备硝酸时加入铂 B.中和滴定时,边滴边摇锥形瓶
C.锌粉和盐酸反应时加水稀释 D.石墨合成金刚石时增大压强
【答案】C
【详解】A.催化剂可以改变化学反应速率,一般来说,催化剂可以用来加快化学反应速率,故催化氧化氨制备硝
酸时加入铂可以加快化学反应速率,A错误;
B.中和滴定时,边滴边摇锥形瓶,可以让反应物快速接触,可以加快化学反应速率,B错误;
C.锌粉和盐酸反应时加水稀释会降低盐酸的浓度,会降低化学反应速率,C正确;
D.石墨合成金刚石,该反应中没有气体参与,增大压强不会改变化学反应速率,D错误;
故选C。
5.X、Y、Z、W、Q为短周期元素,原子序数依次增大,最外层电子数之和为18。Y原子核外有两个单电子,Z
和Q同族,Z的原子序数是Q的一半,W元素的焰色试验呈黄色。下列说法错误的是
A.X、Y组成的化合物有可燃性 B.X、Q组成的化合物有还原性
C.Z、W组成的化合物能与水反应 D.W、Q组成的化合物溶于水呈酸性
【答案】D
【分析】X、Y、Z、W、Q为短周期元素,W元素的焰色试验呈黄色,W为Na元素;Z和Q同族,Z的原子序数
是Q的一半,则Z为O、Q为S;Y原子核外有两个单电子、且原子序数小于Z,Y为C元素;X、Y、Z、W、Q
的最外层电子数之和为18,则X的最外层电子数为18-4-6-1-6=1,X可能为H或Li。
【详解】A.若X为H,H与C组成的化合物为烃,烃能够燃烧,若X为Li,Li与C组成的化合物也具有可燃性,
A正确;
B.X、Q组成的化合物中Q(即S)元素呈-2价,为S元素的最低价,具有还原性,B正确;
C.Z、W组成的化合物为Na O、Na O ,Na O与水反应生成NaOH,Na O 与水反应生成NaOH和O ,C正确;
2 2 2 2 2 2 2
D.W、Q组成的化合物Na S属于强碱弱酸盐,其溶于水所得溶液呈碱性,D错误;
2
故选D。
6.下列实验操作对应的装置不正确的是
A B C D
灼烧海带制海带灰 准确量取 稀盐酸 配制一定浓度的 溶液 使用电石和饱和食盐水制备
15.00mL NaCl C2H2
A.A B.B C.C D.D
【答案】A
【详解】A.灼烧海带制海带灰应在坩埚中进行,并用玻璃棒搅拌,给坩埚加热时不需要使用石棉网或陶土网,A
错误;
B.稀盐酸呈酸性,可用酸式滴定管量取15.00mL稀盐酸,B正确;C.配制一定浓度的NaCl溶液时,需要将在烧杯中溶解得到的NaCl溶液通过玻璃棒引流转移到选定规格的容量瓶
中,C正确;
D.电石的主要成分CaC 与水发生反应CaC +2H O→Ca(OH) +CH≡CH↑制取C H ,该制气反应属于固体与液体常
2 2 2 2 2 2
温制气反应,分液漏斗中盛放饱和食盐水,具支锥形瓶中盛放电石,D正确;
故选A。
7.某固体电解池工作原理如图所示,下列说法错误的是
A.电极1的多孔结构能增大与水蒸气的接触面积
B.电极2是阴极,发生还原反应:
C.工作时 从多孔电极1迁移到多孔电极- 2 2-
O2+4e=2O
D.理论上电2-源提供 能分解
O
【答案】B -
2mole 1molH2O
【分析】多孔电极1上H O(g)发生得电子的还原反应转化成H (g),多孔电极1为阴极,电极反应为
2 2
2H O+4e-=2H +2O2-;多孔电极2上O2-发生失电子的氧化反应转化成O (g),多孔电极2为阳极,电极反应为
2 2 2
2O2--4e-=O 。
2
【详解】A.电极1的多孔结构能增大电极的表面积,增大与水蒸气的接触面积,A正确;
B.根据分析,电极2为阳极,发生氧化反应:2O2--4e-=O ,B错误;
2
C.工作时,阴离子O2-向阳极移动,即O2-从多孔电极1迁移到多孔电极2,C正确;
电解
D.根据分析,电解总反应为2H O(g) 2H +O ,分解2molH O转移4mol电子,则理论上电源提供2mol电子能
2 2 2 2
分解1molH O,D正确;
2
故选B。
8.曲美托嗪是一种抗焦虑药,合成路线如下所示,下列说法错误的是
A.化合物I和Ⅱ互为同系物
B.苯酚和 在条件①下反应得到苯甲醚
C.化合物Ⅱ能与 溶液反应
(CH3O)2SO2
D.曲美托嗪分子中含有酰胺基团
NaHCO3【答案】A
【详解】A.化合物Ⅰ含有的官能团有羧基、酚羟基,化合物Ⅱ含有的官能团有羧基、醚键,官能团种类不同,化合
物Ⅰ和化合物Ⅱ不互为同系物,A错误;
B.根据题中流程可知,化合物Ⅰ中的酚羟基与 反应生成醚,故苯酚和 在条件①下反应得到
苯甲醚,B正确;
(CH3O)2SO2 (CH3O)2SO2
C.化合物Ⅱ中含有羧基,可以与NaHCO 溶液反应,C正确;
3
D.由曲美托嗪的结构简式可知,曲美托嗪中含有的官能团为酰胺基、醚键,D正确;
故选A。
9.下列实验操作、现象和结论相对应的是
实验操作、现象 结论
A 用蓝色石蕊试纸检验某无色溶液,试纸变红 该溶液是酸溶液
B 用酒精灯灼烧织物产生类似烧焦羽毛的气味 该织物含蛋白质
C 乙醇和浓硫酸加热,产生的气体使溴水褪色 该气体是乙烯
D 氯化镁溶液中滴入氢氧化钠溶液,生成沉淀 氢氧化钠的碱性比氢氧化镁强
A.A B.B C.C D.D
【答案】B
【详解】A.用蓝色石蕊试纸检验某无色溶液,试纸变红,该溶液显酸性,但不一定是酸溶液,也有可能是显酸性
的盐溶液,A错误;
B.动物纤维主要成分是蛋白质,灼烧后有类似烧焦羽毛的味道,若用酒精灯灼烧织物产生类似烧焦羽毛的味道,
说明该织物含有动物纤维,含有蛋白质,B正确;
C.乙醇和浓硫酸加热,会产生很多产物,如加热温度在170℃,主要产物为乙烯;如加热温度在140℃,主要产物
为二乙醚;同时乙醇可在浓硫酸下脱水生成碳单质,继续和浓硫酸在加热条件下产生二氧化碳、二氧化硫等,其中
的产物二氧化硫也能使溴水褪色,不能说明产生的气体就是乙烯,C错误;
D.氯化镁溶液中滴入氢氧化钠溶液,会发生复分解反应,生成难溶的氢氧化镁,与氢氧化钠和氢氧化镁的碱性无
关,不能由此得出氢氧化钠的碱性比氢氧化镁强,D错误;
故选B。
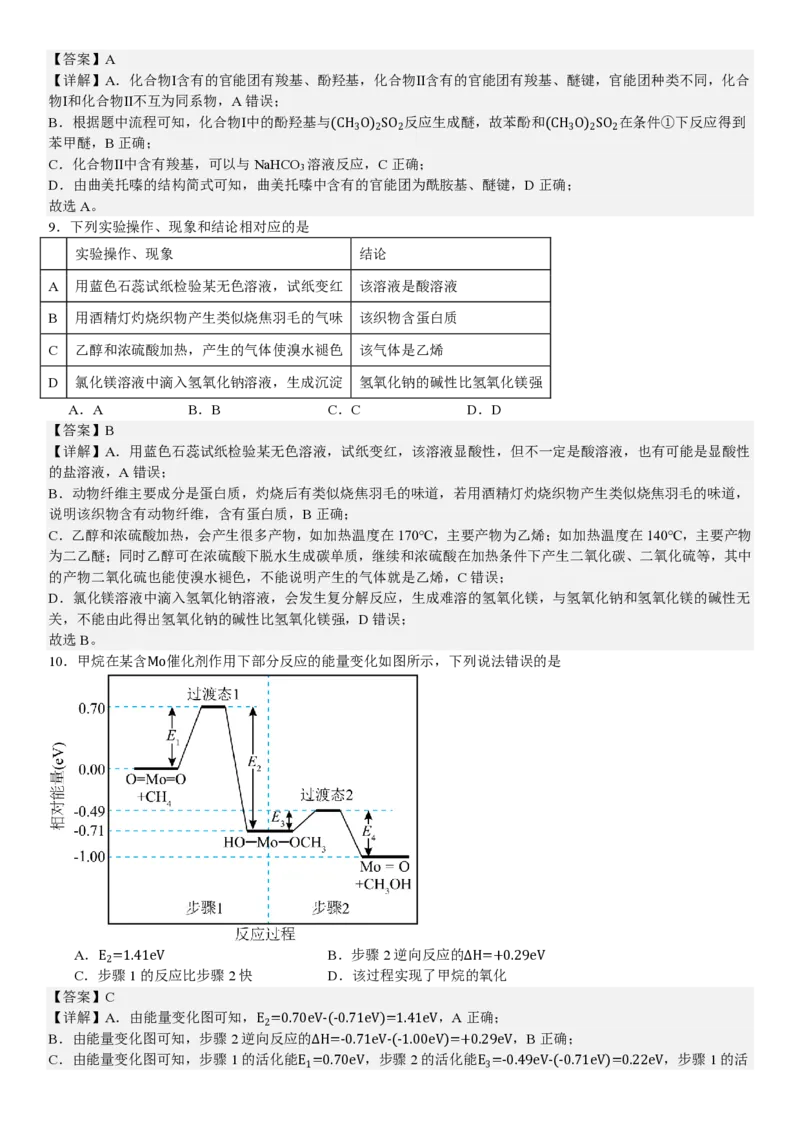
10.甲烷在某含 催化剂作用下部分反应的能量变化如图所示,下列说法错误的是
Mo
A. B.步骤2逆向反应的
C.步骤1的反应比步骤2快 D.该过程实现了甲烷的氧化
E2=1.41eV ΔH=+0.29eV
【答案】C
【详解】A.由能量变化图可知, ,A正确;
B.由能量变化图可知,步骤2逆向反应的 ,B正确;
E2=0.70eV-(-0.71eV)=1.41eV
C.由能量变化图可知,步骤1的活化能 ,步骤2的活化能 ,步骤1的活
ΔH=-0.71eV-(-1.00eV)=+0.29eV
E1=0.70eV E3=-0.49eV-(-0.71eV)=0.22eV化能大于步骤2的活化能,步骤1的反应比步骤2慢,C错误;
D.该过程甲烷转化为甲醇,属于加氧氧化,该过程实现了甲烷的氧化,D正确;
故选C。
11.兴趣小组设计了从 中提取 的实验方案,下列说法正确的是
AgCl Ag
A.还原性:
B.按上述方案消耗 可回收
Ag>Cu>Fe
C.反应①的离子方程式是
1molFe 1molAg
D.溶液①中的金属离子是 2+ + 2+ +
[Cu(NH3)4] +4H =Cu +4NH4
【答案】C 2+
Fe
【详解】A.金属活动性越强,金属的还原性越强,而且由题中的实验方案能得到证明,还原性从强到弱的顺序为 Fe >
Cu > Ag,A错误;
B.由电子转移守恒可知,1 mol Fe可以置换1 mol Cu,而1 mol Cu可以置换2 mol Ag,因此,根据按上述方案消
耗1 mol Fe可回收2 mol Ag,B错误;
C.反应①中,氯化四氨合铜溶液与浓盐酸反应生成氯化铜和氯化铵,该反应的离子方程式是
,C正确;
D.向氯化铜2+和氯化+铵的混2+合液中+加入铁,铁置换出铜后生成 ,然后 被通入的氧气氧化为 ,氯化铵水
[Cu(NH3)4] + 4H = Cu +4NH4
解使溶液呈酸性,在这个过程中,溶液中的氢离子参与反应,因2此+氢离子浓2度+减少促进了铁离子水解3生+成氢氧化铁
Fe Fe Fe
沉淀,氢氧化铁存在沉淀溶解平衡,因此,溶液①中的金属离子是 ,D错误;
故选C。 3+
Fe
12. 晶体中,多个晶胞无隙并置而成的结构如图甲所示,其中部分结构显示为图乙,下列说法错误的是
β-MgCl2
A.电负性: B.单质 是金属晶体
C.晶体中存在范德华力 D. 离子的配位数为3
Mg