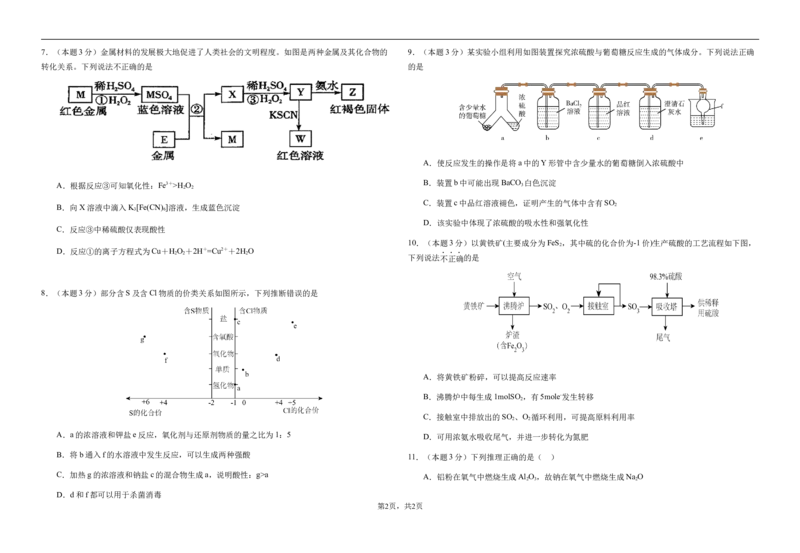文档内容
4.(本题3分)下列有关钠及其化合物的说法正确的是
甘谷二中 2023—2024 学年度高三级第二次检测考试试题
A.将一小块金属钠投入到硫酸铜溶液中,有红色物质析出
化 学
B.Na O 和Na O均属于碱性氧化物,阴、阳离子的个数比均为1:2
2 2 2
可能用到的相对原子质量:H:1 C:12 N: 14 O:16 S:32 Na:23 Mg:24
C.相同物质的量的Na CO 和NaHCO 与足量盐酸反应时,产生CO 气体的质量相同
2 3 3 2
Al:27 Fe:56 Ba:137
D.Na CO 和NaHCO 可以用澄清石灰水鉴别
2 3 3
一、单选题(共45分)
5.(本题3分)下列选项中,为完成相应实验,所用仪器或相关操作合理的是
1.(本题3分)下列说法中不正确的有
A B C D
A.钠钾合金在常温下为液态,可用于原子反应堆的导热剂
苯萃取碘水中的碘,分出水 制备并观察Fe(OH) 配制0.10mol/LNaOH
测量氯气的体积 2
B.火灾现场有大量活泼金属存放时,可用干燥的沙土灭火 层后的操作 的颜色 溶液
C.明矾溶于水会形成胶体,因此可用于自来水的净化和杀菌消毒
D.在月饼包装盒中放入铁粉,可防止月饼氧化变质
2.(本题3分)设N 为阿伏加德罗常数,下列说法正确的是
A
A.常温常压下,Na O 与足量H O反应,生成0.2 mol O ,转移电子的数目为0.4N
2 2 2 2 A
B.反应KIO +6HI= KI+3I +3H O中,每生成3 mol I 转移的电子数为6N
3 2 2 2 A
C.将0.1mol FeCl 水解制成胶体,所得胶体粒子数为0.1N 6.(本题3分)下列表示对应化学反应的离子方程式正确的是
3 A
D.常温下,0.1 mol Fe与一定量的稀硝酸反应,转移电子数为0.3N
A A.等体积、等浓度的Ca(HCO ) 溶液和NaOH溶液混合:Ca2++2 +2OH-= CaCO ↓+
3 2 3
3.(本题3分)下列说法正确的是
+2H O
2
A.同温同压下的两种气体,只要所含微粒数目相等,则所占体积一定相等
B.醋酸溶液与水垢中的CaCO 的反应:CaCO +2H+= Ca2++H O+CO ↑
3 3 2 2
B.质量相等,密度不相等的N 和C H 分子数目一定相等
2 2 4
C.向溴化亚铁溶液中通入少量的氯气:2Fe2+ + Cl =2Fe3+ + 2Cl-
2
C.标准状况下11.2L甲烷和氨气混合物中氢原子数目为2N
A
D.用FeCl 溶液腐蚀铜线路板:3Cu+2Fe3+ = 3Cu2++2Fe
3
D.两个体积相同的容器,若气体物质的量相等,则两容器的压强一定相等
第1页,共2页
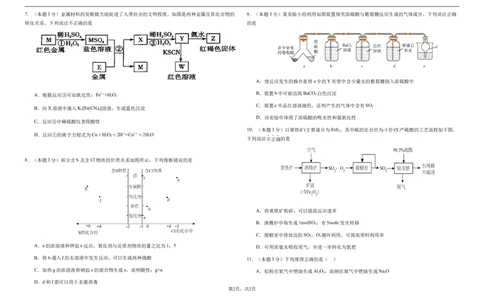
学学科科网网((北北京京))股股份份有有限限公公司司7.(本题3分)金属材料的发展极大地促进了人类社会的文明程度。如图是两种金属及其化合物的 9.(本题3分)某实验小组利用如图装置探究浓硫酸与葡萄糖反应生成的气体成分。下列说法正确
转化关系。下列说法不正确的是 的是
A.使反应发生的操作是将a中的Y形管中含少量水的葡萄糖倒入浓硫酸中
A.根据反应③可知氧化性:Fe3+>H O B.装置b中可能出现BaCO 3 白色沉淀
2 2
C.装置c中品红溶液褪色,证明产生的气体中含有SO
B.向X溶液中滴入K [Fe(CN) ]溶液,生成蓝色沉淀 2
3 6
D.该实验中体现了浓硫酸的吸水性和强氧化性
C.反应③中稀硫酸仅表现酸性
10.(本题3分)以黄铁矿(主要成分为FeS ,其中硫的化合价为-1价)生产硫酸的工艺流程如下图,
2
D.反应①的离子方程式为Cu+H O +2H+=Cu2++2H O
2 2 2
下列说法不正确的是
8.(本题3分)部分含S及含Cl物质的价类关系如图所示,下列推断错误的是
A.将黄铁矿粉碎,可以提高反应速率
B.沸腾炉中每生成1molSO ,有5mole-发生转移
2
C.接触室中排放出的SO 、O 循环利用,可提高原料利用率
2 2
A.a的浓溶液和钾盐e反应,氧化剂与还原剂物质的量之比为1:5
D.可用浓氨水吸收尾气,并进一步转化为氮肥
B.将b通入f的水溶液中发生反应,可以生成两种强酸
11.(本题3分)下列推理正确的是( )
C.加热g的浓溶液和钠盐c的混合物生成a,说明酸性:g>a
A.铝粉在氧气中燃烧生成Al O ,故钠在氧气中燃烧生成Na O
2 3 2
D.d和f都可以用于杀菌消毒
第2页,共2页B.铁能从硫酸铜溶液中置换出铜,故钠也能从硫酸铜溶液中置换出铜
FeSO ·4H O FeSO +4H O
4 2 4 2
C.活泼金属钠保存在煤油中,故活泼金属铝也保存在煤油中
D.温度为380 ℃时,固体物质P的化学式为FeSO ·H O
D.钠与氧气、水等反应时钠均作还原剂,故金属单质参与反应时金属单质均作还原剂 4 2
12.(本题3分)SO 气体与足量Fe (SO ) 溶液完全反应后,再加入K Cr O 溶液,发生如下反应: 15.(本题3分)某100mL溶液可能含有Na+、 、Fe3+、 、 、Cl-中的若干种,取该溶
2 2 4 3 2 2 7
①SO +2Fe3++2H O= +2Fe2++4H+ ② +6Fe2++14H+=2Cr3++6Fe3++7H O。则下列有关说法不正
2 2 2
液进行连续实验,实验过程如图(所加试剂均过量,气体全部逸出)。下列说法正确的是( )
确的是
A.氧化性: >Fe3+
B.标准状况下,若有6.72LSO 参加反应,则最终消耗0.2molK Cr O
2 2 2 7
C.反应②中,每有1molK Cr O 参加反应,转移电子6mol
2 2 7
D.由上述反应原理推断,K Cr O 可以将Na SO 氧化成Na SO A.原溶液一定存在 和 ,一定不存在 Fe3+
2 2 7 2 3 2 4
13.(本题3分)镁和铝分别和等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与反应时间 B.原溶液可能存在 Cl- 和 Na+
(t)的关系如图所示。则下列说法正确的是
C.原溶液中 c( )是 0.01mol•L-1
A.镁和铝消耗硫酸的物质的量之比是2∶3
D.若原溶液中不存在 Na+,则 c(Cl-)<0.1mol•L-1
B.参加反应的镁、铝的质量之比是8∶9
二、非选择题
C.反应中消耗的镁、铝的物质的量之比是3∶2
16.(本题12分)用含ZnCO 的菱锌矿(主要含有Fe、Al、Pb、SiO 杂质)制备硫酸锌晶体
3 2
D.反应中镁、铝转移电子的物质的量之比是2∶3 (ZnSO ·7H O)、Al O 和Fe O ,流程如下:
4 2 2 3 2 3
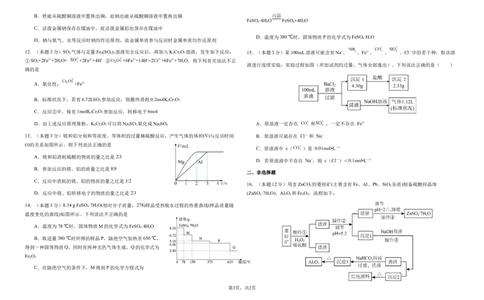
14.(本题3分)8.34 g FeSO ·7H O(相对分子质量:278)样品受热脱水过程的热重曲线(样品质量随
4 2
温度变化的曲线)如图所示。下列说法不正确的是
A.温度为78 ℃时,固体物质M的化学式为FeSO ·4H O
4 2
B.取适量380 ℃时所得的样品P,隔绝空气加热至650 ℃,
得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为
Fe O
2 3
C.在隔绝空气的条件下,M得到P的化学方程式为
第3页,共2页
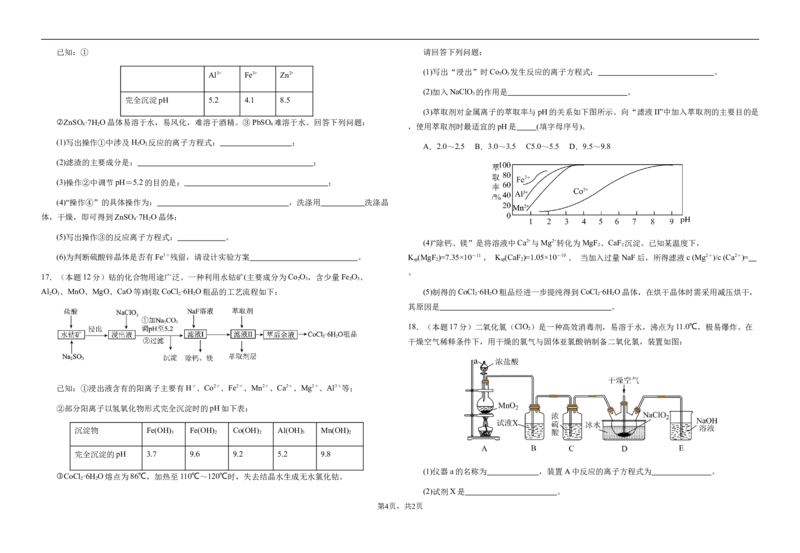
学学科科网网((北北京京))股股份份有有限限公公司司已知:① 请回答下列问题:
(1)写出“浸出”时Co O 发生反应的离子方程式: 。
Al3+ Fe3+ Zn2+ 2 3
(2)加入NaClO 的作用是 。
3
完全沉淀pH 5.2 4.1 8.5
(3)萃取剂对金属离子的萃取率与pH的关系如下图所示。向“滤液II”中加入萃取剂的主要目的是
②ZnSO ·7H O晶体易溶于水,易风化,难溶于酒精。③PbSO 难溶于水。回答下列问题:
4 2 4 ,使用萃取剂时最适宜的pH是 (填字母序号)。
(1)写出操作①中涉及H O 反应的离子方程式: ;
2 2 A.2.0~2.5 B.3.0~3.5 C5.0~5.5 D.9.5~9.8
(2)滤渣的主要成分是: ;
(3)操作②中调节pH=5.2的目的是: ;
(4)“操作④”的具体操作为: ,洗涤用 洗涤晶
体,干燥,即可得到ZnSO ·7H O晶体;
4 2
(5)写出操作③的反应离子方程式: 。
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF 、CaF 沉淀。已知某温度下,
2 2
(6)为判断硫酸锌晶体是否有Fe3+残留,请设计实验方案 。 K (MgF )=7.35×10-11 , K (CaF )=1.05×10-10 。 当加入过量NaF后,所得滤液c (Mg2+)/c (Ca2+)=
sp 2 sp 2
。
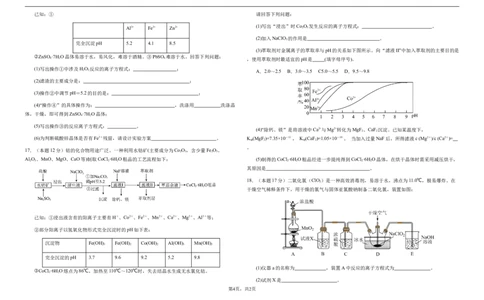
17.(本题12分)钴的化合物用途广泛。一种利用水钴矿(主要成分为Co O ,含少量Fe O 、
2 3 2 3
Al O 、MnO、MgO、CaO等)制取CoCl ·6H O粗品的工艺流程如下: (5)制得的CoCl ·6H O粗品经进一步提纯得到CoCl ·6H O晶体,在烘干晶体时需采用减压烘干,
2 3 2 2 2 2 2 2
其原因是 。
18.(本题17分)二氧化氯(ClO )是一种高效消毒剂,易溶于水,沸点为11.0℃,极易爆炸。在
2
干燥空气稀释条件下,用干燥的氯气与固体亚氯酸钠制备二氧化氯,装置如图:
已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式完全沉淀时的pH如下表:
沉淀物 Fe(OH) Fe(OH) Co(OH) Al(OH) Mn(OH)
3 2 2 3 2
完全沉淀的pH 3.7 9.6 9.2 5.2 9.8
(1)仪器a的名称为 ,装置A中反应的离子方程式为 。
③CoCl ·6H O熔点为86℃,加热至110℃~120℃时,失去结晶水生成无水氯化钴。
2 2
(2)试剂X是 。
第4页,共2页(3)装置D中冰水的主要作用是 。装置D内发生反应的化学方程式为 。 出,原因是 。制备、收集干燥的SO 气体时,所需仪器如下。装置A是气体发生装置,按气
2
流方向连接各仪器口,顺序为a→ → → → →f。装置D的作用是
(4)装置E中主要反应的离子方程式为: 。
(5)已知NaClO 饱和溶液在不同温度时析出的晶体情况如下表。
2
温度 <38℃ 38℃~60℃ >60℃
析出晶体 NaClO ·3H O NaClO 分解成NaClO 和NaCl
2 2 2 3
。
利用NaClO 溶液制得NaClO 晶体的操作步骤: 55℃蒸发结晶、 、38~60℃的温水洗
2 2
涤、低于60℃干燥。
(6)工业上也常用以下方法制备ClO 。
2
(2)步骤①反应的离子方程式为 。
(3)在强碱性条件下利用Na S O 氧化HCOONa的方法可制备保险粉连二亚硫酸钠(Na S O ),
2 2 5 2 2 4
当生成0.5molNa S O 时,消耗Na S O mol。
2 2 4 2 2 5
(4)工业上用焦亚硫酸钠法制备保险粉带来的主要问题是废水中含有大量的有机物,有机物总
含碳量用TOC表示,常采用Fenton氧化法去除废水中的有机物,即通过向废水中加入H O ,以
2 2
Fe2+作催化剂,产生具有强氧化性的羟基自由基(·OH)来氧化降解废水中的有机物。
①其他条件一定时,n(H O )∶n(Fe2+)的值对TOC去除效果的影响如图1所示:
2 2
①酸性条件下双氧水与NaClO 反应,则反应的离子方程式为 。
3
②如图所示为直接电解氯酸钠、自动催化循环制备高纯ClO 的实验。则阴极电极反应式为
2
。
19.(本题14分)焦亚硫酸钠(Na S O )有广泛的用途,实验室中通过如下方法制备:
2 2 5
①不断搅拌条件下,在饱和Na CO 溶液中缓缓通入SO 至反应 完全;
2 3 2
②取下三颈烧瓶,测得反应液的pH=4.1;
③将溶液蒸发浓缩、结晶、过滤得焦亚硫酸钠晶体
当TOC的去除率最大时,n(H O )∶n(Fe2+)= 。
请回答下列问题: 2 2
②在pH=4.5,其他条件一定时,H O 的加入量对TOC去除效果的影响如图2所示,当H O 的
(1)实验室可利用Na SO 和浓的硫酸制备少量SO 气体,但硫酸浓度太大不利于SO 气体逸 2 2 2 2
2 3 2 2
第5页,共2页
学学科科网网((北北京京))股股份份有有限限公公司司加入量大于40mL·L−1时,TOC去除率反而减小的原因是 。
第6页,共2页