文档内容
2021 级高三上学期 10 月份考试
化学试卷
一、单选题:本题共14小题,每题3分,共42分。
1.化学与生活、生产和科技息息相关。下列叙述正确的是
A.活性炭具有除异味和杀菌作用
B.用于文物年代鉴定的14C与12C互为同素异形体
C.“用胶泥刻字 烧令坚”所描写的印刷术陶瓷活字属于传统无机非金属材料
D.“天宫”空间站使用了钛合金,其属于无机非金属材料
2.下列化学用语正确的是
A.N 的电子式: B.甲烷分子的比例模型:
2
C.二氧化碳的结构式:O=C=O D.HF的电子式:
3. 为阿伏加德罗常数的值.下列说法正确的是
A.1.8g 中含有的中子数为
B.3.9g 与水完全反应时转移的电子数为
C. 溶液含有 数目为
D.常温常压下, 酒精水溶液中含氧原子总数为
4.下列反应的离子方程式书写正确的是
A.向 溶液中通入过量 :
B.饱和 溶液中通入过量 :
C.将 溶液滴入酸性 溶液:
D.向 溶液中加入 溶液:
5.某矿石的主要成分为 ,还含有 、 、 、 及少量其它杂质。某工厂
采用该矿石为主要原料生产碱式碳酸镁,流程如下(已知:温度低于700℃时, 不会与
等反应)。下列有关说法不正确的是
A.煅烧过程所发生的主要化学反应方程式为:
B.滤渣1的成分是 和
第 1 页 共 9 页
学科网(北京)股份有限公司C.氧化步骤发生反应的离子方程式可以是:Fe2++HO+2H+=Fe3++2HO
2 2 2
D.加X调pH的X是氧化镁
6.工业上制备下列物质的生产流程合理的是
A.
B.从海水中提取镁:
C.由NaCl制漂白粉:
D.由铝土矿冶炼铝:
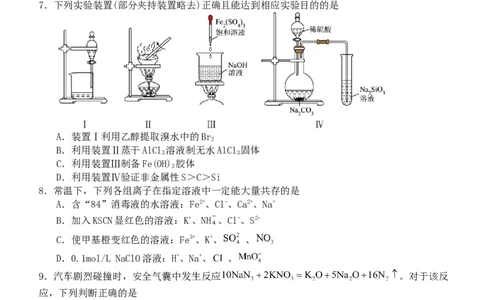
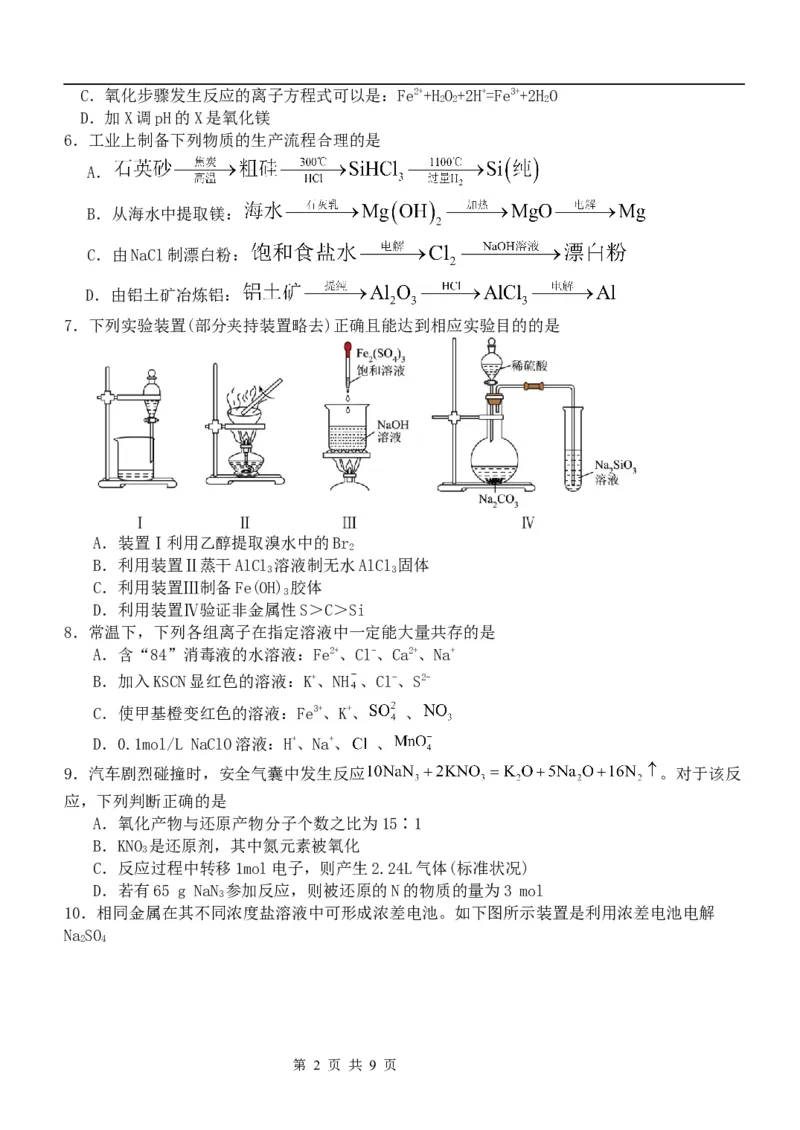
7.下列实验装置(部分夹持装置略去)正确且能达到相应实验目的的是
A.装置Ⅰ利用乙醇提取溴水中的Br
2
B.利用装置Ⅱ蒸干AlCl 溶液制无水AlCl 固体
3 3
C.利用装置Ⅲ制备Fe(OH) 胶体
3
D.利用装置Ⅳ验证非金属性S>C>Si
8.常温下,下列各组离子在指定溶液中一定能大量共存的是
A.含“84”消毒液的水溶液:Fe2+、Cl-、Ca2+、Na+
B.加入KSCN显红色的溶液:K+、NH 、Cl-、S2-
C.使甲基橙变红色的溶液:Fe3+、K+、 、
D.0.1mol/L NaClO溶液:H+、Na+、 、
9.汽车剧烈碰撞时,安全气囊中发生反应 。对于该反
应,下列判断正确的是
A.氧化产物与还原产物分子个数之比为15∶1
B.KNO 是还原剂,其中氮元素被氧化
3
C.反应过程中转移1mol电子,则产生2.24L气体(标准状况)
D.若有65 g NaN 参加反应,则被还原的N的物质的量为3 mol
3
10.相同金属在其不同浓度盐溶液中可形成浓差电池。如下图所示装置是利用浓差电池电解
NaSO
2 4
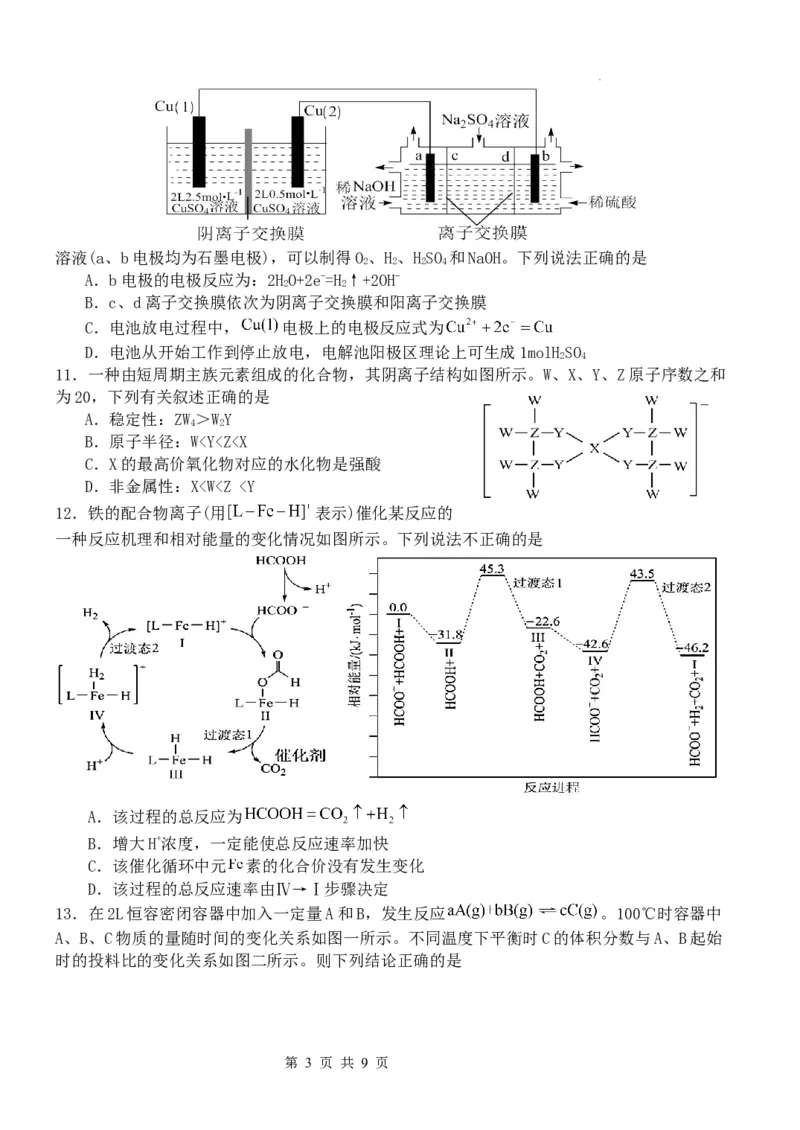
第 2 页 共 9 页溶液(a、b电极均为石墨电极),可以制得O、H、HSO 和NaOH。下列说法正确的是
2 2 2 4
A.b电极的电极反应为:2HO+2e-=H↑+2OH-
2 2
B.c、d离子交换膜依次为阴离子交换膜和阳离子交换膜
C.电池放电过程中, 电极上的电极反应式为
D.电池从开始工作到停止放电,电解池阳极区理论上可生成1molHSO
2 4
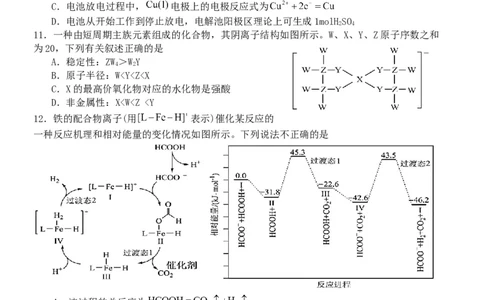
11.一种由短周期主族元素组成的化合物,其阴离子结构如图所示。W、X、Y、Z原子序数之和
为20,下列有关叙述正确的是
A.稳定性:ZW>WY
4 2
B.原子半径:Wv(正)
C.100℃时前5min平均化学反应速率
D.某温度下平衡时B的转化率随起始 的增大而减小
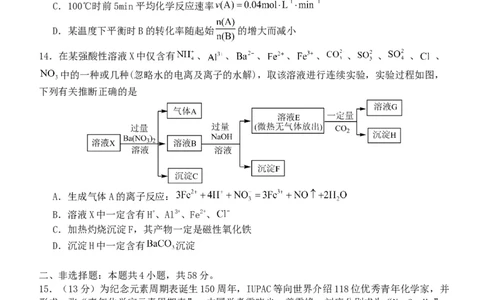
14.在某强酸性溶液X中仅含有 、 、 、 、 、 、 、 、 、
中的一种或几种(忽略水的电离及离子的水解),取该溶液进行连续实验,实验过程如图,
下列有关推断正确的是
A.生成气体A的离子反应:
B.溶液X中一定含有H+、Al3+、Fe2+、
C.加热灼烧沉淀F,其产物一定是磁性氧化铁
D.沉淀H中一定含有 沉淀
二、非选择题:本题共4小题,共58分。
15.(13分)为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并
形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”
元素的代言人。回答下列问题:
(1)汞的原子结构示意图,汞在周期表中位于第 周期。
(2)氮是自然界各种生物体生命活动不可缺少的重要元素,
磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是 ,它的中子数为 。
②已知 与 的性质相似,则对 性质的推测不正确的是 (填序号)。
a含有离子键和共价键
b能与 溶液反应
第 4 页 共 9 页c与 加热充分分解产物的种类完全一样
③下列关于第ⅤA族元素及其化合物的说法不正确的是 (填字母)。
a.热稳定性: b.酸性:
c. 的氧化物的水化物是强碱 d.形成的简单离子半径随着原子序数递增而增大
(3)砷酸( )可用于制造杀虫剂、药物。 溶于稀硝酸中可得砷酸,此反应的化学方
程式: 。
(4)科学家合成了一种新化合物(如图所示),其中R、X、Y、Z为同一短周期元素,Z核外最外层
电子数是Y核外电子数的一半。
①R的元素符号为 。
②X的氢化物的电子式: 。
③写出Y的最高价氧化物的一种用途 。
16.(15分)无水氯化亚铁是重要的还原剂,可直接用于污、废水处理,还常用于检测硒、生
产聚合氯化铝铁絮凝剂等。实验室常用氢气还原无水氯化铁法制备无水氯化亚铁。
已知:①还原性的强弱与溶液的酸碱性、溶液的浓度和反应温度等有关,其中温度越高物质还
原性越强。② 和 的部分物理性质如下表所示
熔点/℃ 672 306
沸点/℃ 1023 315
易潮解 易潮解
Ⅰ.制备无水氯化铁
工业上,向550~600℃的铁屑中通入氯气生产无水氯化铁,化学兴趣小组用如图所示的装置
模拟上述过程进行实验。
第 5 页 共 9 页
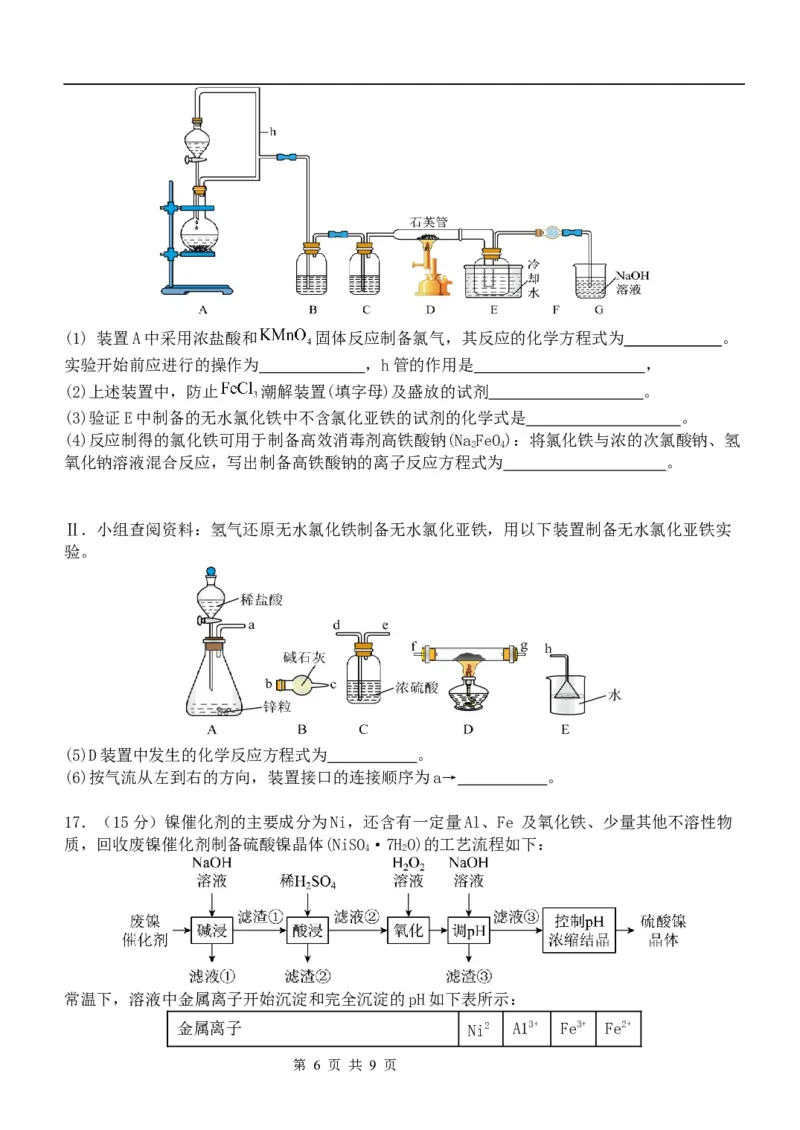
学科网(北京)股份有限公司(1) 装置A中采用浓盐酸和 固体反应制备氯气,其反应的化学方程式为 。
实验开始前应进行的操作为 ,h管的作用是 ,
(2)上述装置中,防止 潮解装置(填字母)及盛放的试剂 。
(3)验证E中制备的无水氯化铁中不含氯化亚铁的试剂的化学式是 。
(4)反应制得的氯化铁可用于制备高效消毒剂高铁酸钠(NaFeO):将氯化铁与浓的次氯酸钠、氢
2 4
氧化钠溶液混合反应,写出制备高铁酸钠的离子反应方程式为 。
Ⅱ.小组查阅资料:氢气还原无水氯化铁制备无水氯化亚铁,用以下装置制备无水氯化亚铁实
验。
(5)D装置中发生的化学反应方程式为 。
(6)按气流从左到右的方向,装置接口的连接顺序为a→ 。
17.(15分)镍催化剂的主要成分为Ni,还含有一定量Al、Fe 及氧化铁、少量其他不溶性物
质,回收废镍催化剂制备硫酸镍晶体(NiSO·7HO)的工艺流程如下:
4 2
常温下,溶液中金属离子开始沉淀和完全沉淀的pH如下表所示:
金属离子 Ni2 A13+ Fe3+ Fe2+
第 6 页 共 9 页+
开始沉淀时(c=0.01 mol·L-1)的pH 7.2 3.7 2.2 7.5
沉淀完全时(c=1.0×10-5 mol·L-1)的
8.7 4.7 3.2 9.0
pH
(1)提高“碱浸”速率的措施是 (任写两点即可)。
(2)为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。该反应的化学反应方程式是
。
(3)“氧化”步骤中加入HO 的目的是 (用离子方程式表示)
2 2
(4)“调pH”时,最适宜的pH范围是 。
(5)若工艺流程改为先“调pH”后“氧化” ,“滤液③”中可能含有的杂质离子为 。
(6)资料显示,硫酸镍结晶水合物的形态与温度有如下关系:
30.8℃-
温度 低于30.8℃ 53.8℃-280℃ 高于280℃
53.8℃
晶体形态 NiSO·7HO NiSO·6HO 多种结晶水合物 NiSO
4 2 4 2 4
从NiSO 溶液获得稳定的NiSO·6HO晶体的操作依次是 。
4 4 2
(7) 硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。该反应的
离子方程式是 。
(8)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是 。
18.(15分)我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,其中的关键
技术是运用催化转化法实现二氧化碳的碳捕集和碳利用。请回答下列问题:
Ⅰ、一定温度下, 和 在催化剂作用下可发生a、b两个平行反应,分别生成 和
。
a:
b:
(1)相同温度下,反应 的 。
(2)若 ,下列温度下反应能自发
进行的是_______(填序号)。
A. B.10℃ C. D.
(3)投料比 ,在恒温恒容条件下发生反应,下列说法能作为反应 达到平衡状态的判
据是 (填选项字母)。
A.气体密度不再变化
B.CO 的体积分数不再变化
2
C.气体平均相对分子质量不再变化
第 7 页 共 9 页
学科网(北京)股份有限公司D. 不再变化
E. 、 、 、 的物质的量之比为
(4)按照 投料,在恒容密闭容器中进行反应, 的平衡转化率随温度和压
强变化如图所示。
①压强 、 、 由大到小的顺序是 。
②同时增大 的平衡转化率和 的产率可采取的措施是 。
③一种应用双极膜(由阳离子和阴离子交换膜构成)通过电化学还原 制备甲醇的电解原理如
图所示。催化电极的电极反应式为 ,双极膜内每消耗
水,理论上石墨电极产生标准状况下 。
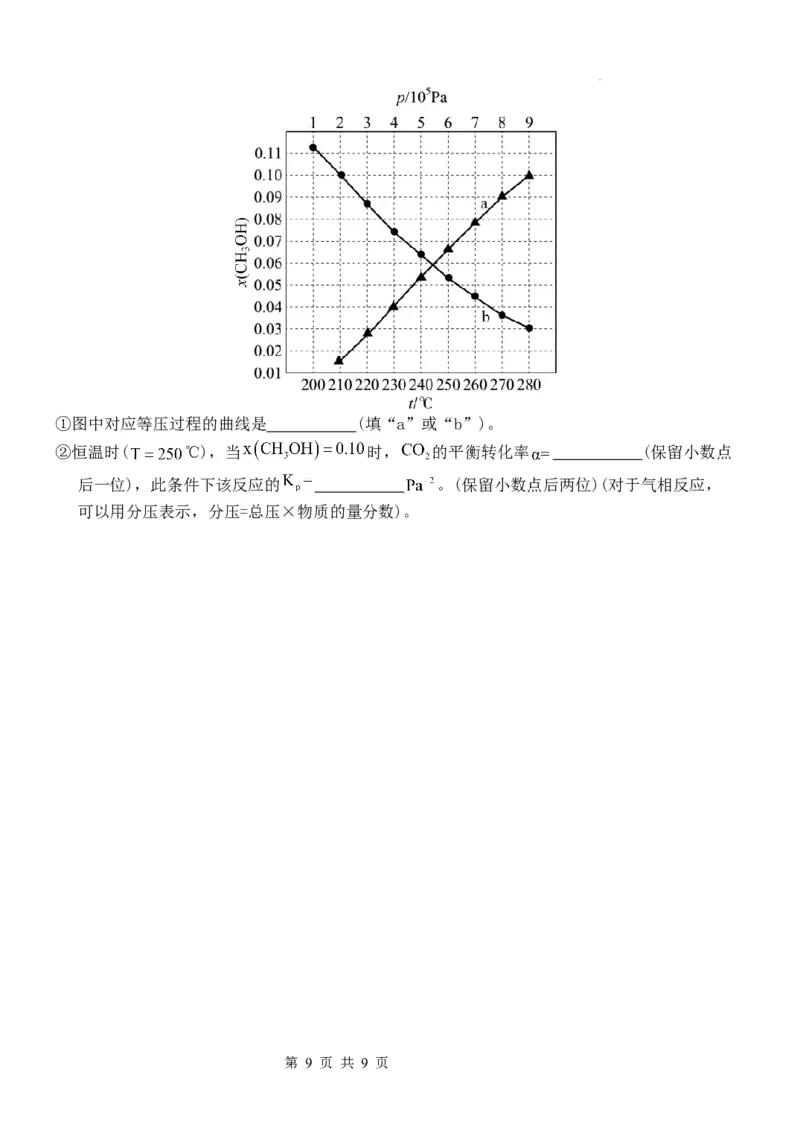
(5)二氧化碳催化加氢制甲醇的反应中 在起始
物 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为 ,在
℃时, 随压强(p)的变化及在 时 随温度(T)的变化,如
图所示。
第 8 页 共 9 页①图中对应等压过程的曲线是 (填“a”或“b”)。
②恒温时( ℃),当 时, 的平衡转化率 (保留小数点
后一位),此条件下该反应的 。(保留小数点后两位)(对于气相反应,
可以用分压表示,分压=总压×物质的量分数)。
第 9 页 共 9 页
学科网(北京)股份有限公司