文档内容
重庆市高三化学考试参考答案
1.B 【解析】本题主要考查高分子化合物,侧重考查学生对基础知识的认知能力。大理石、玉石均为无
机物,B项符合题意。
2. D 【解析】本题主要考查化学用语,侧重考查学生对基础知识的理解能力。基态O原子的轨道表示式
为
,D项错误。
3. B 【解析】本题主要考查化学与生活,侧重考查学生对基础知识的认知能力。K₂FeO₄可用于水体杀菌
消毒,但不能软化硬水,B项错误。
4. C 【解析】本题主要考查与氧化还原有关的化学变化,侧重考查学生对基础知识的认知能力和简单应
用能力。能够吸收氧气防止食品变质,该过程涉及氧化还原反应,C项符合题意。
5. A 【解析】本题主要考查离子键的相关知识,侧重考查学生分析和解决问题的能力。金属元素的电负
性:Li25.00 mL一10.00 mL=15.00. mL,a
项符合题意。
③ 根 据 方 程 式 可 知 关 系 式 I ∼2S O2− ∼2KI, n(KI)=n(S O2−)=0.2×14.5×10−3=
2 2 3 2 3
0.4814
0.0029(mp4),其质量: m(KI)=0.0029×166=0.4814(g),样品的纯度 = ×100%≈96%。
0.5000
16.(10)适当升高温度(或搅拌等合理答案均可,1分)
(2)Nd₂(SO₄)₃+Na₂SO₄+xH₂O═Nd₂(SO₄)₃·Na₂SO₄·xH₂O↓( (2分)
(3)取最后一次洗涤液于试管中,向其中先滴加稀盐酸,再滴加氯化钡溶液,无白色沉淀生成(2分);坩
埚(1分)
(4)3.0×10⁻⁴(2分)
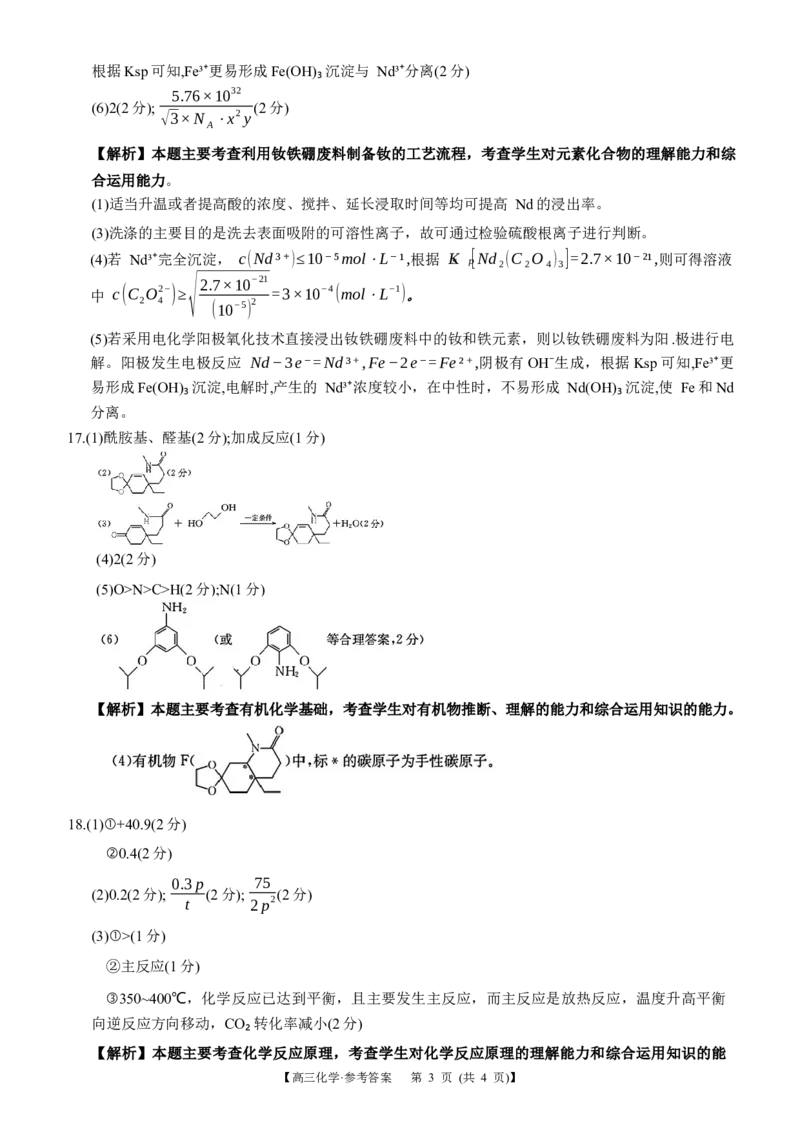
(5)钕铁硼废料(1分);阳极发生电极反应 Nd−3e⁻=Nd³⁺,Fe−2e⁻=Fe²⁺,Fe²⁺易被氧化为Fe³⁺,
【高三化学·参考答案 第 2 页 (共 4 页)】根据Ksp可知,Fe³⁺更易形成Fe(OH)₃沉淀与 Nd³⁺分离(2分)
5.76×1032
(6)2(2分); (2分)
√3×N ⋅x2y
A
【解析】本题主要考查利用钕铁硼废料制备钕的工艺流程,考查学生对元素化合物的理解能力和综
合运用能力。
(1)适当升温或者提高酸的浓度、搅拌、延长浸取时间等均可提高 Nd的浸出率。
(3)洗涤的主要目的是洗去表面吸附的可溶性离子,故可通过检验硫酸根离子进行判断。
(4)若 Nd³⁺完全沉淀, c(Nd³⁺)≤10⁻⁵mol⋅L⁻¹,根据 Kₛ ₚ[Nd₂(C₂O₄)₃]=2.7×10⁻²¹,则可得溶液
√2.7×10−21
中 c(C O2−)≥ =3×10−4(mol⋅L−1)。
2 4 (10−5) 2
(5)若采用电化学阳极氧化技术直接浸出钕铁硼废料中的钕和铁元素,则以钕铁硼废料为阳.极进行电
解。阳极发生电极反应 Nd−3e⁻=Nd³⁺,Fe−2e⁻=Fe²⁺,阴极有OH⁻生成,根据Ksp可知,Fe³⁺更
易形成Fe(OH)₃沉淀,电解时,产生的 Nd³⁺浓度较小,在中性时,不易形成 Nd(OH)₃沉淀,使 Fe和Nd
分离。
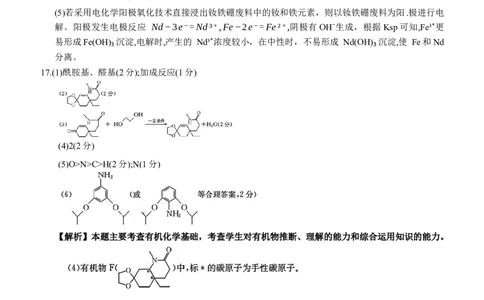
17.(1)酰胺基、醛基(2分);加成反应(1分)
(4)2(2分)
(5)O>N>C>H(2分);N(1分)
【解析】本题主要考查有机化学基础,考查学生对有机物推断、理解的能力和综合运用知识的能力。
18.(1)①+40.9(2分)
②0.4(2分)
0.3p 75
(2)0.2(2分); (2分); (2分)
t 2p2
(3)①>(1分)
②主反应(1分)
③350~400℃,化学反应已达到平衡,且主要发生主反应,而主反应是放热反应,温度升高平衡
向逆反应方向移动,CO₂转化率减小(2分)
【解析】本题主要考查化学反应原理,考查学生对化学反应原理的理解能力和综合运用知识的能
【高三化学·参考答案 第 3 页 (共 4 页)】力。
(2)设平衡时 CO₂的物质的量为xmol,H₂的物质的量为ymol,CO的物质的量为z mol,根据
C守恒:x+n+z=0.5
H守恒: 2y+4n+0.3×2=0.9×2
O守恒:2x+n+0.3+z=0.5×2
0.5+0.9 1.4
=
x+ y+n+0.3+z 1
解得:x=0.2,y=0.2,z=0.1,n=0.2
平衡后物质的总量:0.2+0.2+0.2+0.1+0.3=1.0(mol)
平衡后各物质分压:p(CO₂)=0.2p kPa、p(H₂)=0.2p kPa、p(CH₃OH)=0.2p kPa、 p(H₂O)=0.3p kPa
5
起始时分压 p' (CO )= p,kPa=0.5p,kPa,p(CO )=0.5p,kPa−0.2p,kPa=0.3p,kPa,则 CO₂的
2 14 2
0.3p 0.2p×0.3p 75
分压变化率为 kPa⋅min−1,K = (kPa) −2= (kPa) −2 。
t p (0.2p) 3×0.2p 2p2
(3)①根据图像可知,400℃之前,CH₄的选择性为100%,即400℃之前,发生主反应,主反应为放热反应,
根据温度与CO₂转化率的关系图可知,350℃时反应达到平衡,350℃之前 CO₂的转化率逐渐增大,
说明反应未达到平衡,即 v (a)>v (a)。
iE 追
②根据题中图像可知,低温下,CH₄ 的选择性为100%,即该催化剂在较低温度主要选择主反应。
③根据上述分析,350.℃时主反应达到平衡,350~400℃,化学反应已达到平衡,且主要发生主反
应,而主反应是放热反应,温度升高平衡向逆反应方向移动,CO₂转化率减小。
【高三化学·参考答案 第 4 页 (共 4 页)】